信迪利單抗、貝伐珠單抗聯合肝動脈化療栓塞術在中晚期肝癌患者中的臨床應用*
惠鋒,馬守成,裴霞霞
(1.慶陽市中醫醫院 腫瘤科,甘肅 慶陽 745000;2.蘭州大學第一附屬醫院 腫瘤內科,甘肅 蘭州 730000;3.蘭州大學第二附屬醫院 腫瘤內科,甘肅 蘭州 730000)
肝動脈化療栓塞術(transcatheter arterial chemoembolization,TACE)短時間內可實現肝腫瘤供血血管栓塞,控制病情進展。但相關研究報道,TACE并非手術治療,無法實現對腫瘤病灶的完整性切除,TACE治療后殘存病灶因腫瘤供血血管栓塞,可能表現為應激性過表達血管內皮生長因子(vascular endothelial growth factor,VEGF),促進肝腫瘤的復發及轉移,且肝臟血供豐富,單純TACE治療后VEGF的應激性表達更明顯,不利于患者長期預后[1-4]。貝伐珠單抗是VEGF抗體,可抑制內皮細胞有絲分裂,減少新生血管形成,具有強效抑制作用,并且可增強TACE達到腫瘤細胞的化療藥物濃度,發揮抗腫瘤作用[5-6]。2009年貝伐珠單抗首次經美國食品藥品監督管理局(FDA)批準可聯合標準化化療方案治療轉移性結腸癌[7]。信迪利單抗是我國自主研發的全人源化抗程序性死亡受體-1(programmed cell death protein 1,PD-1)單克隆抗體,通過抑制PD-1與PD-1配體(programmed death ligand-1,PD-L1)結合,阻斷PD-1/PD-L1引起的免疫抑制,提高免疫監視,發揮抗腫瘤作用[8]。本研究采用前瞻性研究方法分析信迪利單抗、貝伐珠單抗聯合TACE治療中晚期肝癌患者的臨床療效,為后續臨床實踐的合理用藥提供參考。
1 資料與方法
1.1 研究對象
選取2018年12月—2019年12月慶陽市中醫醫院收治的中晚期肝癌患者84例,隨機分為研究組、對照組,每組42例。對照組女性16例,男性26例;年齡43~77歲,平均(57.13±4.02)歲;中華醫學會肝癌學組(China Liver Cancer,CNLC)肝癌分期:ⅡB期14例、ⅢA期28例;Child-puugh分級:A級10例、B級32例;東部合作腫瘤組織(Eastern Cooperative Oncology Group,ECOG)體能狀況評分:0分7例、1分35例;瘤體最大徑25~146 mm,平均(8.17±1.64)mm;合并乙型肝炎病毒感染39例。研究組女性13例,男性29例;年齡44~78歲,平均(57.25±3.79)歲;CNLC肝癌分期:ⅡB期12例、ⅢA期30例;Childpuugh分級:A級11例、B級31例;ECOG體能狀況評分:0分8例、1分34例;瘤體最大徑29~135 mm,平均(8.23±1.58)mm;合并乙型肝炎病毒感染40例。兩組上述一般資料比較,差異均無統計學意義(P>0.05),具有可比性。本研究經醫院醫學倫理委員會批準,患者簽署知情同意書。
1.2 納入與排除標準
1.2.1 納入標準 ①符合《原發性肝癌規范化病理診斷指南(2015年版)》[9]中原發性肝癌的臨床診斷,且經手術病理或肝穿刺活檢病理檢查確診;②年齡> 18歲;③可檢測活化腫瘤病灶≥ 1個;④無法實施手術根治性切除;⑤CNLC肝癌分期ⅡB~ⅢA期。1.2.2 排除標準 ①存在活動性出血病灶;②合并多器官功能障礙;③入組前1個月接受外科手術;④嚴重精神疾病;⑤遠端轉移;⑥合并其他惡性腫瘤。
1.3 治療方法
所有受試者接受TACE治療。經股動脈行肝動脈穿刺血管造影,確定病灶位置和供血動脈方向后,將雷替曲塞4 mg經2.7 F微導管置入腫瘤供血動脈,微導管越過膽囊動脈分支預防膽囊穿孔,將罌粟乙碘油6 mL、洛鉑40 mg、表柔比星30 mg經導管注入腫瘤供血支,行肝動脈栓塞化療。待血管中血流變緩至停止后,再次行肝動脈造影,觀察到腫瘤病灶顏色消失后,閉塞供血動脈。
對照組采用貝伐珠單抗治療。TACE術后靜脈滴注貝伐珠單抗(瑞士羅氏制藥,規格:100 mg,批號:H0162B09,)15 mg/kg,每3周給藥1次。所有患者維持治療至病情進展或無法耐受。
研究組在對照組基礎上聯合信迪利單抗治療。靜脈滴注信迪利單抗(蘇州信達生物制藥有限公司,規格:10 mL∶100 mg,批號:S20180016)200 mg,每3周給藥1次。所有患者維持治療至病情進展或無法耐受。
1.4 觀察指標
1.4.1 療效評估 治療3個月后,根據CT及MRI等影像學結果,參考實體瘤評價標準1.1[10]評估患者抗腫瘤效果,包括進展(progressive disease,PD)、穩定(stable disease,SD)、部分緩解(partial response,PR)和完全緩解(complete response,CR),疾病控制率=(SD+PR+CR)例數/總例數×100%,客觀緩解率=(PR+CR)例數/總例數×100%。
1.4.2 腫瘤標志物 治療前、治療后3個月采集兩組患者外周靜脈血,采用酶聯免疫吸附試驗檢測兩組患者血清甲胎蛋白(alpha-fetoprotein,AFP)、癌胚抗原(carcinoembryonic antigen,CEA)、糖類抗原199(carbohydrate antigen 199,CA199)水平。
1.4.3 免疫指標 治療前、治療后3個月采集兩組患者外周靜脈血,采用流式細胞儀檢測CD3+、CD4+、CD8+、自然殺傷(natural killer,NK)細胞,并計算CD4+/CD8+。
1.4.4 不良反應 參考美國國家癌癥研究所不良反應事件通用術語標準[11]評價研究藥物不良反應,包括消化道毒性(食欲不振、腹瀉)、皮膚黏膜毒性(手足皮膚反應、口腔黏膜出血、皮疹、水泡、頭皮毛囊炎)、肌肉組織毒性(面部浮腫、肚臍下方疼痛、乏力、后背疼痛、關節酸痛)。
1.4.5 隨訪 自患者首次給藥始,采用電話回訪、門診復查等方式進行3年的跟蹤隨訪,記錄總生存期(overall survival,OS)和無進展生存期(progressionfree survival,PFS)。PFS為首次給藥日期到疾病進展或者患者死亡或失訪日期;OS為入組診斷日期到患者死亡或失訪日期。
1.5 統計學方法
數據分析采用SPSS 19.0統計軟件。計數資料以構成比或率(%)表示,比較用χ2檢驗;計量資料以均數±標準差(±s)表示,比較用t檢驗;Kaplan-Meier法繪制生存曲線,比較用Log-rank χ2檢驗。P<0.05為差異有統計學意義。
2 結果
2.1 兩組臨床療效比較
研究組與對照組客觀緩解率分比較,經χ2檢驗,差異有統計學意義(χ2=4.850,P=0.028);研究組客觀緩解率高于對照組。研究組與對照組疾病控制率比較,經χ2檢驗,差異無統計學意義(χ2=1.120,P=0.290)。見表1。

表1 兩組臨床療效比較 [n=42,例(%)]
2.2 兩組治療前后腫瘤標志物的變化
兩組治療前后AFP、CEA、CA199的差值比較,經t檢驗,差異均有統計學意義(P<0.05),研究組治療前后AFP、CEA、CA199的差值均高于對照組。見表2。
表2 兩組治療前后腫瘤標志物的差值比較(n=42,±s)
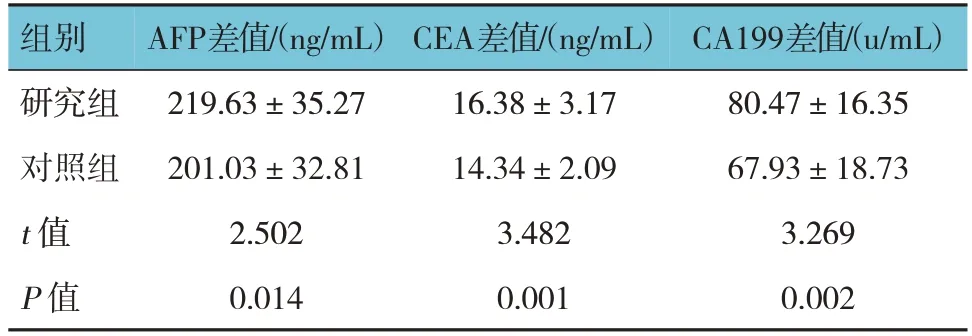
表2 兩組治療前后腫瘤標志物的差值比較(n=42,±s)
組別研究組對照組t 值P 值AFP差值/(ng/mL)219.63±35.27 201.03±32.81 2.502 0.014 CEA差值/(ng/mL)16.38±3.17 14.34±2.09 3.482 0.001 CA199差值/(u/mL)80.47±16.35 67.93±18.73 3.269 0.002
2.3 兩組治療前后免疫指標的變化
兩組治療前后CD3+、CD4+/CD8+、NK的差值比較,經t檢驗,差異均有統計學意義(P<0.05),研究組治療前后CD3+、CD4+/CD8+、NK的差值均高于對照組。見表3。
表3 兩組治療前后免疫指標的差值比較 (n=42,±s)
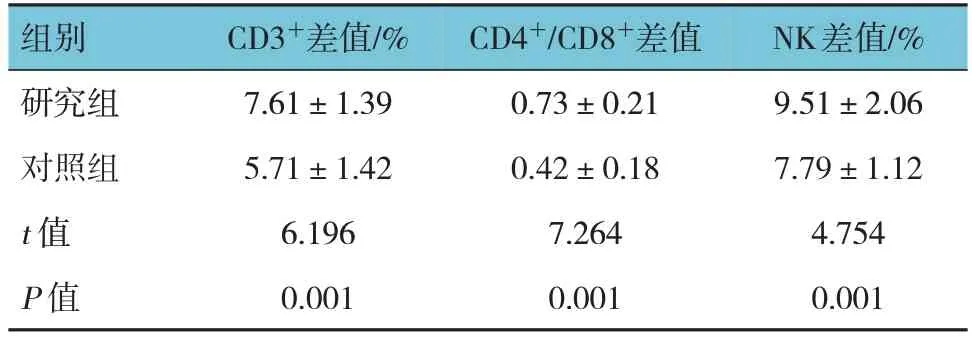
表3 兩組治療前后免疫指標的差值比較 (n=42,±s)
組別研究組對照組t 值P 值CD3+差值/%7.61±1.39 5.71±1.42 6.196 0.001 CD4+/CD8+差值0.73±0.21 0.42±0.18 7.264 0.001 NK差值/%9.51±2.06 7.79±1.12 4.754 0.001
2.4 兩組不良反應發生率比較
兩組食欲不振、腹瀉、手足皮膚反應、口腔黏膜出血、皮疹、水泡、頭皮毛囊炎、面部浮腫、肚臍下方疼痛、乏力、后背疼痛、關節酸痛的發生率比較,經χ2檢驗,差異均無統計學意義(P>0.05)。見表4。
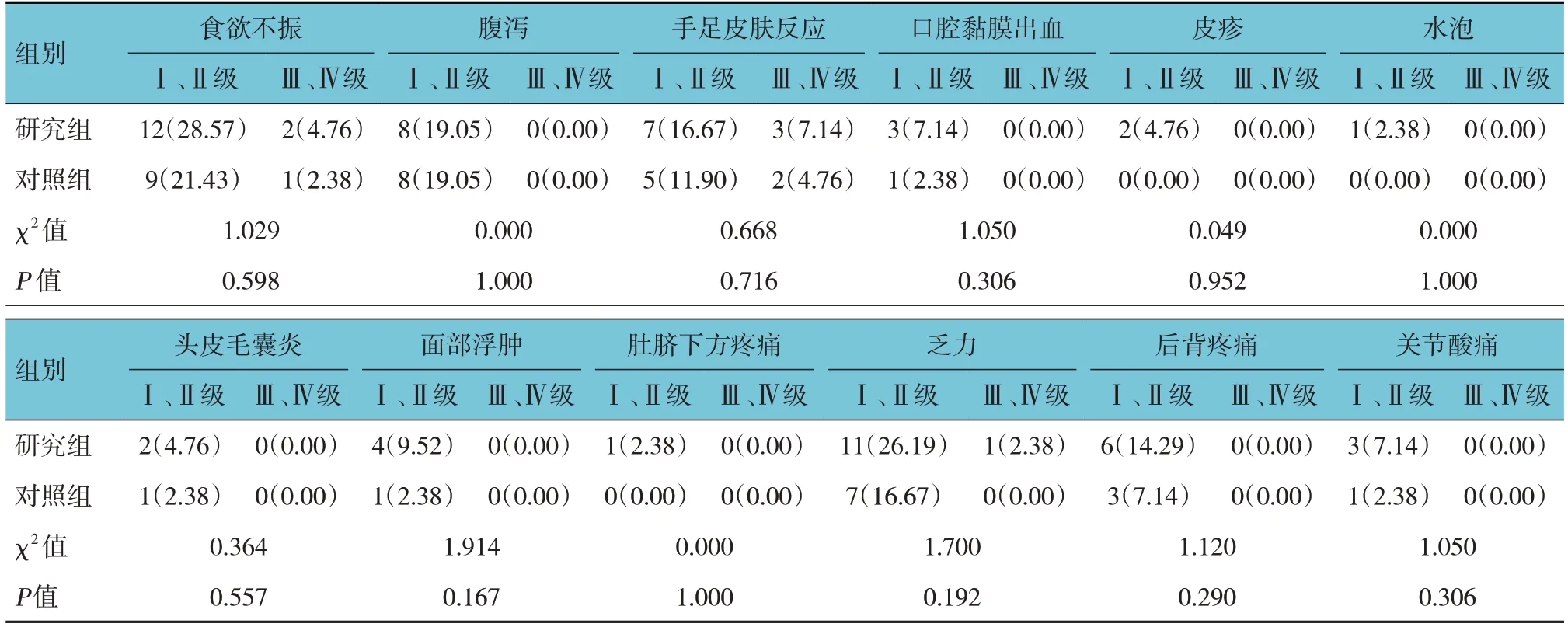
表4 兩組不良反應發生率比較 [n=42,例(%)]
2.5 兩組預后
截止隨訪結束,研究組失訪2例,對照組失訪4例,總隨訪率為92.86%。研究組死亡23例,中位PFS 14個月,中位OS 23個月,3年總生存率為42.50%;對照組死亡26例,中位PFS 10個月,中位OS 20個月,3年總生存率為31.58%。兩組PFS、OS生存曲線比較,經Log-rank χ2檢驗,差異均有統計學意義(χ2=5.144和2.702,P=0.002和0.036),研究組PFS、OS優于對照組。見圖1、2。

圖1 兩組PFS生存曲線
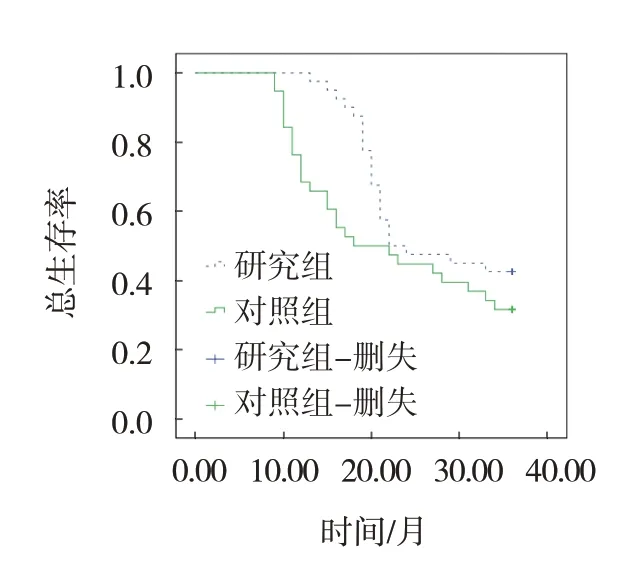
圖2 兩組OS生存曲線
3 討論
肝癌作為我國常見的一類惡性腫瘤,發病率、病死率居高不下。相關研究認為,缺乏典型性臨床癥狀、體征可能是早期檢出率低、遠期生存預后差的重要原因;目前我國臨床報道的多數原發性肝癌患者多以乙型病毒性肝炎為基礎病因,且可能通過肝炎-肝纖維化-肝硬化-肝癌病理途徑逐步向肝癌過渡,加之臨床實踐過程中患者對肝臟穿刺活檢的接受率低,導致多數患者確診時已至中晚期,錯失行根治性手術切除的最佳時機,長期預后差[12-14]。部分學者發現,肝臟腫瘤的血供幾乎全部來源于肝動脈,有效阻斷肝臟供血動脈,對促進腫瘤細胞壞死、凋亡具有積極作用[15-16]。TACE是不可切除原發性肝癌的首選治療方案之一,在中晚期肝癌患者中應用逐漸廣泛且表現出較好的臨床效果[17]。但近些年相關研究提出,TACE在肝癌治療后的短期療效雖較理想,但伴隨病情進展,殘存病灶和繼發性新病灶仍然是威脅患者遠期生存的關鍵,因此在TACE治療基礎上聯合其他治療方案進一步提高抗腫瘤效果成為近些年臨床醫師不斷探索的重點[18-19]。
腫瘤新生血管抑制劑是近些年免疫治療的研究熱點之一,其中貝伐珠單抗作為一種人源化免疫球蛋白是目前最廣泛抑制腫瘤血管生成的單克隆抗體。早期研究證實,貝伐珠單抗治療晚期腎細胞癌、復發性非小細胞肺癌、轉移性或復發性宮頸癌、膠質母細胞瘤、原發性腹膜癌、上皮性卵巢癌等惡性腫瘤療效較好[20-21]。PD-1抑制劑和PD-L1抑制劑是免疫治療中不同于抗腫瘤新生血管生成的另一作用機制的生物靶向藥物。越來越多的證據表明PD-1通路損傷在肝癌發病機制中發揮重要作用[20-21]。其中PD-1是免疫T細胞上的一種跨膜受體,主要在CD4+T細胞、CD8+T細胞、樹突狀細胞、NK細胞、B細胞等免疫細胞中表達。正常狀態下,當抗原進入機體后,T細胞被激活并分化、增殖為效應T細胞發揮免疫殺傷作用,且T細胞激活過程中,誘導表達的PD-1與樹突細胞上表達的PD-L1結合后可向T細胞傳達抑制指令,避免T細胞無限增殖,維持機體免疫T細胞表達的動態平衡;當正常細胞癌變后,PD-L1、PD-L2表達上調,PD-1/PD-L1、PD-1/PD-L2信號路徑被激活,對T細胞的活化、增殖產生負反饋調節作用,誘導腫瘤免疫逃逸,減少對腫瘤細胞的殺傷作用[22]。此外效應T細胞上的PD-1表達升高可加重患者自身免疫紊亂。結合既往研究報道,本研究嘗試使用我國自主研發的PD-1抑制劑信迪利單抗聯合貝伐珠單抗應用于中晚期肝癌的治療效果,結果顯示,研究組總生存率高于對照組,客觀緩解率高于對照組,AFP、CEA及CA199低于對照組,表明信迪利單抗、貝伐珠單抗聯合TACE治療中晚期肝癌,更有助于提升抗腫瘤效果。在機體對腫瘤細胞的免疫監視、識別、殺傷過程中,腫瘤細胞中過表達的PD-L1配體和浸潤在腫瘤組織中的T細胞過表達的PD-1,通過PD-1/PD-L1信號途徑相互作用實現了對機體細胞免疫反應的抑制作用,進而使腫瘤細胞得以逃避免疫細胞的監視。信迪利單抗則通過阻斷PD-1/PD-L1信號通路,提高免疫監視,從而達到抗腫瘤的作用,提升整體抗腫瘤效果。本研究結果顯示,研究組治療前后CD3+、CD4+/CD8+、NK的差值均高于對照組,表明信迪利單抗、貝伐珠單抗聯合TACE治療中晚期肝癌,更有助于調節患者的免疫細胞水平,其原因可能與信迪利單抗阻斷PD-1/PD-L1信號途徑,激活T細胞活性有關。藥物毒性反應一直是臨床抗腫瘤治療中無法攻克的難點。信迪利單抗作為我國新研發的全人源性抗PD-1,其安全性尚需大量研究不斷證實。趙慧等[23]研究報道,患者在接受信迪利單抗治療30~180 d出現1例嚴重放射性召回性肺炎;吳玉佩等[24]研究發現信迪利單抗治療后出現罕見紫癜樣皮膚血管炎;田丹杏[25]報道在連續3次使用信迪利單抗治療后,患者出現大面積皮疹。本研究中兩組患者均未出現嚴重的不良反應,僅少數患者出現較為嚴重的食欲不振、手足皮膚病和乏力癥狀,經治療后癥狀緩解,均可耐受,提示信迪利單抗、貝伐珠單抗聯合TACE治療中晚期肝癌患者,安全性良好。
研究存在的不足之處:本研究納入樣本量有限,可能無法完全客觀反映對藥物毒性的分析,后續研究中仍需針對早期報道中有關信迪利單抗可能出現的嚴重不良反應進行佐證。此外,由于生物靶向制劑的藥價高于多數常規抗腫瘤化療藥物,盡管信迪利單抗作為國產抗PD-1生物靶向制劑,相對于進口生物靶向制劑價格有所降低,但對于長期接受抗腫瘤治療的家庭仍是一筆不小的負擔,因此后續研究針對中晚期肝癌患者的整體治療方案設計時,仍需進行成本-效益分析,以確定適合患者的最佳治療方案。
綜上所述,信迪利單抗、貝伐珠單抗聯合TACE治療中晚期肝癌患者,可有效調節腫瘤標志物和免疫因子水平,延長患者生存時間,且安全性良好。

