M1型乙酰膽堿受體在微波輻射致小鼠認知行為改變中的作用
何鋼華 , 潘 婷 , 馮志華 , 崔智琳 , 楊鎂楹 , 李 楊 , 左紅艷 , 鄧 樺
(1. 佛山科學技術學院生命科學與工程學院 , 廣東 佛山 528231 ; 2. 中國人民解放軍軍事科學院軍事醫學研究院輻射醫學研究所 , 北京 海淀 100850)
伴隨各種電子設備的發展和應用,微波輻射對人體健康的影響備受關注。微波輻射(Microwave radiation,MR)是指頻率在300 MHz~300 GHz,波長為1 mm~1 m的電磁波輻射[1],其作為一種嚴重的環境污染源,可對人或動物的中樞神經系統造成影響。研究表明,中樞神經系統是對微波輻射敏感的重要靶器官,且海馬是微波輻射敏感的重要靶部位,微波輻射可導致認知功能障礙[2],但其作用機制尚未闡明。眾所周知,膽堿能神經系統由能夠合成乙酰膽堿(Acetylcholine,ACh)的膽堿能神經元組成,ACh和乙酰膽堿受體(Acetylcholine receptors,AChRs)在學習和記憶中發揮關鍵作用[3]。然而,關于微波輻射對腦內AChRs的影響及其在認知功能障礙中的作用尚不明確。
本試驗在前期工作基礎上,建立微波輻射動物模型[4],基于微波輻射對海馬各亞區組織形態結構的影響,以及海馬AChRs亞型基因表達變化,選取M1型AChR(M1-AChR)特異性激動劑,進一步探討M1-AChR在微波輻射致小鼠認知行為改變中的作用,以期為微波輻射腦損傷效應機制及其防治研究提供新思路。
1 材料與方法
1.1 主要試劑 蘇木精-伊紅(Hematoxylin-Eosin,H.E.)染液,購自北京雷根(Leagene)生物技術有限公司;RNA Isolater Total RNA Extraction Reagent、HiScript Ⅲ RT SuperMix RNA逆轉錄試劑盒和TaqPro Universal SYBR qPCR Master Mix試劑盒,均購自南京諾唯贊生物科技股份有限公司;VU0357017 hydrochloride M1-AChR激動劑,購自TargetMol中國(陶術生物)公司。
1.2 主要儀器 RM2255石蠟切片機,德國徠卡(Leica)儀器有限公司產品;Pannoramic MIDI Ⅱ數字切片掃描系統,匈牙利 3DHISTECH公司產品;N60-Touch超微量紫外分光光度儀,因普恩(北京)國際貿易有限公司產品;CFX Opus 96熒光定量PCR儀,伯樂生命醫學產品(上海)有限公司產品;Any-maze動物行為學視頻分析系統,美國Stoelting公司產品。
1.3 實驗動物 10周齡SPF級C57BL/6N健康小鼠共49只,體重(26 ± 2)g,雌雄各半,購自斯貝福(北京)生物技術有限公司[生產許可證號:SCXK(京)2019—0010],飼養于中國人民解放軍軍事科學院軍事醫學研究院(以下稱軍科院)實驗動物中心。動物試驗符合軍科院實驗動物中心醫學倫理委員會標準(倫理批準號:IACUC-DWZX-2021-685)。
1.4 微波輻射動物模型建立 將小鼠隨機分為空白對照組(Con組)和微波輻射組(MR組),MR組利用軍科院自建微波輻射模擬源對小鼠進行單次全身照射。將小鼠放置于透明帶孔的圓形有機玻璃盒中,自由體位,采用中心頻率為2.856 GHz,平均功率密度為8 mW/cm2,SAR值為6.12 W/kg的微波對小鼠全身均勻輻射15 min(單次);Con組小鼠放置于相同的有機玻璃盒內,在同樣的照射環境中進行單次偽輻射15 min。
1.5 海馬組織病理學觀察 Con組和MR組小鼠各6只。微波輻射后7 d,小鼠經腹腔注射1%戊巴比妥鈉[50 mg/(kg·bw)]麻醉后取腦組織,經4%多聚甲醛室溫固定2周,依次進行梯度乙醇脫水、二甲苯透明、浸蠟、包埋和石蠟切片,切片厚度3 μm;經H.E.染色后,采用Pannoramic MIDI Ⅱ 數字切片掃描系統觀察海馬組織形態結構改變。
1.6 實時熒光定量PCR(Real-time fluorescence quantitative PCR,RT-qPCR)檢測海馬AChRs基因表達 Con組和MR組小鼠各5只。微波輻射后7 d,小鼠經腹腔注射1%戊巴比妥鈉[50 mg/(kg·bw)]麻醉后取腦組織,冰上剝離雙側海馬。采用TRIzol試劑提取海馬組織總RNA,利用超微量紫外分光光度儀測定RNA濃度以及A260/A280和A260/A230比值。取1.8

表1 實時熒光定量PCR引物信息
1.7 VU0357017 hydrochloride給藥方法 將小鼠隨機分為空白對照組(Con-NS組)、輻射對照組(MR-NS組)和輻射給藥組(MR-VU組),每組各9只。微波輻射后7 d,MR-VU組小鼠腹腔注射M1-AChR特異性激動劑VU0357017 hydrochloride,注射劑量為10 mg/(kg·bw);Con-NS組和MR-NS組注射同等體積生理鹽水,各組于給藥后30 min進行行為學試驗。
1.8 行為學試驗
1.8.1 新物體識別(Novel object recognition,NOR)試驗 采用40 cm×40 cm×40 cm曠場箱,將大小相同但顏色不同的2個正方體(4 cm×4 cm×4 cm)沿對角線置于距箱體邊緣10 cm處。試驗前將小鼠置于試驗環境中,每天對其進行適應性操作30 min,連續3 d。試驗開始時,采用Any-maze動物行為學視頻分析軟件記錄小鼠運動軌跡5 min,采集小鼠探索新和舊物體的時間。分別按公式(1)和(2)計算動物的辨別指數(Discrimination index,DI)和認知指數(Recognition index,RI),檢測小鼠新物體探索行為的改變。
DI=(探索新物體時間-探索舊物體時間)÷(探索新物體時間+探索舊物體時間)
(1)
RI(%)=探索新物體時間÷(探索新物體時間+探索舊物體時間)×100%
(2)
1.8.2 Y迷宮(Y maze)試驗 采用臂長30 cm、寬8 cm、高15 cm的Y迷宮,試驗前將小鼠置于試驗環境中,每天對其進行適應性操作30 min,連續3 d。試驗開始時,采用Any-maze動物行為學視頻分析軟件記錄小鼠運動軌跡8 min,采集小鼠進入Y迷宮各臂的時間和次數,按公式(3)計算自由交替率(Spontaneous alternation),檢測小鼠空間探索能力的改變。
自由交替率(%)=連續進入3個不同臂的次數 ÷ (進臂總次數-2)×100%
(3)
2 結果
2.1 微波輻射對小鼠海馬各亞區組織形態結構的影響 微波輻射后7 d,H.E.染色結果顯示,空白對照組小鼠海馬阿蒙氏角1(Cornu ammonis 1,CA1)、阿蒙氏角2(Cornu ammonis 2,CA2)、阿蒙氏角3(Cornu ammonis 3,CA3)和齒狀回(Dentate gyrus,DG)區組織結構均基本正常(圖1A~1E);微波輻射組小鼠海馬CA1和CA3區部分錐體神經元核固縮深染,血管周圍間隙略增寬,其中CA3區組織病理學改變更為明顯;CA2和DG區組織結構變化不明顯(圖1F~1J)。
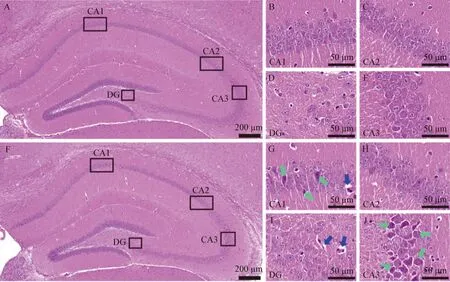
圖1 微波輻射后小鼠海馬的組織病理學變化(H.E.染色,A和F:8×; B~E和G~J:40×)
2.2 微波輻射對小鼠海馬組織AChR亞型基因表達的影響 RT-qPCR結果如圖2所示,微波輻射后7 d,與空白對照組相比較,微波輻射組小鼠海馬組織M1和M3型AChR mRNA相對表達量均顯著下調(M1-AChR,P<0.01;M3-AChR,P<0.05),M2、M4、α4和α7型AChR mRNA相對表達量均顯著上調(P<0.05),M5和β2型AChR mRNA相對表達量均未見統計學差異變化(P>0.05)。
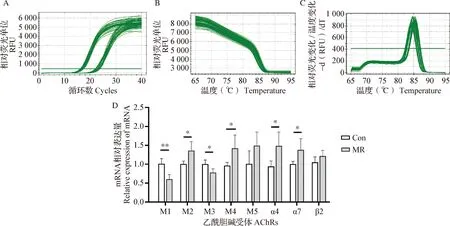
圖2 微波輻射后小鼠海馬乙酰膽堿受體基因mRNA表達的變化
2.3 M1型AChR激活對微波輻射致小鼠認知行為改變的影響 新物體識別試驗結果顯示,微波輻射后7 d,與空白對照組(Con-NS組)相比,輻射對照組(MR-NS組)小鼠對新物體的DI和RI均顯著下降(P<0.05);腹腔注射M1-AChR激動劑VU0357017 hydrochloride(VU)后,與輻射對照組相比較,輻射給藥組(MR-VU組)小鼠對新物體的DI和RI均顯著升高(P<0.05),且與Con-NS組相比無統計學差異(P>0.05,圖3E~3F)。Y迷宮試驗結果顯示,微波輻射后7 d,各試驗組之間小鼠的自由交替率均未見顯著性變化(P>0.05,圖3G)。
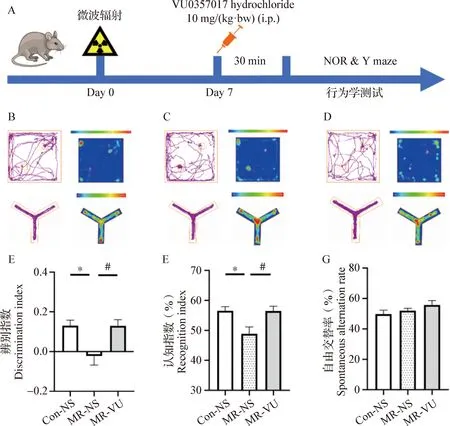
圖3 M1型乙酰膽堿受體激活對微波輻射所致小鼠認知行為改變的影響
3 討論
流行病學研究表明,長期微波輻射暴露可導致頭痛、腦電波異常、神經衰弱、記憶力減退和睡眠障礙等[2,5]。嚙齒類動物暴露于一定條件的電磁波輻射可造成其長時記憶、短時記憶和運動性記憶能力下降,并伴隨興奮和焦慮等神經行為的異常[6]。
海馬是參與學習和記憶功能的重要腦區,也是電磁波輻射的敏感靶部位之一[7]。本課題組前期采用Morris水迷宮和穿梭箱行為學試驗發現,2.856 GHz、8 mW/cm2、15 min的微波輻射可引起小鼠空間參考記憶能力和聯合型學習記憶能力下降,同時導致海馬CA3區組織病理學改變[8]。本試驗在前期工作基礎上,進一步分析了微波輻射后海馬CA1、CA2、CA3和DG區的組織形態結構變化,發現CA3區病變最為明顯,表明海馬CA3區對微波輻射較為敏感。Wang等[9]分別利用1.5 GHz、5 mW/cm2,1.5 GHz、30 mW/cm2和1.5 GHz、50 mW/cm2微波輻射大鼠6 min,以及Hasan等[10]通過2 400 MHz、738 μW/cm2射頻電磁輻射暴露小鼠40 min,均發現海馬神經元固縮深染,血管周隙增寬,與本試驗中海馬病理形態學改變特點基本一致。
ACh是中樞膽堿能系統的重要神經遞質,ACh及其受體的表達調控與認知功能密切相關[3]。AChRs可分為毒蕈堿型乙酰膽堿受體(Muscarinic acetylcholine receptors,mAChRs,主要包括M1~M5五個亞型)和煙堿型乙酰膽堿受體(Nicotinic acetylcholine receptors,nAChRs,主要包括α4、α7、β2和α4β2型)[11]。研究表明,mAChRs通過偶聯G蛋白進行信號轉導,nAChRs通過調節神經突觸膜上Ca2+通道通透性而激活蛋白激酶C(Protein kinase C,PKC)信號通路,并調節Ca2+依賴的蛋白激酶Ⅱ而發揮作用[12-13]。關于微波輻射對海馬中AChRs的影響尚不明確。Kumar等[14]采用2.45 GHz、0.029 mW/cm2微波輻射小鼠1個月(2 h/d),發現輻射組小鼠海馬M1-AChR上調且AChE活性增加;Hassanshahi等[15]采用2.45 GHz、23.6 dBm微波輻射大鼠1個月(12 h/d),海馬mAChRs表達升高,AChE活性及其胞內Ca2+濃度升高。本課題組前期研究發現,大鼠經2.856 GHz、8 mW/cm2、15 min微波輻射后6 h,其海馬中僅α4型AChR mRNA相對表達量顯著上調,其余AChRs mRNA相對表達量均未見明顯變化;微波輻射后7 d,大鼠海馬M1、M3和β2型AChR mRNA相對表達量顯著下調,α7型AChR mRNA相對表達量顯著上調[16]。以上研究表明,一定條件的微波輻射可引起腦內ACh合成和代謝紊亂,造成AChRs表達失調。
本試驗在前期工作基礎上進一步利用微波輻射小鼠模型,確證了微波輻射后7 d,海馬M1和M3型AChR mRNA相對表達量顯著下調,M2、M4、α4和α7型AChR mRNA相對表達量均顯著上調,進一步提示微波輻射可引起海馬AChRs亞基構成比發生變化,且不同亞型AChRs對微波輻射的敏感程度存在差異,其中,微波輻射可引起海馬M1、M2、M3、M4、α4和α7型AChR基因表達異常,而對M5和β2型AChR基因表達影響不明顯。
研究表明,M1-AChR占mAChRs的50%~60%,其主要在海馬中表達[17]。M1-AChR可通過促進谷氨酸和γ-氨基丁酸神經傳遞而改善學習記憶[18-20]。此外,M1-AChR基因敲除小鼠在長時程增強中表現出認知缺陷[21-22]。目前,M1-AChR已成為治療阿爾茲海默和老年癡呆癥等中樞神經系統疾病的潛在靶點[23-24]。以上研究提示,M1-AChR對學習和記憶功能具有正向調控作用。因此,可推測海馬M1-AChR mRNA相對表達量下調可能在微波輻射致認知行為改變中發揮重要作用。本試驗通過對微波輻射小鼠腹腔注射M1-AChR特異性激動劑,并結合行為學評估其對認知功能的影響,結果發現,微波輻射可導致小鼠新物體探究和識別記憶功能障礙,而M1-AChR激活可有效改善微波輻射所致小鼠新物體識別記憶受損,表明M1-AChR對于微波輻射所致認知功能障礙具有重要調控作用。
綜上所述,本試驗發現,微波輻射可引起海馬AChRs亞基構成比變化和CA3區組織病理學改變,M1-AChR mRNA相對表達量于輻射后顯著下調,并在微波輻射所致認知行為功能下降中發揮重要調控作用,進一步揭示了微波輻射致海馬結構和功能損傷的分子機制,同時為其藥物研發和醫學防護提供了理論依據和試驗參考。

