2023年諾貝爾生理學或醫學獎與mRNA疫苗的研發和利用
張俊先 張凱程
[摘 要]2023年諾貝爾生理學或醫學獎授予卡塔林·卡里科和德魯·魏斯曼以表彰他們在核苷堿基修飾方面的發現,這一發現使得開發出針對COVID-19的有效mRNA疫苗成為可能。mRNA疫苗的研發和利用是全球的熱點。文章從與2023年諾貝爾生理學或醫學獎相關的內容,mRNA疫苗的研發歷程、技術原理、作用機制及制備過程,mRNA疫苗的臨床應用,mRNA疫苗的發展前景等方面為中小學生科普mRNA疫苗的相關知識。
[關鍵詞]諾貝爾生理學或醫學獎;mRNA疫苗;研發
[中圖分類號]? ? G633.91? ? ? ? [文獻標識碼]? ? A? ? ? ? [文章編號]? ? 1674-6058(2024)05-0095-04
2023年10月2日,瑞典斯德哥爾摩卡羅林斯卡學院的諾貝爾大會宣布,將諾貝爾生理學或醫學獎項授予匈牙利裔美國科學家卡塔林·卡里科(Katalin Karikó)和美國科學家德魯·魏斯曼(Drew Weissman),以表彰他們在核苷堿基修飾方面的發現,這一發現為mRNA疫苗前所未有的開發速度作出了重要貢獻,使得開發出針對COVID-19的有效mRNA疫苗成為可能。本文從四個方面為中小學生科普mRNA疫苗的相關知識。
一、與2023年諾貝爾生理學或醫學獎相關的內容
(一)mRNA相關知識
mRNA即信使RNA,mRNA作為蛋白質合成的模板,其大小在幾百個核苷酸至數千個核苷酸之間,一般不穩定,壽命較短。mRNA數占細胞總RNA數的1%~5%。
mRNA在成熟過程中會發生RNA編輯,RNA編輯是指通過化學修飾或堿基轉化使mRNA的堿基序列發生改變,從而導致遺傳信息發生改變。
RNA病毒感染人體時,RNA正鏈翻譯出所需的蛋白質,RNA正鏈又在RNA復制酶的作用下復制成雙鏈RNA,雙鏈RNA解旋釋放出正鏈RNA,繼續翻譯蛋白質,負鏈RNA則作為RNA復制的模板。
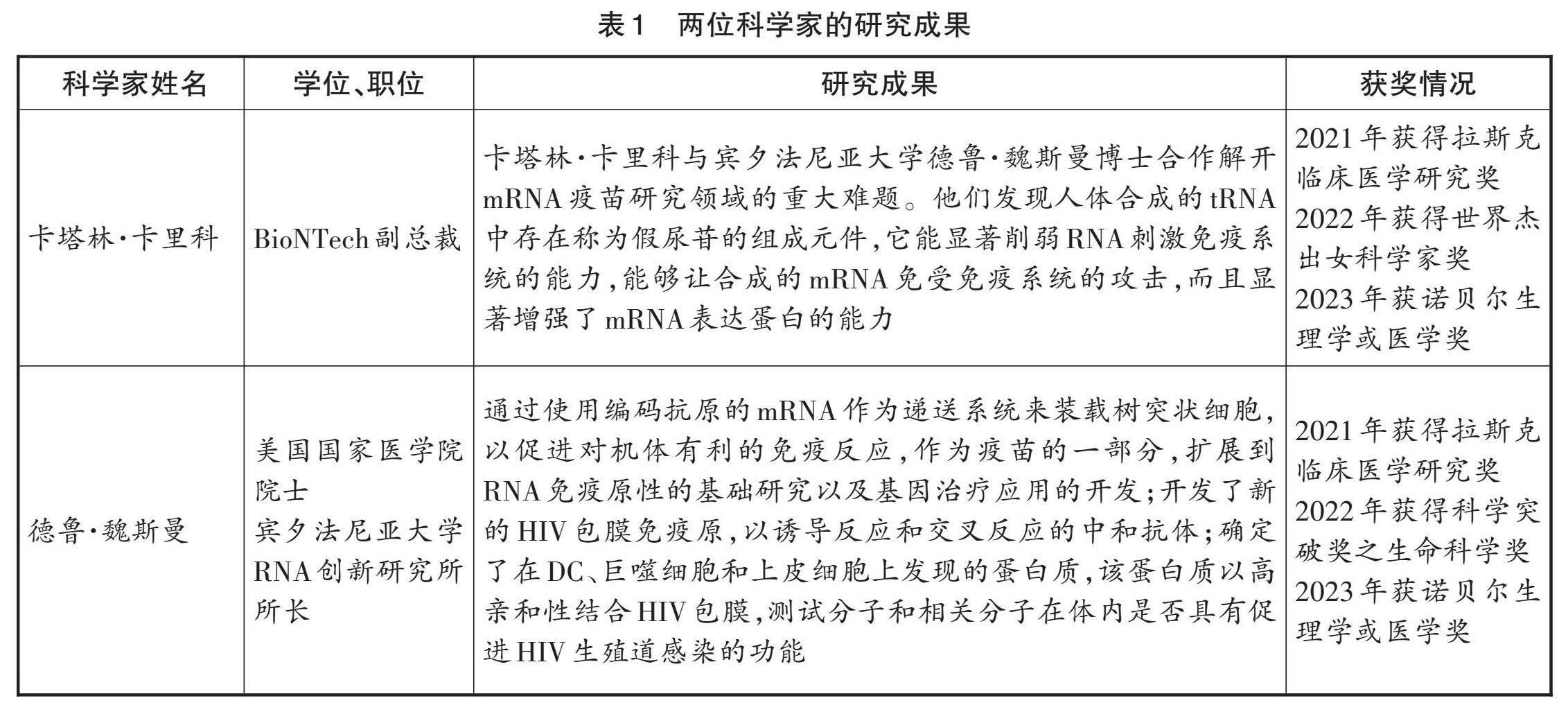
(二)兩位科學家的研究成果
卡塔林·卡里科和德魯·魏斯曼兩位科學家的研究成果如表1所示。
(三)疫苗知識
滅活疫苗:選免疫應答能力強的病菌首先進行人工培養,再用物理或者化學方法將其殺滅制成疫苗,這類疫苗是死疫苗。
減毒活疫苗:病原體經過甲醛處理后,毒性亞單位的結構改變,毒性減弱,但結合亞單位的活性保持不變,即保持了抗原性。這種疫苗接種后會在體內生長繁殖,接近自然感染,激發的免疫時間長。
類毒素疫苗:有些病原微生物自身所產生的致病作用并不是它本身,而是由它產生的外毒素在起作用,外毒素是一種特殊蛋白質,也具有抗原性。類毒素在人體內刺激可以產生更高濃度的抗體,免疫效果較好。
mRNA疫苗:mRNA疫苗是繼傳統疫苗和新型疫苗之后的第三代疫苗。mRNA疫苗分為病毒衍生的自我擴增型和非復制型兩種。自我擴增型mRNA疫苗不僅可以編碼目標抗原,還可以編碼病毒的復制機制。這樣相對低劑量的這類疫苗可以產生高水平的抗原表達。非復制型mRNA疫苗只含有體外轉錄好的編碼抗原蛋白的mRNA,且這種合成的mRNA在人體內無法自我復制,其結構簡單,體積小,對插入目標抗原轉錄本的大小限制更少。由于mRNA進入人體內不插入宿主的基因組,因此這種疫苗具有較強的安全性。
mRNA疫苗的特有優勢是:①mRNA只在細胞質內表達抗原,并不進入細胞核;②mRNA沒有感染性,也容易被降解,沒有感染風險;③mRNA能表達出特定的靶蛋白,修飾或優化使其穩定性和翻譯效率提高;④mRNA的設計和合成方法簡單方便,容易開展工廠化生產。
二、mRNA疫苗的研發歷程、技術原理、作用機制及制備過程
(一)mRNA疫苗的研發歷程
1961年,雅各布、悉尼·布雷內和馬修·梅塞爾森通過實驗證實了mRNA的存在,mRNA被發現。
1978年,科學家用脂質體將 mRNA 轉運到小鼠和人類細胞中,以誘導蛋白質表達。
1984年,分子生物學家湯姆·馬尼亞蒂斯 (Tom Maniatis) 和邁克爾·格林 (Michael Green)等人用RNA合成酶和其他材料,人工合成了具有活性的mRNA。
1987年,梅爾頓發現mRNA能激活或抑制蛋白質的表達;1987年底,羅伯特·馬龍(Robert Malone)將mRNA鏈與脂肪滴混合,發現人體細胞能吸收mRNA并產生蛋白質。這是一項里程碑式的實驗。
1993年,開始針對流感病毒的mRNA疫苗在鼠身體上的測試。
1995年,開始針對癌癥的mRNA疫苗在鼠身體上的測試;1995年,卡塔林·卡里科誘導細胞產生了具有治療作用的蛋白質。
1997年,卡塔林·卡里科和德魯·魏斯曼開發了一種基于mRNA的 HIV/AIDS 疫苗,但將其注射到小鼠體內后,引發了大規模的炎癥。發現原因是:合成的mRNA會激活一系列Toll樣受體的免疫傳感器[1],它們會充當病原體的危險信號。隨后,兩人發現重新排列mRNA的一個核苷酸(尿苷)的化學鍵,并用天然的修飾堿基,即用假尿苷代替尿苷的mRNA堿基,可以大大減少炎癥反應,這樣,他們就發現了防止mRNA觸發破壞性免疫反應的方法,清除了mRNA疫苗在臨床應用上的關鍵障礙。
2013年,德國慕尼黑大學醫院醫學中心對狂犬病mRNA疫苗進行首次臨床試驗。
2015年,開始對流感的納米mRNA疫苗進行首次臨床試驗。
2017年,開始進行mRNA腫瘤疫苗應用于治療黑色素瘤患者的臨床試驗[2]。雖然mRNA疫苗已進入臨床試驗,但一直沒有正式投入臨床應用。
2020年,新冠疫情蔓延全球,危害人類生命。為此,美國食品藥品監督管理局通過了Moderna和BioNTech兩家公司的新冠mRNA疫苗授權,并開始疫苗接種,這使得mRNA疫苗在研發和應用方面進展加快,對拯救人類生命起了很大的作用。
(二)mRNA疫苗的技術原理、作用機制及制備過程
1. mRNA疫苗的修飾技術
mRNA疫苗是一種外源核酸,進入人體內容易被識別和降解。保證mRNA疫苗的穩定性和免疫活性的方法為采用修飾技術,主要包括:①通過引入抗反轉帽子的類似物,能提高mRNA的翻譯效率,在抗反轉帽子的類似物的基礎上修飾Cap結構,能提高mRNA的穩定性,防止核酸外切酶對其降解;②修飾Poly(A)尾巴的長度(保持在100至120個核苷酸),可以調控mRNA的穩定性和翻譯效率;③5′UTR的長度和結構對翻譯起始有重要影響,3'UTR區域引入Kozak序列能加強起始密碼子的識別, 在5′UTR和3'UTR區域內引入穩定元件增加可調控序列,讓mRNA更容易翻譯,避免錯誤啟動,能顯著提高mRNA的穩定性;④優化mRNA序列,修飾核酸,減少固有免疫激活,提高翻譯效率;⑤在mRNA開放閱讀框(ORF)中,用常用密碼子去代替不常用密碼子,可以提高mRNA的穩定性和翻譯效率[3]。
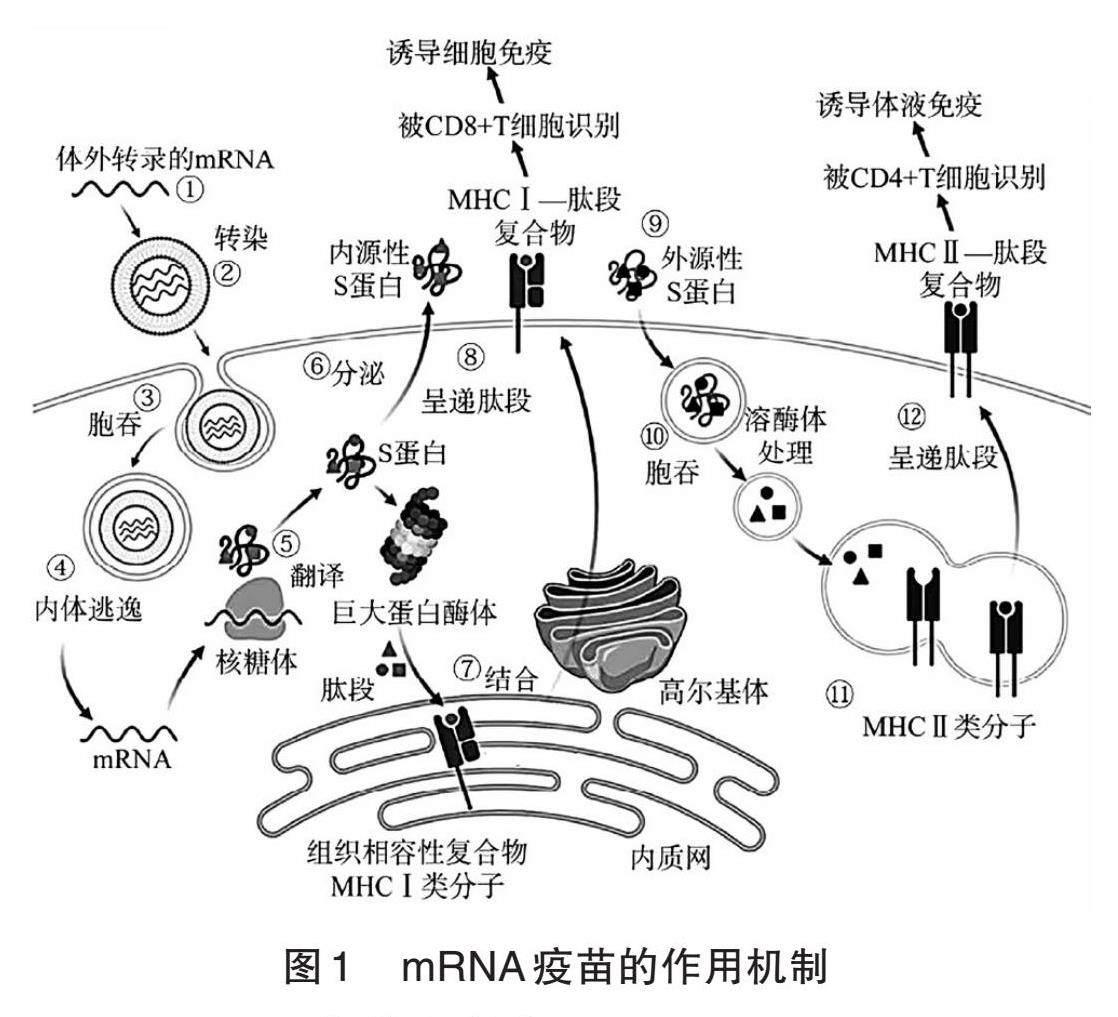
2. mRNA疫苗的作用機制
mRNA疫苗發揮作用一般需要經過以下步驟:一是mRNA被各種載體包裹;二是通過注射進入人體;三是包裹mRNA的脂質體通過胞吞進入細胞內;四是mRNA在細胞內釋放后利用人體細胞器翻譯并表達抗原蛋白,刺激人體產生相應免疫反應。如圖1所示是mRNA疫苗的作用機制圖。
3. mRNA疫苗的制備過程
第一步,從冷庫中提取病毒的DNA。
第二步,將大腸桿菌以及質粒的細胞裝在實驗瓶中并促使細胞生長繁殖。
第三步,將生長繁殖了一晚的細菌轉移至一個含300升營養液的容器里,發酵混合物。
第四步,將發酵四天后的細菌用一種化學物質來分解細菌的細胞壁,采集并凈化DNA。
第五步,將提取出來的質粒進行質量檢測,以確認剛剛生產的質粒病毒基因序列并沒有出現變異。
第六步,把病毒基因從環狀切割成直線段,即把環狀質粒切割開來。
第七步,將已經很純的混合物進行凈化,用于濾出任何殘留的細菌或質粒片段,凈化DNA。
第八步,將每瓶DNA冷凍、裝袋、密封,放入一個裝有足夠干冰的容器里進行運輸。
第九步,解凍DNA,并摻入由mRNA組成的部分,一段時間后,酵素將DNA模板轉化為mRNA,即進行DNA到mRNA的轉變。
第十步,需要反復測試過濾后的mRNA,以確保其精確度以及基因序列的準確性,即mRNA檢測。
第十一步,將mRNA在-20 ℃下冷藏、打包和再次運輸。
第十二步,準備mRNA,收到mRNA的包裹后,保持冷凍直到需要用時。
第十三步,準備脂質,這種物質能保護mRNA進入人體細胞時不會被破壞。
第十四步,制作mRNA疫苗,當脂質和mRNA 片段相遇時,電極以毫微秒的速度將它們聚集起來,mRNA 片段被納米脂肪粒包裹起來形成一個疫苗顆粒。
第十五步,準備疫苗瓶,并清洗和高溫消毒。
第十六步,罐裝疫苗。將0.45毫升疫苗注射到一個瓶子,稀釋后,成為6個劑量的疫苗。
第十七步,打包、冷藏和測試。灌注完的疫苗經過檢查貼上標簽,然后放進盒子里打包,盒子要在-70 ℃的極冷溫度下冷凍數天,同時送檢該批次的疫苗。
第十八步,打包和運輸成品疫苗。給測試合格的疫苗裝上溫度計,并放45磅的干冰。
這樣,mRNA疫苗就制備好了,下一步就是接種疫苗了。
三、mRNA疫苗的臨床應用
mRNA疫苗技術的落地,是人類文明史上的又一次“盜火”。目前,mRNA疫苗制備技術不斷更新,多種mRNA疫苗研發速度快,并在臨床研究和臨床應用上取得了較好的結果。
目前,全球范圍內布局mRNA疫苗的三巨頭分別是德國的BioNTech和CureVac、美國的Moderna。我國布局該領域的主要有艾博生物、珠海麗凡達、斯微生物、深信生物、藍鵲生物、美諾恒康、瑞吉生物、海昶生物、厚存納米、嘉晨西海等企業,它們有的是中外合資企業,有的是海歸團隊創立的企業。
首個用于疾病預防的mRNA疫苗是流感疫苗,由于流感病毒容易發生變異,因此缺少有效的廣譜性疫苗。現在研發的mRNA疫苗對甲型流感具有明顯的預防保護作用。針對SARS-CoV-2引起的疫情,多個國家采用多種技術進行相關疫苗的研發。BNT162b2疫苗和mRNA-1273疫苗,臨床試驗效果較好;已開展了肺癌、胰腺癌、黑色素瘤等多種腫瘤樹突狀細胞疫苗的臨床試驗。另外,mRNA疫苗在抗細菌和寄生蟲感染方面也有應用。
四、mRNA疫苗的發展前景
mRNA疫苗是一種新型疫苗,它改變疫苗接種方式,為預防傳染病提供新的解決方案,并為人們提供一種更安全、更有效的疫苗接種方式。
mRNA疫苗在研發、生產等方面具備諸多優勢。一是研發周期短、抗原選擇范圍廣(廣泛應用于預防傳染病、抗腫瘤以及蛋白替代療法等領域);二是安全性高;三是有效性高且穩定;四是生產難度低、速度快且安全;五是能同時激活體液免疫和細胞免疫,效果顯著。
我國“十四五”醫藥工業規劃就提升mRNA疫苗供應能力及其質量技術水平提出了新的要求。由于RNA病毒大多數為單鏈,遺傳信息一般在一條鏈上,且RNA病毒具有快速變異特性,因此mRNA疫苗市場需求巨大。
據統計,2020年,全球mRNA藥物市場規模(不含新冠)約為39億美元,預計到2025年超過63億美元。加上新冠方面,按照投產和接種進度,將為全球mRNA藥物行業帶來超690億美元的市場規模增幅。
[? ?參? ?考? ?文? ?獻? ?]
[1]? 陳彥,孫英.mRNA疫苗研究進展:2021年拉斯克獎臨床醫學研究獎 [J].首都醫科大學學報,2021(5):893-899.
[2]? 生命科學前沿.mRNA疫苗制造的19個步驟:以新冠mRNA疫苗為例[EB/OL].(2023-10-24)[2023-12-23].https://mp.weixin.qq.com/s?__biz=MzAxNzEwNjY2MA==&mid=2651110758&idx=5&sn=1517448
eda8adf95adb83f5ab8322cbd&chksm=801a8eedb76d07fb8dc1c80565ea4a783d627f47e411d4c2663214eb6173b67002077c9b5f35&scene=27.
[3]? 未來智庫.醫藥行業專題研究報告:mRNA疫苗前景廣闊[EB/OL].(2022-02-21)[2023-12-23].https://zhuanlan.zhihu.com/p/470160697.
(責任編輯 黃春香)

