鉬、鎘聯合暴露介導氧化應激和鐵死亡致綿羊腎損傷
摘" 要: 旨在探究氧化應激及鐵死亡在鉬、鎘及其聯合暴露致綿羊腎組織損傷中的作用。以24只2月齡綿羊為試驗對象,隨機分為4組,即對照組(Control)、鉬組(Mo)、鎘組(Cd)和鉬鎘聯合組(Mo+Cd),對照組灌服等體積蒸餾水,Mo組灌服45 mg·kg-1 BW的Mo,Cd組灌服1 mg·kg-1 BW的Cd,Mo+Cd組灌服1 mg·kg-1 BW Cd+45 mg·kg-1 BW Mo。正試期為75 d。試驗結束,取綿羊血清和腎組織,觀察綿羊腎組織病理及超微病理學變化,并檢測血清腎功能指標、腎組織氧化應激和鐵死亡相關因子水平。結果顯示,鉬、鎘及其聯合暴露提高了血清腎功能指標(肌酐、尿素和尿酸)水平。Mo組、Cd組和Mo+Cd組中腎小管上皮細胞變性腫脹、結構模糊和溶解,在細胞質中有微小的紅色顆粒和空泡,表現出顆粒變性、空泡變性和壞死。此外,腎小管管腔內有粉紅色著染的絲縷樣成分,部分腎小球及間質內紅細胞數量增多。透射電鏡結果顯示,鉬、鎘及其聯合暴露導致腎小管上皮細胞中線粒體體積變小且出現嵴模糊和空泡化。Mo組和Cd組中氧化損傷相關因子(H2O2、MDA)及Fe離子含量,鐵死亡相關因子(NCOA4、ACSL4、TFR1和PTGS2)mRNA表達水平及PTGS2蛋白表達水平升高;抗氧化相關因子(GSH、CAT和GSH-Px)水平,鐵死亡相關因子(SLC7A11、GPX4和FTH1)mRNA及蛋白表達水平降低,且上述變化在Mo+Cd組中更為明顯。皮爾森相關性分析表明,氧化損傷相關因子(H2O2、MDA)和Fe離子水平與鐵死亡相關因子(NCOA4、ACSL4、TFR1和PTGS2)表達水平呈正相關,與鐵死亡相關因子(SLC7A11、GPX4和FTH1)表達水平呈負相關;抗氧化相關因子(GSH、CAT和GSH-Px)水平和鐵死亡相關因子(NCOA4、ACSL4、TFR1和PTGS2)表達水平呈負相關,而與鐵死亡相關因子(SLC7A11、GPX4和FTH1)表達水平呈正相關。本研究表明,鉬鎘及其聯合暴露誘發綿羊腎氧化應激和鐵死亡致腎組織損傷,且鉬鎘毒性具有協同效應。
關鍵詞: 羊;鉬;鎘;氧化應激;鐵死亡
中圖分類號:S856.9
文獻標志碼:A
文章編號:0366-6964(2024)12-5802-11
doi: 10.11843/j.issn.0366-6964.2024.12.042
開放科學(資源服務)標識碼(OSID):
收稿日期:2024-01-02
基金項目:江西省現代農業產業技術牛羊體系疫病防控崗(JXRS-13)
作者簡介:熊志偉(1997-),男,江西南昌人,博士生,主要從事臨床獸醫學研究,E-mail:13698091664@163.com
*通信作者:胡愛明,主要從事畜牧獸醫研究,E-mail:15807969386@163.com
Molybdenum and Cadmium Combined Exposure Mediates Oxidative Stress and Ferroptosis Induced Kidney Damage in Sheep
XIONG" Zhiwei1,2, WANG" Yun2, CAO" Huabin1, PENG" Chengcheng3, YANG" Fan1, DAI" Xueyan1, XING" Chenghong1, LIU" Lingli1, LI" Jingni1, HU" Aiming4*
(1.Jiangxi Key Laboratory of Animal Disease Diagnosis and Control, College of Animal Science and
Technology, Jiangxi Agricultural University, Nanchang 330045," China;
2.Jiangxi Vocational College of Biotechnology, Nanchang 330100," China;
3.Department of Pharmacy, Faculty of Medicine, Guangxi
University of Science and Technology, Liuzhou 545005," China;
4.Ji’an Agricultural and Rural Industry Development Service Center, Ji’an 343000," China)
Abstract:" The aim of this study was to investigate the role of oxidative stress and ferroptosis in renal tissue injury caused by molybdenum, cadmium and their combined exposure in sheep. Twenty-four sheep aged 2 months were randomly divided into 4 groups, namely control group (Control), molybdenum group (Mo), cadmium group (Cd) and molybdenum cadmium combined group (Mo+Cd). The control group was given equal volume of distilled water, the Mo group was given 45 mg Mo·kg-1BW, group Cd was given 1 mg Cd·kg-1BW, and group Mo+Cd was given 1 mg Cd+45 mg Mo·kg-1BW. The experimental period lasted for 75 d. At the end of the experiment, serum and kidney tissue were collected, pathological and ultrapathological changes of sheep kidney were observed, and the levels of serum renal function indexes, renal tissue oxidative stress and ferroptosis related factors were detected. The results showed that molybdenum, cadmium and their combined exposure increased the levels of serum renal function indicators (creatinine, urea and uric acid). In the Mo, Cd, and Mo+Cd groups, the renal tubular epithelial cells underwent degeneration, manifesting as swelling, structural blurring, and lysis. The cytoplasm contained minute red granules and vacuoles, indicating granular degeneration, vacuolar degeneration, and necrosis. Additionally, the renal tubular lumens were observed to contain pink-stained filamentous components, while the number of red blood cells was elevated in some glomeruli and interstitial spaces. The results of transmission electron microscopy showed that molybdenum, cadmium and their combined exposure resulted in the reduction of mitochondrial volume, blurring of ridge and vacuolation in renal tubular epithelial cells. The contents of oxidative damage related factors (H2O2, MDA) and Fe ions, the mRNA expression levels of ferroptosis related factors (NCOA4, ACSL4, TFR1 and PTGS2) and the protein expression levels of PTGS2 were increased in Mo and Cd groups. The mRNA and protein expression levels of antioxidant related factors (GSH, CAT and GSH-Px) and ferroptosis related factors (SLC7A11, GPX4 and FTH1) were decreased, and the above changes were more obvious in Mo+Cd group. Pearson correlation analysis showed that the levels of oxidative damage related factors (H2O2, MDA) and Fe ions were positively correlated with the expression levels of ferroptosis related factors (NCOA4, ACSL4, TFR1 and PTGS2), and negatively correlated with the expression levels of ferroptosis related factors (SLC7A11, GPX4 and FTH1). The correlation of antioxidant related factors (GSH, CAT and GSH-Px) and ferroptosis related factors was opposite to that of oxidative damage related factors. This study shows that molybdenum cadmium and its combined exposure induced renal oxidative stress and ferroptosis in sheep, resulting in renal tissue damage, and molybdenum, cadmium toxicity has a synergistic effect.
Key words: sheep; molybdenum; cadmium; oxidative stress; ferroptosis
*Corresponding author:" HU Aiming, E-mail:15807969386@163.com
鉬作為機體必需微量元素,廣泛存在于植物、動物和人體中,具有促進生長發育的作用,但攝入過量會引發毒性損傷[1]。鎘是一種在生物體內具有器官毒性和較長的生物半衰期的微量元素[2]。隨著工業化進程的推進,化石的燃燒、金屬礦產的冶煉以及污、廢水的排放,使得大量重金屬遷移到自然界中,并通過食物鏈富集到動物機體中。研究表明,低劑量的鎘能夠引發機體氧化應激并觸發NF-κB介導的NLRP3炎性小體活化致肝毒性[3],而高劑量的鉬可通過線粒體途徑誘導鴨腎小管上皮細胞氧化應激和凋亡[4]。重金屬污染的形式是復雜多樣的,在自然界中重金屬復合污染較單一污染現象更為普遍,通常具有伴生性和綜合性[5]。前人研究表明,鉬、鎘具有協同毒性,并能夠引發鴨腎小管上皮細胞氧化應激致細胞焦亡[6]。在江西贛南地區,鉬、鎘是引起畜禽中毒最重要的環境污染物,而與單胃動物相比,反芻動物由于放牧式飼養管理、生產周期長及瘤胃微生物的轉化作用,對環境中的重金屬毒性更為敏感[7],但其毒性作用機制有待進一步探究。
氧化應激是指機體受到有害刺激時,體內產生過多的活性氧自由基,導致氧化與抗氧化作用失衡的一種狀態。氧化應激與機體損傷具有密切的關聯,過多的氧自由基可以引起細胞和組織的氧化損傷,從而導致多種疾病的發生與發展。重金屬毒性常能引發機體氧化應激,并伴隨自噬、焦亡和壞死等細胞損傷[8]。本課題組前期研究表明,鉬、鎘共處理能夠引發綿羊腎氧化應激和線粒體質量控制紊亂[9]。與此同時,鐵死亡作為一種獨特的細胞死亡方式,其主要特征是細胞內鐵離子的異常積聚[10]。這種積聚促使細胞內產生過量的氧自由基,進而引發細胞的氧化應激反應,最終導致細胞死亡。研究表明,鎘能夠引起小鼠肝氧化應激和自噬進而誘發鐵死亡[11]。然而,鉬、鎘的協同毒性在反芻動物體內致氧化應激對鐵死亡的影響值得進一步探究。因此,本研究以綿羊為試驗對象,通過檢測綿羊腎功能血清生化相關指標、腎組織病理學和超微病理學變化、氧化應激和鐵死亡相關因子水平變化,探究鉬、鎘及其聯合暴露造成綿羊腎損傷的毒性作用機制。
1" 材料與方法
1.1" 試驗材料
鉬酸銨[(NH4)6Mo7O24·4H2O]和氯化鎘(CdCl2)購自西隴科學股份有限公司。血清肌酐(creatinine,CREA)、尿素(UREA)和尿酸(uric acid,UA)生化檢測試劑盒購自美康生物科技股份有限公司;過氧化氫(H2O2)、過氧化氫酶(catalase,CAT)、丙二醛(malondialdehyde,MDA)、谷胱甘肽(glutathione,GSH)和谷胱甘肽過氧化物酶(glutathione peroxidase,GSH-Px)試劑盒購自南京建成生物工程有限公司;總鐵離子比色法測試盒購自武漢伊萊瑞特生物科技有限公司;TRIzol試劑購于南京諾唯贊生物科技有限公司;反轉錄試劑盒購自北京全式金生物技術有限公司;PTGS2、SLC7A11、GPX4和GAPDH抗體購自艾比瑪特醫藥科技有限公司,FTH1抗體購自杭州華安生物技術有限公司。
1.2" 動物處理
本試驗在江西農業大學實驗羊場進行,并遵循倫理道德準則,由江西農業大學動物管理與倫理委員會批準(No. JXAULL-2023-06-05)。選用24只2月齡綿羊,根據公母對半原則,將綿羊隨機分為4組:對照組(Control組),鉬組(Mo組),鎘組(Cd組)和鉬鎘聯合組(Mo+Cd組)。試驗期間,將配制好的鉬酸銨[(NH4)6Mo7O24·4H2O]或氯化鎘(CdCl2)按綿羊體重(BW)使用一次性胃管導服。根據課題組前期研究確定試驗動物攻毒劑量[12],鉬組染毒劑量為:45 mg·kg-1 BW(以Mo元素計),鎘組染毒劑量為:1 mg·kg-1 BW (以Cd元素計),鉬、鎘聯合組接毒劑量為:45 mg·kg-1 BW Mo+1 mg·kg-1 BW Cd,對照組給予相應劑量蒸餾水,連續灌服75天。在試驗第75 d,取血清樣品于-80℃保存備用,并在肌肉注射過量的戊巴比妥進行麻醉后,采集腎組織樣品進行后續檢測。
1.3" 腎功能指標測定
使用全自動生化分析儀(日立7600)配合對應試劑盒,測定血清中CREA、UREA和UA含量。
1.4" 組織病理切片觀察
參考陳亞杰等[13]的方法進行石蠟切片制作。將綿羊腎組織置于4%多聚甲醛溶液中固定24 h,并經乙醇梯度脫水處理后溶于透明劑(二甲苯)中透明。將已透明的組織塊置于溶化的石蠟中,放入溶蠟箱中保溫,待石蠟完全浸入組織塊后進行包埋。隨后,使用切片機進行切片并在37℃溫度下烘片過夜。蘇木精-伊紅(hematoxylin-eosin,HE)染色后,在光學顯微鏡下觀察并拍照。
1.5" 超微結構觀察
各組取1 mm3的腎組織置于2.5%戊二醛溶液中固定,隨后將組織片置于1%四氧化鋨固定劑中,并用乙醇進行梯度脫水處理。將脫水后的組織包埋在環氧樹脂中,固定后進行染色。最后,在透射電子顯微鏡下觀察腎組織超微結構變化。
1.6" 氧化應激指標測定
參考陳敬宜等[14]的方法,稱取一定質量的腎組織,按質量(g)∶體積(mL)=1∶9的比例,加入相應量的生理鹽水并進行勻漿處理。H2O2、CAT、MDA、GSH和GSH-Px指標水平通過使用商品化試劑盒進行測定,步驟嚴格參照試劑盒說明書,最終使用酶標儀對各孔測定OD值進行讀數。
1.7" 鐵離子水平測定
總鐵離子比色法測試試劑盒用于檢測綿羊腎組織中鐵離子水平,試驗方法根據總鐵離子比色法測試試劑盒說明書進行。將一定量的腎組織按質量(g)∶體積(mL)=1∶9的比例加入生理鹽水,通過組織勻漿處理制成10%腎組織勻漿液,12 000×g離心10 min,取上清液備用。300 μL不同濃度的標準品和樣本分別加入對應的1.5 mL離心管中,隨后加入相應試劑,混合均勻,37℃孵育40 min。將各管以12 000×g離心10 min,并取300 μL上清液加入酶標板對應孔中,在酶標儀593 nm處測定各孔OD值。最后,通過公式計算相應樣品中總鐵離子含量水平。
1.8" 實時熒光定量聚合酶鏈式反應測定
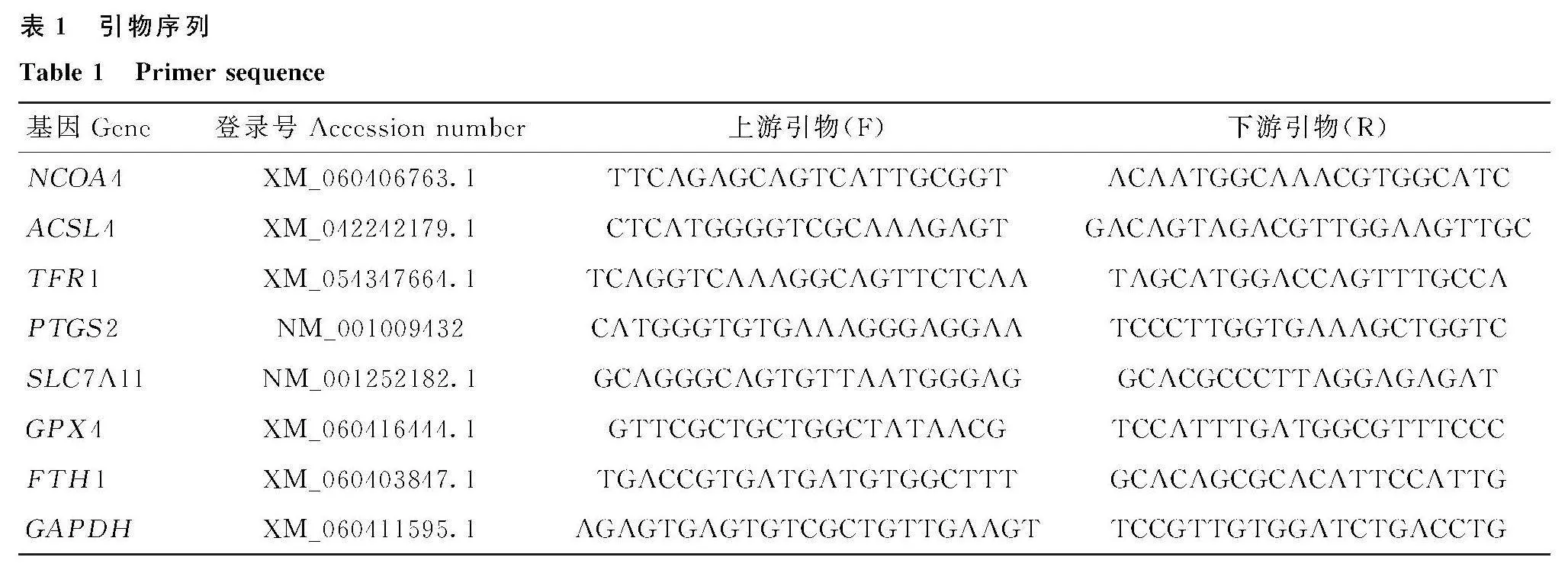
取約0.1 g綿羊腎組織置于1 mL TRIzol試劑中并進行勻漿處理,隨后通過TRIzol法對組織中的總RNA進行提取,再根據反轉錄試劑盒說明書,將RNA反轉錄為cDNA,并使用實時熒光定量PCR儀(QuantStudio7 Flex Real-Time PCR)對cDNA進行擴增反應。反應使用兩步法,反應條件為:預變性95℃ 30 s;95℃ 10 s、60℃ 30 s,循環40次。以GAPDH為內參基因,使用2-ΔΔCt法對結果進行分析。使用Primer 5.0設計NCOA4、ACSL4、TFFR1、PTGS2、SLC7A11、GPX4、FTH1和GAPDH基因的引物(表1)。
1.9" 蛋白免疫印跡分析
取0.1 g腎組織置于RIPA裂解緩沖液孵育10 min。隨后,使用BCA蛋白濃度測定試劑盒(索萊寶,中國)進行蛋白定量。將相同量的蛋白樣品加入6倍SDS-PAGE裝載緩沖液中,煮沸10 min。將蛋白通過SDS-PAGE分離后轉印到聚偏氟乙烯(PVDF)膜上后,使用5%脫脂乳對PVDF膜進行封閉2 h處理,以及4℃孵育相應一抗PTGS2(1∶1 000),GPX4(1∶1 000),SLC7A11(1∶2 000),FTH1(1∶1 000)和GAPDH(1∶1 000)過夜,室溫孵育二抗(1∶1 000)40 min,將PVDF膜置于成像儀上滴加顯影液成像。使用ImageJ軟件分析條帶的灰度值。
1.10" 數據分析
Excel 2022和SPSS 22.0軟件用于數據統計分析,使用GraphPad Prism 8.0軟件進行作圖。所有統計分析均通過單因素方差分析和最小顯著差異檢驗計算,用皮爾森相關系數檢驗變量之間的相關性。Plt;0.05作為顯著差異的標準。
2" 結" 果
2.1" 鉬鎘及其聯合暴露致綿羊腎組織損傷
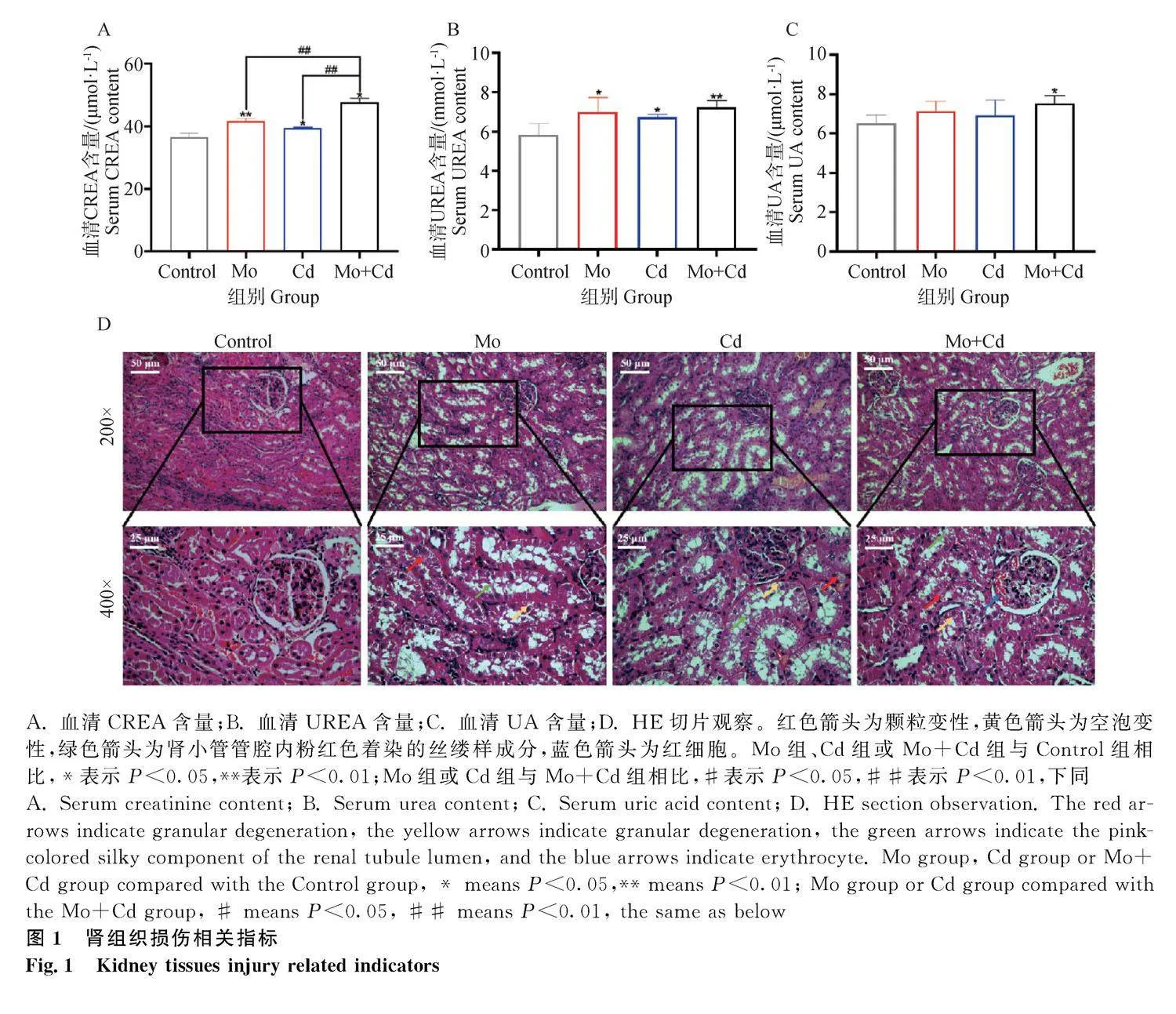
試驗第75天,綿羊血清生化腎功能指標如圖1A~1C所示。與Control組相比,Mo組和Cd組血清CREA和UREA水平均顯著升高(Plt;0.01或Plt;0.05)。Mo+Cd組血清CREA、UREA和UA水平顯著(Plt;0.01或Plt;0.05)高于Control組。Mo組和Cd組血清CREA水平顯著低于Mo+Cd組(Plt;0.05)。通過光學顯微鏡觀察75 d綿羊腎組織病理學變化,如圖1D所示。Control組腎組織病理學未見異常,腎小球及腎小管結構完整。Mo組、Cd組和Mo+Cd組,腎小管上皮細胞變性腫脹、結構模糊和溶解,在細胞質中有微小的紅色顆粒和空泡,表現出顆粒變性、空泡變性和壞死。此外,腎小管管腔內有粉紅色著染的絲縷樣成分,部分腎小球及間質內紅細胞數量增多。
2.2" 鉬鎘及其聯合暴露致綿羊腎氧化應激及鐵離子水平變化
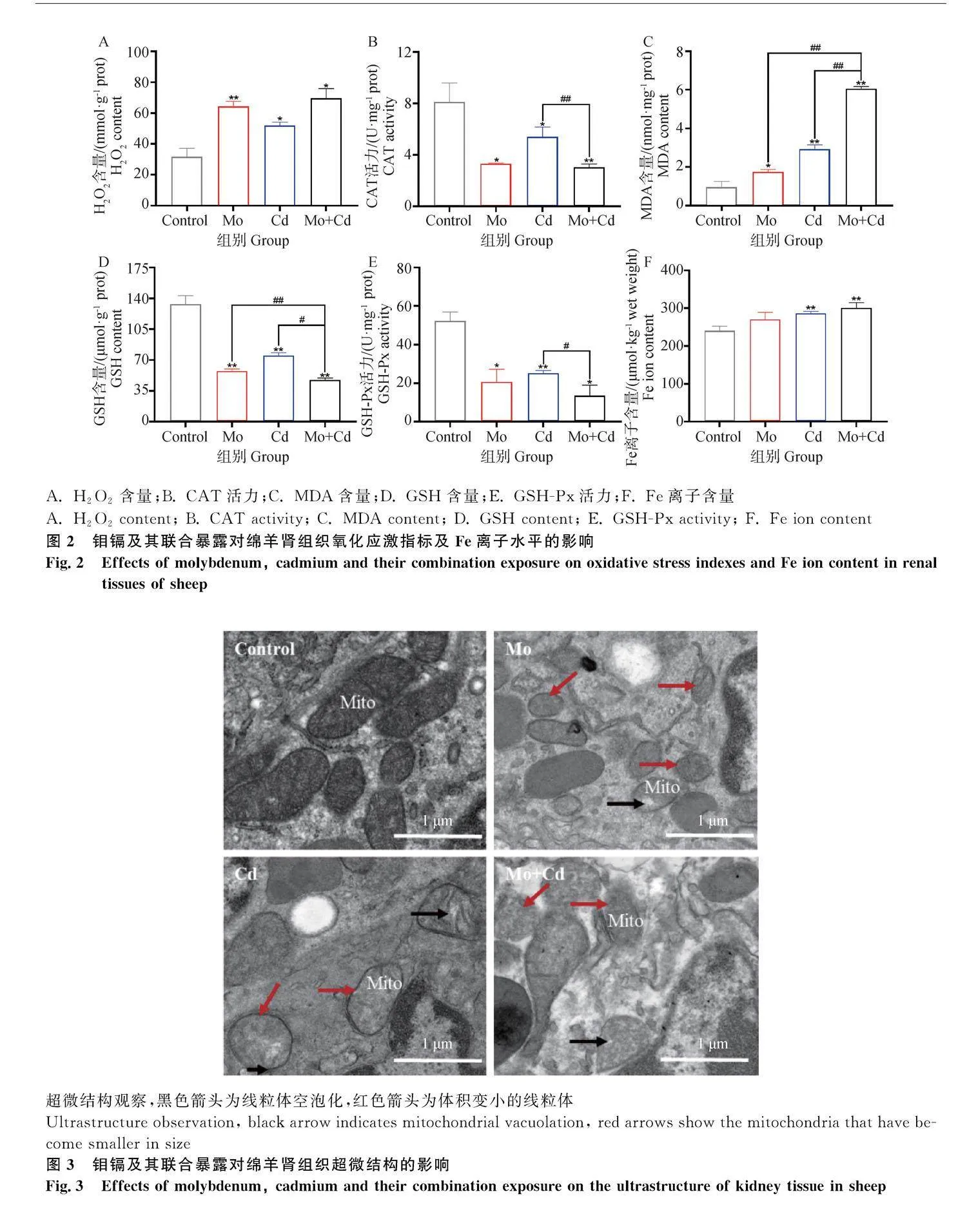
試驗第75天,綿羊腎氧化應激指標及鐵離子水平變化如圖2所示。與Control組相比,Cd組和Mo+Cd組中H2O2、MDA和Fe離子含量顯著升高(Plt;0.01或Plt;0.05);與單獨Mo組、Cd組相比,Mo+Cd組腎組織中H2O2和Fe離子含量上升但差異不顯著(P>0.05),而MDA含量顯著升高(Plt;0.01)。此外,鉬鎘及其聯合暴露顯著降低了CAT和GSH-Px活力、GSH含量(Plt;0.01或Plt;0.05),且與單獨Mo組、Cd組相比,Mo+Cd組GSH含量顯著降低(Plt;0.01或Plt;0.05)。與此同時,與Cd組相比,Mo+Cd組CAT和GSH-Px活力顯著降低(Plt;0.01或Plt;0.05)。
2.3" 鉬鎘及其聯合暴露誘導綿羊腎組織鐵死亡
通過透射電鏡觀察腎組織超微結構變化,結果如圖3所示。Control組超微結構觀察未見異常,線粒體結構完整,而Mo組、Cd組和Mo+Cd組線粒體體積變小且出現嵴模糊和空泡化。
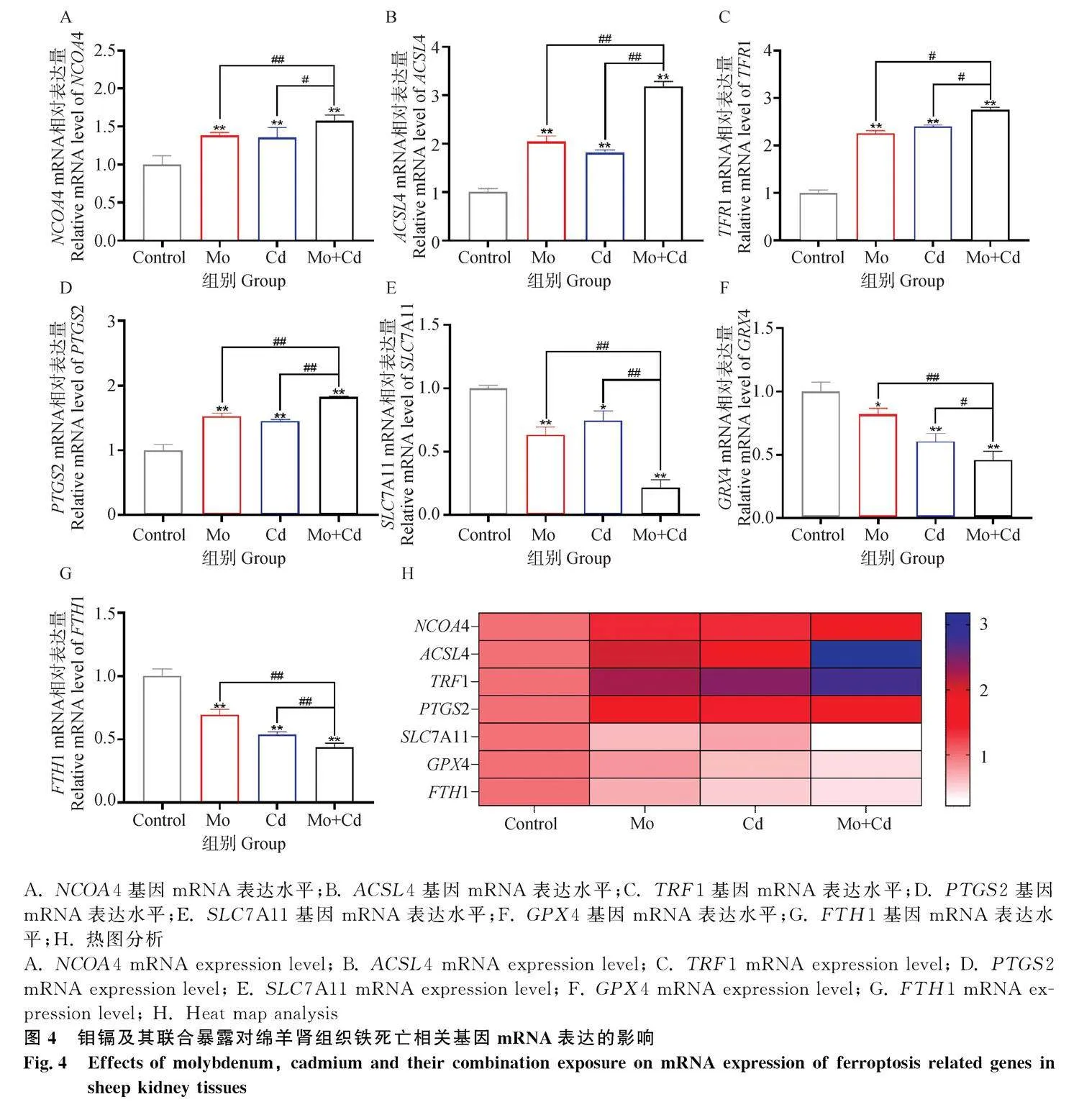
腎組織鐵死亡相關基因mRNA表達水平變化如圖4所示。與Control組相比,Mo組、Cd組和Mo+Cd組NCOA4、ACSL4、TFR1和PTGS2基因mRNA表達水平顯著升高(Plt;0.05),且NCOA4、ACSL4、TFR1和PTGS2基因mRNA表達水平在單獨Mo和Cd組中顯著低于Mo+Cd組(Plt;0.01或Plt;0.05)。此外,與Control組相比,Mo組、Cd組和Mo+Cd組SCL7A11、GPX4和FTH1基因mRNA表達水平顯著降低(Plt;0.01或Plt;0.05)。并且Mo+Cd組相比于單獨Mo組和Cd組,SCL7A11、GPX4和FTH1基因mRNA表達水平呈現顯著降低變化(Plt;0.01或Plt;0.05)。
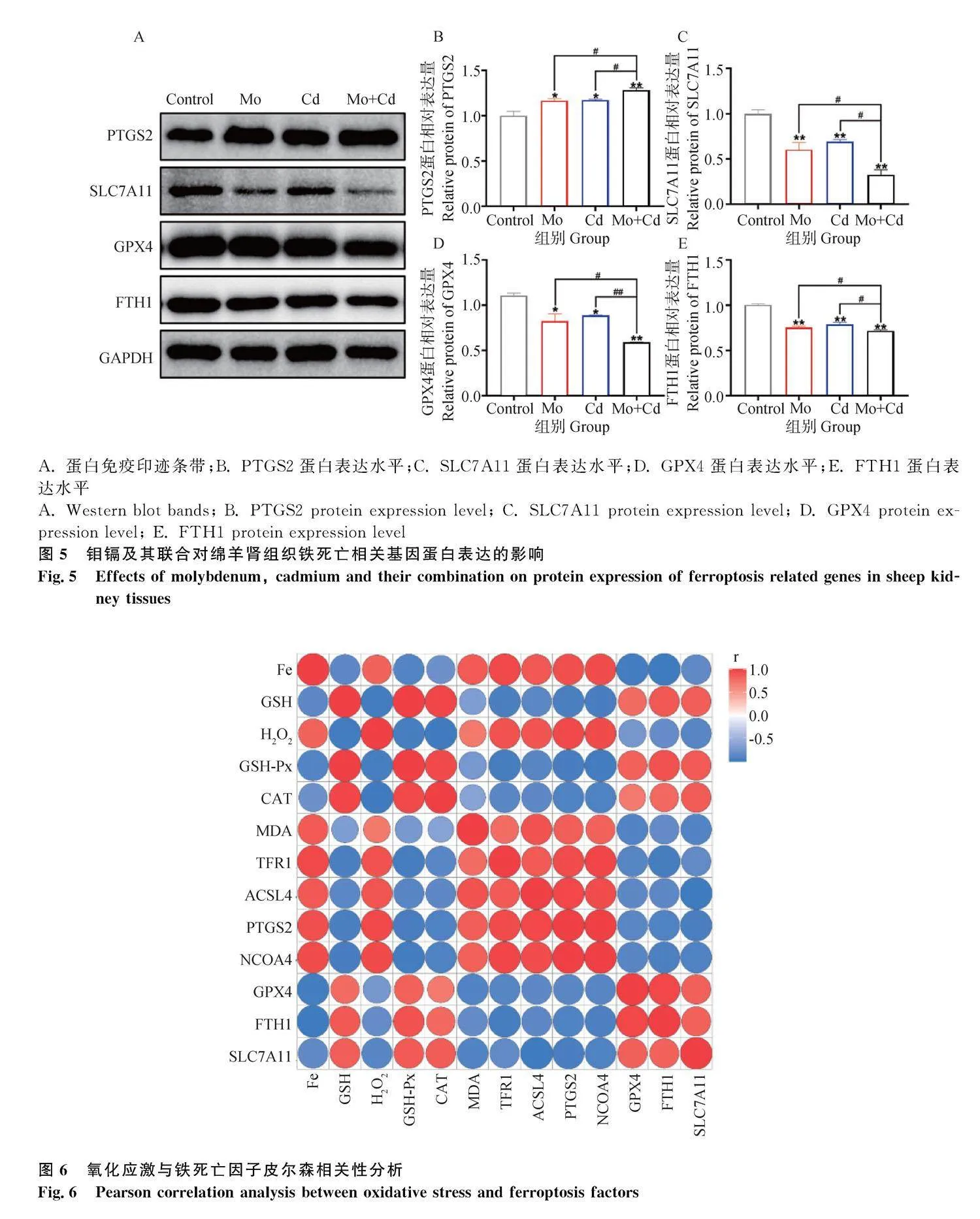
進一步檢測鐵死亡相關因子蛋白表達水平,結果如圖5所示。與Control組相比,Mo組、Cd組和Mo+Cd組PTGS2基因蛋白表達水平顯著升高(Plt;0.01或Plt;0.05),而SLC7A11、GPX4和FTH1基因蛋白表達水平降低(Plt;0.01或Plt;0.05)。與此同時,Mo+Cd組相較于單獨Mo組和Cd組,PTGS2蛋白表達水平顯著升高(Plt;0.05),而SLC7A11、GPX4和FTH1蛋白表達水平顯著降低(Plt;0.01或Plt;0.05)。
2.4" 氧化應激指標和鐵死亡指標變化相關性分析
氧化應激指標與鐵死亡指標變化相關性分析結果如圖6所示。氧化損傷相關指標(H2O2和MDA)和Fe離子含量與鐵死亡相關因子(NCOA4、ACSL4、TFR1和PTGS2)水平呈正相關,而與鐵死亡相關因子(GPX4、FTH1和SLC7A11)水平呈負相關。抗氧化相關指標(GSH、GSH-Px和CAT)與鐵死亡相關因子(NCOA4、ACSL4、TFR1和PTGS2)水平呈負相關,而與鐵死亡相關因子(GPX4、FTH1和SLC7A11)水平呈正相關。
3" 討" 論
鎘是一種廣泛存在于環境中的重金屬,長期攝入會對動物機體造成一定的損傷。鉬是一種微量營養素,過量攝入也會引起機體損傷。腎作為鉬、鎘毒性損傷的重要靶器官,常在鉬、鎘暴露下表現出較為明顯的病理變化。丁小麗等[15]的研究表明,低鎘暴露提高大鼠腎功能相關血清生化指標(CREA、UREA和UA),提示鎘暴露能夠引起大鼠腎功能損傷。宋超[16]的研究表明,過量的鉬攝入同樣能夠引發綿羊腎功能指標(CREA和UREA)升高,提示高鉬對綿羊腎臟造成損傷。與此同時,鉬、鎘聯合暴露毒性具有生物放大效應,與單獨鉬或鎘的暴露相比能進一步造成腎小管上皮細胞的損傷[17]。本研究結果顯示,鉬、鎘及其聯和暴露能夠引發綿羊腎功能血清生化相關指標(CREA、UREA和UA)水平升高,且與單獨鉬或鎘處理相比,鉬鎘聯合處理造成的腎功能指標提升更為明顯,表明鉬鎘及其聯合暴露能夠引發綿羊腎功能障礙。為進一步確認鉬鎘及其聯合暴露是否引發綿羊腎損傷,本研究通過對綿羊腎組織HE切片染色進行病理組織學觀察。前人研究表明,鎘暴露能夠導致腎小管上皮細胞變性、腫脹并出現顆粒變性和空泡變性以及腎小球充血[9,18]。本研究顯示,鉬鎘及其聯合暴露引發腎小管上皮細胞變性、腫脹、結構模糊和溶解,出現顆粒變性、空泡變性和壞死,且腎小管管腔內有粉紅色著染的絲縷樣成分,部分腎小球及間質內紅細胞數量增多,提示綿羊腎組織在鉬、鎘及其聯合暴露下出現組織損傷。
大量研究表明,腎組織損傷往往伴隨著氧化應激的出現[19-20]。氧化應激通過自由基反應鏈引發多種有害反應,如脂質過氧化、蛋白質氧化、核酸氧化等,能夠進一步加劇細胞損傷并影響細胞的正常生理功能。其中,H2O2、CAT、MDA、GSH、GSH-Px是評價氧化應激狀態的生物標志物。H2O2是氧化應激過程中常見的一種氧化劑,是細胞內氧化還原反應中產生的重要中間體,而CAT和GSH-Px能夠催化H2O2生成水和氧氣,進而緩解氧化應激的發生。MDA則是脂質過氧化的毒性代謝產物,其含量水平能夠反映氧化損傷程度。GSH-Px能夠特異性催化GSH與氧化物質反應,從而保護生物膜免受氧化物質的損害,維持細胞的正常功能。研究表明,鎘能夠促進H2O2和MDA含量水平的升高,且降低GSH含量及CAT和GSH-Px活力,從而誘發氧化應激[21-22]。本研究顯示,在單獨鉬或鎘及其聯合處理下,綿羊腎組織中H2O2和MDA含量升高,GSH含量降低以及CAT和GSH-Px活力下降,且鉬鎘共處理下指標變化更為顯著。因此,該結果揭示鉬、鎘及其聯合暴露能夠引起綿羊腎組織氧化應激。
氧化應激與鐵死亡的發生和發展在腎損傷中展現出緊密的聯系[23]。鐵死亡是一種鐵依賴性的,以細胞內脂質過氧化物堆積為典型特征的細胞死亡方式。鐵死亡參與了鎘誘導的腎小管上皮細胞死亡[24],且在氧化應激過程中,鐵離子的積累可通過芬頓反應和鐵依賴性酶產生大量的活性氧,導致氧化應激反應加劇,進而誘導鐵死亡的發生[25]。研究表明,鎘暴露以劑量依賴性方式引發腎小管上皮細胞鐵過載,并進一步誘發鐵死亡[24]。本研究顯示,鉬、鎘及其聯合暴露能夠引起綿羊腎組織總鐵離子含量水平升高,且鉬、鎘聯合暴露下更為明顯,提示鉬、鎘及其聯合暴露能夠引發綿羊腎組織鐵過載,并可能誘發鐵死亡。前人研究表明,線粒體體積變小、嵴模糊和空泡化是細胞鐵死亡的生物標志[26]。本研究顯示,鉬鎘及其聯合處理致綿羊腎組織線粒體體積變小、嵴模糊和空泡化,提示鉬鎘及其聯合可能通過鐵死亡致綿羊腎損傷。在鐵死亡進程中,NCOA4作為一種胞質自噬受體,通過與FTH1結合誘發鐵蛋白自噬,進而調控細胞內鐵含量水平穩態。同時,TFR1作為轉鐵蛋白受體,通過與轉鐵蛋白結合使細胞攝入外源性鐵,調控細胞的鐵離子代謝進程。此外,ACSL4調控進入細胞中的亞鐵離子發生芬頓反應,使多不飽和脂肪酸生成脂質過氧化物,導致生物膜結構損傷并誘發鐵死亡[27]。GPX4通過催化反應將脂質過氧化反應產物還原,即脂質過氧化物轉化為相應的脂質羥基,從而保護細胞膜的完整性和功能。SLC7A11是胱氨酸/谷氨酸反向轉運蛋白的組成成分,調控細胞內GSH的合成,進而影響細胞氧化應激水平和鐵死亡進程。與此同時,大量研究表明PTGS2水平變化與鐵死亡進程存在密切的聯系[28-29]。前人研究表明,鎘能夠通過促進NCOA4、ACSL4、TFR1和PTGS2基因表達水平,抑制SLC7A11、GPX4和FTH1基因表達水平,從而誘發鐵死亡[24,30]。本研究中,鉬、鎘及其聯合暴露能夠引發綿羊腎組織NCOA4、ACSL4、TFR1和PTGS2基因表達水平上升,SLC7A11、GPX4和FTH1基因表達水平降低,提示綿羊腎細胞發生鐵死亡。
4" 結" 論
綜上所述,鉬、鎘及其聯合暴露能夠誘發綿羊腎氧化應激和鐵死亡,并引起腎組織損傷,且鉬鎘毒性具有協同效應。
參考文獻(References):
[1]" ZHANG C Y,HU Z S,HU R M,et al.New insights into crosstalk between pyroptosis and autophagy co-induced by molybdenum and cadmium in duck renal tubular epithelial cells[J].J Hazard Mater,2021,416:126138.
[2]" BHARDWAJ J K,BIKAL P,SACHDEVA S N.Cadmium as an ovarian toxicant:a review[J].J Appl Toxicol,2024,44(1):129-147.
[3]" PANG Y T,WU D M,MA Y,et al.Reactive oxygen species trigger NF-κB-mediated NLRP3 inflammasome activation involvement in low-dose CdTe QDs exposure-induced hepatotoxicity[J].Redox Biol,2021,47:102157.
[4]" WANG C,NIE G H,YANG F,et al.Molybdenum and cadmium co-induce oxidative stress and apoptosis through mitochondria-mediated pathway in duck renal tubular epithelial cells[J].J Hazard Mater,2020,383:121157.
[5]" 趙曉祥,馮" 璐,王宇暉.鋅、鎘單一及復合脅迫下番茄幼苗生理響應及聯合毒性的研究[J].安全與環境學報,2020,20(3):1176-1184.
ZHAO X X,FENG L,WANG Y H.Physiological responses and joint toxicity of tomato seedlings under single and combined stress of zinc and cadmium[J].Journal of Safety and Environment,2020,20(3):1176-1184.(in Chinese)
[6]" ZHANG C Y,LIN T J,NIE G H,et al.Cadmium and molybdenum co-induce pyroptosis via ROS/PTEN/PI3K/AKT axis in duck renal tubular epithelial cells[J].Environ Pollut,2021,272:116403.
[7]" 王紅梅,江春雨,韓雪峰,等.反芻動物鎘暴露及其危害的研究進展[J].黑龍江畜牧獸醫,2023(16):35-39.
WANG H M,JIANG C L,HAN X F,et al.Research progress on cadmium exposure and its hazards in ruminants[J].Heilongjiang Animal Science and Veterinary Medicine,2023(16):35-39.(in Chinese)
[8]" TESCHKE R.Aluminum,arsenic,beryllium,cadmium,chromium,cobalt,copper,iron,lead,mercury,molybdenum,nickel,platinum,thallium,titanium,vanadium,and zinc:molecular aspects in experimental liver injury[J].Int J Mol Sci,2022,23(20):12213.
[9]" WU Y H,YANG F,ZHOU G B,et al.Molybdenum and cadmium co-induce mitochondrial quality control disorder via FUNDC1-mediated mitophagy in sheep kidney[J].Front Vet Sci,2022,9:842259.
[10]" 王" 浩,肖金龍,沈 "玨,等.細胞死亡的新方式——鐵死亡與銅死亡[J].畜牧獸醫學報,2024,55(2):461-470.
WANG H,XIAO J L,SHEN J,et al.New ways of cell death—ferroptosis and cuproptosis[J].Acta Veterinaria et Zootechnica Sinica,2024,55(2):461-470.(in Chinese)
[11]" HE Z Q,SHEN P,FENG L J,et al.Cadmium induces liver dysfunction and ferroptosis through the endoplasmic stress-ferritinophagy axis[J].Ecotoxicol Environ Saf,2022,245:114123.
[12]" 柏" 合.鉬鎘聯合誘導綿羊肝細胞線粒體質量控制失調的作用機制[D].南昌:江西農業大學,2022.
BAI H.The mechanism of mitochondrial quality control dysregulation co-induced by molybdenum and cadmium in ovine hepatocytes[D].Nanchang:Jiangxi Agricultural University,2022.(in Chinese)
[13]" 陳亞杰,尤" 朵,范宗民,等.食管癌旁組織席卷包埋大切片的臨床病理特征[J].臨床與實驗病理學雜志,2023,39(6):641-645.
CHEN Y J,YOU D,FAN Z M,et al.Clinicopathological characteristics of large tissue sections wrapped around esophageal carcinoma[J].Journal of Clinical and Experimental Pathology,2023,39(6):641-645.(in Chinese)
[14]" 陳敬宜,于" 淼,張金洋,等.鐵死亡參與鎘暴露雞肝損傷的研究[J].畜牧獸醫學報,2023,54(02):787-802.
CHEN J Y,YU M,ZHANG J Y,et al.Study on the involvement of ferroptosis in liver injury of cadmium-exposed chickens[J].Acta Veterinaria et Zootechnica Sinica,2023,54(2):787-802.(in Chinese)
[15]" 丁小麗,宮中桂,陳淑芳,等.海藻糖抑制NF-κB介導的炎性反應緩解鎘致大鼠腎臟損傷[J].揚州大學學報:農業與生命科學版,2023,44(3):37-43.
DING X L,GONG Z G,CHEN S F,et al.Trehalose alleviates cadmium-induced kidney injury by inhibiting NF-κB-mediated inflammatory response in rats[J].Journal of Yangzhou University:Agricultural and Life Sciences Edition,2023,44(3):37-43.(in Chinese)
[16]" 宋" 超.高鉬對綿羊肝腎毒性及其機理的研究[D].洛陽:河南科技大學,2014.
SONG C.Effect of high molybdenum on the toxic effect and damage mechanism of the liver and kidney in sheep[D].Luoyang:Henan University of Science and Technology,2014.(in Chinese)
[17]" ZHANG C Y,WANG X R,PI S X,et al.Cadmium and molybdenum co-exposure triggers autophagy via CYP450s/ROS pathway in duck renal tubular epithelial cells[J].Sci Total Environ,2021,759:143570.
[18]" 龍夢菲.葛根素對鎘致大鼠腎臟損傷的保護效應[D].揚州:揚州大學,2018.
LONG M F.Protective effect of puerarin on cadmium-induced renal injury in rats[D].Yangzhou:Yangzhou University,2018.(in Chinese)
[19]" 李冰心,龔淑影,許丹寧,等.白術多糖通過花生四烯酸代謝通路緩解環磷酰胺誘導的小鼠腎損傷[J].食品工業科技,2024,45(10):325-334.
LI B X,GONG S Y,XU D N,et al.Polysaccharide of atractylodes macrocephala koidz alleviate kidney injury induced by cyclophosphamide in mice through arachidonic acid metabolic pathway[J].Science and Technology of Food Industry,2024,45(10):325-334.(in Chinese)
[20]" 邱文粵,蘇依曼,葉嘉莉,等.積雪草酸通過調控細胞凋亡和自噬緩解脂多糖誘導肉雞急性腎損傷的研究[J].畜牧獸醫學報,2024,55(2):809-821.
QIU W Y,SU Y M,YE J L,et al.Study on asiatic acid alleviates LPS-induced acute kidney injury by regulating apoptosis and autophagy of broilers[J].Acta Veterinaria et Zootechnica Sinica,2024,55(2):809-821.(in Chinese)
[21]" KONG Z Y,LIU C H,OLATUNJI O J.Asperuloside attenuates cadmium-induced toxicity by inhibiting oxidative stress,inflammation,fibrosis and apoptosis in rats[J].Sci Rep,2023,13(1):5698.
[22]" ZHANG Q,ZHANG C,GE J,et al.Ameliorative effects of resveratrol against cadmium-induced nephrotoxicity via modulating nuclear xenobiotic receptor response and PINK1/Parkin-mediated Mitophagy[J].Food Funct,2020,11(2):1856-1868.
[23]" 孫曉怡.基于鐵死亡與氧化應激相關信號通路探討鉑類抗腫瘤藥物腎毒性的機制研究[D].蘇州:蘇州大學,2022.
SUN X Y.Investigation of the mechanism of platinum-based antitumor drugs nephrotoxicity based on ferroptosis and oxidative stress signaling pathway[D].Suzhou:Soochow University,2022.(in Chinese)
[24]" 李" 敏,楊" 前,劉亞軒,等.鎘通過誘導自噬促進腎小管上皮細胞鐵死亡的研究[J].陸軍軍醫大學學報,2022,44(17):1705-1711.
LI M,YANG Q,LIU Y X,et al.Cadmium promotes ferroptosis in renal tubular epithelial cells by inducing autophagy[J].Journal of Army Medical University,2022,44(17):1705-1711.(in Chinese)
[25]" 李" 鵬,楊" 晶,馬艷梅,等.枸杞糖肽通過抑制鐵死亡減輕高血糖大鼠腦缺血/再灌注損傷[J].中國藥理學通報,2023,39(11):2043-2049.
LI P,YANG J,MA Y M,et al.Lycium barbarum glycopeptide attenuates cerebral ischemia/reperfusion injury in hyperglycemic rats through inhibition of ferroptosis[J].Chinese Pharmacological Bulletin,2023,39(11):2043-2049.(in Chinese)
[26]" LEWERENZ J,ATES G,METHNER A,et al.Oxytosis/Ferroptosis-(Re-) emerging roles for oxidative stress-dependent non-apoptotic cell death in diseases of the central nervous system[J].Front Neurosci,2018,12:214.
[27]" 張雪姣.靶向NCOA4抑制高糖誘導胰島素樣細胞鐵死亡機制的研究[D].長春:吉林大學,2023.
ZHANG X J.Mechanism of inhibition effect of high-glucose induced ferroptosis in insulin-producing cells via targeting NCOA4[D].Changchun:Jilin University,2023.(in Chinese)
[28]" ZHOU Y Q,ZHOU H X,HUA L,et al.Verification of ferroptosis and pyroptosis and identification of PTGS2 as the hub gene in human coronary artery atherosclerosis[J].Free Radical Biol Med,2021,171:55-68.
[29]" CHEN G Z,LI L,TAO H M.Bioinformatics identification of ferroptosis-related biomarkers and therapeutic compounds in ischemic stroke[J].Front Neurol,2021,12:745240.
[30]" WANG L,YANG F,HU M W,et al.GPX4 utilization by selenium is required to alleviate cadmium-induced ferroptosis and pyroptosis in sheep kidney[J].Environ Toxicol,2023,38(4):962-974.
(編輯" 范子娟)

