術中超早期亞低溫治療重型顱腦損傷的應用研究
鄭慶棠,陳 卓,解叢民
(廣東醫學院附屬石龍博愛醫院神經外科,廣東東莞 523325)
亞低溫治療重型顱腦損傷已經過大量的基礎研究得到證實其對腦損傷的保護作用,并廣泛應用于臨床[1],但絕大多數是安排在術后進行的。本文中筆者收集2007年1月~2009年6月我科符合條件的重型顱腦損傷需行開顱手術的患者62例,將其隨機分為術中超早期亞低溫治療組和術后亞低溫治療組,對多項參數指標進行監測并加以對比研究,以探討術中超早期亞低溫治療重型顱腦損傷的治療機制和臨床效果。
1 資料與方法
1.1 一般資料
本組62例患者,入選標準:傷后24 h內入院格拉斯哥昏迷評分(GCS)為 4~7分,其中,男 40例,女 22例;年齡 17~60歲;主要病理類型:大面積腦挫裂傷16例,顱內血腫46例。將其隨機分為術中超早期亞低溫治療組(30例,術中亞低溫組)和術后亞低溫治療組(32例,對照組)。入院時術中亞低溫組 GCS 為(5.5±1.5)分,對照組為(5.8±1.7)分;年齡術中亞低溫組為(46.3±15.0)歲,對照組為(48.5±13.0)歲。 兩組一般資料比較,差異無統計學意義(P>0.05),具有可比性。
1.2 方法
兩組患者均行開顱手術治療,結合術后降低腦水腫的脫水治療,穩定細胞膜的激素治療,預防出血后腦血管痙攣治療,保持呼吸道通暢的氣管插管或氣管切開呼吸機輔助治療,防治消化道出血、營養神經、改善腦循環治療,以及防止感染的抗感染治療。
1.3 亞低溫治療和參數指標監測
術中亞低溫組進入手術室即行亞低溫治療,于傷后(2.0±0.8)h接受亞低溫治療。對照組于術后亞低溫治療,于傷后(8.0±2.0)h接受亞低溫治療。所有患者皆術中經腦室或硬膜下置管監測顱內壓(ICP);術中或術后持續應用生理鹽水500 ml+氯丙嗪100 mg+異丙嗪100 mg+卡肌寧200~400 mg混合泵入,誘導降溫時40 ml/h,亞低溫維持階段10 ml/h左右,必要時加用芬太尼協同鎮靜;采用恒邦牌醫用電子降溫毯全身降溫治療,監測直腸溫度降至32~35℃,平均(33.7±2.0)℃。兩組亞低溫治療時間為7~10 d,于術前及術后36、96、120 h時分別進行血糖和全血乳酸測定,于術前及術后24、72、168 h 時分別進行 ICP 測定。
1.4 遠期療效評定
傷后6個月依據GCS預后評分(GOS)評定法判定治療效果。Ⅰ級:死亡;Ⅱ級:植物狀態;Ⅲ:重度殘殘;Ⅳ級:輕度殘疾;Ⅴ級:恢復良好。統計良好率包括Ⅳ級及Ⅴ級。
1.5 統計學方法
2 結果
2.1 術中亞低溫組和對照組亞低溫治療對血糖和全血乳酸的影響
亞低溫治療后36、96及120 h時術中亞低溫組血糖和全血乳酸較對照組均有明顯降低(均P<0.05)。見表1。
表1 術中亞低溫組和對照組對血糖和全血乳酸的影響(,mmol/L)Tab.1 The influence on blood sugar and blood lactate of intraoperativehypothermiagroupandcontrolgroup(,mmol/L)

表1 術中亞低溫組和對照組對血糖和全血乳酸的影響(,mmol/L)Tab.1 The influence on blood sugar and blood lactate of intraoperativehypothermiagroupandcontrolgroup(,mmol/L)
與對照組比較,*P<0.05
2.2 術中亞低溫組和對照組對ICP的影響
亞低溫治療72 h及168 h后術中亞低溫治療組ICP較對照組明顯降低(P<0.05)。見表2。
2.3 傷后6個月GOS評分
術中亞低溫組良好率為63.3%(19/30),對照組良好率為43.7%(14/32),術中亞低溫組良好率明顯高于術后亞低溫組良好率,兩組比較,差異有統計學意義(P<0.05)。術中亞低溫組重殘4例,植物狀態1例,死亡6例;對照組重殘8例,植物狀態2例,死亡8例。兩組死亡率比較,差異無統計學意義(P>0.05)。
表2 術中亞低溫組和對照組對ICP的影響(,kPa)Tab.2 The influence on ICP of intraoperative hypothermia group and control group(,kPa)
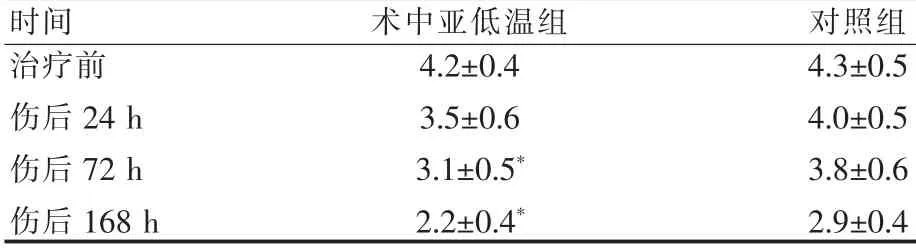
表2 術中亞低溫組和對照組對ICP的影響(,kPa)Tab.2 The influence on ICP of intraoperative hypothermia group and control group(,kPa)
與對照組比較,*P<0.05
時間 術中亞低溫組 對照組治療前4.2±0.44.3±0.5傷后24 h3.5±0.64.0±0.5傷后72 h3.1±0.5*3.8±0.6傷后168 h2.2±0.4*2.9±0.4
3 討論
3.1 亞低溫治療對腦組織保護作用的機制
亞低溫治療對腦組織保護作用的機制可能為[2]:①降低腦組織細胞氧耗量,減少乳酸堆積;②保護血-腦屏障,減輕腦水腫;③抑制內源性毒性產物對腦組織的損害作用;④減少神經細胞鈣內流,阻斷鈣超載所致的細胞損害;⑤減少腦細胞結構蛋白的破壞,促進腦細胞結構和功能修復;⑥減輕彌漫性軸索損傷。經研究證實,30~33℃低溫對實驗性顱腦損傷動物有顯著的保護作用,并證明越早使用亞低溫腦組織保護的效果越好。
3.2 亞低溫治療對ICP的影響
腦水腫是引起顱內高壓最常見的原因之一,顱內高壓程度和預后密切相關。半數以上重型顱腦損傷患者死于難以控制的顱內高壓,80%以上重型顱腦損傷患者顱內高壓會導致腦血流下降、腦組織缺血缺氧并加重腦水腫[3],反過來又使顱內壓進一步增高形成惡性循環,早期亞低溫治療明顯減輕了腦水腫,打斷了腦水腫與顱內壓增高的惡性循環,從而降低死亡率和致殘率并改善預后。故亞低溫治療能有效地防止繼發性顱內高壓,能明顯減少顱內高壓所造成的腦病理損害程度和范圍。特別是術中超早期亞低溫治療能更快更明顯地降低重型顱腦損傷患者的ICP。本研究顯示,經亞低溫治療24 h后升高的ICP已有明顯下降,尤其是術中亞低溫組于傷后72 h較對照組降顱壓更為顯著;本研究中筆者觀察到行術中亞低溫治療的患者顱壓呈進行性惡化的較對照組少,部分患者避免因需切除額顳部來達到內減壓的進一步損傷,從而縮短手術時間,減少醫源性創傷。
3.3 術中超早期亞低溫對血糖和全血乳酸影響
高血糖和高乳酸血癥反應是影響重型顱腦損傷患者預后的兩個重要因素[4]。本研究證實,亞低溫可抑制重型顱腦損傷急性期高血糖和高乳酸血癥,特別是術中超早期亞低溫治療能更快更明顯地降低重型顱腦損傷患者血糖和全血乳酸。術中超早期亞低溫于傷后36 h在降低全血乳酸及血糖方面明顯優于對照組,兩組比較差異均有統計學意義(均P<0.05)。這主要是術中超早期亞低溫治療能更早抑制重型顱腦損傷的應激反應,抑制傷后兒茶酚胺等內源毒性物質生成和釋放,使應激反應降低,高代謝狀態降低,更有利于早期降低氧耗量保護腦組織,促進腦組織中后期的康復。
綜上所述,亞低溫是治療急性重型顱腦損傷一種有效的手段,急性重型顱腦損傷越早使用亞低溫治療,患者的神經功能恢復及預后就越好[5-6]。術中超早期亞低溫治療重型顱腦損傷,有利于更早更好地發揮亞低溫的降低氧耗、改善腦缺血損傷、抑制自由基誘導的脂質化過程保護血-腦屏障作用,從而提高重型顱腦損傷患者的生存率和康復良好率。將既往亞低溫治療提前至術中應用,雖然只提前數小時,卻更有利于通過抑制脂質過氧化反應來降低腦代謝、減輕酸中毒,降低腦壓改善腦灌注,提高重型顱腦損傷的療效。
[1]江基堯,朱誠,盧亦成,等.亞低溫治療重型顱腦損傷患者的臨床療效[J].中華創傷雜志,1997,13(1):1-3.
[2]江基堯,朱誠.顱腦創傷臨床救治指南[M].上海:第二軍醫大學出版社,2002:101-103.
[3]江基堯,朱誠.現代顱腦損傷學[M].上海:上海科學技術文獻出版社,1995:12-21.
[4]劉敬業,張賽,只達石,等.亞低溫治療急性重型顱腦損傷的臨床研究[J].中華創傷雜志,1999,15(1):35-37.
[5]劉堅,郭文勝.重型顱腦損傷的臨床治療體會[J].中國現代醫生,2009,47(1):150-151.
[6]劉連松.亞低溫治療重型顱腦損傷32例體會[J].中國現代醫生,2008,46(35):64,66.

