丙種球蛋白無反應性川崎病相關因素及治療探討
劉 燕, 楊曉麗 (山西省人民醫院兒科, 太原 030012)
川崎病(Kawasaki disease KD)是一種病因不明的急性發熱性全身性血管炎綜合征,主要見于5歲以下兒童;其可累及心臟及冠狀動脈,甚至死亡。目前靜脈注射丙種球蛋白(IVIG)聯合阿司匹林治療是現行KD組的標準療法,但仍有少部分患兒對首次IVIG治療無效,稱為IVIG無反應、難治性KD或耐藥KD[1]。本文通過回顧性分析,探討IVIG無反應KD組發生的危險因素及再治療方案的選擇。
1 資料與方法
1.1 診斷及納入標準 KD診斷標準參照2004年美國心臟協會(AHA)川崎病診斷指南[2]。冠脈擴張標準為:<5歲,冠狀動脈內徑>3 mm;≥5歲,冠狀動脈內徑>4 mm。冠狀動脈瘤診斷標準為冠狀動脈局限或彌漫性擴張,其直徑超過相鄰正常冠脈的1.5倍,內徑為4.1-4.9 mm 為小冠狀動脈瘤,5.0-7.9 mm為中等冠狀動脈瘤≥8 mm為巨大冠狀動脈瘤。
1.2 IVIG無反應型KD的定義[1]IVIG治療48 h后,體溫仍高于38℃或治療后2-7 d,甚至2周內再次發熱,并符合至少一項KD診斷標準者,即為IVIG無反應性川崎病。
1.3 方法 分析2006-03~2010-05我院收治的川崎病患兒臨床資料,選擇符合診斷標準并在急性期應用IVIG治療者,共152例。
2 結果
2.1 IVIG無反應性川崎病發生率及相關因素分析152例符合川崎病診斷標準,且于急性期接受IVIG治療,所有患兒均接受阿司匹林30-50 mg/(kg·d)口服治療,其中98例接受1 g/(kg·d)連用2 d用藥方案;38例接受2 g/(kg·d)一次性給藥方案;16例接受400 mg/(kg·d)連續用藥5 d方案。140例首次用藥后體溫減退,屬初始IVIG治療敏感,為敏感組(92.1%),12例對首次IVIG治療無反應,發生率7.89%(12/152),為無反應組。敏感組和無反應組臨床表現比較見表1。
由表1可見,兩組間IVIG治療前發熱時間相比,差異無統計學意義,但IVIG無反應組總發熱時間較長(P<0.05)。兩組在發病年齡、性別比例及其他臨床表現方面比較,差異無統計學意義。敏感組有25例發生冠脈病變,包括冠脈擴張及冠狀動脈瘤,發生率17.9%,無反應組有7例發生冠脈病變,發生率58.3%,較敏感組顯著增高(P<0.01)。
表1 KD患兒敏感組與無反應組臨床表現比較(±s)Tab 1Clinical characteristics of IVIG non-response and response patients(±s)
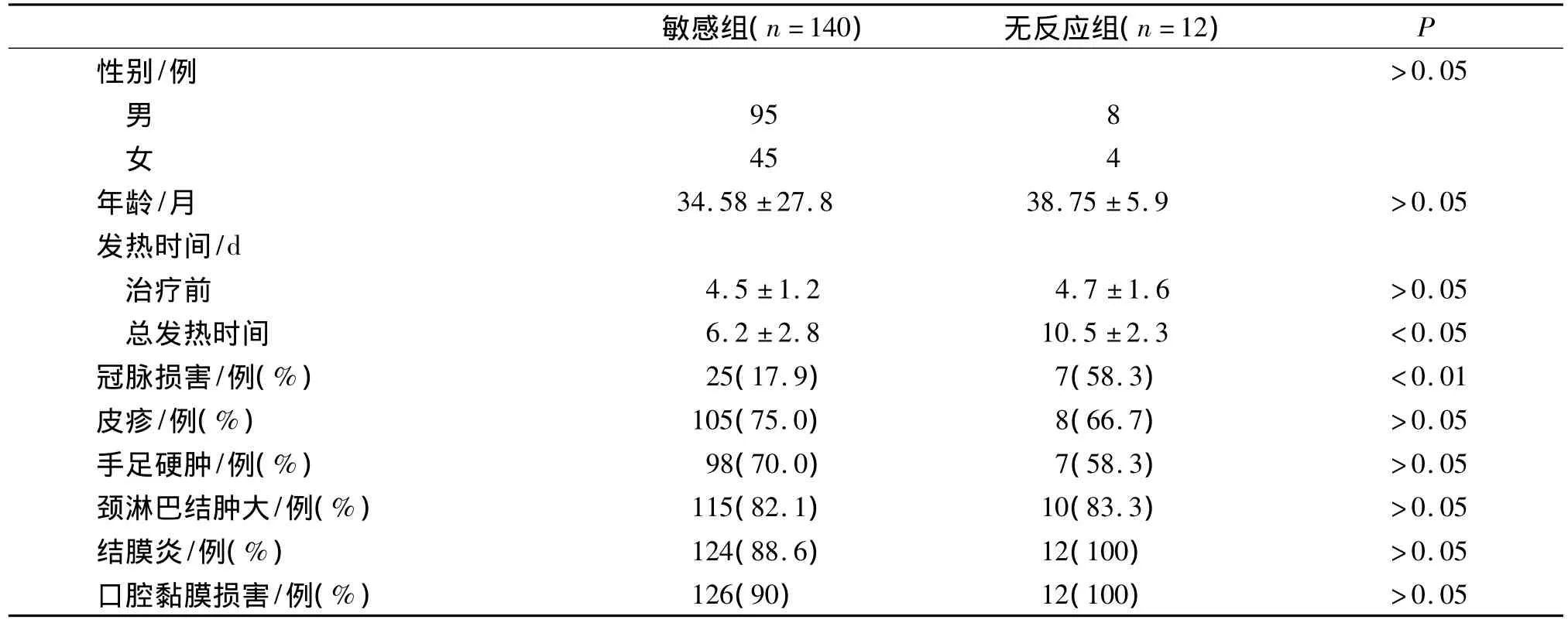
表1 KD患兒敏感組與無反應組臨床表現比較(±s)Tab 1Clinical characteristics of IVIG non-response and response patients(±s)
?
由表2可見,在血沉(ESR)、總蛋白(TP)、血小板(Plt)計數、谷丙轉氨酶(ALT)、乳酸脫氫酶(LDH)、血鈉方面敏感組和無反應組間比較差異無統計學意義。無反應組全血WBC計數、中性粒細胞百分比、C反應蛋白(CRP)明顯高于敏感組,差異有統計學意義(P<0.01);而血紅蛋白、白蛋白均明顯低于敏感組,差異有統計學意義(P<0.05)。2.2 IVIG無反應組KD再治療 12例無反應組全部接受IVIG 2 g/(kg·d)再次治療,有效者10例,占83.3%;2例未控制者,加用糖皮質激素治療,其中1例口服強的松1-2 mg/(kg·d),1例靜脈滴注甲基強的松龍2 mg/(kg·d),連用3 d后改為口服潑尼松1-2 mg/(kg·d),2周后漸減量至停藥。以上病例均同時口服阿司匹林。
表2 KD患兒敏感組與無反應組實驗室檢查結果比較(±s)Tab 2Laboratory findings of IVIG non-response and response patients(±s)
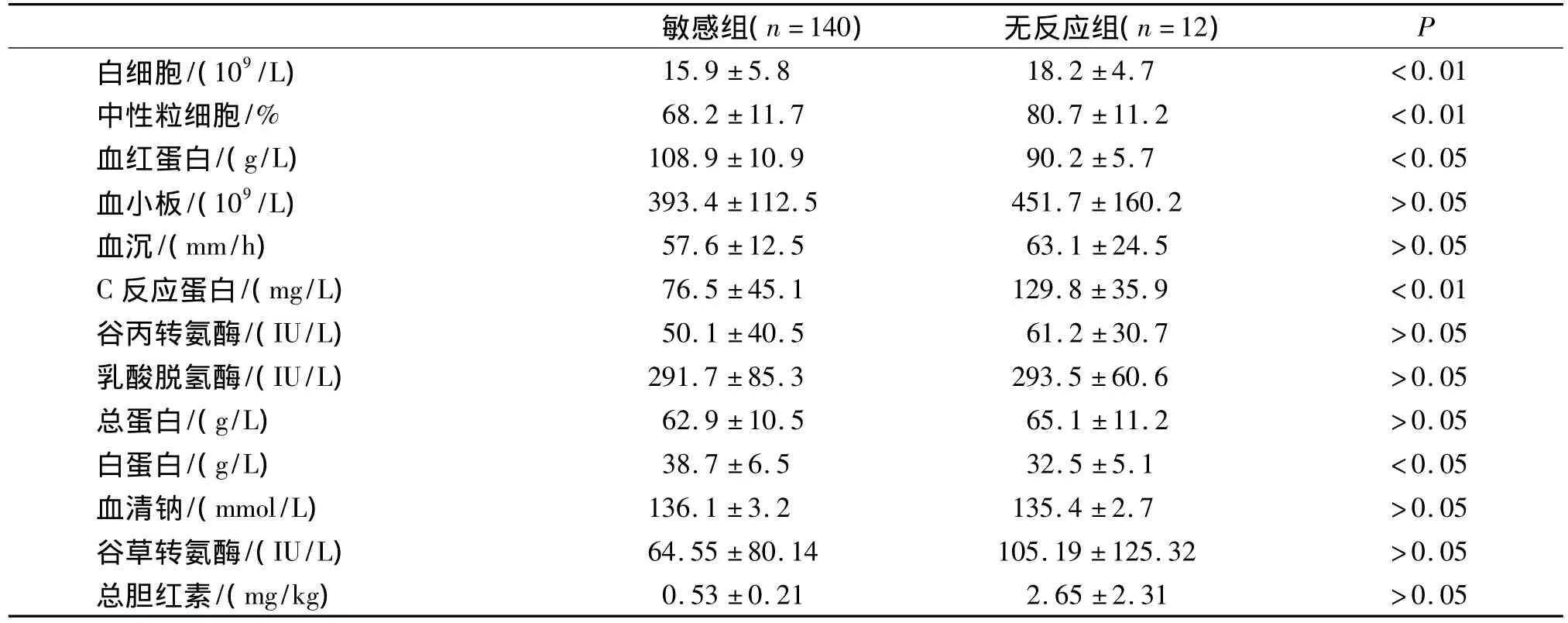
表2 KD患兒敏感組與無反應組實驗室檢查結果比較(±s)Tab 2Laboratory findings of IVIG non-response and response patients(±s)
?
3 討論
川崎病是一種累及全身的非特異性血管炎,多侵犯冠狀動脈,部分患兒可形成冠狀動脈瘤,甚至危及生命。急性期KD的治療目的是控制炎癥和防止冠狀動脈受累。大劑量丙種球蛋白靜脈注射可減輕免疫異常激活,改善癥狀,減輕冠狀動脈損傷,但仍有大約10%-20%病例對首次治療效果欠佳,成為KD急性期治療難點之一。這部分病例稱為IVIG無反應、難治性KD或耐藥KD,還需進一步研究取得一致定義。持續反復發熱增加冠狀動脈病變危險,出現冠狀動脈病變的KD患兒,其發熱時間明顯延長。因此,研究無反應KD組對丙種球蛋白耐藥的相關因素,積極治療,減少初治IVIG無反應性可以改善KD治療效果,減少冠脈并發癥。本研究對152例KD組患兒進行了回顧性分析,其中IVIG無反應發生率 7.89%,與國內外相關報道類似[3,4]。同時IVIG無反應合并冠脈病變者明顯增多。Sungho等[5]報道2001-2004年IVIG無反應發病率2.2% -11.5%,合并冠狀動脈病變者44.4%,其中出現冠狀動脈瘤等嚴重冠脈并發癥者8%。國內樸金花等[6]報道IVIG無反應發病率16.67%,合并冠狀動脈病變者37.84%,其中出現冠狀動脈瘤等嚴重冠脈并發癥者7.5%。
Fukunishi等[4]分析發現初始IVIG無反應患兒血CRP水平、乳酸脫氫酶和總膽紅素升高,Hb水平降低,提出CRP>100 mg/L,LDH>590 IU/L及血紅蛋白<100 g/L可以預測IVIG無反應性。Tohru等[7]研究認為血鈉≤133 mmol/L,首次IVIG治療小于4 d,AST≥100 IU/L,中性粒細胞百分比≥80%,CRP≥10 mg/dl,年齡≤12 月,PLT≤30 ×104/mm3是丙種球蛋白耐藥的高危因素。本驗結果顯示IVIG無反應KD組患兒血紅蛋白和血漿白蛋白均明顯低于IVIG敏感性KD組,中性粒細胞比例、白細胞、CRP明顯高于IVIG敏感性KD組,差異有統計學意義(P<0.05)。而兩組年齡、性別、ESR、LDH、TBIL、PLT等差異無統計學意義(P>0.05)。無反應KD組發生冠脈并發癥明顯升高,差異有統計學意義(P<0.05)。因此,在本研究中,具有低白蛋白血癥、貧血、中性粒細胞比例增高、WBC高、CRP明顯升高的KD組患兒對IVIG無反應的可能性較大,冠脈病變發生率增加。另Fukunishi等[4]曾報道KD患兒總膽紅素、r-GTP水平升高,可能反應膽道系統炎癥反應,并未顯示增加冠脈病變危險性,同樣,AST/ALT在IVIG無反應KD組升高,但無統計學意義。在本研究中,我們未檢測 r-GTP等,檢測血ALT、AST、TBIL濃度明顯升高,但差異無統計學意義。在約1/3 KD患兒血清ALT升高,18%可大于100 U/L[8]。
對IVIG無反應性KD的再治療,包括IVIG追加治療,糖皮質激素治療等。目前最常用的方法是IVIG追加治療,也有部分病例對IVIG追加治療仍無反應,約占2% -6%,這類病人冠脈病變發生率也較高[9]。本次研究無反應KD組患兒12例,接受IVIG再治療后10例緩解,2例加用糖皮質激素治療后緩解。糖皮質激素可以直接作用于細胞膜糖皮質激素受體,具有明顯的穩膜及阻斷受體活化的作用,發揮阻斷炎癥作用。但其也可破壞成纖維細胞,影響冠脈病變的修復,增加血小板聚集,促進血栓形成,因此使用時機的選擇非常重要。Hung等[10]報道認為對糖皮質激素應用前已形成冠脈瘤的病例,激素應用好處有限。AL-Mayouf等[11]認為反復應用丙球仍未奏效(有嚴重并發癥:冠脈瘤、嗜血細胞增多癥),即使病程已較長,糖皮質激素沖擊可作為救命療法。Wright等[12]認為甲強龍沖擊療法至少在2次IVIG治療后仍發熱,冠狀動脈病變在進展,以及有發生冠狀動脈瘤高危因素(如年齡<1歲等)才考慮使用。大劑量激素沖擊可加重血液高凝狀態,故需注意抗凝,及使用激素時不良反應:如感染、高血壓等。如應用激素治療,發熱仍不退,可加用如下治療:血漿置換、烏司他丁、MTX、環孢素 A、TNF-α 等。
綜上所述,IVIG無反應KD組較易發生嚴重的CAL,故治療前實驗室檢查全血WBC計數、中性粒細胞比值、CRP明顯增高者,ALB、Hgb較低者,需引起足夠重視,采取及時、積極有效治療措施,以防嚴重冠脈并發癥發生。復用IVIG及必要時在抗凝基礎上加用激素治療,對無反應性KD組有較好療效,但應注意使用時機及量的選擇。
[1] 王永清,曹曉軍.靜脈注射丙種球蛋白無反應性川崎病的診治現狀[J].中華兒科雜志,2005,43(3):226 -228.
[2] Newburger JW,Takahashi M,Gerber MA,et al.Diagnosis,treatment and long-term management on rheumatic fever it is and Kawasaki disease.A Statement for Health Professionals From the Committee on Rheumatic Fever,Endocarditis and Kawasaki Disease,Council on Cardiovascular Disease in the Young,American Heart Association[J].Circulation,2004,110(17):2747 -2771.
[3] 陳嫕,王榮發,劉芳.對大劑量靜脈注射丙種球蛋白初治無效的川崎病的處治及相關因素探討[J].中國當代兒科雜志,2004,6(1):59 -61.
[4] Fukunishi M,Kikkawa M,Hamana K,et al.Prediction of non-responsiveness to intravenous high-dose gamma-globulin therapy in patients with Kawasaki disease at onset[J].J Pediatr,2000,137:172-176.
[5] Cha S,Yoon M,Ahn Y,et al.Risk factors for failure of initial intravenous immunoglobulin treatment in Kawasaki disease[J].J Korean Med Sci,2008,23:718 - 722.
[6] 樸金花,金蓮花,孫景輝,等.大劑量靜脈注射丙種球蛋白無反應性川崎病的臨床分析[J].臨床兒科雜志,2009,27(5):480-483.
[7] Kobayashi T,Inoue Y,Beiser AS,et al.Prediction of intravenous immunoglobulin unresponsiveness in patientswith Kawasaki disease[J].Circulation,2006,112:2606 -2612.
[8] Burns JC,Mason WH,Glode MP,et al.Clinical and epidemiologic characteristics of patients referred for evaluation of possible Kawasaki disease[J].J Pediatr,1991,118:680 -686.
[9] Wallace CA,French JW,Kash SJ,et al.Initial intravenous gamma-globulin in treatment failure in Kawasuki disease[J].J Pediatr,2000,105(6):E78 -81.
[10] Hung JJ,Chiu CH.Pulse methylprednisolone therapy in the treatment of immune globulin-resistant Kawasaki disease:case report and review of the literature[J].Ann Trop Pediatr,2004,24:89 -93.
[11] AL-Mayouf S,Brown M.The use of corticosteroid therapy in refractory Kawasaki patients[J].Clin Rheumatol,2004,23:11 -13.
[12] Wright DA,Newburger JW,Baker A,et al,Treatment of immune globulin-resistant Kawasaki disease with pulsed dose of corticosteroids[J].J Pediatr,1996,12:146 -149.

