免疫過濾法、平板雙向擴散法、酶聯免疫吸附試驗法血清學檢驗技術對農民肺診斷價值的Meta分析
王 群,許 蕾,劉 軍,趙明靜,王笑歌
(中國醫科大學附屬第四院,遼寧沈陽110032)
農民肺(farmer's lung disease,FLD),是人體吸入具有抗原性的有機粉塵引起的過敏性肺泡炎,是過敏性肺泡炎最常見的形式,依據治病抗原的不同又分為由甘蔗熱放線菌引起的蔗塵肺,黃青霉引起的伐木工人肺[1],以及大棚內作業的農民因經常接觸霉變物質引起的大棚肺[2]。一項對遼寧省部分農村地區從事大棚作業農民的流行病學調查中報告遼寧省農業大棚肺患病率為5.7%[3]。因農民肺臨床癥狀不典型、影像學及肺功能檢查均無特征性改變,臨床上極易將其誤診為哮喘,慢性阻塞性肺疾病而延誤了最佳的治療時機[4]。免疫學試驗可以在農民肺早期階段病變不典型時對其進行診斷,目前研究中用于診斷農民肺的血清學技術主要有3種:免疫過濾法(electrosyneresis,ES),平板雙向擴散法(ouchterlony double diffusion,DD),酶聯免疫吸附試驗法(ELISA)。但其在農民肺的診斷效用上存在很大爭議:一些研究者認為血清學技術是一種很好的診斷技術,而對于其他研究者血清學技術僅僅提示受試者曾經暴露在抗原環境中,并不能區分農民肺病人與健康者[5]。為科學評價各血清學技術診斷農民肺的價值,本文收集相關文獻進行系統評價。
1 材料與方法
1.1 檢索策略 檢索CNKI中國學術期刊網全文數據庫(1979-2010.12)、中國生物醫學文獻數據庫(1978-2010.12)、維普資訊網中文科技期刊數據庫(1989-2010.12),中文檢索詞包括過敏性肺炎、農民肺、外源性過敏性肺泡炎、實驗室檢查技術。檢索 PUBMED(1960-2010.12)、Cochrane Librar y,英文檢索詞包括 Hypersensitivity pneumonitis、farmer's lung、diagnosis。并用Google搜索引擎查找相關文獻,追查納入文獻的參考文獻。
1.2 納入與排除標準 根據Cochrane篩選與診斷試驗中關于診斷性研究的納入標準制定文獻納入標準[6],①中文和英文文獻;②評價ES、DD、ELISA法檢測農民肺與對照組的診斷性研究(可聯合使用但在診斷過程中不是序貫性的);③以臨床表現、體格檢查、影像學及肺功能改變、纖維支氣管鏡檢查為金標準;④文獻直接或間接提供原始數據,可分別計算真陽性值(true-positive,TP)、假陽性值(false-positive,FP)、真陰性值(true-negative,TN)、假陰性值(false-negative,FN);⑤研究納入人群包括農民肺患者、其他肺部疾病患者或相同工作環境中的正常人,且每項研究超過10例患者;排除標準:排除未描述具體診斷標準、動物性試驗研究、數據不全、重復發表的文獻。
1.3 資料提取與分析 2名研究人員獨立按預先制定的納入、排除標準對文獻進行納入和排除,并對最終納入的文獻數據進行提取,通過協商或與第三者討論解決分歧。提取的信息包括作者、發表年份、納入研究者例數、檢測方法、真陽性值(TP)、假陽性值(FP)、真陰性值(TN)、假陰性值(FN)。 參照詢證醫學指南中證據水平的分級標準對納入的文獻進行質量分析。
敏感性分析:將各組的每個研究逐一排除后再對剩余研究進行分析,若結果無明顯改變,說明納入文獻的穩定性好;反之,納入文章的穩定性差。
1.4 統計分析 采用 Review Manager 5.0統計學軟件,χ2檢驗結合I2進行異質性分析。用P值和I2評估異質性大小:若P>0.05,I2≤50%,則認為無明顯統計學異質性;若P<0.05,I2>50%,認為研究間的異質性較大。有明顯統計學異質性的研究結果采用隨機效應模型進行合并分析;反之采用固定效應模型分析[6]。如同一診斷試驗之間無異質性,用Meta-disc(version1.4)軟件通過固定效應模型計算合并敏感度(SEN合并)、合并特異度(SPE合并)、合并陽性似然比(+LR合并)、合并陰性似然比(-LR合并)、DOR值及其95%CI。 相反,采用隨機效應模型;繪制綜合受試者工作特征曲線(SROC)并計算曲線下面積(AUC)、Q*值。曲線越接近坐標軸左上角,AUC越接近100%,說明該檢查的診斷價值越高,Q*值越大提示診斷試驗的準確率越高。
2 結果
2.1 文獻檢索結果 文獻檢索及排除流程見圖1。中文數據庫未檢索出符合檢索條件的中文文獻,最終納入符合納入標準的文獻5篇[7-11],全部為英文。
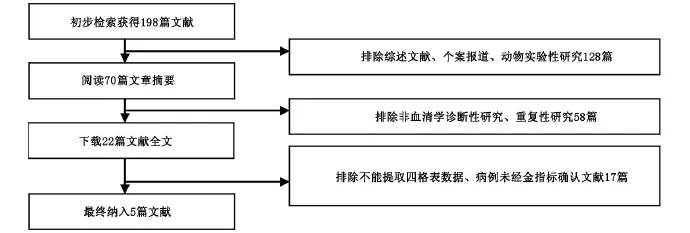
圖1 文獻檢索及排除流程
2.2 納入研究的基本特征與質量評價 納入研究的基本特征詳見表1。5個研究共納入 192例農民肺患者,健康對照 214人,相似病例91例。各研究納入的農民肺患者均經金標準確認。納入的5篇文獻中4篇[8-11]文獻質量為A級,1篇文獻[7]質量為B級。敏感性分析顯示各納入文獻的穩定性良好。
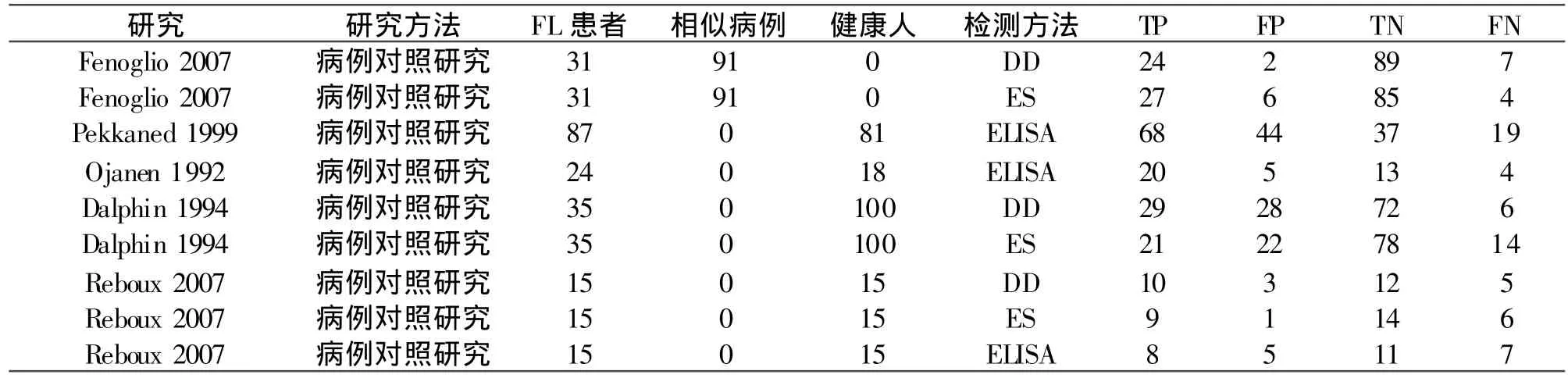
表1 納入研究的基本特征
2.3 數據分析
2.3.1 匯總敏感度、匯總特異度 DD法納入3個研究[8-10],各研究間有統計學異質性(P=0.02,I2=75%)。ES法納入3個研究[8,10,11],各研究間有統計學異質性(P=0.001,I2=85%)。ELISA法納入3個研究[7-9],各研究間無明顯統計學異質性(P=0.17,I2=43%)。DD法、ES法以隨機效應模型,ELISA法以固定效應模型計算SEN合并、SPE合并、+LR合并、-LR合并和 DOR值及其 95%CI,見表 2。

表2 DD、ES、ELISA法的匯總靈敏度、匯總特異度、匯總陽性似然比、匯總陰性似然比和 DOR值
2.3.2 SROC曲線 DD法繪制SROC曲線并計算AUC=0.8543,SE(AUC)=0.064 1,Q*=0.785 3,SE(Q*)=0.061 1(圖2 A)。ES法繪制SR OC曲線并計算AUC=0.904 4,SE(AUC)=0.168 0,Q*=0.836 0,SE(Q*)=0.182 3(圖2 B)。ELISA法繪制SR OC曲線并計算AUC=0.719 7,SE(AUC)=0.1125,Q*=0.668 7,SE(Q*)=0.090 7(圖2 C)。
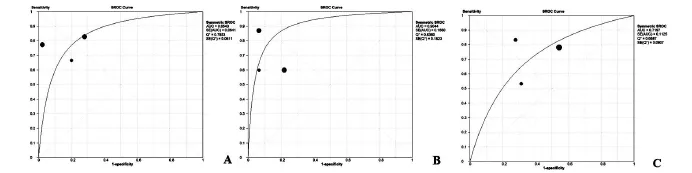
圖2 A:DD法SROC曲線;B:ES法SROC曲線;C:ELISA法SROC曲線
3 討論
系統分析的結果顯示:合并敏感性和特異性后,DD法表現出最高的敏感性(78%)和相對較高的特異性(84%);ES法特異性雖高(86%)但敏感性較低(70%);ELISA法敏感性(76%)、特異性(53%)均較低。DOR是病例組中陽性結果與對照組中陽性結果的比值,表示診斷試驗的判斷能力,DOR值越大,判斷能力越強。本研究中DD法DOR值較ES法、ELISA法高(DD:23.56;ES:21.03;ELISA:4.06),表明 DD法對農民肺的判斷能力較ES法、ELISA法強。
通過Meta分析計算的合并加權靈敏度和特異度,盡管可以在一定程度上說明各血清學試驗對農民肺的診斷價值,但診斷試驗的Meta分析方法與臨床試驗的Meta分析不同,需同時考慮靈敏度和特異度,如果分別對靈敏度和特異度加權,然后采用一般的平均率進行Meta分析,將會失去靈敏度與特異度間的非線性關系:當診斷閾值一定時,隨著靈敏度的提高,特異性會降低;反之,特異性提高靈敏度亦會降低。當診斷閾值變化時,其靈敏度和特異度也會隨之發生變化。SROC不受閾值變化的影響,其AUC值可通過圖形和面積直觀的對診斷性試驗進行比較[12]。對DD法、ES法、ELISA法的SROC曲線定量分析顯示ES法的AUC值最大(ES:0.904 4;DD:0.854 3;ELISA:0.719 7),提示ES法在3種血清學檢驗中具有最大的檢驗效能。SROC曲線分析中的Q*值考慮了靈敏度和特異度之間的非線性關系,是診斷試驗中靈敏度和特異度的合并指標,提示診斷試驗的準確率。本系統分析的結果顯示ES法SROC曲線分析中的Q*值最大(ES:0.836 0;DD:0.785 3;ELISA:0.668 7),提示ES法在3種血清學檢驗中表現出最高的準確率。
由于目前各研究中所選用的實驗技術不同,以及選擇的抗原是否是本地區主要的致病菌和是否存在其他次要致病菌而研究中并未選入等因素均可造成各研究之間出現結論不統一的現象[13]。Reboux[8]在研究中提取了用法國南部最主要的3種農民肺致病菌:Absidia corymbifera,Eurotium amstelodami,Wallemia sebi,以及一種次要致病菌S.rectivirgula做抗原,分別用ES法、DD法、ELISA法3種血清學技術對農民肺患者以及健康對照組受試者的血清進行檢測:ES法對主要致病菌抗原Absidia corymbifera表現出最佳的診斷效能,其敏感性和特異性分別達到了86.7%,100%。DD法僅次于ES法,敏感性及特異性為73.3%,93.3%。而ELISA法的敏感性及特異性僅為46.7%,86.7%。本研究中DD法靈敏度最高、DOR值最大,提示DD法對農民肺具有較高的判斷能力;綜合AUC、DOR、Q*值,ES法的檢驗效能最大、檢驗準確率最高;而ELISA不僅敏感性、特異性低,且檢驗效能及檢驗準確率均不及DD法和ES法。與Reboux研究中得出的結論基本一致。
通過對DD法、ES法、ELISA法對農民肺診斷價值進行Meta分析后發現,免疫過濾法、平板雙向擴散法是對農民肺診斷效能較高的血清學檢查方法。在可靠的血清學檢測技術支持下并確定本地區主要的農民肺致病菌后,血清學技術可以成為一種很好的農民肺診斷手段。但目前關于血清學診斷農民肺的文獻較少,研究可能存在偏倚,仍需進一步的研究證實血清學技術在診斷農民肺中的臨床價值。
[1]Ashok M,Patel MD,Jay H,et al.Hypersensitivity pneumonitis:current concepts and future questions[J].J Allergy Clin Immunol,2001,108:661.
[2]何曉雨,吳立華,王笑歌,等.遼寧省部分農村地區大棚作業農民肺危險因素分析[J].中國實用內科雜志,2010,30(12):1094.
[3]付 爽,陳東紅,許 蕾,等.遼寧省部分農村地區農民大棚肺流行病學調查概況分析[J].中國實用內科雜志,2009,29(9):808.
[4]M.Girard,Y.Lacasse,Y.Cormier;Hypersensitivity pneumonitis[J].Allergy,2009,64:322.
[5]Jordan N.Fink,HectorG.Ortega,Herbert Y.Reynolds,Yvon F.Cormier,Leland L.Fan,Teri J.Franks;Needs and opportunities for research in hypersensitivity pneumonitis[J].Am J Respir Crit Care Med,2005,171:792.
[6]The Cochrane methods group on systematic review of screening and diagnostic test:recommended methods[OL].[http://www.cochrane.org/resources/handbook/handbook4.pdf].
[7]R Erkinjuntti-Pekkanen,M Reiman,JIKokkarinen,et al.IgG antbodies,chronic bronchitis,and pulmonary function values in farmer's lung patients and matched controls[J].Allergy,1999,54:1181.
[8]Gabriel Reboux,Renaud Piarroux,Sandrine Roussel,et al.Assessment of four serological techniques in the immunological diagnosis of far mer's lung disease[J].Jouranl of Medical Micribiology,2007,56:1317.
[9]Tarja Ojanen;Class specific antibodies in serodiagnosis of farmer's lung[J].Br J Ind Med,1992,49:332.
[10]C-M.Fenoglio,G.Reboux,B.Sudre.M.Mercier;Diagnostic value of serum precipitins to mould antigens in active hypersensitivity pneumonitis[J].Eur Respir J,2007,29:706.
[11]Dalphin JC,Toson B,Monet E,et al.Farmer's lung precipitins in doubs(a department of France):prevalence and diagnostic value[J].Allergy,1994,49:744.
[12]Deeks JJ.Systematic reviews in health care:systematic reviews of evaluations of diagnostic and screening tests[J].B MJ,2001;323:157.
[13]SelmanM,Lacasse Y,Pardo A,et al.Hypersensitivity pneumonitis caused by fungi[J].Proc Am Thorac Soc,2010,7(3):229.

