軟骨母細(xì)胞瘤臨床病理分析
程文德 王偉源 冷敏芳 陳艷芬 林梅英 王春燕
軟骨母細(xì)胞瘤(Chondrohlastoma)是一種少見的良性骨腫瘤,好發(fā)于20歲以下的年青人,常發(fā)生于骺板軟骨尚未消失的長骨骺端[1],但也可發(fā)生于短骨、扁骨等不典型部位。本文報(bào)道我院2006年至2010年收治的3個(gè)病例,并結(jié)合文獻(xiàn)資料就其臨床與病理特點(diǎn)進(jìn)行分析。
1 資料與方法
1.1 一般資料 例1,男,18歲,出現(xiàn)左膝部脹痛半年多,活動后加重、負(fù)重時(shí)明顯,CT示左脛骨干骺端囊性占位,干骺后端外側(cè)可見一大小為5.5 cm×4.5 cm×3.5 cm的低密度腫物,邊緣骨質(zhì)硬化,腫物內(nèi)可見多個(gè)砂粒狀鈣化灶(圖1),手術(shù)刮取病變組織送檢。例2,男,15歲,一年前開始出現(xiàn)跑步后右膝關(guān)節(jié)部位疼痛,后進(jìn)行性加重,即使休息也感到脹痛難受,隨入院診治。查休:右膝關(guān)節(jié)未見異形,股骨下端內(nèi)側(cè)明顯壓痛,X線檢查示右股骨下端干骺端內(nèi)側(cè)有一大小為4 cm×3 cm×2.5cm的低密度囊性改變區(qū),邊界清楚。臨床考慮為骨囊腫而行病灶刮除植骨術(shù)。術(shù)中見右股骨下端內(nèi)側(cè)囊腫性病變,囊內(nèi)見肉芽組織樣結(jié)構(gòu),囊壁質(zhì)硬,刮取病灶送檢。例3,女,22歲,因右髖關(guān)節(jié)部隱痛1年多,加重一個(gè)月而入院,X線檢查示右股骨頭見一大小為3 cm×3 cm×2.5 cm的低密度區(qū),CT示右股骨頭囊性占位,邊界清楚,內(nèi)可見鈣化點(diǎn)。臨床考慮為軟骨母細(xì)胞瘤而行病灶刮除術(shù),術(shù)后病灶組織送檢。
1.2 方法
1.2.1 組織學(xué):對3例手術(shù)切除標(biāo)本均行10%中性甲醛固定,乙醇梯度脫水,石蠟包埋,骨組織作脫鈣處理,4 μm切片,HE染色,光鏡觀察。
1.2.2 免疫組織化學(xué)采用 SP法:所用抗體 S-100、Vimentin、D2-40、CK、CD68均購自福州邁新公司。所有抗體濃度均為工作濃度。免疫組化具體步驟按照說明書進(jìn)行,并設(shè)有陰性對照。
2 結(jié)果
2.1 巨檢 例1,灰紅灰白色碎組織一堆,共約4.5 cm×3.5 cm×3.5 cm,部分呈肉芽組織樣,部分豆渣樣并有砂粒感,部分質(zhì)較硬作脫鈣處理。例2,灰紅色碎組織一堆,共3.5 cm×3.0 cm×2 cm,部分有砂粒感。例3,淺紅白色肉芽腫樣碎組織一小堆,共3 cm×2.5 cm×2.0 cm。部分為骨樣組織,作脫鈣處理。
2.2 鏡檢 例1,腫瘤細(xì)胞圓形或多邊形,細(xì)胞邊界清楚,胞質(zhì)輕度嗜酸性,部分胞質(zhì)透明。核圓形或卵圓形,部分細(xì)胞核可見較明顯的核溝;核分裂象罕見;腫瘤細(xì)胞豐富,呈彌漫片狀生長,細(xì)胞間可見散在的、核無明顯異型性的破骨巨細(xì)胞樣多核巨細(xì)胞(圖2、3)。細(xì)胞間可見粉紅色的軟骨基質(zhì),并有軟骨島形成(圖4);部分區(qū)域可見細(xì)胞胞膜鈣化形成所謂的“窗格樣”鈣化。例2,腫瘤細(xì)胞中等大小,為圓形、多角形,少部分短梭形,胞質(zhì)多較豐富、紅染,部分胞質(zhì)稍透明;核圓形或卵圓形,核內(nèi)含有一個(gè)或多個(gè)小的核仁,核分裂象罕見,無病理性核分裂。腫瘤細(xì)胞呈彌漫片狀生長,瘤細(xì)胞間可見隨意分布的破骨巨細(xì)胞樣巨細(xì)胞;可見軟骨基質(zhì)及軟骨島,并可見“窗格樣”鈣化及散在的藍(lán)染的不規(guī)則鈣化灶(圖5),部分血管壁也可見鈣鹽沉著。例3,腫瘤細(xì)胞呈彌漫片狀生長,細(xì)胞圓形、卵圓形或多角形、梭形,胞漿豐富,胞界清楚,細(xì)胞核圓、卵圓形、并可有分葉狀,可見核溝,可有輕度的多形性,核分裂象罕見,并可見破骨巨細(xì)胞樣多核巨細(xì)胞,局部見有少量“窗格樣”鈣化(圖6)。免疫表型(圖7~10):3個(gè)病例均表達(dá)腫瘤細(xì)胞S-100(+)、Vimentin(+)、D2-40(+)、CD68(-),破骨巨細(xì)胞樣多核巨細(xì)胞CD68(+),例1、例2 CK-pan(-),而例3在未經(jīng)脫鈣處理的標(biāo)本切片中有CK-pan弱陽性表達(dá)。診斷:3個(gè)病例均診斷為軟骨母細(xì)胞瘤。
3 討論
3.1 一般情況 軟骨母細(xì)胞瘤是一種少見的骨良性腫瘤,約占良性骨原發(fā)性腫瘤的1% ~2%[2,3],好發(fā)年齡為11~20歲。骨骼的任何部位都可受累,主要見于長骨末端,如股骨、脛骨及肱骨等處,也可見于肋骨、顳骨及盆骨等扁骨。好發(fā)部位為骺板軟骨尚未消失的骨骺端,特別是股骨遠(yuǎn)端、肱骨近端及脛骨近端[3]。男性多于女性,男女發(fā)病率約2∶1。臨床上常表現(xiàn)為局部疼痛,個(gè)別患者可出現(xiàn)劇痛,可持續(xù)數(shù)年,部分患者伴有局部脹痛、關(guān)節(jié)僵硬、活動障礙、跛行等癥狀,嚴(yán)重者可出現(xiàn)病理性骨折。顳骨患者可伴有進(jìn)行性聽力下降、耳鳴、眩暈等癥狀。影像學(xué)表現(xiàn):軟骨母細(xì)胞瘤的影像學(xué)表現(xiàn)一般為中央型溶骨性病變,形成低密度囊性樣病灶,圓形或卵圓形,邊界清楚,有的在腫瘤周圍有薄層硬化帶,一般沒有骨膨脹或骨膜反應(yīng)。發(fā)生于手足骨及扁骨者可見膨脹性改變及骨膜反應(yīng)。腫瘤內(nèi)可出現(xiàn)細(xì)小的斑點(diǎn)狀鈣化或骨化影。同時(shí)累及骺及干骺部的腫瘤常見[1,4]。本組3例年齡為15~22歲,均發(fā)生于長骨末端,均有局部疼痛癥狀,影像學(xué)均表現(xiàn)為局部低密度囊腫樣病灶。
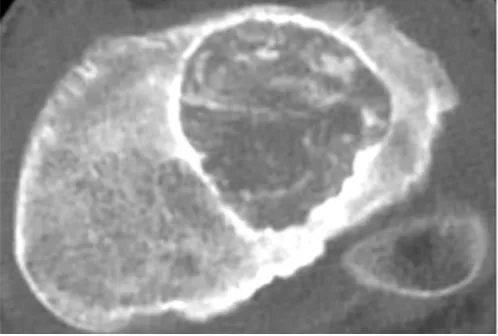
圖1 干骺后端外側(cè)可見低密度腫物,邊緣骨質(zhì)硬化,腫物內(nèi)可見多個(gè)砂粒狀鈣化灶

圖2 形態(tài)一致的軟骨母細(xì)胞呈彌漫片狀生長
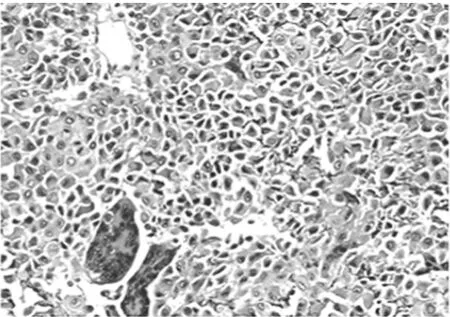
圖3 軟骨母細(xì)胞間可見隨意分布的破骨巨細(xì)胞樣多核巨細(xì)胞,部分細(xì)胞胞膜可見鈣化
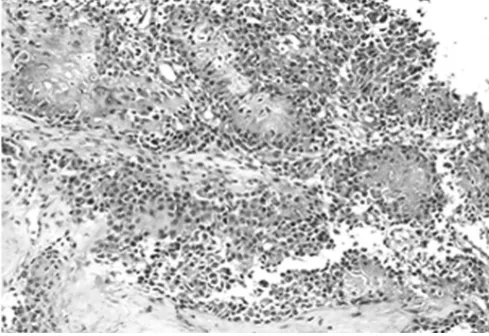
圖4 軟骨母細(xì)胞間可見粉紅色的軟骨基質(zhì),并形成軟骨島樣結(jié)構(gòu)
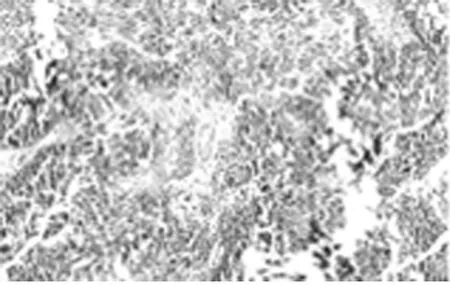
圖5 可見不規(guī)則的鈣化灶

圖6 局部見細(xì)胞胞膜鈣化,形成所謂的“窗格樣”鈣化

圖7 軟骨母細(xì)胞S-100核陽性

圖8 軟骨母細(xì)胞D2-40胞質(zhì)陽性

圖9 軟骨母細(xì)胞CK-pan胞質(zhì)弱陽性表達(dá)

圖10 破骨巨細(xì)胞樣多核巨細(xì)胞CD68胞質(zhì)陽性
3.2 病理學(xué)特征 大體特征 多為手術(shù)刮出標(biāo)本,棕褐色,部分灰白色或暗紅色呈肉芽組織樣,質(zhì)碎,可有砂粒感。部分患者術(shù)中所見類似動脈瘤樣骨囊腫結(jié)構(gòu)。鏡下特點(diǎn):鏡下見軟骨母細(xì)胞增生,細(xì)胞多中等大小,為圓形、卵圓形或多邊形,亦可為梭形,胞漿多豐富紅染,輕度嗜酸性,部分細(xì)胞胞漿可透明。細(xì)胞膜界限清楚。核圓形或卵圓形,可有核溝,并可呈分葉狀,還可呈郎格罕細(xì)胞樣[3]。核內(nèi)含有一個(gè)或數(shù)個(gè)小的或不明顯的核仁,核分裂象少見,但無病理性核分裂。有時(shí)部分瘤細(xì)胞有較明顯的異型性,核不規(guī)則增大或深染,但這并不意味著為惡性。瘤細(xì)胞常呈彌漫片狀分布,瘤細(xì)胞間可見隨意分布的碎骨細(xì)胞樣多核巨細(xì)胞,有時(shí)易誤診為骨巨細(xì)胞瘤。在軟骨母細(xì)胞周圍有粉紅色的軟骨基質(zhì)或顆粒狀鈣化,軟骨基質(zhì)可過渡為原始軟骨或骨。約35%的病例可見胞膜鈣化,形成特征性的“窗格樣鈣化”[5]。部分病例可伴有動脈瘤樣骨囊腫改變。本組3個(gè)病例腫瘤細(xì)胞均有軟骨母細(xì)胞特點(diǎn),3例均有不同程度的鈣化并出現(xiàn)“窗格樣”鈣化。
免疫表型 腫瘤細(xì)胞常表達(dá)vimentin及S-100陽性[6],其它抗原如細(xì)胞角蛋白也可表達(dá),最近有研究顯示腫瘤細(xì)胞也常表達(dá) D2-40 陽性[7],本組3 個(gè)病例均表達(dá) vimentin、S-100、及 D2-40陽性,其中例3也可見表達(dá)CK-pan陽性。軟骨分化不明顯的軟骨母細(xì)胞瘤S-100可以陰性。脫鈣也常可影響免疫組化結(jié)果,如本組病例3脫鈣的標(biāo)本CK-pan陰性,而未經(jīng)脫鈣處理的標(biāo)本CK-pan有弱陽性表達(dá)。
3.3 診斷與鑒別診斷 軟骨母細(xì)胞瘤依據(jù)典型的組織學(xué)特征及免疫組化檢查,并結(jié)合影像學(xué)表現(xiàn)一般可以確診。本病一般需與以下幾種疾病鑒別。(1)骨巨細(xì)胞瘤:骨巨細(xì)胞瘤與軟骨母細(xì)胞瘤均常發(fā)生于骨骺,X線也常表現(xiàn)有溶骨性改變,并可出現(xiàn)多核巨細(xì)胞。但前者發(fā)病年齡較晚,X線檢查局部常見膨脹,病灶周圍無硬化帶,病灶內(nèi)一般不見鈣化及骨化影。組織學(xué)上骨巨細(xì)胞瘤破骨細(xì)胞樣巨細(xì)胞多均勻分布,細(xì)胞可很大,核可達(dá)50~100個(gè)。基質(zhì)細(xì)胞界限不清,無胞膜鈣化,核常與巨細(xì)胞的核相似。而軟骨母細(xì)胞瘤巨細(xì)胞分布多不均勻,細(xì)胞較小,核多在10個(gè)以下,軟骨母細(xì)胞界限清楚,有時(shí)可見胞膜鈣化,并可有粉紅色的軟骨基質(zhì)。骨巨細(xì)胞瘤S-100常陰性,而軟骨母細(xì)胞瘤S-100常陽性。(2)軟骨肉瘤:軟骨肉瘤發(fā)病年齡高,大部分患者年齡>50歲,組織學(xué)上常呈分葉狀結(jié)構(gòu),常有大量的軟骨基質(zhì),細(xì)胞稀疏散在,瘤細(xì)胞周圍常形成陷窩。而軟骨母細(xì)胞瘤多發(fā)生于年青人,瘤細(xì)胞豐富,常呈彌漫片狀生長,細(xì)胞周圍無陷窩形成。X線檢查少部分軟骨母細(xì)胞瘤也可浸潤軟組織,但與軟骨肉瘤不同,軟骨母細(xì)胞瘤浸潤軟組織常形成境界清楚的結(jié)節(jié),且結(jié)節(jié)周圍常有薄層新骨形成。(3)動脈瘤性骨囊腫:約有1/3的軟骨母細(xì)胞瘤可見到類似動脈瘤樣骨囊腫的改變[4],當(dāng)囊腫大而實(shí)質(zhì)較小時(shí),容易誤診為單純性的動脈瘤樣骨囊腫。當(dāng)動脈瘤樣骨囊腫囊壁或囊壁周圍可見軟骨母細(xì)胞增生時(shí),應(yīng)考慮有軟骨母細(xì)胞瘤的可能,而S-100及D2-40等標(biāo)志有助于進(jìn)一步鑒別診斷。本組3個(gè)病例均有典型的軟骨母細(xì)胞瘤的組織特點(diǎn),免疫組化均表達(dá)vimentin、S-100及D2-40陽性,支持軟骨母細(xì)胞瘤診斷。
3.4 預(yù)后及治療 軟骨母細(xì)胞瘤為良性骨腫瘤,預(yù)后好。部分病例也可出現(xiàn)浸潤性生長或肺部轉(zhuǎn)移,轉(zhuǎn)移者多在肺內(nèi)形成孤立性病灶,外科手術(shù)可以治愈,極少數(shù)情況下轉(zhuǎn)移灶可為彌漫性的,可導(dǎo)致患者死亡。治療以手術(shù)為主,大多數(shù)病例可作病灶刮除或刮除后植骨,有骨皮質(zhì)破壞和軟組織浸潤者可作局部切除術(shù)。術(shù)后復(fù)發(fā)率為14% ~18%[8]。一般認(rèn)為化療及放療對本病無明顯的效果,且有惡變?yōu)檐浌侨饬龅奈kU(xiǎn)[9]。本組3病例均行病灶刮除及刮除后植骨術(shù),術(shù)后隨訪1~2年均未發(fā)現(xiàn)復(fù)發(fā)。
1 Bloem JL,Mulder JD.Chondroblastoma:a clinical and radiological study of 104 cases.Skeletal Radiol,1985,14:1-9.
2 Dahlin DC,Ivins JC.Benign chondroblastoma.A study of 125 cases.Caner,1972,30:401-413.
3 Springfield DS,Capanna R,Gherlinzoni F,et al.Chondroblastoma.A review of seventy cases.J Bone Joint Surg,1985,67:748-754.
4 Turcotte RE,Kurt AM,Sim FH,et al.Chondroblastoma.Hum Pathol,1993,24:944-949.
5 Kurt AM,Unni KK,Sim FH,et al.Chondroblastoma of bone,Hum Pathathol,1989,20:965-976.
6 Monda L,Wick MR.S-100 protein immunostaining in the differential diagnosis of chondroblastoma.Hum Pathol,1985,16:287-293.
7 Daugaard EN,Lise HC,Estrid HG.Markers aiding the diagnosis of chondroid tumors:an immunohistochemical study including osteonectin,bcl-2,cox-2,actin,calponin,D2-40(podoplanin),mdm-2,CD117(c-kit),and YKL-40.APMIS,2009,117:518-525
8 Christopher DM,F(xiàn)letcher K,Krishnan unni,F(xiàn)redrik Mertens著;程虹等譯.WHO軟組織與骨腫瘤病理學(xué)和遺傳學(xué)(2002).北京:人民衛(wèi)生出版社,2006.282-285.
9 Joshi DD,Anderson PM,Matsumoto J,et al.Metastatic chondroblastoma with elevated creatine kinase and paraneoplastic neurologic autoimmunity.J Pediatr Hematol Oncol,2003,25:900-904.

