雙黃連注射液HPLC指紋圖譜研究
王艷偉, 宋立言, 代雪平, 宋漢敏
(1.河南省食品藥品檢驗所,河南鄭州450003;2.鄭州大學臨床藥理研究所,河南 鄭州450052)
雙黃連注射液是由金銀花、黃芩、連翹制成的現代中藥制劑,具有清熱解毒、清宣風熱的作用。臨床上用于外感風熱引起的發熱、咳嗽、咽痛。適用于病毒及細菌感染的上呼吸道感染、肺炎、扁桃體炎、咽炎等[1]。但隨著使用范圍日漸擴大,應用人群增加,加之臨床應用不當及生產工藝不穩定多方面因素,引起的不良反應例數也相應增加,甚至有致人死亡的個案[2-3]。為進一步規范雙黃連注射液的生產,提高其質量,減少不良反應的發生,根據國家食品藥品監督管理局《中藥注射劑安全性再評價基本技術要求》,本實驗建立了雙黃連注射液的HPLC指紋圖譜,為雙黃連注射液的全面質量控制提供依據。
1 儀器與試藥
1.1 儀器 Waters Alliance 2695系統,含四元梯度泵、在線脫氣機、自動進樣器、柱溫箱以及Waters Empower色譜工作站,Waters二極管陣列檢測器(PDA 996);Phenomenex Luna C18(2)100A(4.6 mm×250 mm,5 μm)色譜柱。
1.2 試劑與樣品 綠原酸對照品(批號110753-200413,中國藥品生物制品檢定所),咖啡酸對照品(批號110885-200102,中國藥品生物制品檢定所),黃芩苷對照品(批號110715-200514,中國藥品生物制品檢定所),黃芩素對照品(批號111595-200604,中國藥品生物制品檢定所);甲醇、乙腈為色譜純(Merck公司),磷酸為分析純(天津市風船化學試劑科技有限公司),水為超純水;黃芩、金銀花、連翹藥材由河南福森藥業有限公司提供,并經河南省食品藥品檢驗所雷留成副主任藥師鑒定;注射用黃芩提取物、注射用金銀花連翹提取物由河南福森藥業有限公司提供;雙黃連注射液由河南福森藥業有限公司提供(批號:0910001,0910002,0910003,0910004,0910005,0910006,0910009,0910010,0910011,0910012,0910016,0910018,0910019,0910020)。
2 方法與結果
2.1 色譜條件 雙黃連注射液:Phenomenex Luna C18(2)100A 色譜柱:(250 mm ×4.6 mm,5 μm);流動相為乙腈(A)-0.5%磷酸溶液(B)進行梯度洗脫,0 ~5 min,5%A ~5%A,5 ~15 min,5%A ~10%A,15 ~20 min,10%A ~14%A,20 ~50 min,14%A~18%A,50 ~70 min,18%A ~25%A,70 ~85 min,25%A ~30%A,85 ~110 min,30%A ~50%A,體積流量1 mL/min;檢測波長350 nm;柱溫40℃。理論板數按綠原酸峰計算應不低于6000。
黃芩藥材、注射用黃芩提取物、金銀花藥材、注射用金銀花連翹提取物色譜條件同上,連翹藥材檢測波長為280 nm,其余條件同上。
2.2 對照品溶液的制備 精密稱取綠原酸對照品適量,置棕色量瓶中,加50%甲醇制成每1 mL含60 μg的溶液,即得(10℃以下保存)。
2.3 供試品溶液的制備
2.3.1 黃芩 取本品粉末約0.5 g,精密稱定,置具塞錐形瓶中,精密加入甲醇25 mL,稱定質量,加熱回流2 h,放冷,再稱定質量,用甲醇補足減失的質量,搖勻,濾過,取續濾液,即得。
2.3.2 注射用黃芩提取物 取本品約50 mg,精密稱定,置25 mL量瓶中,加水20 mL,超聲處理10 min,振搖并滴加0.1 mol/L氫氧化鈉溶液使完全溶解(pH值不大于7.0),加水稀釋至刻度,搖勻,濾過,取續濾液,即得。
2.3.3 金銀花 取本品粉末約1 g,精密稱定,置具塞錐形瓶中,精密加入甲醇25 mL,稱定質量,加熱回流2 h,放冷,再稱定質量,用甲醇補足減失的質量,搖勻,濾過,取續濾液,即得。
2.3.4 連翹 取本品粉末約1 g,精密稱定,置具塞錐形瓶中,精密加入水50 mL,稱定質量,加熱回流4 h,放冷,再稱定質量,用水補足減失的質量,搖勻,濾過,取續濾液,即得。
2.3.5 注射用金銀花連翹提取物 精密吸取本品2 mL,置100 mL量瓶中,加50%甲醇稀釋至刻度,搖勻,即得。
2.3.6 雙黃連注射液 取本品,搖勻,濾過,作為供試品溶液。
2.4 樣品測定 精密吸取對照品溶液與供試品溶液各10 μL,注入液相色譜儀,記錄110 min色譜圖。將色譜圖導入中藥色譜指紋圖譜相似度評價系統,與對照指紋圖譜相比較,計算相似度。
3 方法學考察
3.1 精密度試驗 取同一批次供試品溶液(批號:0910001),連續進樣6次,測定指紋圖譜。結果表明,各色譜峰相對保留時間的RSD均在0.2%以內,相對峰面積的RSD均在5%以內,有較高的相似度(均在0.95以上),精密度良好。
3.2 穩定性試驗 取同一批次供試品溶液(批號:0910001),分別在第 0、2、4、6、8、10 h 進樣,測定指紋圖譜。結果表明,各色譜峰相對保留時間的RSD均在0.2%以內,相對峰面積的RSD均在5%以內,有較高的相似度(均在0.95以上),供試品溶液在10 h內基本穩定。
3.3 重復性試驗 取同一批次樣品(批號:0910001),平行制備6份供試品溶液,測定指紋圖譜。結果表明,各色譜峰相對保留時間的RSD均在0.2%以內,相對峰面積的RSD均在5%以內,有較高的相似度(均在0.95以上),重復性良好。
4 雙黃連注射液指紋圖譜的建立
測定本品14批樣品的指紋圖譜,將其結果導入中藥色譜指紋圖譜相似度評價系統(2004,1.0A版),以平均數法生成對照圖譜,評價各樣品的相似度,結果見圖1、表1(屏蔽12號黃芩苷峰)。確定特征峰14個,統計了各批總出峰數,特征峰數與總出峰數的百分比及特征峰與總出峰面積的百分比。見表2。
5 雙黃連注射液對照指紋圖譜中色譜峰的確認
取大黃酚、大黃素甲醚、咖啡酸、綠原酸、連翹苷、黃芩苷、蘆丁、金絲桃苷、槲皮苷、木犀草苷、木犀草素、槲皮素、黃芩素、漢黃芩素、漢黃芩苷、隱綠原酸、新綠原酸、異綠原酸A、異綠原酸B、異綠原酸C、連翹酯苷A等對照品,分別配制成適當質量濃度的對照品,按照指紋圖譜測定方法,測定對照品色譜圖,并與對照指紋圖譜中的相關峰進行光譜圖比對,最后確認對照指紋圖譜中1號峰為新綠原酸,2號峰為綠原酸,3號峰為隱綠原酸,4號峰為咖啡酸,7號峰為連翹酯苷A,9號峰為異綠原酸B,10號峰為異綠原酸A,11號峰為異綠原酸C,12號峰為黃芩苷,14 號峰為黃芩素[4]。

表1 14批雙黃連注射液指紋圖譜相似度結果Tab.1 The results of the 14 batches of Shuanghuanglian Injection Similarity analysis
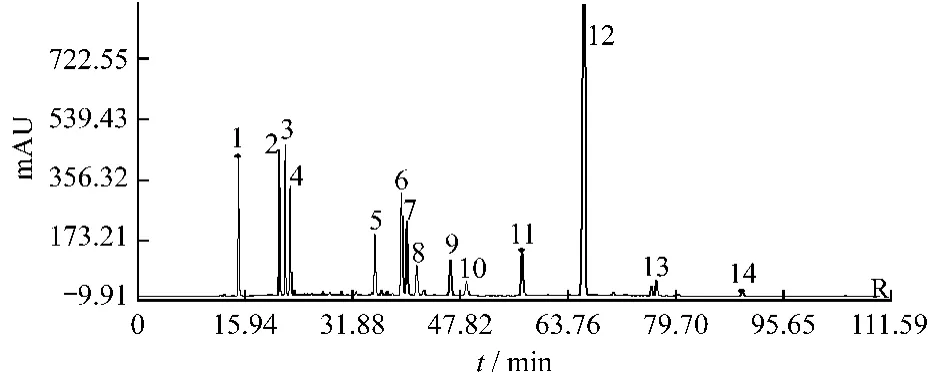
圖1 雙黃連注射液對照指紋圖譜Fig.1 The HPLC fingerprint of Shuanghuanglian Injection
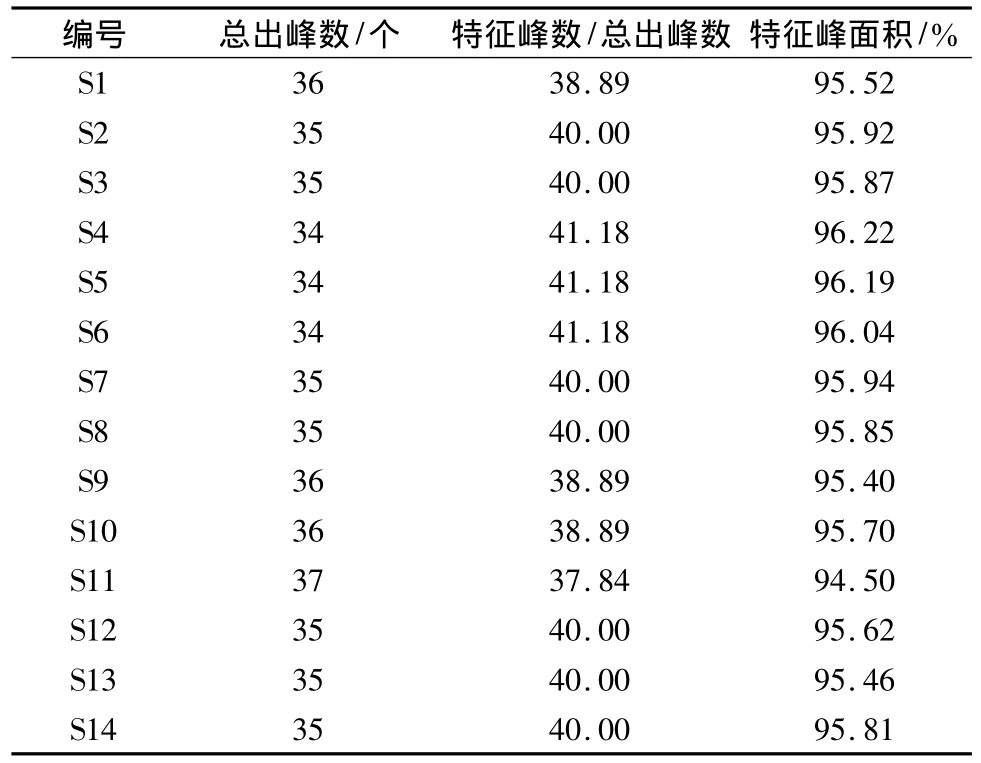
表2 14批雙黃連注射液的總出峰數及其特征峰所占比例Tab.2 The total numbers of the peaks of Shuanghuanglian Injection and its proportion of the characteristic peaks
6 雙黃連注射液對照指紋圖譜中特征峰的歸屬
取黃芩、黃芩提取物、金銀花、連翹、金銀花連翹提取物制成適當濃度的供試品溶液,按照指紋圖譜測定方法,測定各自色譜圖,并與對照指紋圖譜中的相關峰進行光譜圖比對,最后確認對照指紋圖譜中1號峰為新綠原酸,2號峰為綠原酸,3號峰為隱綠原酸,9號峰為異綠原酸B、10號峰為異綠原酸A、11號峰為異綠原酸C,上述峰均來自金銀花;4號峰為咖啡酸,來自金銀花和連翹;7號峰為連翹酯苷A,與5、6號峰均來自連翹;12號峰為黃芩苷,14號峰為黃芩素,與8號、13號峰均來自黃芩[5](圖2~圖6)。
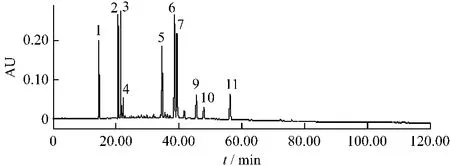
圖2 注射用金銀花連翹提取物指紋圖譜Fig.2 The HPLC fingerprint of extract of Loniceral japonicae Flos and Forsythiae Fructus
7 討論
7.1 洗脫系統的選擇 試驗過程中共選擇了甲醇-0.5% 冰醋酸溶液[6]、乙腈 - 0.5% 冰醋酸溶液[7]、乙腈 -0.5%磷酸溶液等3種流動相系統,結果表明乙腈-0.5%磷酸溶液分離效果最好。

圖3 連翹指紋圖譜Fig.3 The HPLC fingerprint of Forsythiae Fructus
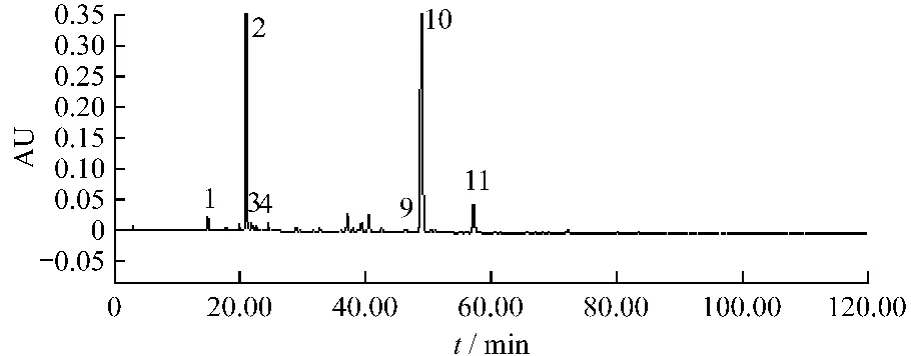
圖4 金銀花指紋圖譜Fig.4 The HPLC fingerprint of Lonicerae japonicae Flos
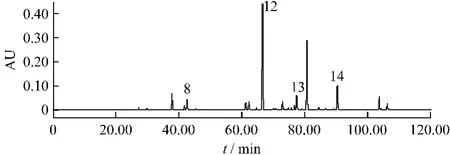
圖5 黃芩指紋圖譜Fig.5 The HPLC fingerprint of Scutellariae Radix
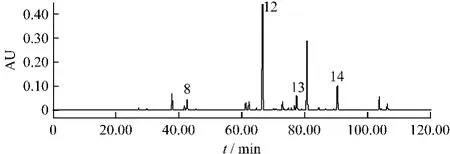
圖6 注射用黃芩提取物指紋圖譜Fig.6 The HPLC fingerprint of Scutellariae Radix extract
7.2 檢測波長的選擇 試驗過程中,波長為254 nm和280 nm下,黃芩苷峰過大,其他峰相對峰面積不穩定,不易分開,波長350 nm下各峰比例良好,峰與峰間距良好,易于分辨,故選擇350 nm為測定波長。
7.3 柱溫的選擇 為了保持色譜分析的一致性,設定柱溫來控制不同實驗環境下的色譜分析,試驗中考察了25℃、30℃、35℃、40℃柱溫下的分離情況,結果表明,柱溫40℃時分離效果較好。
7.4 實驗中發現雙黃連注射液指紋圖譜與注射用金銀花連翹提取物指紋圖譜存在一定差異,原因可能是雙黃連注射液制備工藝中用40%氫氧化鈉溶液調pH值,在加熱滅菌及放置過程中使綠原酸同系物及連翹酯苷同系物發生了水解反應所致,具體反應機理尚需進一步研究。
7.5 實驗中確定了14個特征色譜峰,較為全面的反映了雙黃連注射液藥理作用的物質基礎,為加強雙黃連注射液質量控制提供了依據。但雙黃連注射液有效成分復雜[8-12],尚需進一步研究其藥理、毒理的物質基礎和作用機理,確定雙黃連注射液臨床療效和不良反應產生的根源,為臨床合理用藥提供科學依據。
[1]中華人民共和國衛生部藥典委員會.中華人民共和國衛生部藥品標準:中藥成方制劑第十一冊[S].1996:38.
[2]劉文濤.雙黃連注射液的不良反應[J].醫藥導報,2003,22(增):142-143.
[3]張志強.雙黃連注射液不良反應概述[J].實用中醫藥雜志,2003,19(6):334-335.
[4]郭 潔,宋殿榮,王躍飛,等.雙黃連凍干粉HPLC指紋圖譜特征色譜峰的歸屬研究[J].天津中醫藥,2009,26(6):497-499.
[5]張 潔,馬百平,趙 陽,等.雙黃連粉針劑指紋圖譜中特征色譜峰的組成藥味歸屬及定性[J].中成藥,2005,27(12):1365-1369.
[6]李 方,姜文紅,劉麗娟,等.注射用雙黃連(凍干)指紋圖譜的建立及其在質量控制中的應用[J].中成藥,2007,29(8):1196-1198.
[7]王新宏,安 睿,鄒 云,等.數字化色譜指紋譜技術在雙黃連制劑質量及藥材鑒定中的應用[J].中草藥,2002,33(2):115-118.
[8]鈕旭升,閆海霞,高慧媛,等.雙黃連粉針中抗病毒部位活性與化學成分研究[J].中國現代中藥,2006,8(1):16.
[9]劉 悅,宋少江,徐綏緒,等.連翹化學成分研究[J].沈陽藥科大學學報,2003,20(2):101.
[10]高玉敏,王名洲,王建平,等.金銀花化學成分的研究[J].中草藥,1995,26(11):568.
[11]楊得坡,張小莉.中藥黃芩揮發性化學成分的研究[J].中藥新藥與臨床藥理,1999,10(4):234.
[12]呂本強.注射用雙黃連粉針劑物質基礎研究[D].廣州:第一軍醫大學,2007.