慢性肝病患者血脂和膽堿酯酶檢測的臨床意義
薛宏麗 單 洪 秦麗莉 馮國和
1.遼寧省人民醫院感染科,遼寧沈陽 110016;2.中國醫科大學附屬盛京醫院感染科,遼寧沈陽 110004
肝臟是人體最重要的代謝器官,在蛋白質、糖、脂類、維生素和激素代謝以及生物轉化等方面起著重要的作用。當肝臟發生病變時,必然會影響脂類、酶類等物質的代謝,導致血液中脂類的濃度和膽堿酯酶的活性發生變化。該研究收集2011年10月—2012年10月該院30例測定原發性肝癌等慢性肝病患者血清中血脂水平和膽堿酯酶活性的變化,進行統計學分析,旨在探討其在病毒性肝炎、肝硬化、原發性肝癌的診斷和治療中的臨床價值。
1 資料與方法
1.1 一般資料
該院住院的原發性肝癌30例,均符合原發性肝癌診斷標準,其中男25例,女5例,年齡44~78歲,平均58歲;肝炎后肝硬化患者30例,系同期住院患者,男性20例,女性10例,年齡42~74歲,平均55.9歲,診斷符合肝硬化的診斷標準;慢性病毒性肝炎30例,男性21例,女性9例,年齡 35~70歲,平均 51.3歲,診斷符合2010年由中華醫學會肝臟病學分會公布的《慢性乙型肝炎防治指南》;健康對照組30例,來自門診健康體檢者,男性20例,女性10例,年齡38~76歲,平均52.3歲。所有檢查對象均排除其他影響脂質代謝的疾病,無口服降血脂藥物史。
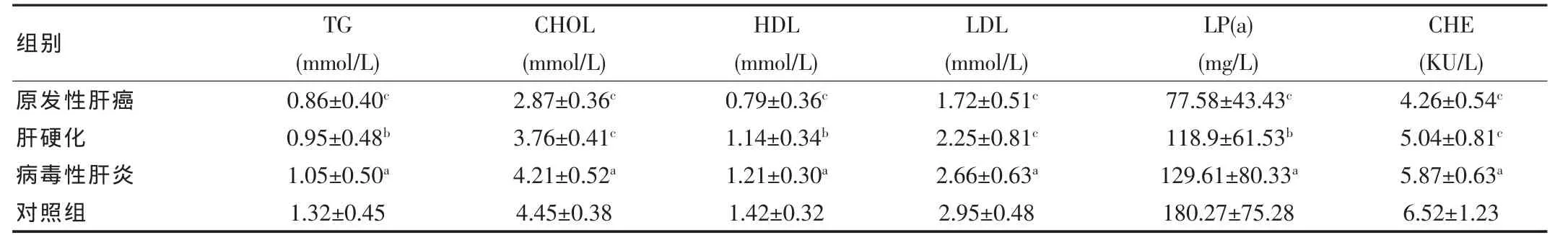
表1 各組患者血脂及膽堿酯酶檢測結果
1.2 研究方法
受試者清晨空腹經肘靜脈采血2 mL,分離血清后,采用全自動生化分析儀測定血清 TG、CHOL、HDL、LDL、 LP(a)、CHE,試劑采用羅氏試劑。
1.3 統計方法
所有有數據采用SPSS17.0軟件分析,檢測數據計量資料以均數±標準差(±s)表示,對組間指標的比較采用兩樣本均數比較的t檢驗。
2 結果
①慢性肝病患者和正常人群的 TG、CHOL、HDL、LDL、LP(a)水平差異有統計學意義(P<0.05或P<0.01或P<0.001),見表1。TG、CHOL、HDL、LDL、LP(a)隨著肝功能障礙嚴重程度的增加而下降,以CHOL下降最為顯著。見圖1。
②慢性肝病患者和正常人群的CHE水平差異有統計學意義(P<0.05或P<0.01或P<0.01)(表1)。CHE活力隨著肝功能障礙嚴重程度的增加而下降。肝硬化和肝癌患者的CHE活力與正常人群相比差異最顯著(P<0.01)。見圖1。
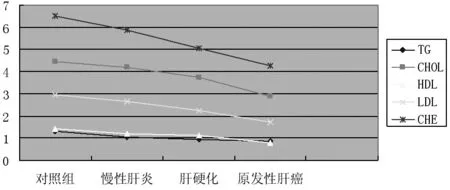
圖1 不同肝病血脂和膽堿酯酶變化趨勢圖
3 討論
肝臟是脂類物質代謝的中樞器官,在脂代謝中具有攝取、轉運、合成、轉化及降解作用。血脂主要包括膽固醇、甘油三酯和類脂(磷脂、糖脂、固醇、類固醇),主要在肝臟合成,廣泛存在于人體中。血液中以脂蛋白形式存在,是人體生命細胞代謝的必需物質[1],因此對于血脂水平的檢測至關重要。最近研究表明,血脂檢測在臨床診斷中的價值已不僅僅限于心血管病的研究,對肝臟疾病診斷的臨床價值更具意義。研究發現肝病患者肝細胞腫脹、變性、壞死,特別是肝硬化和肝癌時,肝細胞對一些參與脂代謝的酶、激素和影響脂代謝的蛋白類物質的代謝發生變化,從而引起脂類代謝紊亂[2-3],因此脂類代謝又可反映肝功能受損情況,是反映肝實質性損傷的一個重要指標。
血清CHE是一類催化酰基膽堿水解的酶類,人體內的CHE分為乙酰膽堿酯酶(ACHE)和丁酰膽堿酯酶(BuCHE)兩種。ACHE來源于神經細胞和新生紅細胞,BuCHE主要來源于肝臟,在血清里的活性取決于肝細胞的正常功能,CHE不受外源性影響,合成后立即釋放至血液中,因此,血液中CHE的濃度能夠很好地反映肝臟細胞的合成速率,甚至比白蛋白在反應肝臟合成功能方面更加靈敏[4]。當肝細胞損傷時,肝細胞變性壞死,間質炎癥細胞浸潤,纖維組織和結締組織增生,導致CHE合成減少,使血清CHE活力下降,其下降程度與病情的嚴重程度相平行[5]。
該研究表明,和對照組比較,慢性肝炎、肝硬化及原發性肝癌患者血清 TG、CHOL、HDL、LDL、LP(a)、CHE 水平均下降,下降水平差異有統計學意義(P<0.05或P<0.01或P<0.001),血脂水平和CHE活力隨著肝功能障礙嚴重程度的增加而下降,其中以CHOL、CHE和LDL下降最明顯,原發性肝癌比肝硬化CHOL、HDL、LDL、LP(a)水平低,差異有統計學意義。 分析CHOL 顯著下降的原因如下:①可能與肝臟嚴重損傷時合成膽固醇所必需的羥甲基戊二酸單酰CoA(HMGCoA)還原酶合成減少有關。研究發現,HMGCoA還原酶基因的啟動子中含有類似于SRE-1的膽固醇調節原件 (SRE),SRE-1可以通過調節LDLR基因,HMGCoA合酶基因的翻譯,控制細胞外源性膽固醇的攝取量和內源性膽固醇的合成速率,調節細胞內CHOL的含量[6];②肝細胞受損,導致磷脂酰膽堿膽固醇酯酰轉移酶(LCAT)產生減少或活性下降,以及體內胰島素、胰高血糖素、甲狀腺激素等發生變化,使血脂及載脂蛋白合成減少和降解增多;③肝硬化和肝癌時低蛋白血癥、營養不良影響膽鹽代謝;小腸細菌過度生長,膽固醇向膽汁酸的轉化率增加;禁食及饑餓時,CoA、ATP、NADPH+-H+不足均導致CHOL降低。CHOL的顯著下降能夠準確反映肝損傷的嚴重程度。最近有研究報道[7],在失代償期慢性肝病患者體內的CHOL水平與Chlid-Pugh評分有關聯,CHOL有可能成為第六個Chlid-Pugh評分的指標,因此,CHOL可以評估肝臟的儲備功能,有助于估計預后。有研究表明[1]原發性肝癌中發生轉移的患者較未轉移組CHOL、TG、HDL等血脂指標下降明顯,因此血脂檢測亦有助于判定原發性肝癌是否發生轉移。該研究中,CHE活力隨著肝病的進展而下降,差異有統計學意義。由于CHE不受外源性因素的影響且對肝功能變化反映靈敏,因此可更加客觀地反映肝功能損傷程度,尤其是反映肝臟的合成能力方面具有重要的臨床意義。
LP(a)是由ApoA和ApoB及類似LDL的脂質核心組成,主要由肝臟合成,肝硬化和肝癌時由于白蛋白和ApoB合成減少,導致LP(a)水平明顯下降[7],與該研究的結果相一致。但有研究發現在乳腺癌、結腸癌等患者的 LP(a)升高,提示LP(a)與腫瘤細胞的活動有關[9]。也有研究發現在肝癌患者中出現LP(a)升高,并隨著肝癌腫塊直徑的增大而增高,提示肝癌細胞同樣可產生大量 LP(a)[10]。
影響肝病患者血脂水平的因素除了肝臟的功能狀態外,還與感染病毒的類型、病毒的基因型以及抗病毒藥物治療的效果有關[11-12]。大量研究證明丙型肝炎病毒本身是誘發血脂異常的因素之一[11,13]。國內有報道抗病毒治療后隨著肝功能的改善血脂水平除TG外均有顯著性升高[6]。
綜上所述,血清 TG、CHOL、HDL、LDL、LP(a)和 CHE 水平隨著肝病病情的進展而下降,與正常人群相比差異有統計學意義。監測肝病患者的血脂和CHE水平,可反映肝功能損害程度,對肝硬化患者是否存在惡變可有一定的提示作用,對原發性肝癌與轉移性肝癌的鑒別和診斷具有參考價值[14],對臨床療效觀察、判斷預后及腫瘤復發具有重要意義。
[1]龍顯科,唐任光,黃宏全.肝癌患者血清血脂和膽堿酯酶檢測水平分析[J].實用醫技雜志 ,2007,14(12):1574-1575.
[2]T Acke F,Schoffski P,Trautwein C,et al.Tissue factor and thrombomodu lin levels are correlated with stage of cirrhosis in patients with liver disease[J].Blood Coagul Fibrinolysis,2001,12(7):539-545.
[3]Jiang J,Nilsson-Ehle P,Xu N.Influence of liver cancer on lipid and lipoprotein metabolism[J].Lipids Health Dis,2006,5:4.
[4]陳雅萍,李燕.肝病患者血脂、膽堿酯酶檢測的臨床價值[J].中國中醫藥咨訊,2011,3(14):126-127.
[5]朱建一,聞平.血清膽堿酯酶和前白蛋白對肝臟合成功能檢測的意義[J].臨床檢驗雜志,2004,22(6):458.
[6]盧羅生.抗病毒治療對乙肝患者血脂水平的影響[J].熱帶醫學雜志,2008,8(5):474-476.
[7]Abbasi A,Bhutto AR,Butt N,et al.Serum cholesterol:could it be a sixth parameter of Child-Pugh scoring system in cirrhotics due to viral hepatitis[J].Aug,2012,22(8):484-487.
[8]Alessandri C,Basili S,Maurelli M,et al.Relationship between lipoprotein(a)levels in serum and some indices of protein synthesis in liver cirrhosis[J].Clin chim Acta,1994,224:125-129.
[9]Wright LC,Sullivan DR,Muller M,et al.Elevated apolopoprotein(a)levels in cancer patients[J].Int J Cancer,1989,43:241-244.
[10]何燕,周伏喜.原發性肝癌患者血脂測定的臨床意義[J].中國現代醫學雜志,2002,12(17):86-88.
[11]Petit JM,Benichou M,Duvillard L,et al.Hepatitis C virus-associated hypobetalipoproteinemia is correlated with plasma viral load,steatosis and liver fibrosis[J].Am J Gastroenterol,2003,98(5):1150-1154.
[12]Serfaty L,Andreani T,Giral P,et al.Hepatitis C virus induced hypobetalipoproteinemia:a possible mechanism for steatosis in chronic hepatitis C[J].J Hepatol,2001,34(3):428-434.
[13]李蘊銣,凌 偉,陳鳳新,等.慢性丙型肝炎患者脂類代謝與丙型肝炎病毒復制以及肝臟病理的關系[J].世界華人消化雜志,2010,18(17):1820-1823.
[14]金雷,朱峰,秦錫虎.原發性肝癌患者血脂檢測的臨床意義[J].中國醫師進修雜志,2011,34(10)39-40.