低體質指數對慢性阻塞性肺疾病急性加重期患者氣道阻塞及高凝狀態的預警作用研究
李偉國,劉 紅,王 靜
慢性阻塞性肺疾病(chronic obstructive pulmonary disease,COPD)患病率和病死率逐年升高,已成為全球范圍內的重要公共衛生問題。隨著肺功能的逐步下降,常出現體質指數(body mass index,BMI)、凝血功能的改變及全身各系統慢性損傷。COPD急性加重期(acute exacerbation of chronic obstructive pulmonary disease,AECOPD)患者普遍存在氣道阻塞及BMI的改變,其血漿D-二聚體水平明顯高于正常,提示機體處于高凝狀態[1-4],具體機制目前尚不清楚。關于BMI對氣道阻塞的影響仍存在較大爭議,且兩者對D-二聚體水平有無預測作用仍缺乏相應研究及報道。第一秒用力呼吸容積占預計值百分比(forced expiratory volume in one second%,FEV1%pre)是簡單有效且可信的氣道阻塞評定方法,通常聯合第一秒用力呼吸容積/用力肺活量(FEV1/FVC)對COPD嚴重程度進行分期,D-二聚體常作為凝血功能紊亂的早期靈敏指標。本研究通過對AECOPD患者不同BMI組間FEV1%pre及FEV1/FVC進行比較,研究BMI對氣道阻塞的影響;同時分析兩者對D-二聚體水平預測作用,從而對AECOPD患者的機體高凝狀態起到一定的預警作用。
1 對象與方法
1.1 研究對象 收集2011年11月—2012年6月在鄭州大學第一附屬醫院住院治療的AECOPD患者,入選標準依據2011年COPD全球倡議(global initiative for chronic obstructive pulmonary disease,GOLD)關于COPD定義[5]。并排除冠心病、糖尿病、支氣管擴張、肺栓塞、靜脈血栓形成、全身任何部位腫瘤、自身免疫性疾病等對D-二聚體值影響較大的疾病。
1.2 研究方法 將符合上述標準的受試者按BMI高低分為低體質量組(BMI<18.5 kg/m2)、正常體質量組(18.5 kg/m2≤BMI<24 kg/m2)及超重組(BMI≥24 kg/m2),比較不同分組間FEV1%pre及FEV1/FVC,同時分析BMI及FEV1%pre對D-二聚體的影響。
1.3 指標測量 BMI:受試對象身穿薄衣,赤足測量身高及體質量,根據體質量/身高2計算BMI值;肺功能:采用耶格肺功能儀(德國生產)測量吸入支氣管舒張劑后患者FEV1/FVC及FEV1%pre;D-二聚體測量:入院24 h內抽取所有受試對象肘正中靜脈血,利用全自動血凝分析儀檢測D-二聚體數值。
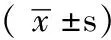
2 結果
2.1 一般資料 共收集136名AECOPD患者,平均年齡為(64±11)歲,最小40歲,最大87歲,男106名,女30名,三組患者的一般資料見表1。
2.2 三組FEV1%pre及FEV1/FVC比較 低體質量組與正常組比較,FEV1%pre差異有統計學意義(q=7.49,P=0.020);FEV1/FVC差異有統計學意義(q=10.20,P=0.031)。低體質量組與超重組比較FEV1%pre差異有統計學意義(q=7.97,P=0.009);FEV1/FVC差異有統計學意義(q=16.90,P=0.001)。正常體質量組與超重組FEV1%pre及FEV1/FVC差異無統計學意義(P>0.05)。見表2。
2.3 三組間D-二聚體比較 低體質量組D-二聚體水平為(0.44±0.23)mg/L,正常組為(0.33±0.24)mg/L,超重組為(0.24±0.11)mg/L,差異有統計學意義(F=3.264,P=0.038);低體質量組D-二聚體水平高于超重組,差異有統計學意義(q=7.642,P<0.05);低體質量組與正常組,正常組與超重組之間D-二聚體差異無統計學意義(P>0.05)。
2.4 BMI對D-二聚體的預測作用 通過多重線性回歸分析對D-二聚體值進行預測,身高、體質量、FEV1/FVC因其與BMI及FEV1%pre的高度共線性,未列入分析對象;在表1所列出的各項因素中,BMI是D-二聚體最主要的預測因素(P<0.05),發病年齡及FEV1%pre對D-二聚體值無預測作用(P>0.05);BMI解釋了D-二聚體水平的18%(R2=0.18,見表3)。

表1 三組患者一般資料的比較
注:*為χ2值,余檢驗統計量值為F值;BMI=體質指數
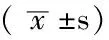
表2 三組患者FEV1%pre及FEV1/FVC比較
注:FEV1%pre=第一秒用力呼吸容積占預計值百分比,FEV1/FVC=第一秒用力呼氣容積/用力肺活量
表3 BMI及FEV1%pre對D-二聚體影響的多重線性回歸分析
Table3 Multiple linear regression analysis of effects of BMI and FEV1%pre on D-dimer

模型非標準化系數β值 標準誤差標準系數試用版t值P值常量 0 7760 146 5 3320 000BMI-0 0150 006-0 284-2 4740 016FEV1%pre-0 0030 001-0 255-2 1440 056發病時間 0 0010 003 0 057 0 4890 627
3 討論
3.1 BMI對氣道阻塞的影響 COPD患者由于慢性缺氧,普遍存在營養不良,主要表現為體質量減輕,呼吸肌萎縮,收縮力下降[6-7],不可避免的加重氣道阻塞。陳國忠等[8]認為穩定期COPD患者的氣道阻塞和全身炎性反應與BMI下降密切相關;Vrieze等[9]關于骨質疏松的研究發現,機體質量減輕及游離脂肪酸含量的降低是骨質疏松的主要危險因素,尤其見于GOLD 4期患者,其機制可能與AECOPD患者易并發全身炎性反應、體力活動限制及長期吸入皮質醇有關[10],骨質疏松反過來又進一步降低BMI,損害肺功能,三者相互作用,形成惡性循環。提高BMI可增加呼吸肌營養,改善骨質疏松,增加FEV1%pre及FEV1/FVC,進而改善氣道阻塞。
與之相反,有報道稱肥胖易降低呼吸系統順應性,增加呼吸肌負荷和氧耗,從而引起呼吸系統損傷,加重氣道阻塞,引起肺功能下降,增加呼吸道相關癥狀[11-12],與非肥胖患者相比,肥胖患者易出現呼吸肌強度及張力損傷,最大吸氣壓力下降,胸壁順應性降低,引起肺容量降低[11]。BMI通常與體內脂肪含量正相關,而過多的腹部脂肪可以改變胸壁壓力狀態,限制膈肌移動,從而妨礙肺正常擴張,促進外周氣道閉塞[10]。另外,肥胖是哮喘發作的危險因素之一,過多的脂肪組織及其在機體分布狀態及局部炎性反應均可引起肺功能降低,加重氣道阻塞,此現象也見于兒童患者[6,13-14]。
本研究發現,低體質量組平均FEV1%pre及FEV1/FVC分別為37%、41%,明顯低于正常體質量組54%、52%和超重組57%、58%,BMI值與FEV1%pre及FEV1/FVC之間正相關,BMI降低可加重氣道阻塞,與其他研究相符[8-10]。Fukahori等[10]認為,BMI不僅與機體脂肪數量有關,也與肌肉組織尤其是呼吸肌組織數量相關,由于BMI僅僅簡單的計算體質量與身高平方比值,不能有效區分機體脂肪含量、分布狀況及肌細胞數量及強度,單單BMI并不能有效預測肺功能狀況。Scott等[15]研究了哮喘患者脂肪數量、瘦素數量在身體各部位分布情況與肺功能的關系,指出女性患者軀干以上脂肪組織含量與肺功能負相關,男性患者軀干瘦素水平與肺功能正相關,肌肉組織尤其呼機肌是肺功能的保護性因素,而脂肪量為肺功能危險因素,相關研究在AECOPD患者中較為少見。
3.2 BMI對發病時間的影響 Sava等[16]研究發現,雖然BMI與肺功能呈正相關,然而肥胖患者更易出現呼吸困難、活動耐力下降等癥狀,相對于正常體質量及低體質量患者,發病早期即易引起醫療關注及干預,故肥胖可能影響COPD的自然進程,不同BMI患者發病時間可能有差異,BMI越高,發病時間越短,從而形成BMI與FEV1%pre及FEV1/FVC正相關現象,本研究對低體質量組、正常體質量組及超重組發病時間的比較結果提示三組間發病時間并無差異,BMI并不能影響發病時間。近期的一項隊列研究稱,在3年的觀察期內,雖然FEV1絕對值明顯降低,但FEV1%pre無明顯變化[17],提示發病時間對GOLD程度分期并無影響。
3.3 BMI及FEV1%pre對D-二聚體的預測作用 D-二聚體作為纖溶酶降解交聯纖維蛋白的終產物,其水平的增高表明體內有血栓形成及繼發性纖溶的發生,是凝血功能紊亂的早期靈敏指標,對體內高凝狀態和血栓性疾病的療效觀察與預后判斷具有廣泛的應用價值[1-2,18]。
本研究發現,低體質量組與超重組間D-二聚體有差異,體質量降低可引起D-二聚體增高。多重線性回歸分析模型可以看出,D-二聚體水平與BMI呈負相關。這與Vrieze等[9]及陳國忠等[7]研究結果一致,而Silva等[19]關于D-二聚體的病例對照研究發現BMI的增加可造成炎性因子如C反應蛋白及纖維蛋白原增加,促進機體凝血活性,D-二聚體水平升高。這兩種關于BMI與炎性反應關系的相悖觀點基于一共同前提:炎性反應可促進機體高凝狀態,因此,關于BMI與全身及氣道局部炎性反應的進一步深入研究很有必要。此外,本研究未發現FEV1%pre與D-二聚體之間有相關性,同樣結論也見于Silva等[19]關于D-二聚體的研究,說明單純氣道阻塞并不引起機體凝血狀態的改變。
回歸分析中R2=18%表明,BMI只解釋了D-二聚體水平的18%,這也說明仍存在其他影響D-二聚體水平的因素,例如缺氧狀態、用藥情況、是否有微小血栓形成、患者營養狀態等等,由于D-二聚體具有高度敏感性,將所有可能的因素盡可能進行綜合分析可能具有重要臨床意義。
1 周洋,龔建化,黃河,等.COPD患者D-二聚體和纖維蛋白原檢測的臨床價值[J].臨床肺科雜志,2012,17(1):16-17.
2 李碩,鄭亞安,劉桂花.慢性阻塞性肺疾病急性加重期急診住院患者預后影響因素研究[J].中國全科醫學,2012,15(12):4163.
3 黃秀霞,龐寶森,楊媛華,等.慢性阻塞性肺疾病急性加重期凝血功能的變化及其意義[J].中華醫學雜志,2011,9(22):1543-1545.
4 王同生,毛毅敏,孫瑜霞,等.慢性阻塞性肺疾病急性加重合并肺栓塞的臨床特征與高危因素研究[J].中國全科醫學,2012,15(7):2163.
5 Global strategy for the diagnosis,management and prevention of chronic obstructive pulmonary disease(revised 2011)[Z].2011.
6 范敏娟,海冰,趙國厚,等.體質指數和慢性阻塞性肺疾病患者肺功能及呼吸困難的研究[J].中國老年保健醫學,2011,9(1):6-7.
7 宋莉紅,馬衛華,冉瑞華.慢性阻塞性肺疾病患者肺功能與體重指數的相關性研究[J].河北醫藥,2010,32(8):963.
8 陳國忠,曹霞,余昌平,等.慢性阻塞性肺疾病的炎性反應與體質指數密切相關[J].臨床肺科雜志,2010,15(6):777-779.
9 Vrieze A,de Greef MH,Wijkstra PJ,et al.Low bone mineral density in COPD patients related to worse lung function,low weight and decreased fat-free mass[J].Osteoporos Int,2007,18(9):1197-1202.
10 Fukahori S,Matsuse H,Takamura N,et al.Body mass index correlated with forced expiratory volume in 1 second/forced vital capacity in a population with a relatively low prevalence of obesity[J].Chin Med J,2010,123(20):2792-2796.
11 D′Avila Melo SM,Melo VA,Menezes Filho RS,et al.Effects of progressive increase in body weight on lung function in six groups of body mass index[J].Rev Assoc Med Bras,2011,57(5):509-515.
12 O′Donnell DE,Deesomchok A,Lam YM,et al.Effects of BMI on static lung volumes in patients with airway obstruction[J].Chest,2011,140(2):461-468.
13 Santamaria F,Montella S,Greco L,et al.Obesity duration Is associated to pulmonary function impairment in obese subjects[J].Obesity,2011,19(8):1623-1628.
14 Gundogdu Z,Eryilmaz N.Correlation between peak flow and body mass index in obese and non-obese children in Kocaeli,Turkey[J].Prim Care Respir J,2011,20(4):403-406.
15 Scott HA,Gibson PG,Garg ML,et al.Relationship between body composition,inflammation and lung function in overweight and obese asthma[J].Respir Res,2012,1(13):10.
16 Sava F,Laviolette L,Bernard S,et al.The impact of obesity on walking and cycling performance and response to pulmonary rehabilitation in COPD[J].BMC Pulm Med,2010,6(10): 55.
17 Ferrari R,Tanni SE,Faganello MM,et al.Three-year follow-up study of respiratory and systemic manifestations of chronic obstructive pulmonary disease[J].Braz J Med Biol Res,2011,44(1):46-52
18 陳昌枝,朱貴朝,覃家盟,等.慢性阻塞性肺疾病急性加重期凝血特征的研究[J].廣西醫學,2011,33(12):1560-1563.
19 Silva DR,Coelho AC,Gazzana MB,et al.D-dimer levels in stable COPD patients:A case-control study[J].COPD,2012,9(4):426-431.

