探究氫氧化鈉與二氧化碳發生反應的一體化實驗設計
林丹 周文榮
摘要:通過對比分析不同版本教材中對氫氧化鈉與二氧化碳反應不同的處理方式,尋找一線教師留下的實驗設計發展空間,創新設計了一體化的實驗裝置,從壓強變化、堿性強弱、溫度變化、產物檢驗四個視角證明反應的發生。該裝置有對比明顯、整合性強、定量視角、節約藥品等特點,有利于發展學生的科學探究能力和證據推理的意識。
關鍵詞:氫氧化鈉與二氧化碳反應;無明顯現象反應;一體化實驗;創新實驗
文章編號:1008-0546(2022)12-0089-04
中圖分類號:G632.41
文獻標識碼:B
doi: 10.3969/j .issn.1008-0546.2022.12.022
一、裝置設計緣起
1.教材內容分析
氫氧化鈉能與二氧化碳反應,是堿的一條重要的化學性質,不同版本的教材處理略有不同。滬教版和人教版僅給出了NaOH和CO2反應的化學方程式,沒有具體的實驗。魯教版則提供了在塑料瓶里完成反應的實驗。教材對沒有明顯現象反應的發生沒有作深入的探究,給一線教師的研究留下了一定的空間。
2.一線教師研究現狀
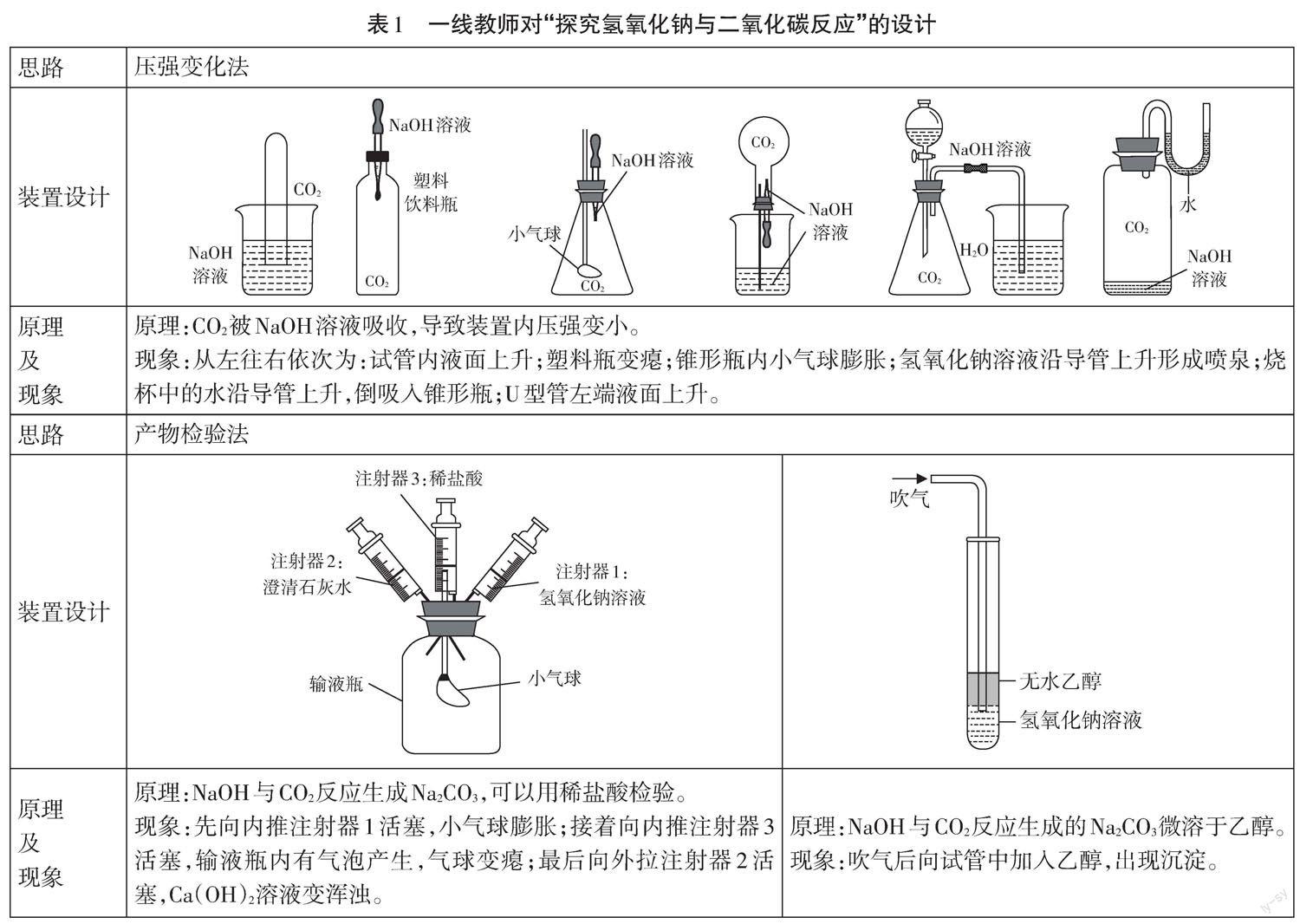
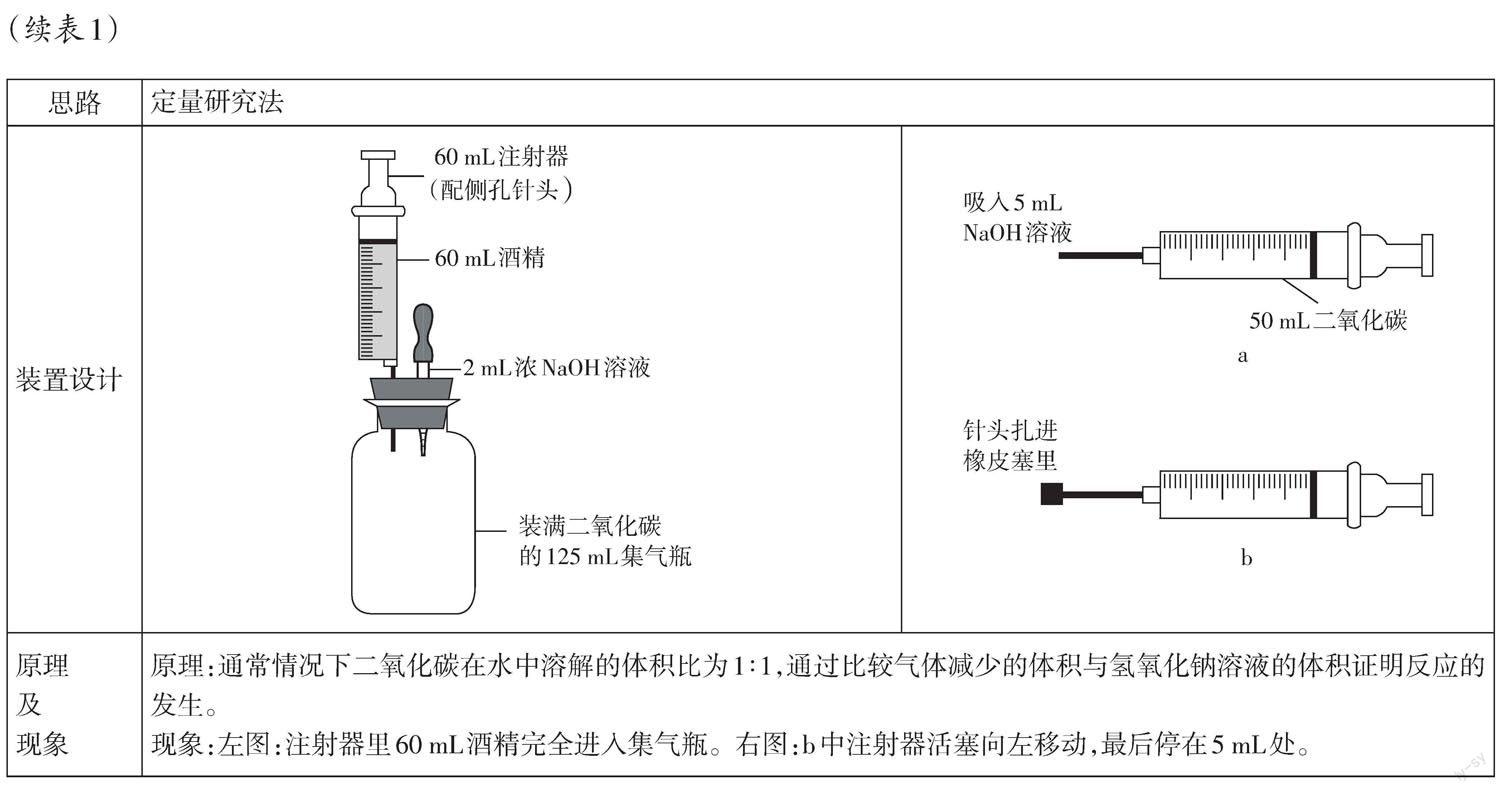
許多一線教師積極思考,不斷探索,從不同角度出發,設計了不同的原理來探究氫氧化鈉與二氧化碳的反應(見表1)。[1-5]
3.裝置設計的發展空間
梳理以上實驗設計,教師們主要是從三個角度證明NaOH能與CO2反應:壓強變化的角度、檢驗產物碳酸鹽的角度、定量角度。現有成果給教師們后續研究提供了寶貴的思路和方法,給進一步研究留下了發展空間。
(1)從壓強角度設計實驗證明氫氧化鈉與二氧化碳的反應需要排除二氧化碳溶于水造成的干擾,可以用等體積的水代替氫氧化鈉溶液進行實驗,作為對照。可以將對照實驗與定量實驗結合起來,定量地對比等體積氫氧化鈉溶液與等體積水吸收二氧化碳的差異。
(2)現有實驗一般是從二氧化碳減少的角度證明反應的發生,也可以從氫氧化鈉減少的角度設計實驗。雖然反應產物碳酸鈉溶于水也是堿性,但堿性相對而言已經減弱,可尋找合適的酸堿指示劑證明氫氧化鈉被消耗。
(3)氫氧化鈉與二氧化碳反應放熱,可以從能量的角度證明反應的發生,利用生活中的電子溫度計可以實時測量溫度的變化。
(4)以上裝置僅僅是從一個或兩個角度設計,可以將實驗進行有機整合,利用一套實驗從多角度證明反應的發生,實現實驗的一體化。
二、一體化實驗裝置和藥品
1.實驗用到的儀器藥品
實驗所需的儀器有:醫用輸液袋1個(實測體積260 mL)、20 mL注射器5個、三通閥2個、電子溫度計1個。
實驗所需的藥品有:二氧化碳、2 mol/L氫氧化鈉溶液、2 mol/L鹽酸、蒸餾水、達旦黃指示劑。
選擇達旦黃作指示劑出于以下思考與實踐:輸液袋的體積為260 mL,除去與水作用的10 mL氣體外,與氫氧化鈉反應的二氧化碳為250 mL,物質的量約為0.01 mol。10 mL 2 moVL的氫氧化鈉溶液能與二氧化碳恰好完全反應,生成的碳酸鈉溶液的pH約為12。經資料查閱,找到兩種潛在可行的酸堿指示劑:孔雀綠和達旦黃。孔雀綠變色的pH范圍為11.5(藍綠)-13.2(無色),達旦黃變色的pH范圍為12.0(黃)-13.0(紅)。經過實驗,發現孔雀綠在反應前后溶液均為無色;而達旦黃在反應中隨著堿性的減弱,溶液由紅色變為淺黃,能作為該反應的指示劑,指示氫氧化鈉被消耗。
2.裝置的制作
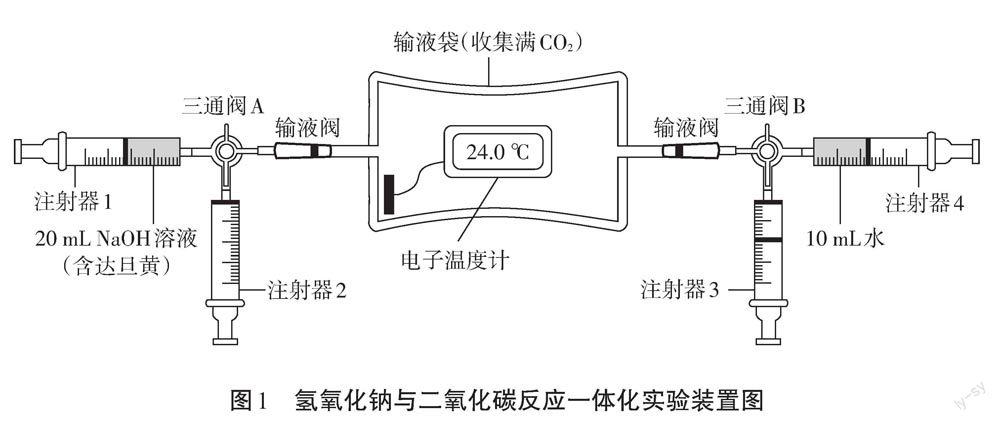
“探究氫氧化鈉與二氧化碳的反應”一體化裝置如圖1所示。將輸液袋兩端多余的塑料軟管裁去,保留兩端的輸液閥。在兩端塑料管上分別連接一個三通閥,三通閥的另外兩個出口分別與兩個20 mL的注射器相連。用泡沫膠水將電子溫度計的數字顯示屏粘在輸液袋上,將溫度探頭用透明膠固定在輸液袋邊。
三、利用裝置進行系列實驗的步驟與現象
在檢查好裝置的氣密性后,在袋中收集滿二氧化碳(約260 mL),關閉輸液袋兩端的輸液閥。注射器1和注射器4中分別抽取10 mL滴有達旦黃的氫氧化鈉溶液或10 mL水,注射器2和注射器3的活塞推至最高處,排盡其中的空氣,如圖1所示將裝置連接好。觀察到達旦黃溶液呈紅色,電子溫度計讀數為24.0℃。
實驗1:從定量角度證明
如圖2所示,轉動三通閥A至輸液袋與注射器2相通,打開輸液袋左端輸液閥,向外拉注射器2的活塞,抽取10 mL二氧化碳,關閉左端輸液閥。用相同的方法在注射器3中抽取10 mL_氧化碳。旋轉三通閥A至注射器1、2相通,推動注射器1的活塞,將10mL滴有達旦黃的氫氧化鈉溶液注入注射器2中,與二氧化碳充分接觸。旋轉三通閥B至注射器3、4相通,推動注射器3的活塞,將10 mL水注入注射器3中,與二氧化碳充分接觸。半分鐘后觀察到注射器2的活塞移動至11.0 mL刻度處,注射器3的活塞移動至17.6 mL刻度處,裝NaOH溶液的注射器活塞移動距離更大,說明等體積氫氧化鈉溶液比水吸收更多二氧化碳,證明氫氧化鈉能與二氧化碳反應。
實驗2:從反應物減少、能量角度證明
旋轉三通閥A至輸液袋與注射器2相通,打開左端輸液閥,將氫氧化鈉溶液全部注入輸液袋,關閉輸液閥,將輸液袋與三通閥分離,振蕩。從側面觀察,與實驗前相比(見圖3-a),注入NaOH溶液后,輸液袋明顯變癟(見圖3-b),溶液由紅色轉為黃色,電子溫度計示數從24.0℃上升至28.1℃。反應物二氧化碳、氫氧化鈉減少,過程溫度上升,均能證明氫氧化鈉與二氧化碳反應。
實驗3:從生成物角度證明
如圖4所示,在注射器5中吸取10 mL 2 mol/L鹽酸,注入輸液袋中,觀察到有氣泡產生,輸液袋重新膨脹。說明反應后有碳酸鹽產生,證明氫氧化鈉能與二氧化碳反應。
反應結束后,向外拉注射器5的活塞,將袋中的液體抽去,重新得到一袋二氧化碳氣體,便于連續教學,循環利用物質。
四、一體化裝置的優點
1.對比明顯,清晰可視。反應過程現象豐富,產生了四處對比現象:兩端注射器讀數、輸液袋前后體積、達旦黃前后顏色、電子溫度計前后讀數。將原本無明顯現象的反應可視化,便于學生更深刻地體會反應過程中壓強、酸堿性、溫度的變化,加深對反應特征的理解。通過對實驗的細致觀察,借助直觀的現象,獲得豐富的感性認識,以此為基礎,證明反應的發生,讓化學實驗成為學生“證據推理”意識與思維邏輯性培養的最主要途徑。[6]
2.整合性強,發展思維。利用一體化實驗裝置實現了從四個角度證明反應發生:壓強變化、堿性強弱、溫度變化、產物檢驗,操作連貫,一氣呵成。在實驗過程中學生既對NaOH能與CO2反應有了深刻的認識,還能構建驗證無明顯現象的反應確實發生的一般模型:新物質生成、反應物減少,能量變化,可以指導他們后續的學習。
3.定量視角,方法指導。相同體積的NaOH溶液和水,接觸等體積的CO2,通過活塞移動的刻度定量指示NaOH與CO2反應。排除了二氧化碳溶于水使壓強變小的干擾,進一步加深了對比實驗控制單一變量的方法指導。 4.節約藥品,循環利用。需要使用的藥品的量很少,僅260 mL二氧化碳、10 mL水、10 mL氫氧化鈉溶液、10 mL稀鹽酸。而且反應結束后通過將輸液袋中剩余液體抽去,實現二氧化碳的循環使用,便于班級間連續上課。所用的儀器均為塑料制品,輕便易攜帶。
參考文獻
[1]顧嗚英,讓實驗現象從“無”到“有”的初中化學對比實驗教學設計[J].化學教學,2017(2):74-78.
[2] 么宏業.二氧化碳和氫氧化鈉溶液反應實驗的改進[J].中學化學教學參考,2013(3):29.
[3]楊永俊.基于3P學習的項目式學習在初中化學教學中的實踐——以二氧化碳與氫氧化鈉反應的可視化研究為例[J].化學教與學,2020(7):82-86.
[4] 朱紅杰,李德前.探究“氫氧化鈉溶液和二氧化碳氣體反應”的定量趣味實驗[J].教育與裝備研究,2016,32(11):65-67.
[5] 陳立銘,李德前.基于量的角度設計“氫氧化鈉溶液與二氧化碳反應”的實驗[J].化學教育,2014,35(23):50-51.
[6] 朱玉林.培養學生證據意識與思維邏輯性的有效途徑[J].中學化學教學參考,2021(12):14-16.

