宮頸環形電切除術聯合α-干擾素治療中、重度宮頸糜爛的臨床觀察
鄒麗蘭 堯桂花
宮頸糜爛是婦科的常見病與多發病之一,宮頸糜爛的治療對于預防宮頸癌有著重要的臨床意義。目前傳統治療宮頸糜爛的方法主要有藥物治療、激光錐切、冷凍、微波和手術治療等,然而臨床療效均不理想,復發率高,嚴重威脅著育齡婦女的身心健康和生活質量[1]。本研究探討宮頸環形電切除術(loop electrosurgical excision procedure,LEEP)聯合α-干擾素治療中、重度宮頸糜爛的臨床療效,現報道如下。
1 資料與方法
1.1 研究對象 選取 2010年4月~2012年4月在我院就診的中、重度宮頸糜爛門診患者 400 例為研究對象,年齡范圍在 29~45 歲,其中中度糜爛 262 例,重度糜爛 138 例。入選標準:(1)非妊娠期及哺乳期;(2)治療 3 個月內無性生活;(3)無明顯心肝肺腎等重要臟器疾病;(4)經白帶常規檢查排除滴蟲、淋球菌、支原體、衣原體等感染;宮頸薄層液基細胞學檢查、電子陰道鏡或宮頸活檢排除癌前病變及宮頸癌;(5)短期內無再次生育要求;(6)無明顯出血傾向或凝血機制障礙者;(7)宮頸糜爛>II度。將患者按隨機數字表法分為LEEP術聯合α-干擾素治療組(研究組,共 200 例)和單純LEEP術治療組(對照組,共 200 例)。
1.2 治療方法 所有研究對象均于月經干凈后 3~7 d內在門診行LEEP術。取膀胱截石位,常規消毒鋪單后,用帶排煙管的窺陰器充分暴露宮頸,干棉球拭凈宮頸分泌物,再次消毒。以 2%利多卡因分別于宮頸 6 點、12 點局部麻醉,碘試驗標記糜爛病變區域,根據病變范圍采用合適的環形電切圈,功率選取 50 W,于碘不著色外 3~5 mm環形切除病變組織,深度約為 10~20 mm。宮頸創面采用球形電極電凝止血,術畢即在宮頸創面予上殼聚糖宮頸抗菌膜 1 個,手術標本送病檢。研究組將l粒α-干擾素栓置入陰道后穹隆,填塞帶線棉球一塊(留置線頭于陰道外,囑其于 24 h后取出)。術后換藥方案為隔日1 次,1 粒 1 次,6 次為 1 療程,連用 2 個療程。對照組采用安慰劑處理,余同研究組。所有患者術后常規抗炎 3 d,禁盆浴及性生活 3 個月,避免劇烈運動和重體力活動。
1.3 療效判斷標準 所有患者均以治療 12 周為判定療效的時間終點。治愈:糜爛面愈合或消失,宮頸光滑,臨床癥狀完全消失;顯效:糜爛面積縮小>50%,或由中度轉變為輕度、重度轉變為中度,臨床癥狀消失或減輕;好轉:糜爛面積縮小<50%,癥狀有所減輕;無效:治療前后無明顯變化。總有效率為治愈、顯效和好轉的總和。
1.4 統計學方法 應用SPSS19.0 軟件進行統計分析,計量資料比較采用t檢驗,計數資料比較采用χ2檢驗,P<0.05 為差異有統計學意義。
2 結果
2.1 兩組患者一般資料比較 兩者患者平均年齡、孕次、胎產次等差異均無統計學意義(P>0.05),具有組間可比性。見表1。

表1 兩組患者基本資料對比
2.2 兩組患者治療后的臨床療效比較 研究組治療中、重度宮頸糜爛有效率 98.44%(126/128)和 94.44%(68/72),均分別高于對照組 97.01%(130/134)和 89.39%(59/66),差異無統計學意義(P>0.05);研究組中、重度宮頸糜爛治愈率 81.25%(104/128)和 76.39%(55/72 均分別高于對照組 68.66%(92/134)和 56.06%(37/66),差異有統計學意義(P<0.05)。見表2。
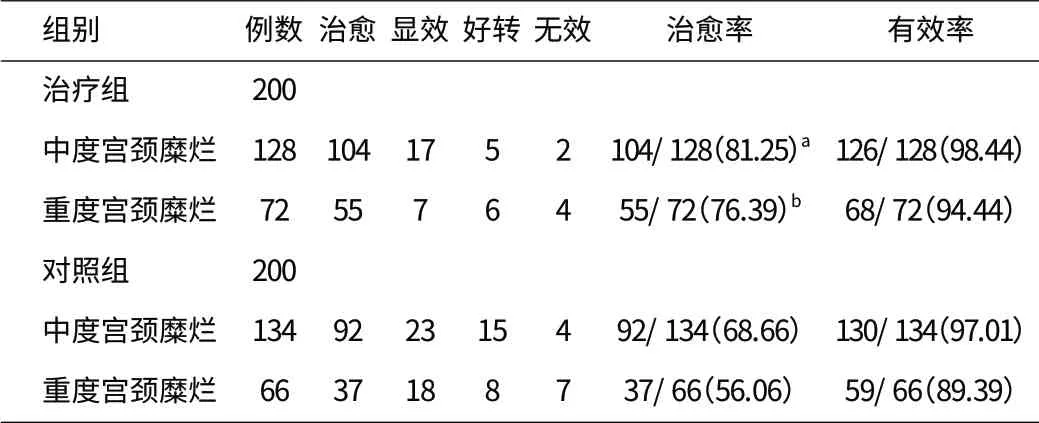
表2 兩組中重度宮頸糜爛患者治療 12 周后療效對比[n(%)]
3 討論
宮頸糜爛是誘發宮頸癌的高危因素之一,循證醫學及流行病學指出,其發病因素與單純皰疹病毒和人乳頭瘤病毒感染密切相關[1-2]。
LEEP術作為一種新型有效的組織電切方法,目前臨床應用于治療宮頸糜爛顯示出較好的優越性:具有切除范圍廣、術中術后出血少、手術歷時短、術時術后患者痛苦少、對生育影響小、術后并發癥低等優點;此外,組織手術切緣無炭化區,便于進行病理學檢查,可同時滿足臨床早期診斷、早期治療的雙要求[2]。
本研究中治療組采用LEEP術聯合α-干擾素治療宮頸糜爛,治愈率顯著高于單純LEEP術。本研究數據顯示,研究組中、重度宮頸糜爛治愈率 81.25%(104/128)和 76.39%(55/72)均分別高于對照組 68.66%(92/134)和 56.06%(37/66),差異有統計學意義(P<0.05),與國內多項研究有相類似的結論[3-8]。α-干擾素具有廣譜的抗病毒作用,其藥理作用是通過競爭性與靶細胞膜蛋白結合,激活細胞內抗病毒蛋白基因,抑制病毒在宿主復制;同時通過調節免疫,增強機體細胞對病毒的吞噬能力。另一方面,它能夠有效減輕組織的局部炎癥反應,加速促進組織鱗狀上皮再生,進一步縮短創面修復時間[9-10]。因此,α-干擾素聯合LEEP術能夠達到相互補充的作用,彌補LEEP術后可能存在的陰道排液多及脫痂期出血多的缺點,進一步提高治愈宮頸糜爛的時效性。
值得一提的是,本研究應用殼聚糖宮頸抗菌膜處理手術創面,獲得了較好的臨床療效。殼聚糖宮頸抗菌膜主要是通過生物膜有效粘附在手術創面黏膜上,釋放活性抗菌物質,有效抑制細菌繁殖,促進纖維細胞的趨化與遷移作用,加速細胞增殖及組織重塑,促進創面修復,有效縮短手術創面滲血滲液的時間,減少LEEP術后脫痂出血等并發癥的發生。殼聚糖宮頸抗菌膜應用于LEEP術后手術創面的處理,亦得到了臨床研究的證實和支持[11]。
綜上所述,LEEP術具有手術時間短、術中出血少、切割速度快、切取組織完整無炭化等優點,便于在基層醫院門診推廣開展;α-干擾素聯合應用于LEEP術治療宮頸糜爛的效果顯著,與LEEP術相輔相成,在治療中、重度宮頸糜爛方面能夠取得較理想的臨床療效,具有臨床推廣價值。
[1]姜軍.LEEP術聯合干擾素栓治療宮頸糜爛[J].現代醫院 2010, 10(6):58-59.
[2]趙改芹.宮頸環形電切術治療宮頸糜爛療效觀察[J].中國基層醫藥,2011,18(12):1637-1638.
[3]賀福嬌.LEEP刀聯合α-干擾素栓治療中重度宮頸糜爛的療效觀察[J].中國醫藥指南,2010,8(34):99-100.
[4]王迅.干擾素α-2 b聯合微波治療宮頸糜爛合并人乳頭狀瘤病毒感染[J].中國基層醫藥,2011,18(2):224-225.
[5]陳建亮.宮頸環形電切除術聯合α-干擾素治療中、重度宮頸糜爛的效果觀察[J].中國醫師進修雜志,2012,35(6):46-47.
[6]賴娟娟,楊曉帆,閔羨蕙.LEEP術后聯合重組人干擾素α-2 a治療慢性中重度宮頸糜爛的療效分析[J].實用醫學雜志,2009,25(20):3427-3429.
[7]夏紅蘭,喻云,范榮萍.宮頸環形電切除術與激光治療宮頸中至重度糜爛及肥大合并多枚納氏囊腫的對比研究[J].中華婦幼臨床醫學雜志,2011,7(5):455-457.
[8]楊志平,吳昕.LEEP聯合干擾素栓及保婦康栓治療宮頸糜爛[J].中國實驗方劑學雜志,2011,17(10):239-241.
[9]徐玲玲.干擾素栓聯合微波治療宮頸糜爛療效觀察[J].現代中西醫結合雜志[J],2007,16(7):884-885.
[10]胡文惠,楊梅.干擾素治療宮頸糜爛 309 例臨床分析[J].海南醫學院學報,2009,15(6):607-609.
[11]張桂萍,梁寧安,洪紅.殼聚糖宮頸抗菌膜聯合宮頸環形電切除術治療宮頸糜爛的療效觀察[J].臨床合理用藥,2010,20(10):93-94.

