冠心病患者頸動脈內膜-中層厚度及微量白蛋白尿與冠狀動脈病變的關系
涂 昌 潘偉彪 蘭 軍 陳本發 葉文衛
南方醫科大學附屬東莞市石龍人民醫院心血管內科,廣東東莞 523326
頸動脈內膜-中層厚度 (intima-media thickness,IMT)及微量白蛋白尿(MA)均為冠心病患者的危險因素,多項研究表明,頸動脈和冠狀動脈硬化有著相同的發病機制及相應的危險因素,頸動脈血管壁內膜-中層厚度增厚是動脈粥樣硬化的早期征象,所以頸動脈IMT及斑塊是預測冠狀動脈粥樣硬化及其程度的一個簡便的指標。頸動脈粥樣硬化與冠狀動脈粥樣硬化均為血管內皮受損引起,反映血管內皮損傷具有多項指標,尿微量白蛋白(MAU)含量最初是作為腎血管內皮功能受損一項指標,目前研究也表明是全身血管內皮功能受損的重要指標之一,可以反映頸動脈粥樣硬化及冠狀動脈粥樣硬化的程度。
1 資料與方法
1.1 一般資料
選擇2009年10月~2011年11月我院行冠狀動脈造影檢查者82例,平均年齡(62±19)歲,入選病例排除糖尿病、各種腎病、腎功能衰竭、泌尿系統感染、肝硬化、心力衰竭病史。行冠狀動脈造影前后48 h內行頸動脈超聲檢查,入院后48 h內檢測MAU(均在造影之前檢測)。
1.2 冠狀動脈造影及分組
采用Judkin技術,由兩位以上經驗豐富的醫師根據造影結果圖片后評估病變冠狀動脈病變部位性質及狹窄程度。其中冠狀動脈病變程度由冠狀動脈病變支數和Gensini的總積分確定。最后診斷冠狀動脈粥樣硬化性心臟病標準:主要的冠狀動脈,包括左冠狀動脈主干、左前降支、回旋支、右冠狀動脈及各冠狀動脈的主要分支如對角支、鈍緣支、左室后降支等直徑有不小于50%的狹窄。冠狀動脈病變支數根據冠狀動脈的狹窄直徑、≥50%病變及累及主要冠狀動脈支數,可分為冠狀動脈正常組、單支病變組、雙支病變組和三支及多支病變組。另外有累及左主干的應該按同時累及左前降支和左回旋支來計算。Gensini積分據美國心臟病協會的標準,最后進行冠狀動脈狹窄程度的病變定量評定。其中狹窄程度≤25%計1分、26%~50%計 2分、51%~75%計 4分、76%~90%計 8分、91%~99%計16分、100%計32分。計算根據節段乘以相應系數:左主干×5.0,左前降支近段×2.5,中段×1.5,遠段×1.0,第一對角支×1.0,第二對角支×0.5,左回旋支×2.5,左回旋支遠段、后降支、鈍緣支均×1.0,后側支×0.5,右冠狀動脈近、中、遠段和后降支均×1.0;總積分為各節段積分之和。
1.3 頸動脈斑塊及IMT的檢測
所有患者采用雙側頸動脈超聲檢查,應用美國飛利浦-ie33彩色多普勒超聲診斷儀。受檢者取仰臥位,頭頸盡量仰伸使頸部血管充分暴露,受檢者的頭轉向被檢查的對側。從頸的根部開始,先進行橫切檢查,后進行縱切檢查,從近至遠,觀察雙側頸總動脈的近中遠端及分叉處,觀察受檢者的頸內動脈、頸外動脈的管壁厚度及頸動脈斑塊形成情況。筆者根據標準設定IMT>0.9 mm為頸動脈內膜-中層增厚,如果存在有頸動脈內膜-中層不規則增厚>1.5 mm或突出頸動脈內膜表面可定義為頸動脈斑塊形成。頸動脈斑塊采用半定量法進行積分評定,無頸動脈斑塊者積0分;只有1處頸動脈斑塊而且頸動脈斑塊厚度≤2 mm者積1分;有2處頸動脈斑塊但厚度均<2 mm或1處頸動脈斑塊且厚度>2 mm者積2分;2處頸動脈斑塊至少1處厚度>2 mm者積3分;2處以上頸動脈斑塊且厚度均>2 mm者積4分。
1.4 尿微量白蛋白測量
所有對象留取清晨中段尿,采用免疫比濁法進行MAU的測定。
1.5 觀察指標
冠狀動脈病變程度 (由冠狀動脈病變支數及Gensini總積分確定);頸動脈IMT;MAU。
1.6 統計學方法
采用統計軟件SPSS 13.0對實驗數據進行分析,計量資料數據以均數±標準差(x±s)表示,多組間比較采用方差分析,兩兩比較采用LSD-t檢驗。用直線相關方法來進行相關性分析,以P<0.05為差異有統計學意義。
2 結果
2.1 各組患者一般情況比較
各組間患者年齡、血壓[包括收縮壓(SBP)及舒張壓(DBP)]、總膽固醇(TC)、三酰甘油(TG)、高密度脂蛋白(HDL-C)、低密度脂蛋白(LDL-C)及體重指數(BMI)及腎功能比較,差異均無統計學意義(均P>0.05)。見表1。
2.2 各組患者IMT及MAU比較
與冠狀動脈正常組比較,單支病變組、雙支病變組和三支及多支病變組的頸總動脈IMT明顯增厚,而且隨著冠狀動脈病變程度的加重,其頸總動脈IMT、斑塊發生率、斑塊積分及MAU亦隨之增加,差異均有統計學意義(均P<0.05)。見表2。冠狀動脈病變支數與頸動脈IMT呈正相關(r=0.68,P < 0.05), 與斑塊積分呈正相關 (r=0.62,P <0.05)。冠狀動脈造影積分與頸動脈IMT呈正相關 (r=0.63,P < 0.05),與頸動脈斑塊積分呈正相關(r=0.62,P <0.05)。 MAU 與 Gensin-S 呈正相關(r=0.54,P < 0.05),與頸動脈 IMT 亦呈正相關(r=0.57,P < 0.05)。
3 討論
動脈粥樣硬化是一種全身性慢性疾病,常見于冠狀動脈、腦動脈、頸動脈及腎動脈等重要臟器的血管,不少研究表明,冠狀動脈及頸動脈常同時出現動脈粥樣硬化,測定頸動脈IMT可反映個體冠狀動脈粥樣硬化的嚴重程度,是心血管疾病強有力的預測因素。通過檢測頸動脈IMT是評價動脈壁粥樣硬化改變的主要指標之一[1-2],本研究表明,隨著冠狀動脈病變程度的加重,其頸動脈IMT明顯增加,頸動脈粥樣硬化斑塊的程度亦有所加重,差異有統計學意義(P<0.05),說明頸動脈斑塊的檢出率及嚴重程度可作為冠狀動脈病變的預測依據[3-4]。目前考慮動脈粥樣硬化的病因較多,而血管內皮受損是微血管和大血管病變的重要因素。相關研究表明,尿白蛋白排泄率增高可能作為冠心病患者內皮功能廣泛受損的標志[5]。
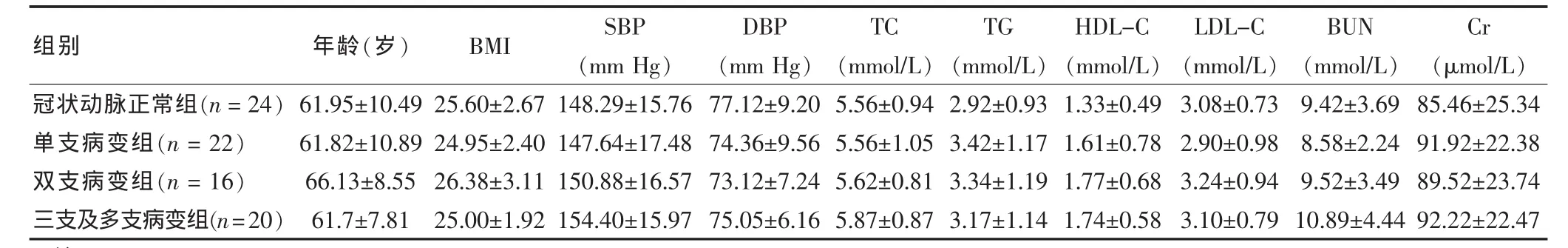
表1 各組患者一般資料比較(x±s)
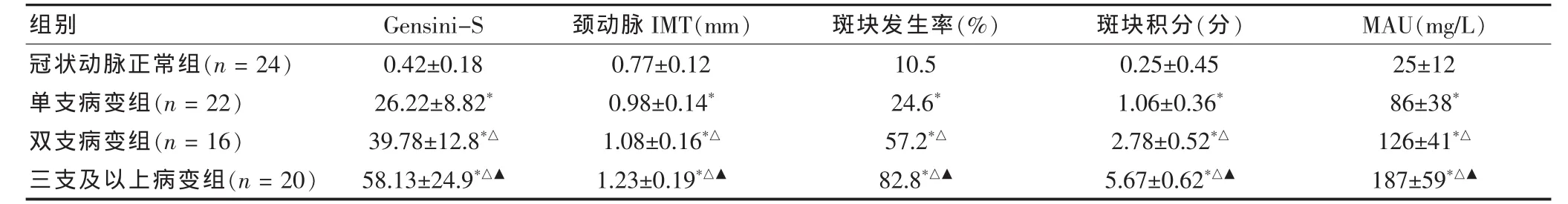
表2 各組患者IMT比較(x±s)
尿白蛋白定量檢測有幾種方法,常見有晨尿的白蛋白定量檢測及24 h尿白蛋白排泄率,MAU指的是晨尿的白蛋白量位于20~200 mg/L之間或者24 h尿液中白蛋白一直處于20~200μg/min的持續排泄濃度。正常情況下,絕大部分白蛋白不能通過腎小球濾過膜。尿中出現微量白蛋白通常是腎小球動脈硬化、腎小動脈內皮受損所致,反映了腎微小血管的病變,同時也是全身血管病變的早期表現。已有研究表明,MAU是心、腦、腎及外周血管損傷的標志,因此它被認為是動脈硬化的早期表現[6-7]。本研究資料顯示,MAU及IMT與冠狀動脈病變程度評分之間呈正相關(r=0.57,P<0.05)。這可能是心血管各種危險因素包括高血壓、糖尿病、吸煙、高脂血癥及其他各種致動脈粥樣硬化危險因素損傷血管內皮,包括有冠狀動脈、頸動脈、腦血管、腎動脈及全身動脈內皮系統,其中各種心血管危險因素影響腎動脈內皮細胞后,導致腎小球血流動力學出現異常,引起腎小球濾過膜損害;同時腎動脈內皮細胞釋放內皮素(ET)和一氧化氮(NO)等血管活性物質使腎小球毛細血管張力改變,引起腎血流動力學變化,導致腎小球長期處于高濾過狀態并致腎損害[6-8]。Lekatsas等[9]有研究證實檢測有微量白蛋白尿的急性心梗患者其冠狀動脈粥樣硬化的程度明顯高于無微量白蛋白尿的急性心梗患者,這說明微量白蛋白尿不僅僅是心血管疾病的一種獨立危險因素,也可以預測全身動脈粥樣硬化相關的各種缺血性心血管事件如冠心病及腎血管病變。
目前冠狀動脈造影是冠狀動脈粥樣硬化診斷的“金標準”,但冠狀動脈造影是一種侵入性檢查,在冠心病高危人群的篩選應用中難以普及,所以臨床上尋找一種簡便,易行無創傷的檢查來早期篩選和發現冠心病是十分必要的,本研究結果顯示頸動脈IMT及MAU的測定對評價冠狀動脈病變具有重要臨床意義,是血管疾病強有力的預測因素,可作為臨床上一種簡便、易行、無創傷的檢查來早期篩選和發現冠心病。
[1]Barghouti N,Elkeles R,Nicolaides A,et al.The ultrasonic evaluation of the carotid intima-media thickness and its relation to risk factors of atherosclerosis in normal and diabetic population [J].Int Angiol,1997;16(1):50-54.
[2]謝秀梅,李志凌,李兢,等.老年原發性高血壓微量白蛋白尿與血管內皮功能及頸總動脈粥樣硬化[J].高血壓雜志,2006,14(2):94-96.
[3]Manami T,Baba S,Ogata J.Strong and significant relationship between aggregation of major coronary risk factors and accleration of carotid atheroscle rosis in general population of a Japanese city:the Suita Study[J].Arch Interm Med,2000,160(15):2297-2303.
[4]Bonithon KC,Jouven X,Taquet A,et al.Early carotid atherosclerosis in healthy middle-aged women:a follow up study[J].Stroke,1993,24(12):1837-1843.
[5]Klausen K,Borch JK,Feldt RB,et al.Very low levels of microalbuminuria are associated with increased risk of coronary heart disease and death independently of renal function,hypertension,and diabetes[J].Circulation,2004,110(1):32-35.
[6]De ZD,Parring HH,Henning RH.Microalbuminuria as an early marker for cardio vascular disease [J].Am See Nephrol,2006,l7 (8):2100-2105.
[7]Casanova C,de Torres JP,Navarro J,et al.Microalbuminuria and hypoxemia in patients with chronic obstructive pulmonary disease[J].Am JRespir Crit Care Med,2010,182(8):1004-1010.
[8]朱雯,李勇,徐旭凌,等.尿微量白蛋白與冠狀動脈粥樣硬化程度相關[J].中華老年多器官疾病雜志,2009,8(6):512-516.
[9]Lekatsas I,Kranidis A,Ioannidis G,et al.Comparison of the extent and severity of coronary artery disease in patients with acute myocardial infarction with and without microalbuminuria [J].AM JCardiol,2004,94(3):334-337.

