HACCP體系在黃芪飲片生產中的應用研究
黃婷婷,張玉梅
(北京大學 公共衛生學院,北京 100191)
?
HACCP體系在黃芪飲片生產中的應用研究
黃婷婷,張玉梅*
(北京大學 公共衛生學院,北京 100191)
目的:建立中藥飲片生產企業HACCP管理體系,提高中藥飲片質量過程控制。方法:選取武漢某中藥飲片廠80批次黃芪飲片的生產過程作為研究對象,通過對影響飲片質量的過程進行危害分析,確定重金屬、霉變、水分、含量為初步危害控制點,其中以前40批次作為對照,采用常規生產過程;后40批次為正試期,實施HACCP體系。在藥品生產質量管理規范(Good Manufacture Practice)實踐的基礎上,設置原藥材驗收、淋洗、浸潤、干燥四個關鍵控制點,制定出HACCP計劃表及相應的預防控制措施并執行,測定和分析比較黃芪飲片理化檢測指標的變化并進行效果驗證。結果:①執行HACCP體系后,黃芪飲片的二氧化硫、水分、總灰分、重金屬鉛、鎘、銅、農殘六六六(總BHC)、滴滴涕(總DDT)的含量下降,水溶性浸出物、黃芪甲苷、毛蕊異黃酮葡萄糖苷有所提高(P<0.05);重金屬砷、汞和五氯硝基苯無顯著差異(P>0.05)。②市場投訴率下降53.20%,一次交驗合格率提高了54.05%。結論:在GMP基礎上引入HACCP體系對于保障黃芪飲片質量可控,促進質量風險管理水平等方面具有可行性。
HACCP;GMP;飲片生產;應用研究;黃芪
作為一種農副產品產業態,在傳統的中藥產業模式中,飲片生產行業發展的實際水平與藥品質量要求的安全性、有效性、質量可控性有著較大的差距,GMP通過全面規范的管理在一定程度上控制質量風險;但由于質量變異活動的特點[1],其針對性不夠,致使效率較低而投入成本高[2]。英國危機管理專家邁克爾·里杰斯特說:“預防是解決危機的最好方法。”危害分析與關鍵控制點(HACCP)體系作為被世界衛生組織(WHO)與人用藥物注冊技術要求國際協調會(ICH)推薦在制藥企業中使用的質量管理工具,具有針對性、預防性、經濟性、實用性的特點[3],在世界各國均得到廣泛的應用和發展,但在中藥飲片生產企業中尚處于初步嘗試階段。本研究探討在黃芪飲片生產中建立HACCP質量控制體系,并對執行該體系的效果進行評價,以達到提高中藥飲片質量過程控制的目的,為HACCP體系在中藥飲片GMP管理中的應用提供可行性依據。
1 對象與方法
1.1 研究對象
選擇武漢某中藥飲片廠2011—2014年生產中藥飲片的共80個批次黃芪飲片生產過程為研究對象。
1.2 研究方法
1.2.1 HACCP小組成員及其職責 為制定有效的HACCP計劃,公司在GMP管理小組的基礎上成立了以總經理為首的HACCP領導小組,確保多部門具有產品專業知識和經驗的人員參與其中,在生產各環節部門成立HACCP小組,構成HACCP體系的組織機構。
1.2.2 產品描述 根據HACCP原理,對黃芪飲片的產品特性進行描述:產品名稱、產品特性(化學、生物、物理)、生產方式、包裝類型、貯存方法、接受準則等。
1.2.3 工藝流程圖及現場確認 由HACCP小組繪制黃芪飲片加工工藝流程圖(原藥材驗收→揀選→淋洗→浸潤→切片→干燥→待包裝品檢驗→內包裝→外包裝→成品入庫→運輸),制定生產工藝規程及詳細的標準操作規程,對每一工序的具體操作提出要求,并通過在加工現場進行驗證,確認以上所規定的內容與流程圖相匹配,與實際生產相符合,能夠通過實施起到質量控制作用。
1.2.4 危害分析與關鍵控制點確定 HACCP小組從原藥材驗收、揀選、淋洗、浸潤、切片、干燥、包裝、入庫、運輸等各個環節列出每個步驟中有理由可能產生的危害,并進行分析,鑒定哪些危害具有在產品安全生產中必須予以消除或降低到可接受水平的屬性。結合以下幾個方面逐一進行危害分析評估[4]:有可能產生的危害并影響健康的嚴重性;定性和/或定量評價出現的危害;相關微生物生存或增殖;產品中毒素、化學或物理因素的存在和持久性;導致上述原因的條件。
依據資料分析和實踐積累,含水量過高導致霉變,重金屬及有害元素、有機氯農藥殘留,以及處理不當導致黃芪甲苷、毛蕊異黃酮葡萄糖苷含量損失過大,均在黃芪飲片生產中對產品造成危害的概率最大,對產品品質和消費者健康的影響也最大,因而將它們消除或降低至可接受水平是必不可少的,而公司原有質量管理中對預防控制措施并沒有做特別規定,因此HACCP小組結合工藝流程圖和產品特性將原藥材驗收、淋洗、浸潤、干燥四個環節確定為關鍵控制點。1.2.5 建立HACCP計劃表 針對以上確定的四個關鍵控制點,HACCP小組制定HACCP計劃工作表,其中規定了關鍵控制點的關鍵限值、控制方法、糾偏措施、驗證方法及相關記錄。
1.2.6 檢測驗證 檢測樣品為黃芪飲片待包裝品,來源于武漢某中藥飲片廠80個生產批次,按照2010年版《中國藥典》一部附錄Ⅱ藥材取樣方法[5]用潔凈取樣器在周轉箱不同部位抽取有代表性的樣品,每批次取樣本3份,每份至少取100g。分別放在清潔的塑料自封袋內封口,做好標記。以企業內控標準為檢驗依據進行檢測驗證。
1.2.7 效果評價 采用SPSS19.0統計軟件對實施HACCP前后的理化檢測數據進行描述性統計,服從正態分布的數據進行兩獨立樣本t檢驗,不服從正態分布的數據進行Mann-Whitney檢驗,比較HACCP體系實施前后黃芪飲片各質量檢測指標的差異,并對市場投訴率及一次交驗合格率進行效果驗證。
2 結果
2.1 確定關鍵控制點(CCP)
關鍵控制點(critical control point,CCP)是指一個可以實施控制的點、步驟或過程,且這一步驟的控制對預防或消除藥品危害和/或使危害降低至合格水平至關重要。在黃芪飲片生產過程中通過對原藥材驗收、淋洗、浸潤、干燥四個關鍵點確定并監控,旨在有效地控制住危害,是HACCP體系控制活動的支點。
2.2 完成HACCP計劃表
依據HACCP原理,明確關鍵控制點后,接著建立關鍵限值(CL)、關鍵控制點的監測程序、建立糾偏措施、驗證程序和記錄保持程序即形成HACCP計劃表,其結果見表1。
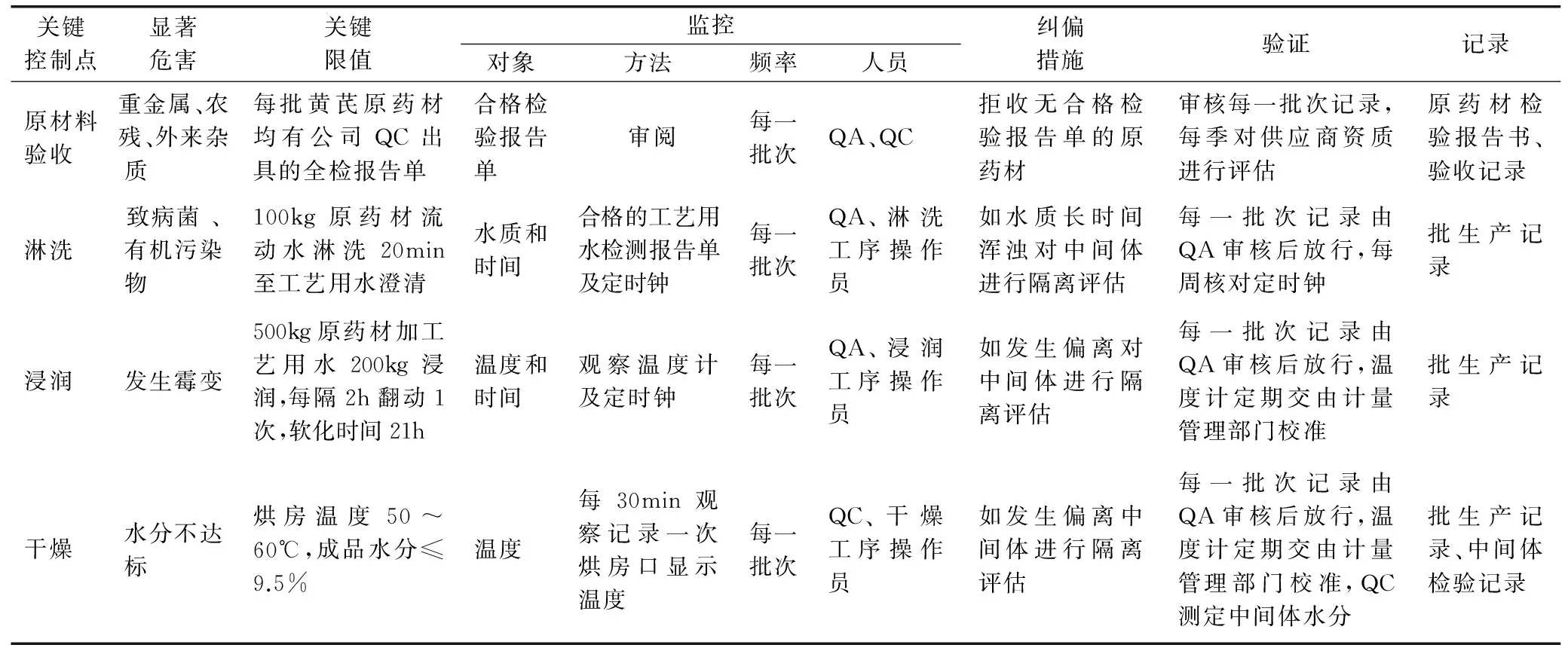
表1 HACCP計劃安排
2.3 實施HACCP體系前后的理化值比較
2.3.1 服從正態分布的數據(兩獨立樣本t檢驗)

表2 實施HACCP前后檢測結果
由表2可以看出實施HACCP體系后,水分和重金銅含量均有所下降,相較于實施HACCP前明顯改善(P<0.05)。
2.3.2 不服從正態分布的數據(Mann-Whitney檢驗)
由表3可知,二氧化硫、總灰分、鉛、鎘、六六六(總BHC)、滴滴涕(總DDT)、水溶性浸出物、黃芪甲苷、毛蕊異黃酮葡萄糖苷的含量較實施HACCP前明顯改善(P<0.05)。砷、汞、五氯硝基苯的含量與實施HACCP前比較無統計學差異,但有一定程度的改善。
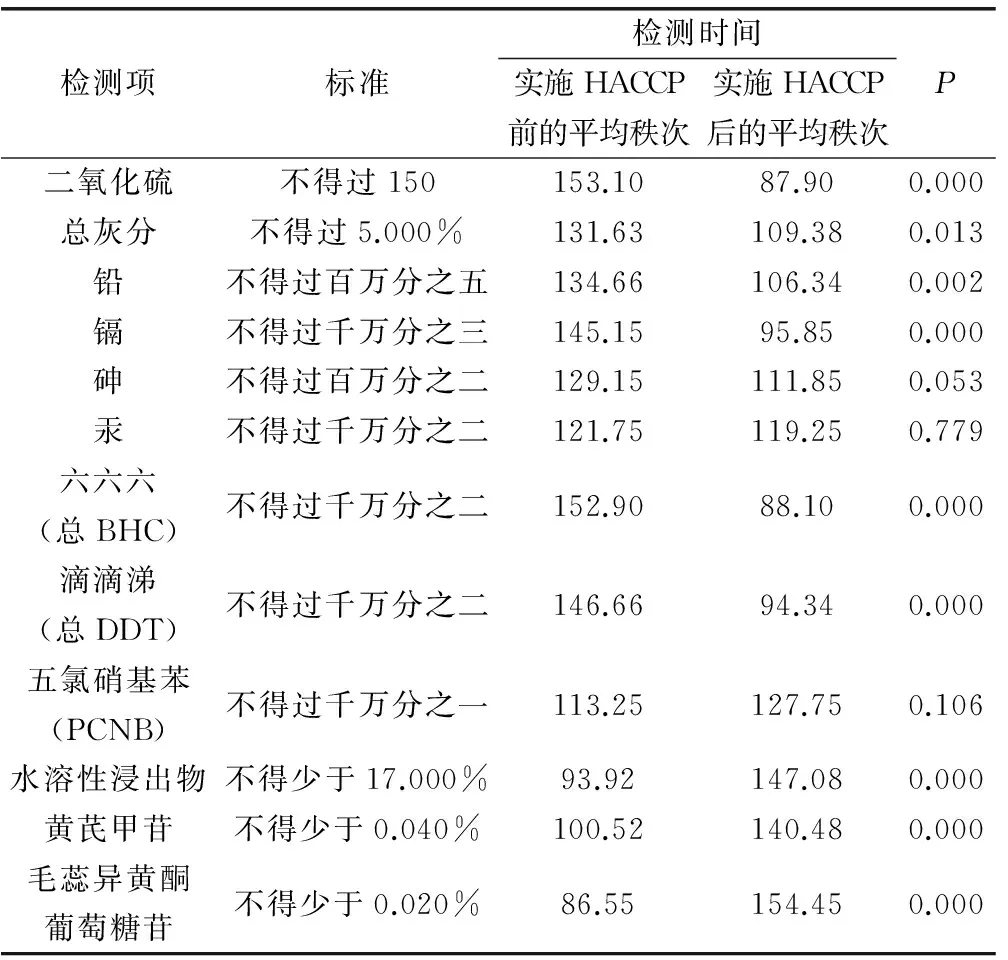
表3 實施HACCP前后檢測結果
3 討論
在飲片生產企業進行HACCP體系的應用研究是一個管理體系的嘗試,本研究將這一系統性、前瞻性的安全管理體系應用到黃芪飲片的生產實踐中,并通過各方面的數據驗證,結果表明,將GMP、SOP和HACCP有機地結合在一起,互為條件互相補充,對黃芪飲片生產的質量控制有著明顯的應用意義。有了GMP、SOP的支撐,HACCP能夠作為最高層次在預防性安全控制體系中起關鍵性的作用[6],能確保產品達到預期的品質要求和安全保障,是一種多元化管理模式結合的初步嘗試。
在企業已經取得GMP認證的基礎上,通過對HACCP整個系統原理的剖析和對黃芪飲片全套生產工藝流程的解構,找出四個關鍵控制點——原藥材驗收、淋洗、浸潤、干燥,并制定出HACCP計劃表,從而在黃芪飲片的生產實踐中建立了HACCP管理體系,這也是本研究的創新點。為了驗證HACCP管理體系的應用效果,對實施前的檢測指標和實施后的檢測指標進行描述性統計,并對比顯著性差異。結果表明:實施HACCP體系后各控制指標均有顯著降低,各成分指標相比實施前有所提高,說明在加工過程中損失減少,其他數據如市場投訴率降低了53.20%,一次交驗合格率提高了54.05%,其效果顯著。
不可否認,實施HACCP計劃在一定程度上取決于對系統的理解認識程度和實施團隊的整體素質,而不是大量的資金、設施設備的投入。以對關鍵控制點的把控為主體,其他過程由GMP和SOP來控制,相較于GMP的全面質量規范更加節省人力、物力、財力,對于企業來說可操作性更大。對飲片生產企業來說,建立完備可操作性強的質量管理體系,才能從根本上解決我國飲片生產中化學物質污染、重金屬及有害元素超標等危害消費者身體健康的不良現象。對于藥品質量而言,建立適宜有效的質量管理體系也是一種理念的實現,盡管需要花很長的實踐時間,但構建HACCP管理體系作為一個具有前瞻性的應用點[7],對于長期效益和質量過程控制系統的完善是非常值得嘗試的[8]。
本研究僅以黃芪飲片的生產加工過程進行HACCP質量管理體系的建立和實施,是對HACCP體系在農副產品產業中廣泛的應用領域的一次初探,希望未來的農副產品加工企業能夠將HACCP管理體系靈活應用到各自領域,以完善的多元化質量控制模式為維護人民的健康和安全起到積極的促進作用。
[1] 詹姆斯·R·埃文斯,威廉·M·林賽. 質量管理與質量控制[M].第7版.北京:中國人民大學出版社, 2010,65-97.
[2] 榮曉陽,梁毅.危害分析和關鍵控制點在GMP管理中的應用[J].中國藥業,2010,19(4): 6-7.
[3] 冷連波.HACCP在中國的應用與思考[J].檢驗檢疫科學,2006,16(5): 3-4.
[4] World Health Organization. Thirty-sixth report of the WHO Expert Committee on Specifications for Pharmaceutical Preparations[R]. Geneva:WHO, 2002.
[5] 國家藥典委員會.中華人民共和國藥典[S].一部.北京:中國醫藥科技出版社,2010.
[6] 李鈞,李志寧. 藥品質量風險管理[M]. 北京:中國醫藥科技出版社, 2011.
[7] International Conference on Harmonisation of Technical Requirements for Registration of Pharmaceuticals for Human Use (ICH).ICH HARMONISED TRIPARTITE GUIDELINE Q9, Quality Risk Management [S]. 2005-11-09.
[8] 錢和. HACCP原理與實施[M]. 北京:中國輕工業出版社, 2003.
(責任編輯:魏 曉)
2014-05-08
黃婷婷(1981-),女,北京大學碩士研究生,研究方向為食品衛生與安全。
張玉梅(1966-),女,北京大學教授、博士生導師,研究方向為食品衛生與安全。
R283
A
1673-2197(2014)17-0128-03

