化療及手術治療對耐藥性妊娠滋養細胞腫瘤的影響
叢豐輝 劉 佳 王曉彬▲
1.遼寧省大連市婦女兒童醫療中心,遼寧大連 116001;2.遼寧省腫瘤醫院婦產科,遼寧沈陽 110042
由于妊娠滋養細胞腫瘤(gestational trophoblastic neoplasia,GTN)對化療藥物敏感,其也成為婦科惡性腫瘤中唯一采取化學藥物治療便可以治愈的腫瘤,治愈率甚至高達80%[1]。隨著診療水平的不斷提高,化療藥物的合理應用,使得GTN 患者治愈率也逐漸升高。但是仍然存在相當比例的患者,其化療后治療結果達不到預期目標,甚至病情會逐步惡化,最終導致患者死亡。 究其原因,主要是這部分患者對化療產生了明顯的耐藥性。經文獻報道,高達30%的高危性GTN 患者在接受合理規范化療后都會產生耐藥性[2]。 因此如何合理有效地解決GTN 的耐藥性成為一個值得研究的問題。
1 資料與方法
1.1 一般資料
從2004 年1~12 月中國醫科大學第一附屬醫院收治的90 例GTN 患者中選擇耐藥性GTN 患者15例為研究對象,年齡21~50 歲,平均(31.7±3.9)歲。其中12 例侵蝕性葡萄胎患者和3 例絨毛膜癌患者,前者中Ⅰ期8 例,Ⅲ期4 例;后者Ⅰ期2 例,Ⅲ期1例。全部腫瘤患者均已化療2~16 個療程,平均(6.5±0.5)個。
1.2 診斷標準
①GTN 的診斷標準:患者葡萄胎排空后半年,出現陰道不規則流血,人絨毛膜促性腺激素(β-hCG)居高不下,或者降后又升高,診斷為侵襲性葡萄胎;若患者葡萄胎排空后1 年或者宮外孕、流產后出現上述相應癥狀與體征,并結合組織學檢查,可診斷為絨毛膜癌[3]。②分期標準:按照2002 年公布的新FIGO 分期,其包括解剖學分期與預后評分[4]。③耐藥標準:GTN 耐藥標準為化療期間患者血清β-hCG 水平出現高平臺期甚至升高不降,并且此過程持續≥2 個療程,或者在化療期間患者出現了轉移病灶[5]。
1.3 治療方法
1.3.1 藥物治療 所有患者均根據WHO 的預后評分標準[4]分為≥7 分的高危組和<7 分的低危組。 高危組接受以5-氟尿嘧啶(5-FU)為主的聯合化療,低危組則只接受甲氨蝶呤或5-FU 等單體化療藥物治療,若低危組的患者在采取同種抗腫瘤藥化療治療期間連續2 個療程后出現耐藥, 則選取另外一種單一藥物代替治療, 若患者對兩種藥物的單一治療均發生耐藥,則采用藥物聯合治療。 同時,對于無生育要求者,或者未發生新轉移灶者, 在經過短期化療控制基本病情后,患者的病灶如果出現明顯萎縮,或者血清βhCG 降低,并幾乎接近正常,此時可聯合手術治療,即根據患者病情行病灶剔除術, 或者行子宮全切除術,以縮短化療療程,降低藥物治療帶來的副作用;手術方式的選擇為對于病灶僅僅局限于子宮的患者可只采取病灶剔除術,但是如果病灶侵襲力強,導致子宮穿孔,并發大出血,或者腹腔內出血,應緊急行全子宮切除術。
1.3.2 護理方法 根據患者個體差異制訂不同的化療治療方案,且治療前給予適當護理關懷,護理人員在患者入院后要為其安排一個舒適安靜的病房,定時進行病房消毒,囑咐患者要勤換衣物,并保持口腔清潔。如患者對自身腫瘤的相關知識了解較少,護理人員應積極主動與患者溝通,了解其心理狀況、病情和性格,綜合評估其精神、生理、心理,以制訂針對個體的合理護理方案。由于治療前患者會產生恐懼、焦慮的情緒,這會對病情的發展以及日后的康復帶來一定的負面影響,因此護理人員可介紹關于疾病治療方面的醫學專業知識并告知患者通過看電視、聽音樂、讀書等方式緩解其不良心理情緒, 提高其對疾病的認知度,改善護患關系,提高治療效果,同時向患者講解成功病例,提高其自信心,樹立積極心態,主動配合治療。 手術過程中給予護理關懷,核對患者的信息,并介紹周圍的環境,減輕患者的心理壓力。 實時監測患者的病情變化,詢問其是否有不適癥狀;嚴格監測生命征的變化,若發現異常情況應立即向醫生匯報。 術后嚴密檢測其生命體征及引流管情況,將床位調至最佳角度以適應患者的要求。 囑患者術后禁食高脂、高熱量食物,建議其進食低鹽、低脂食物,少吃多餐,禁止暴飲暴食,減輕腸胃負擔,促進療效。制訂合適的康復鍛煉計劃,提高患者的免疫能力,使患者保持良好的情緒,禁煙酒,保持正常生活作息規律。
1.4 停藥標準
依據FIGO 提出的停藥標準[4],低危組患者出現血清β-hCG 首次轉陰后,應繼續進行至少1 個療程的治療,如果患者出現血清β-hCG 水平下降較慢,或病灶出現擴散,則應繼續化療2~3 個療程;高危組患者,血清β-hCG 水平首次出現轉陰后應繼續化療3 個療程,且第1 個療程要采取聯合化療,之后治療要依據患者情況可采用單體藥物治療。
1.5 療效評估
化療療程結束到第18 天時,患者血清β-hCG 的水平下降不少于1 個對數為有效;血清β-hCG 的水平達到5.3 U/L 為降至正常。療效判定標準[6]:參照WHO提出的統一標準進行判定,分為無效(NR)、部分緩解(PR)、完全緩解(CR),后兩者均視為治療有效。
1.6 隨診
嚴密隨訪治療結束的患者,第1 年保證每月1次,隨訪12 次;1 年后每年隨訪4 次,第3 年后隨訪1 年1 次,持續隨訪2 年。 隨訪第1 年期間患者必須嚴格避孕,避孕目的及方法參照文獻[3]。
2 結果
2.1 耐藥性GTN 患者一般資料
15 例耐藥性GTN 患者中,<40 歲11 例,≥40 歲4 例;葡萄胎12 例,宮外孕2 例,流產1 例;妊娠終止到開始化療時間:<6 個月者12 例,6~12 個月者3 例;肺轉移4 例;單藥耐藥11 例,多藥耐藥4 例。 見表1。
2.2 治療情況
15 例耐藥GTN 患者在積極護理的前提條件下,采取單體藥物治療者10 例, 化療聯合手術治療者為5 例,經腹全子宮切除術者3 例,子宮病灶剔除術+子宮重建術者1 例,全子宮聯合雙側附件切除術者1例。1 例患者在選用5-FU 方案治療時出現完全緩解。 低危組10 例患者對5-FU 產生耐藥, 其中8 例患者改用聯合化療,2 例改用EMA-CO 方案, 均得到緩解。高危組患者4 例,其中1 例患者因不能耐受藥物副作用而改為單藥5-FU 聯合手術治療方案;3 例改為EMA-CO 方案,其中2 例完全緩解,1 例高危絨癌患者EMA-CO 耐藥,行EMA-EP 方案化療聯合手術治療,達到完全緩解。 在積極護理與治療的情況下,無論單體藥物治療還是化療聯合手術治療,患者完全緩解率均達到100%。
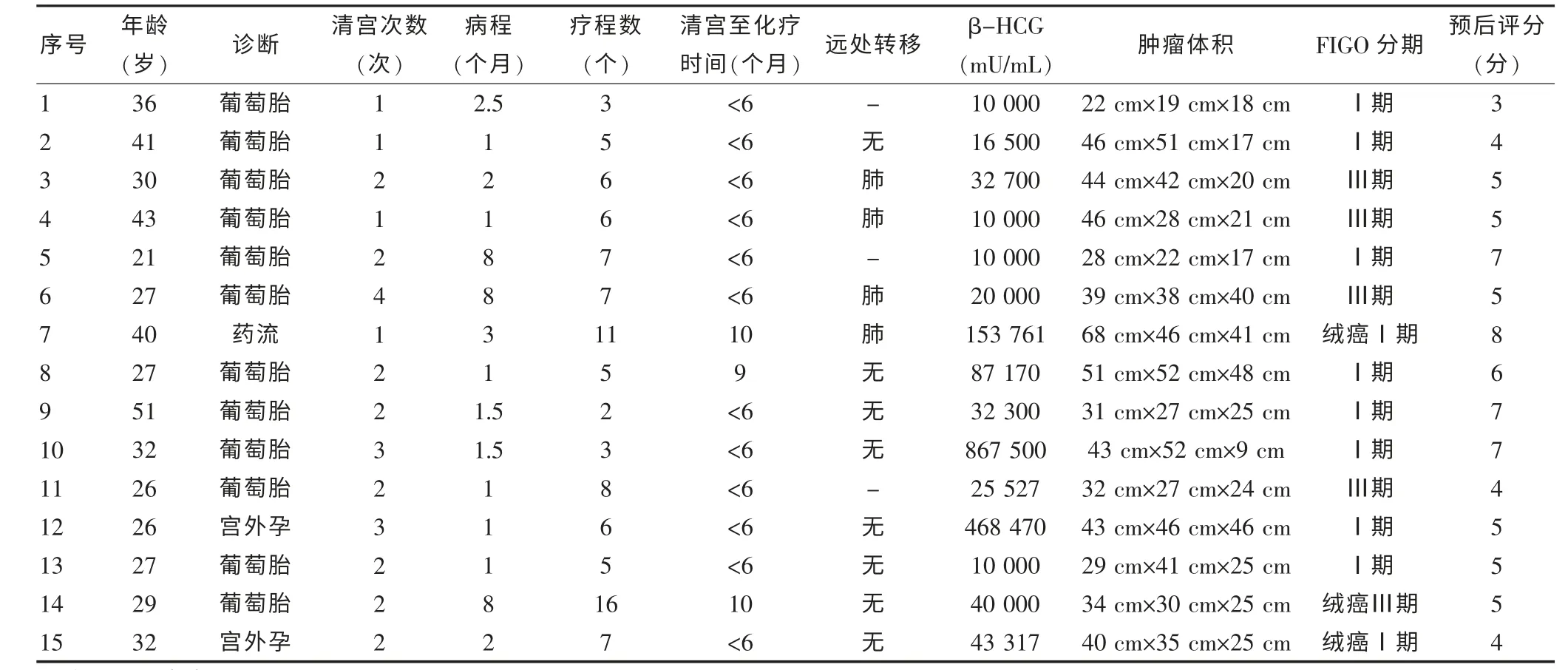
表1 耐藥性滋養細胞腫瘤患者的臨床資料情況
2.3 術后及預后情況
患者出院以后,對其進行隨訪,隨訪時間截止2011 年12 月,全部患者均隨訪0.5~9 年,其中3例治療半年后失訪。 12 例患者達到完全緩解, 即使存在肺轉移,經過治療后其肺部轉移病灶也已消失。 見表2。
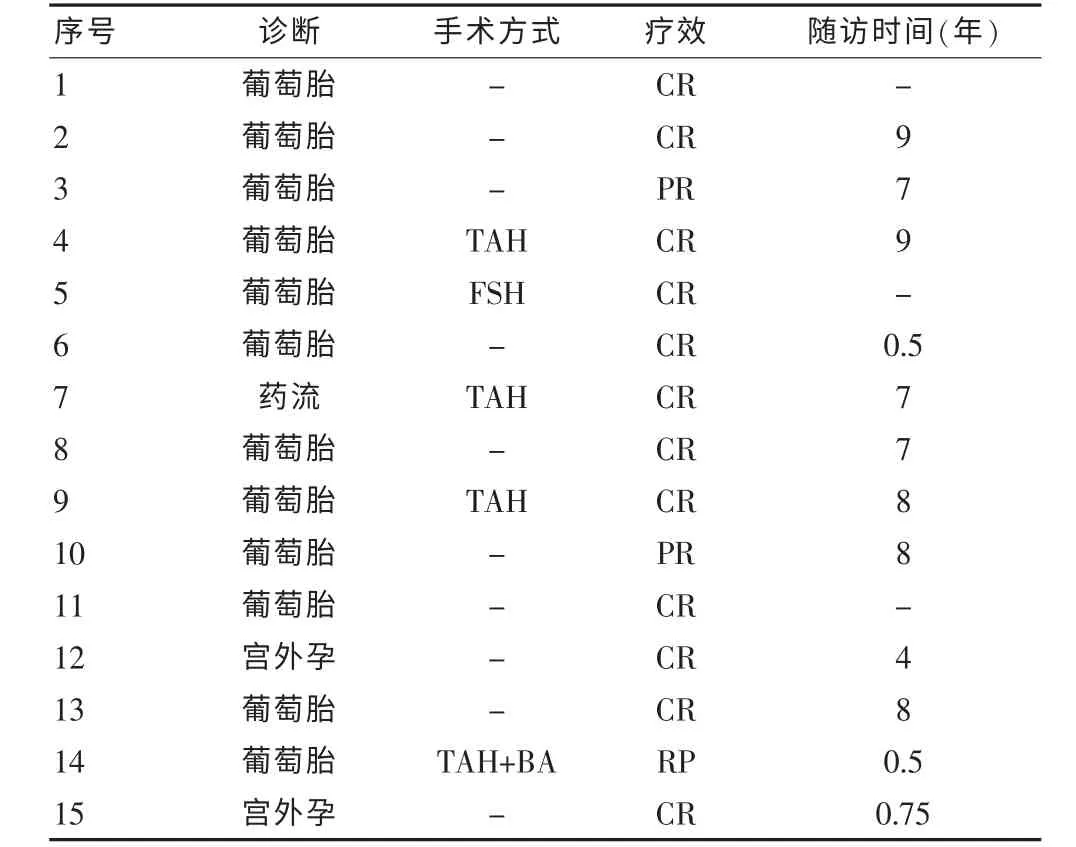
表2 手術及術后隨訪情況
3 討論
3.1 臨床特點
GTN 是育齡婦女中常見的一種惡性腫瘤,本課題中年齡<40 歲者為13 例,符合GTN 的總體發病規律。本研究15 例耐藥性GTN 的患者中,13 例來源于葡萄胎,可見耐藥性GTN 患者大多數來源于葡萄胎。12例侵蝕性葡萄胎中,10 例為終止妊娠后6 個月內發病,可見耐藥性患者的發病時間符合客觀規律,但要特別注意繼發于宮外孕與流產的絨癌患者,其發病時間相對早,且高耐藥。GTN 的轉移途徑主要是經血道轉移,最常見的遠處轉移部位是肺臟,高達80%,其轉移發生時間早且廣泛[3]。 本組數據中,4 例發生肺轉移,主要原因可能是病例數較少,導致誤差明顯偏大,但是絨癌患者的肺轉移率高確是與報道一致,治療時應注意遠處轉移灶,做好治療準備。
3.2 化療
對于高危和耐藥性GTN 患者,采用5-FU 為主的聯合化療方案治療,其CR 可達75%。 對于高危或者耐藥GTN 患者,其能夠耐受的有效的治療方式為EMA-CO 聯合化療方案。 Escobar 等[7]報道的采用EMA-CO 方案治療的45 例高危或耐藥患者中, 其中32 例患者(71%)治療有效,有9 例(20%)患者產生耐藥。 本組結果顯示,低危組10 例對5-FU 產生耐藥,其中8 例患者改用聯合化療,2 例改用EMA-CO 方案,均得到緩解;高危組1 例患者不能耐受藥物副作用而改為單藥5-FU 聯合手術治療;3 例改為EMACO 方案,其中2 例患者完全緩解,提示無論是5-FU為主的聯合化療還是EMA-CO 化療均能使低危耐藥的患者緩解,與文獻報道[7],報道不太一致,可能原因是高危患者數太少,誤差特別大,但是總的結果顯示,5-FU 為主的聯合化療方案對低危耐藥性患者可產生良好療效,EMA-CO 化療方案對高危耐藥性患者有明顯效果。
如果患者在使用EMA-CO 方案后發生耐藥,可以采用三線化療方案,其是以鉑類為主的多藥聯合化療方案。 有報道稱,以EMA-EP 方案為主聯合或不聯合手術治療能夠有效治療對EMA-CO 產生耐藥的患者,其有效率高達70%[8]。Mao 等[8]針對18 例耐藥性腫瘤患者采取EMA-EP 方案治療,其中有11 例患者對EMA-CO 耐藥, 但改用EMA-EP 方案后9 例患者完全緩解,同時使用EMA-CO 治療后復發的患者中,在改用EMA-EP 方案后有3 例患者完全緩解[9]。 本課題中存在1 例高危絨癌患者對EMA-CO 方案產生耐藥,后行EMA-EP 方案化療聯合手術治療,患者完全緩解。 可見EMA-EP 方案能夠有效地治療對EMACO 方案耐藥的患者。
3.3 手術
手術治療對于耐藥或復發的GTN 患者其作用不容忽視。 耐藥的GTN 患者多數為生育期婦女,進行腫瘤治療時保留患者的生育功能十分重要。 本課題中1例患者對5-FU 耐藥,之后改用5-FU 聯合長春新堿聯合更生霉素三聯方案后,因其不能耐受化療帶來的副作用而又改為5-FU 聯合長春新堿治療,其副作用依然存在,而且未見好轉,于是選擇手術治療,術后患者血清β-hCG 水平逐步降至正常。 由于治療后隨訪失敗,未能獲得遠期治療的結果,但是目前為止許多文獻報道聯合化療的基礎上實行手術治療能夠對耐藥的患者產生明顯的療效[5,9-12]。 因此,采取子宮病灶切除術對于有生育要求的年輕女性是一個理想的治療選擇[9]。
研究表明,在對患者進行仔細評估后,如果患者不存在宮外病變,只是單一的產生耐藥,子宮切除術便可以緩解[5],但這類患者數比較少,樣本量不足。 本課題患者中有3 例行全子宮切除術,1 例行全子宮聯合雙附件切除術,4 例患者均獲緩解。 由此可以得出結論:對于耐藥性GTN 患者,子宮切除術是有效、安全的治療方式。
GTN 易發生血道轉移, 發生肺轉移的比例接近75%,其中發生轉移的患者中接近90%的患者可以通過化療方案得到治愈[13-14]。 本組課題中4 例發生肺轉移, 并且只采用化療而均沒有實行肺部手術治療,出院半年后檢查患者肺部,發現病灶都已消失,說明耐藥患者在發生肺部轉移的情況下,大多數也可以通過化療達到治愈,而不需要手術治療。 但是不足之處在于樣本數量少,隨訪時間長短不同,在隨訪期間還未見復發的患者。 但有的資料卻建議通過補救化療后,即使患者的血清β-hCG 下降至正常水平, 仍需選擇肺部手術, 這是因為患者血清β-hCG 水平雖然恢復正常,但是在檢查切除的肺葉時,仍然發現近33.33%的患者肺組織中存在活的腫瘤細胞,如果這些腫瘤病灶不予以徹底切除,將來可能會復發[15-17]。手術前后患者常在心理上會產生很大的心理負擔,更有甚者出現恐懼、焦慮、沮喪等嚴重心理反應,這在患者接受治療時會產生一定的負面影響。因此對患者提供人文關懷護理,不僅能幫助其了解相關疾病的知識,還能增加患者對治療的信心,消除其不良心理,使其積極配合治療,從而縮短綜合治療的時間,減少醫療費用,提高手術效果。 因此,耐藥性GTN 患者發生肺轉移后,實行肺葉切除術,在采取積極護理與治療后,患者的預后良好[18-20]。 可見對于耐藥性GTN 患者,特別是發生了轉移之后,采取化療后的手術治療能夠提高耐藥患者的治療效果。
腫瘤治療失敗的重要原因在于耐藥性的產生,而且到目前為止,對于耐藥性還沒有十分確切的治療方法,另外目前患者例數相對較少,不能做到大規模的前瞻研究,因此,結合相關文獻報道以及前人的經驗總結,再加上臨床上診療水平、技術的提高,為日后提高對耐藥性腫瘤的治療提供強有力的保障。
[1] Wang J,Short D,Sebire NJ,et al. Salvage chemotherapy of relapsed or high-risk gestational trophoblastic neoplasia(GTN)with paclitaxel/cisplatin alternating with paclitaxel/etoposide (TP/TE) [J]. Ann Oncol,2008,19(9):1578-1583.
[2] Lurain JR. Pharmacotherapy of gestational trophoblastic disease [J]. Expert Opin Pharmacother,2003,4(11):2005-2017.
[3] 豐有吉,沈鏗.婦產科學[M].北京:人民衛生出版社,2011:362-366.
[4] Pecorelli S,Ngan HYS,Hacker NF,et al. Staging classifications and clinical practise guidelines for gynecologic cancers [J]. Int J Gynecol Obstet,2000,70:207-312.
[5] 馮鳳芝,向陽,曹楊,等.手術聯合化療治療耐藥性GTN的療效分析[J].中華婦產科雜志,2008,43(10):728-731.
[6] 孫燕,周際昌.臨床腫瘤內科手冊[M].5 版.北京:人民衛生出版社,2007:147-156.
[7] Escobar PF,Lurain JR,Singh DK,et al. Treatment of highrisk gestat ional trophoblastic neop lasia with etoposide,methotrex ate,actinomycin D,cyclophosphamide,and vincristine chemotherapy[J].Gynecol Oncol,2003,91(3):552-557.
[8] Mao Y,Wan X,Lv W,et al. Relapsed or refractory gestational trophoblastic neoplasia treated with the etoposide and cisplatin/ etoposide,methotrexate,and actinomycin D(EP-EMA)regimen [J]. Int J Gynaecol Obstet,2007,98(1):44-47.
[9] Rojas-Espaillat L,Houck KL,Hemandez E,et al. Fertility-sparing surgery for persistent gestational trophoblastie neoplasia in the myometrium:a ease report [J]. J Reprod Med,2007,52(5):431-434.
[10] 唐梅艷,唐冬艷.兩種化療方案治療惡性滋養細胞腫瘤應用分析[J].中國當代醫藥,2012,19(5):166,168.
[11] 雷呈志,向陽.滋養細胞腫瘤動脈化療的臨床應用[J].實用婦產科雜志,2006,22(8):456-458.
[12] 顧宇,范辰辰,馮鳳芝,等.FAV 方案和FAEV 方案作為初始方案治療高危型GTN 的療效比較[J].實用婦產科雜志,2015,31(3):189-193.
[13] 王永學,馮鳳芝,向陽,等.耐藥性GTN 肺轉移患者血β-HCG 正常后肺葉切除術的價值探討[J].實用婦產科雜志,2010,26(11):849-852.
[14] 王景貴,高文萍,王雨紅,等.胎盤部位滋養細胞瘤(PSTT)的病理變化及鑒別診斷[J].中國當代醫藥,2010,17(28):80,83.
[15] 張曉燕,李嬋.米非司酮配合化療藥治療侵蝕性葡萄胎30 例臨床分析[J].中國當代醫藥,2013,20(18):82-83.
[16] 鄭麗娥,曲軍英.惡性滋養細胞腫瘤34 例臨床分析[J].中國醫藥導報,2012,9(24):158-159.
[17] 沙阿代提·吾甫爾,布海切木·卡德爾,古麗娜·阿巴拜克力,等.三種方法治療滋養細胞腫瘤的療效評價[J].中國現代醫生,2015,53(23):44-46,49.
[18] Shrivastava S,Kataki AC,Barmon D,et al. Gestational trophoblastic neoplasia:a 6 year retrospective study[J].South Asian J Cancer,2014,3(1):33-37.
[19] 張彤艷,周虎,韓新彥,等.彩色多普勒超聲在早期診斷滋養細胞腫瘤中的應用價值[J].中國醫藥導報,2012,9(7):81-82.
[20] 曾淑妍,王志龍,黃曉星,等.妊娠疾病的MRI 診斷及病理對照[J].中國醫藥科學,2013,3(8):115-116,122.

