Ⅱ型糖尿病大鼠白內障的ERK通路介導機制及其抑制劑PD98059的改善作用
肖 涵,劉文斌,萬 麗
(南京明基醫院眼科,江蘇 南京 210019)
Ⅱ型糖尿病大鼠白內障的ERK通路介導機制及其抑制劑PD98059的改善作用
肖 涵,劉文斌,萬 麗
(南京明基醫院眼科,江蘇 南京 210019)
目的 分析ERK通路在Ⅱ型糖尿病大鼠白內障發生中的參與機制及PD98059的改善作用。方法35只SD大鼠隨機分為對照組、糖尿病組、PD98059低劑量、中劑量和高劑量組(每組7只)。小劑量STZ聯合高糖高脂飲食120 d復制糖尿病大鼠白內障模型,第64天每天對各組大鼠尾靜脈注射生理鹽水或PD98059。分析各組大鼠晶狀體狀態及胰島素抵抗系數HOMA-IR的變化,Real-time PCR和Western blotting分析晶狀體中ERK通路相關蛋白ERK1/2、p-ERK1/2、p38及內質網應激蛋白ATF6、PERK的表達變化。結果與對照組大鼠比較,糖尿病組大鼠晶狀體明顯渾濁,HOMA-IR明顯增高,晶狀體組織中p-ERK1/2、p38、PERK和ATF6表達上調,而總ERK的表達未發生變化。PD8059可以顯著改善上述晶狀體及相關蛋白表達的異常,且具有劑量依從性。結論激活的ERK信號通路參與了Ⅱ型糖尿病大鼠白內障發病過程,PD95059通過抑制上調表達的p38-pERK1/2及內質網應激起緩解作用。
Ⅱ型糖尿病;白內障;ERK通路;PD98059
現代社會生產和生活方式的改變引起糖尿病的發病率和死亡率逐年升高[1]。糖尿病白內障是糖尿病并發癥中僅次于糖尿病視網膜病變的第二大眼病,嚴重影響患者的視力[2]。糖尿病白內障多發生于病情嚴重的幼年型糖尿病患者,具有發病迅速的特點。糖尿病白內障患者雙眼可能在數天或數周內完全渾濁。白內障的發生與維生素和微量元素的缺乏、紫外線影響以及缺氧等相關。但是,高糖或胰島素抵抗是糖尿病白內障發病的重要因素之一[3]。
ERK1/2(Extracellular signal-regulated kinase)通路是細胞外信號從細胞表面向細胞內傳導的重要媒介,活化的ERK1/2蛋白進入細胞核后促進環腺苷酸應答元件結合蛋白(cAMP response binding protein,CREB)等重要的細胞核內的轉錄因子磷酸化,從而調節一系列的關鍵基因表達,進而參與細胞的增殖、分化和凋亡等過程[4]。內質網是蛋白質合成和翻譯后加工的場所。當受到外部刺激后內質網會發生應激反應,上調內質網應激蛋白PERK(Protein kinase R-like ER kinase)、ATF6(Activating transcription factor 6)等蛋白上調表達,起到對細胞的保護作用。但持續的外部刺激發生時內質網應激會誘導細胞發生凋亡,造成組織損傷。本研究旨在分析ERK通路及內質網應激蛋白在Ⅱ型糖尿病大鼠白內障發生中的參與機制及PD98059的改善作用。
1 材料與方法
1.1 試劑與儀器 鏈脲佐菌素(STZ,Streptozotocin):Sigma,USA(臨用前溶于檸檬酸緩沖液);葡萄糖測定試劑盒:上海榮盛生物藥業有限公司;mRNA提取及逆轉錄試劑盒購自北京天根;冷凍高速離心機(5741R):Eppendorf,Germany;臺式低速離心機(80-2):上海醫療器械(集團)有限公司手術器械廠;電泳儀轉印槽及PVDF膜,Bio-Rad,USA。
1.2 方法 雄性成年SD大鼠35只(220~250 g)購自浙江省實驗動物中心。所有動物操作均符合江蘇省實驗動物管理規范。SD大鼠隨機分為對照組(Cont)、糖尿病組(DM)、PD98059低劑量組(LOW)、中劑量組(MID)和高劑量組(HIGH),每組各7只。對照組大鼠自由飲食,其余各組大鼠給予高糖高脂飼料(74.5%基礎飼料+10%糖+10%豬油+5%蛋黃粉),自由飲水。第29天對照組大鼠給予腹腔注射0.1 mol/L檸檬酸鈉溶液(10 ml/kg),其余各組大鼠腹腔注射小劑量STZ(30 mg/kg,i.p.)。第64天開始各組分別進行尾靜脈治療:對照組和糖尿病組大鼠給予生理鹽水,其余各組分別給予尾靜脈注射等劑量的PD98059(10 μg/L、20 μg/L、40 μg/L)治療。
1.3 胰島素抵抗HOMA-IR 血糖升高和胰島素抵抗是Ⅱ型糖尿病的重要指標,HOMA-IR是用于評價個體的胰島素抵抗水平的指標。胰島素抵抗計算公式:HOMA-IR=空腹血糖水平(Fasting plasma glucose,FPG)×空腹胰島素水平(Fasting insulin,FINS)/22.5。
1.4 Real-time PCR mRNA提取及逆轉錄均按照說明書進行。Real-time PCR反應條件:95℃熱啟動10 min;94℃變性15 s,60℃退火15 s,72℃延伸30 s,72℃收集熒光,共37個循環。反應體系為20 μl:cDNA 2 μl;正向引物(10 μmol/L)0.5 μl;反向引物(10 μmol/L)0.5 μl;2.5×SYBR Green(TianGen)8 μl;無菌水 9 μ l。引物序列如下:β-actin正向引物5'-GGGAAATCGTGCGTGACAT-3';反 向 引 物5'-CAGGAGGAGCAATGATCTT-3';ATF-6正向引物5'-GGATTTGATGCCTTGGGAGTCAGAC-3';反向引物5'-ATTTTTTTCTTTGGAGTCAGTCCAT-3';PERK正向引物5'-AAGATGGTACAGTGGACGGC-3';反向引物5'-CCGTGTTCCTGGTGAAATCT-3'。
1.5 Western blotting 晶狀體組織在冰水浴中用勻漿液充分勻漿,采用考馬斯亮藍法蛋白定量后以等量蛋白進行SDS-PAGE和半干法轉膜。轉至PVDF膜上后5%脫脂牛奶室溫條件下封閉2 h。然后與一抗4℃溫孵12 h,磷酸鹽緩沖液(PBS)漂洗3次后與二抗室溫反應1 h。PVDF膜用PBS漂洗后用ECL混合液顯色、曝光、顯影、定影,用凝膠成像分析系統測定光密度,以β-actin作為參照,進行蛋白表達的定量分析。
1.6 統計學方法 數據統計應用SPSS13.0軟件分析,計量數據以均數±標準差(±s)表示,多組間差異用方差分析法檢驗,事后分析依據方差齊性檢驗結果應用SNK或Dunnett's法檢驗,以P<0.05表示差異有統計學意義。
2 結果
2.1 一般性狀觀察 小劑量注射STZ合并高糖高脂飲食后糖尿病成模大鼠飲水、尿量明顯增加,體重增加明顯。正常對照組大鼠的晶狀體一直清亮,而糖尿病模型組大鼠晶狀體周邊可見到空泡,且有絮狀并呈現乳白色混濁。120 d后糖尿病大鼠晶狀體完全混濁,呈現乳白色。ERK受體阻滯劑PD98059干預組大鼠晶狀體混濁程度較模型組輕,且高劑量組效果最好,具有劑量依從性。
2.2 血糖水平及胰島素抵抗 Ⅱ型糖尿病組大鼠血糖水平、胰島素水平明顯增高,且與對照組比較差異有顯著統計學意義(P<0.01)。而藥物干預后糖尿病組大鼠的FINS水平和HOMA-IR明顯降低,但血糖水平變化不明顯。表明PD98059雖然不具有降低血糖的作用,但能夠改善Ⅱ型糖尿病大鼠的胰島素抵抗狀態,見表1。
表1 糖尿病大鼠血糖及胰島素抵抗及藥物干預作用(±s)
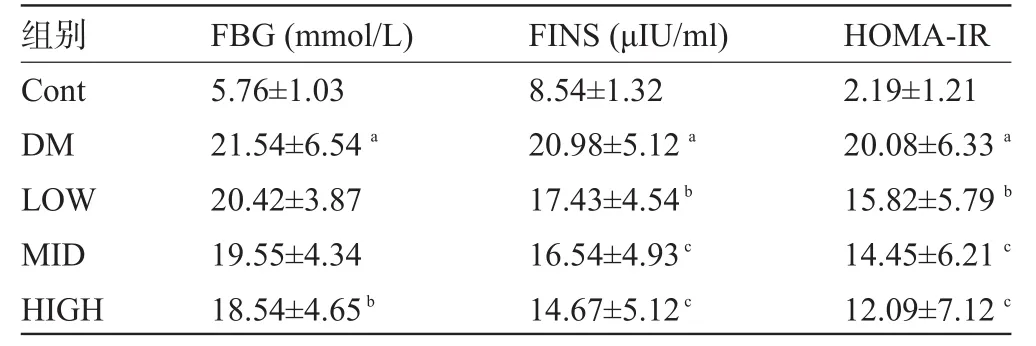
表1 糖尿病大鼠血糖及胰島素抵抗及藥物干預作用(±s)
注:與對照組比較,aP<0.01;與糖尿病組比較,bP<0.05,cP<0.01。
Cont DM LOW MID HIGH 5.76±1.03 21.54±6.54a20.42±3.87 19.55±4.34 18.54±4.65b8.54±1.32 20.98±5.12a17.43±4.54b16.54±4.93c14.67±5.12c2.19±1.21 20.08±6.33a15.82±5.79b14.45±6.21c12.09±7.12c
2.3 p38蛋白的異常表達 與對照組大鼠比較,Ⅱ型糖尿病組大鼠晶狀體的p38蛋白表達明顯增強,且兩組之間差異具有顯著統計學意義(P<0.01)。ERK1/2抑制劑PD98059(20 μg/L、40 μg/L)可以明顯抑制異常表達的p38蛋白,而小劑量的PD98059雖然具有一定的抑制作用,但差異無統計學意義(P>0.05),見圖1。
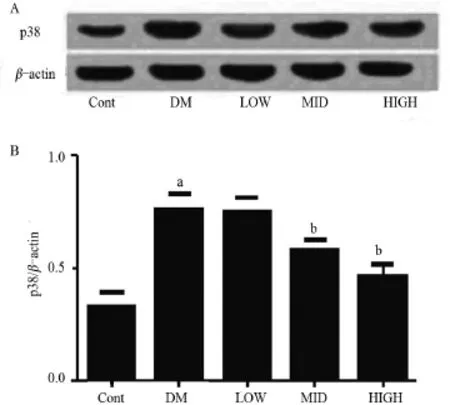
圖1 糖尿病大鼠p38蛋白表達及PD98059的抑制作用
2.4 白內障大鼠ERK通路的激活及PD98059的改善作用 與對照組大鼠比較,糖尿病組大鼠晶狀體的p-ERK1/2蛋白表達明顯上調,且其抑制劑PD98059具有明顯的抑制上調作用,具有劑量依從性,見圖2。提示Ⅱ型糖尿病大鼠白內障并發癥中ERK通路被激活。但是,本文發現各組中ERK1/2蛋白的表達變化差異無統計學意義。
2.5 Real-time PCR和Western blotting檢測內質網應激蛋白ATF6和PERK的表達 糖尿病組大鼠晶狀體的內質網應激分子ATF6及PERK蛋白比對照組明顯上調(P<0.01),而中高劑量的PD98059可以明顯抑制上述異常表達的蛋白,差異具有顯著統計學意義(P<0.01),見圖3。qPCR檢測發現,ATF6和PERK的表達與Western blotting的檢測結果一致,見表2。
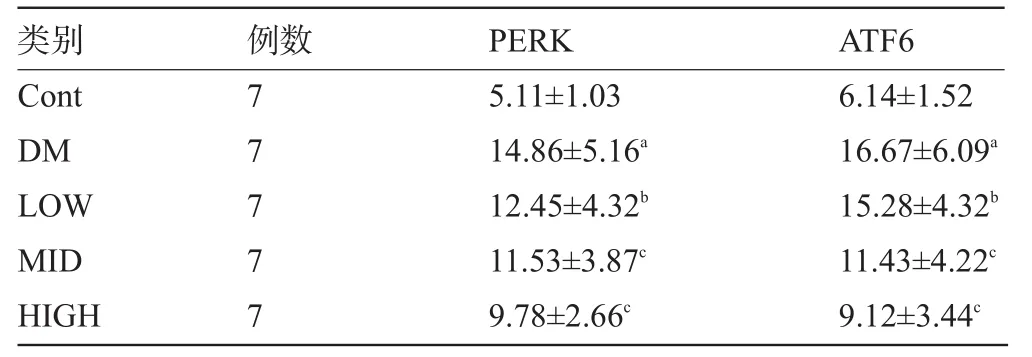
表2 q-PCR分析PERK和ATF6在不同組中mRNA表達的差異性(△Ct)
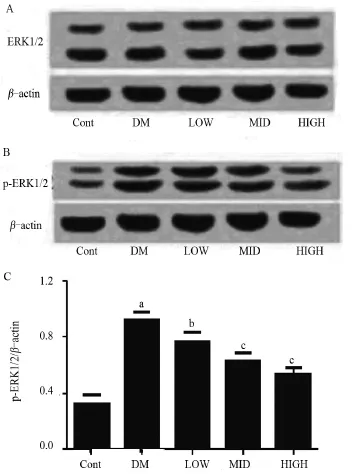
圖2 糖尿病大鼠ERK1/2及p-ERK1/2蛋白表達及PD98059的抑制作用
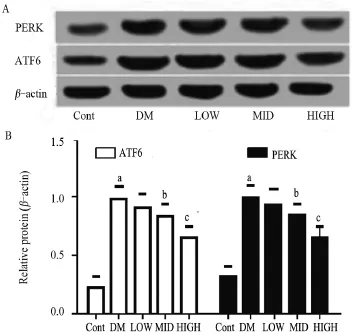
圖3 糖尿病大鼠內質網應激蛋白ATF6及PERK的表達及PD98059的抑制作用
3 討論
糖尿病及其并發癥損傷機體主要通過大血管病變和微血管病變,其中糖尿病眼病是一種糖尿病微血管并發癥[5]。糖尿病白內障患者隨著晶狀體渾濁程度的增加,會出現復視或著多視的病理狀態,并進一步出現視物模糊、怕光,甚至出現看物體顏色較暗或呈黃色的狀態。目前對于糖尿病白內障的病理機制并未完全闡明,臨床上缺乏徹底治療白內障的有效藥物。因此,探索糖尿病白內障的發病機制,對臨床治療和新藥開發具有十分重要的意義。本文在小劑量STZ聯合高糖高脂飲食建立的Ⅱ型糖尿病白內障模型中中發現,激活的ERK通路及內質網應激過程參與了糖尿病白內障模型的發生及發展過程,并且ERK1/2抑制劑PD98059對白內障晶狀體的渾濁具有一定的改善作用,并且對上述異常表達的蛋白都具有一定程度的恢復作用。因此,激活的ERK通路和內質網應激及其引起的細胞凋亡過程可能參與了糖尿病白內障并發癥的發生過程,ERK抑制劑PD98059通過抑制p38和p-ERK1/2蛋白的上調表達及內質網應激分子PERK和ATF6的異常起到對白內障的治療作用。
內質網是細胞內的動態的膜性細胞器,是蛋白質正確合成及修飾的場所。內質網內未折疊或錯誤折疊的蛋白不能轉運到高爾基體內。已有的研究證實,缺氧、應激、高糖及鈣超載等可引起內質網的功能紊亂,導致非折疊蛋白的聚集,引發內質網應激反應。適量應激會激活UPR,使蛋白折疊能力提高、蛋白合成抑制,以適應應激,但是長時間過強的內質網應激狀態則啟動細胞凋亡[6]。ERK通路是細胞外信號向細胞內轉導的重要通路,其中關鍵的蛋白為p38和ERK1/2[7-9]。ERK通路參與了多種病理過程的發生和發展過程,其中涉及多種眼部疾病。本文發現Ⅱ型糖尿病大鼠晶狀體組織中p38蛋白表達顯著上調,同時p-ERK1/2蛋白也顯著增高,表明Ⅱ型糖尿病白內障存在ERK通路的激活。而ERK抑制劑PD98059對上調表達的p38具有明顯的抑制作用,同時對上調的p-ERK1/2也有顯著的恢復作用。因此,PD98059對激活的ERK通路的抑制作用也可能是其恢復糖尿病白內障并發癥的重要途徑。
綜上所述,激活的ERK信號通路參與了Ⅱ型糖尿病大鼠白內障發病過程,而PD95059通過抑制上調表達的p38-pERK1/2及內質網應激異常起緩解作用。
[1]Lim XL,Teo BW,Tai BC,et al.Pentosidine levels in nonproteinuric diabetes associated with both low estimated glomerular filtration rate and cataract[J].Dia Metab Syndr Obes,2012,5:155-164.
[2]Dolber PC,Jin H,Nassar R,et al.The effects of Ins2(Akita)diabetes and chronic angiotensin II infusion on cystometric properties in mice[J].Neurourol Urodyn,2015,34(1):72-78.
[3]Esteves JF,Dai Pizzol MM,Sccoco CA,et al.Cataract and type 1 diabetes mellitus[J].Diabetes Res Clin Pract,2008,82(3):324-328.
[4]Tao Y,Gu YJ,Cao ZH,et al.Endogenous cGMP-dependent protein kinase reverses EGF-induced MAPK/ERK signal transduction through phosphorylation of VASP at Ser239[J].Oncol Lett,2012,4 (5):88-94.
[5]Hermans MP,Ahn SA,Rousseau MF.Statin therapy and cataract in type 2 diabetes[J].Diabetes Metab,2011,37(2):1339-1343.
[6]Mosbah IB,Zaouali MA,Martel C,et al.IGL-1 solution reduces endoplasmic reticulum stress and apoptosis in rat liver transplantation [J].Cell Death Dis,2012,3:e279.
[7]Li J,Zhao Z,Liu J,et al.MEK/ERK and p38 MAPK regulate chondrogenesis of rat bone marrow mesenchymal stem cells through delicate interaction with TGF-beta1/Smads pathway[J].Cell Prolif, 2010,43(4):333-343.
[8]Park SW,Kim HS,Hah JW,et al.Celecoxib inhibits cell proliferation through the activation of ERK and p38 MAPK in head and neck squamous cell carcinoma cell lines[J].Anticancer Drugs, 2010,21(9):823-830.
[9]Wang Z,Ma W,Chabot JG,et al.Calcitonin gene-related peptide as a regulator of neuronal CaMKII-CREB,microglial p38-NFkappaB and astroglial ERK-Stat1/3 cascades mediating the development of tolerance to morphine-induced analgesia[J].Pain,2010,151(1): 194-205.
Involvement of ERK pathway in cataract in typeⅡdiabetes and alleviations of PD98059,inhibitor of ERK.
XIAO Han,LIU Wen-bin,WAN Li.Department of Ophthalmology,Nanjing Benq Hospital,Nanjing 210019,Jiangsu,CHINA
ObjectiveTo explore the involvement of ERK pathway in the pathogenesis of typeⅡdiabetic cataract and the interventions of PD98059(the inhibitor of ERK).MethodsThirty-five male SD rats were divided into five groups:control group,diabetic group,low/middle/high dose of PD98059 group(n=7 in each group).The typeⅡdiabetic cataract model was duplicated by low dose of STZ injections combined with high content of fat and sugar diet for 120 d.All the rats were administrated with normal saline or PD98059.The HOMA-IR was calculated in each group.And at the same time,the expression of ERK1/2,p-ERK1/2,p38,ATF6 and PERK were detected by Western blotting or real-time PCR.ResultsThe HOMA-IR in diabetic group was increased greatly with cloudy lens when compared to the control group.The expression of p-ERK1/2,p38,ATF6 and PERK were up-regulated dramatically in diabetic group,while the expression of total ERK has no change.PD98059 alleviated the cloudy lens in diabetic rats significantly and normalized the aforementioned abnormal proteins greatly.ConclusionActivated ERK pathway and endoplasmic reticulum stress are involved in the pathogenesis of cataract in typeⅡdiabetes.PD98059 alleviates the cataract by inhibiting the aforementioned parameters in a dose dependent manner.
TypeⅡdiabetes;Cataract;ERK pathway;PD98059
R-332
A
1003—6350(2015)07—0944—04
10.3969/j.issn.1003-6350.2015.07.0339
2014-10-29)
劉文斌。E-mail:71655692@qq.com

