利拉魯肽對小鼠脂肪細胞脂肪因子、炎癥因子及其信號通路的影響*
崔智慧,崔 巖,孫高潔,王 姣,王守俊
鄭州大學第一附屬醫院內分泌科鄭州450052
肥胖易引起相關機體紊亂,如胰島素抵抗、糖尿病、動脈粥樣硬化、高血壓和慢性腎臟病變等,并且增加心血管病的發病率和病死率[1]。研究[2]稱約90%的2 型糖尿病患者超重或肥胖。機體肥胖狀態時最主要的病理學改變是脂肪組織增生肥大和脂肪細胞功能受損,由此可誘發脂肪細胞炎癥反應和胰島素抵抗。越來越多的研究[3]證實脂肪組織能夠生成和分泌大量的細胞因子、生長因子和活性肽等。因此,脂肪組織被認為是一種十分重要的內分泌器官,其所分泌的脂肪因子不僅參與生理狀態下糖脂代謝、免疫及心血管功能的維持與調控,而且在肥胖、炎癥、代謝綜合征和心血管疾病等的發生和發展中扮演著重要的角色[4]。對脂肪因子瘦素、脂聯素、CTRP3 和炎癥因子TNF-α、IL-6 的研究,為未來糖尿病及肥胖相關性疾病的治療提供了新的思路[5]。該研究旨在觀察新型降糖制劑胰高血糖素樣肽-1 類似物利拉魯肽對小鼠脂肪細胞脂肪因子、炎癥因子的影響,探討利拉魯肽改善胰島素抵抗的分子機制及其對炎癥信號通路影響的相關機制。
1 材料與方法
1.1 細胞和試劑 小鼠前脂肪細胞株3T3-L1 細胞購自武漢博士德公司。地塞米松(Dex)、胰島素、3-異丁基-1-甲基黃嘌呤(3-isobuthyl-1-methylxanthine,IBMX)購自美國Sigma 公司;Trizol 試劑盒購自Invitrogen 公司;逆轉錄試劑盒購自Thermo Fisher Scientific 公司;熒光定量PCR 試劑盒購自Roche 公司;IKK-β 抗體、磷酸化IKK-β(ser181)抗體及辣根過氧化物酶(HRP)標記的山羊抗兔IgG 均購自上海碧云天生物技術有限公司。
1.2 細胞的培養及誘導分化成熟 將3T3-L1 前脂肪細胞接種于含體積分數10%胎牛血清的DMEM高糖雙抗培養基中,于37℃、體積分數5%CO2條件下培養,待細胞生長至完全融合,48 h 后換用含1 μmol/L Dex、0.5 μmol/L 胰島素、0.5 mmol/L IBMX的DMEM 高糖培養基誘導分化,3 d 后換用含1 μmol/L Dex、0.5 μmol/L 胰島素的DMEM 高糖培養基繼續培養,每2 d 換液1次,至第10天,約90%的細胞呈脂肪細胞表型時行下一步處理。
1.3 實驗分組及處理 將利拉魯肽溶于培養基中,配成終濃度為10-5mol/L 的溶液。0(對照)、1、10和100 nmol/L 利拉魯肽處理細胞48 h 后收集細胞備用,100 nmol/L 利拉魯肽分別處理細胞0、8、24 和48 h 后收集細胞備用,每組均設3個復孔。
1.4 qRT-PCR 檢測各因子的表達水平 根據GenBank 中的瘦素、脂聯素、CTRP3、TNF-α、IL-6 和內參β-actin 的基因序列設計引物,由生工生物工程(上海)股份有限公司合成,引物序列見表1。使用Trizol 法分別提取上述各組脂肪細胞的總RNA,逆轉錄成cDNA,然后行qRT-PCR 擴增。反應體系:上、下游引物(1 μmol/L)各4 μL,SYBR Green 10 μL,Rnase-free 水10 μL,cDNA 2 μL。反應條件:95℃預變性10 min;95℃變性10 s,60℃退火/延伸10 s。每次延伸步驟結束后,通過檢測反應體系中SYBR Green 與雙鏈DNA 結合后所發出的熒光強度來定量PCR 擴增產物大小。
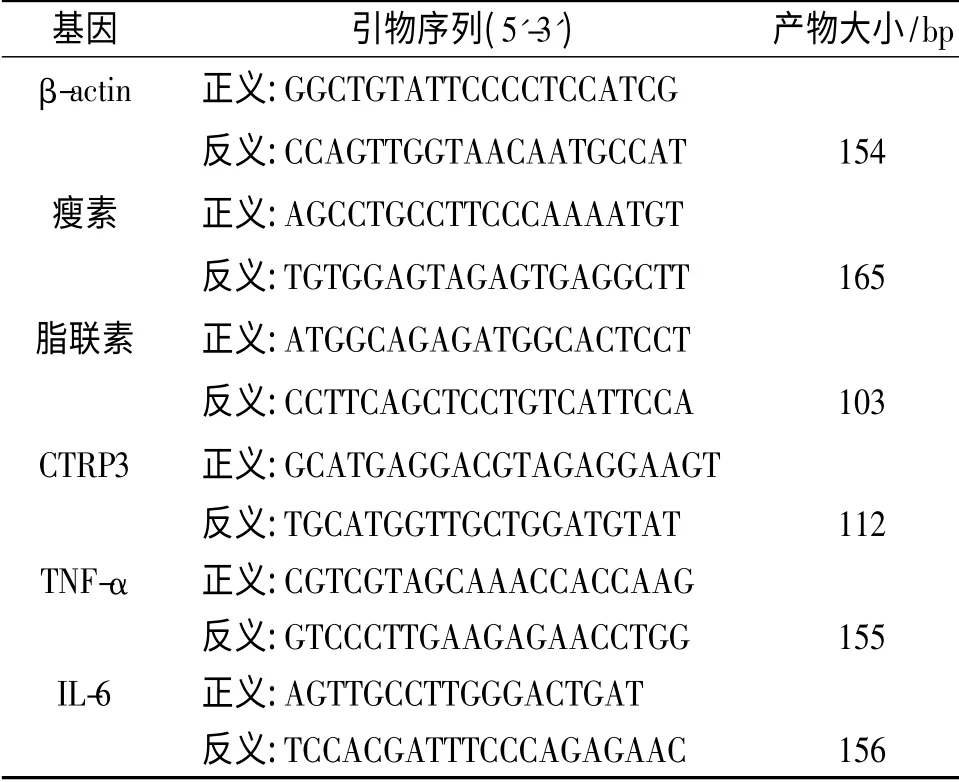
表1 PCR 引物序列
1.5 IKK-β 及ser181 蛋白表達的檢測 收集0、1、10 和100 nmol/L 利拉魯肽處理48 h 后的細胞,提取細胞總蛋白,BCA 法測定蛋白濃度,采用Western blot檢測IKK-β 及ser181 蛋白的表達。SDS-PAGE 膠上樣,電泳、轉膜、封閉,一抗稀釋1 000 倍后使用,搖床4℃孵育過夜,TBST 洗膜5 min ×3次,加HRP 標記的稀釋1 000 倍的二抗孵育1 h,DAB 顯色。
1.6 統計學處理 采用SPSS 17.0 進行數據分析,不同濃度利拉魯肽作用于3T3-L1 脂肪細胞和100 nmol/L 利拉魯肽作用于3T3-L1 脂肪細胞0、8、24、48 h 對脂肪因子和炎癥因子mRNA 表達的影響,以及不同濃度利拉魯肽對3T3-L1 脂肪細胞IKK-β 及ser181 蛋白表達的影響采用單因素方差分析,組間兩兩比較采用LSD-t 法,檢驗水準α=0.05。
2 結果
2.1 不同濃度利拉魯肽作用于3T3-L1 脂肪細胞48 h 后對脂肪因子、炎癥因子mRNA 表達的影響見表2。
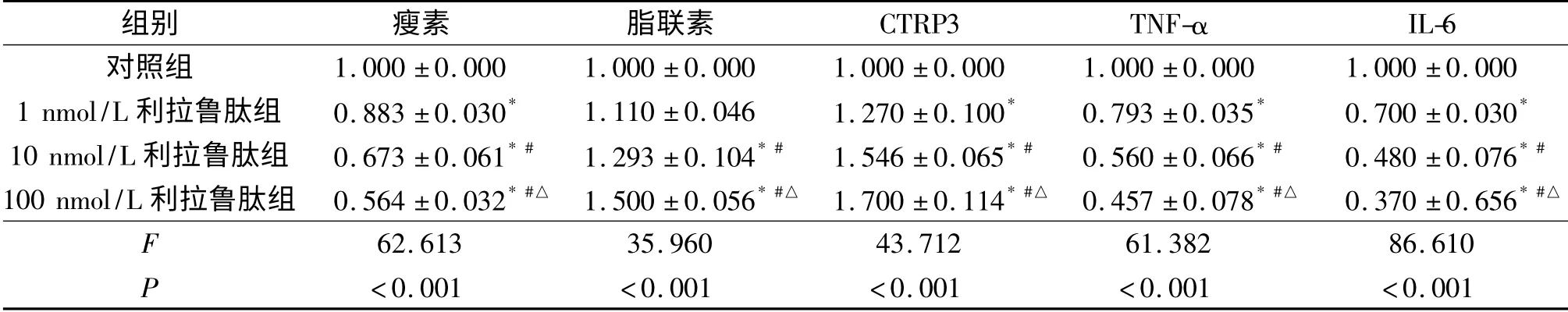
表2 不同濃度利拉魯肽對3T3-L1 脂肪細胞脂肪因子和炎癥因子mRNA 表達的影響(n=3)
2.2 100 nmol/L 利拉魯肽作用于3T3-L1 脂肪細胞不同時間對脂肪因子及炎癥因子mRNA 表達的影響 見表3。
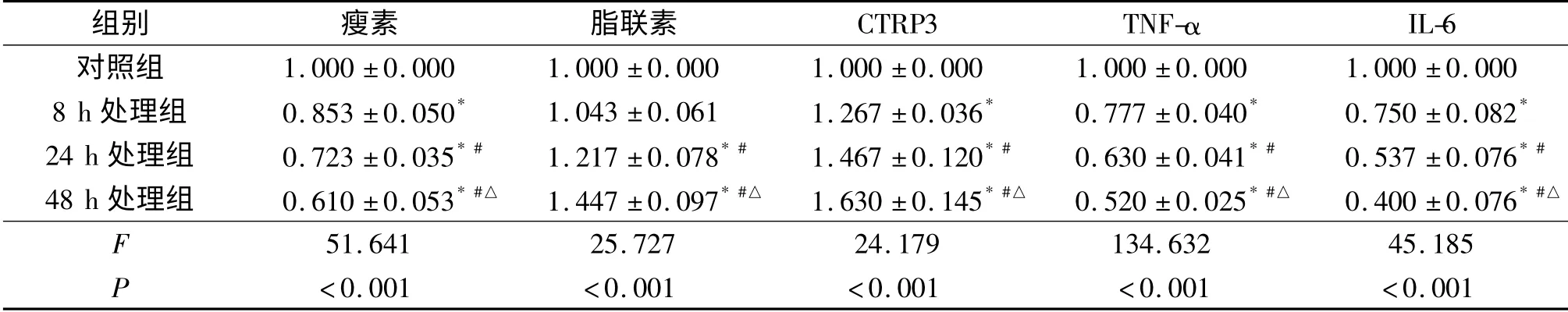
表3 100 nmol/L 利拉魯肽作用不同時間對3T3-L1 脂肪細胞脂肪因子和炎癥因子mRNA 表達的影響(n=3)
2.3 不同濃度利拉魯肽對3T3-L1 脂肪細胞IKKβ、ser181 蛋白表達的影響 0、1、10 和100 nmol/L利拉魯肽作用于3T3-L1 脂肪細胞48 h 后對IKK-β蛋白的表達水平無影響,而對IKK-β 蛋白的磷酸化有抑制作用,且呈劑量依賴性。見圖1。
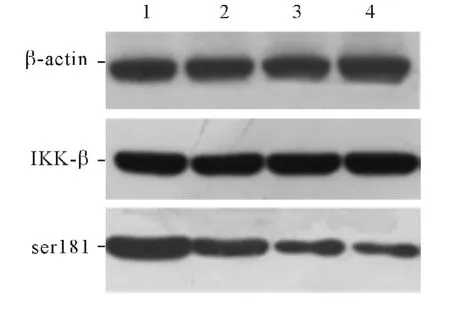
圖1 不同濃度利拉魯肽對3T3-L1脂肪細胞IKK-β、ser181 蛋白表達的影響
3 討論
2 型糖尿病患者常伴有肥胖、血脂紊亂、非酒精性脂肪肝等代謝相關性疾病[6]。新型抗糖尿病藥物利拉魯肽不僅具有控制血糖、減輕體重、改善胰島素抵抗和降低心血管疾病發生風險的作用,還具有潛在的抗炎作用,能夠改善肥胖患者的慢性炎癥狀態。
該研究結果顯示利拉魯肽能夠降低3T3-L1 脂肪細胞瘦素、TNF-α、IL-6 mRNA 的表達。瘦素是由肥胖基因所編碼的一種分泌型蛋白質,其表達的增加與胰島素抵抗呈正相關。TNF-α 可對脂肪細胞的生理功能產生多種影響,如活化細胞因子的基因表達、加速胰島素抵抗的發生等[7]。IL-6 可介導肥胖誘發的慢性炎癥和胰島素抵抗。利拉魯肽降低3T3-L1 脂肪細胞TNF-α、IL-6 mRNA 表達的結果表明其在體外有抗炎作用。該研究結果亦顯示利拉魯肽能夠增加3T3-L1 脂肪細胞脂聯素和CTRP3 mRNA 的表達。脂聯素在體內的生理作用主要是增加胰島素的敏感性和促進糖脂代謝[8],并且通過與其他炎癥因子的相互調節控制炎癥反應。CTRP3 是近年發現的新型脂肪因子,與脂聯素高度同源[9]。相關研究[10]表明,CTRP3 基因敲除的類風濕關節炎小鼠的關節病變更為嚴重,證實CTRP3 具有抗炎作用。該研究結果表明利拉魯肽可通過增加抗炎脂肪因子的表達而改善機體的炎癥狀態。
IKK/Iκ/NF-κ 通路是體內主要的炎癥信號通路。IKK-β 可以直接刺激IRS-1 導致絲氨酸抑制性磷酸化,損害胰島素信號傳導[11],更重要的是IKKβ 激活核轉錄因子NF-κB,后者激活包括TNF-α 和IL-6 在內的多種細胞因子的基因轉錄,進一步抑制胰島素信號傳導[12]。因此,IKK-β 信號通路的激活是導致細胞炎癥反應和胰島素抵抗的重要調節因素。該研究中利拉魯肽在一定的濃度范圍內呈劑量依賴性地抑制ser181 蛋白表達,而不改變IKK-β 蛋白的表達,推測利拉魯肽可能通過降低IKK-β 的磷酸化水平發揮改善機體炎癥狀態的功能。
綜上所述,利拉魯肽不僅能夠減少炎癥因子TNF-α、IL-6 的表達,而且能夠增加抗炎脂肪因子脂聯素、CTRP3 的表達,而這些作用可能通過抑制IKK-β 的磷酸化實現。
[1]Leal Vde O,Mafra D.Adipokines in obesity[J].Clin Chim Acta,2013,419:87
[2]Jiao P,Xu H.Adipose inflammation:cause or consequence of obesity-related insulin resistance[J].Diabetes Metab Syndr Obes,2008,1:25
[3]Waki H,Tontonoz P.Endocrine functions of adipose tissue[J].Annu Rev Pathol,2007,2:31
[4]Maury E,Brichard SM.Adipokine dysregulation,adipose tissue inflammation and metabolic syndrome[J].Mol Cell Endocrinol,2010,314(1):1
[5]祝燁,黃德嘉.脂肪因子的研究進展[J].生物醫學工程學雜志,2010,27(2):476
[6]朱雅靜,朱立勤.利拉魯肽對肥胖2 型糖尿病患者代謝及炎癥指標的影響[J].中國慢性病預防與控制,2014,22(1):88
[7]Ikeoka D,Mader JK,Pieber TR.Adipose tissue,inflammationand cardiovascular disease[J].Rev Assoc Med Bras,2010,56(1):116
[8]Spranger J,Kroke A,M?hlig M,et al.Adiponectin and protection against type 2 diabetes mellitus[J].Lancet,2003,361(9353):226
[9]Maeda T,Abe M,Kurisu K,et al.Molecular cloning and characterization of a novel gene,CORS26,encoding a putative secretory protein and its possible involvement in skeletal development[J].J Biol Chem,2001,276(5):3628
[10]Murayama MA,Kakuta S,Maruhashi T,et al.CTRP3 plays an important role in the development of collagen-induced arthritis in mice[J].Biochem Biophys Res Commun,2014,443(1):42
[11]Gao Z,Hwang D,Bataille F,et al.Serine phosphorylation of insulin receptor substrate 1 by inhibitor kappa B kinase complex[J].J Biol Chem,2002,277(50):48115
[12]Shoelson SE,Lee J,Goldfine AB.Inflammation and insulin resistance[J].J Clin Invest,2006,116:1793

