丙肝檢測單試劑陽性獻血者的分析
陳紅
(九江市中心血站,江西九江332000)
?
丙肝檢測單試劑陽性獻血者的分析
陳紅
(九江市中心血站,江西九江332000)
摘要:目的分析九江地區獻血者丙肝ELISA檢測不合格標本,了解丙肝試劑的使用情況,探討丙肝ELISA檢測灰區設置的必要性和單試劑檢測陽性獻血者的回歸問題。方法2013年1月-2015年12月本地區無償獻血標本用2種丙肝ELISA檢測,陰性標本再進行核酸檢測,單試劑陽性的標本進行核酸檢測和丙肝確認試驗。結果2種抗-HCV ELISA試劑不相符合率高達53.88%(125/232),但2種試劑無統計學差異;125份單試劑陽性的標本中有5份(4.0%)確認試驗為陽性。結論丙肝ELISA檢測灰區設置有必要性,但設置的范圍有待于進一步的探討;抗-HCV ELISA檢測單試劑陽性標本假陽性高,我們應根據本站的實際情況,制定反應性獻血者屏蔽和回歸的方案,既最大限度地保證血液安全,同時減少不必要的血液資源浪費。
關鍵詞:獻血者;丙肝;ELISA檢測;確證試驗;回歸
丙型病毒性肝炎(viral hepatitis type C,HC簡稱丙型肝炎),系丙型肝炎病毒(HCV)感染所引起的疾病,臨床表現與感染途徑和乙型肝炎相似,除了性傳播和母嬰傳播外,主要是經血源性傳播,如輸血、血透析、靜脈注射毒品、移植等。丙肝對人類健康的威脅不亞于乙型肝炎,同時由于丙肝抗體不是中和性抗體,對人體無保護作用,所以人類對丙肝普遍易感。經初步調查,輸血后非甲非乙型肝炎患者血清丙肝抗體(抗HCV)陽性率高達80%以上,已成為大多數輸血后肝炎的原因[1]。所以嚴格篩查獻血者,保證血液安全是血站的職責。目前丙肝的檢測方法主要有酶聯免疫吸附法(ELISA)和核酸檢測法(NAT)。根據國家相關標準[2,3]規定獻血者丙型肝炎病毒(HCV)感染標志物的檢測方法:可采用2個不同廠家的ELISA試劑或1種ELISA試劑和1種NAT試劑。為了解丙肝試劑的使用情況,更好地保障血液安全,對本站2013年1月-2014年12月獻血者,采用2個不同廠家的ELISA試劑檢測丙肝抗體,ELISA檢測陰性和單試劑陽性的樣本再進行NAT檢測,單試劑陽性的樣本進行了丙肝的確證試驗,現將檢測情況分析、報告如下。
1 材料與方法
1.1樣本來源2013年1月-2015年12月九江地區無償獻血者,體檢合格后采血,同時留取2管5± 1ml樣本,其中1管用EDTA-K2抗凝的真空采血
管,用于ELISA檢測;1管用無菌、無DNA酶、無RNA酶、帶分離膠的EDTA-K2抗凝BD真空采血管,用于核酸檢測。采集樣本共計131179份,所有樣本在2~8℃保存,1600g離心20min,48h內完成ELISA和NAT檢測。
1.2試劑與儀器
1.2.1 ELISA試驗丙型肝炎病毒ELISA檢測為檢測丙肝抗體,使用廈門新創和北京萬泰試劑,試劑都具有國家合格的批批檢定證書,在規定的效期內使用;使用在校驗期內的澳斯邦STAR全自動加樣儀和FAME全自動酶免儀儀器完成檢測。
1.2.2核酸試驗試劑使用美國羅氏公司提供的乙型肝炎病毒、丙型肝炎病毒、人類免疫缺陷病毒(1+2型)核酸聯合檢測試劑,在試劑的有效期內使用;使用在校驗期內的美國羅氏Cobas S201全自動核酸檢測系統完成檢測。
1.2.3確證試驗使用北京萬泰丙肝重組免疫印跡確證試劑,在規定的效期內使用。
1.3方法
1.3.1 ELISA試驗用2種ELISA試劑對131179份樣本進行丙肝抗體檢測,按照試劑的操作說明書進行嚴格的操作,試驗結果陰陽性對照均成立,室內質控在可控范圍內。任何1種試劑S/CO值≥1.0為反應性,0.85≤S/CO值<1.0為灰區,任一種試劑檢測S/CO值≥0.85的,則重取血袋上血辮血雙試劑雙孔同時復試,復試后任1種試劑任1孔S/CO值≥的,判為陽性。
1.3.2核酸試驗抗-HCV ELISA試驗陰性和單試劑陽性的樣本共131072份進行核酸檢測,由全自動加樣儀自動進行6份標本的混樣,由羅氏Cobas S201全自動核酸檢測系統使用相配套的羅氏核酸定性篩查試劑進行HBV-HCV-HIV NAT檢測。每批核酸檢測均設置1個陰性質控和5個陽性質控,每個反應池均含有內部對照。反應池檢測為無反應性的,判定6份樣本全合格;反應池檢測為反應性,對該反應池中的6份樣本進行單份拆分檢測,拆分試驗為無反應性的判定為NAT檢測陰性,反之拆分試驗為反應性的判定為NAT檢測陽性。陽性的樣本送羅氏公司委托做鑒別試驗。
1.3.3確證試驗125份HCV單試劑陽性的樣本進行確證檢測(重組免疫印跡法RIBA),至少出現2種HCV抗體特異條帶(Core、NS3、NS4、NS5)強度1+及以上判為陽性,僅出現1種HCV抗體特異條帶強度1+及以上判為不確定[4]。
1.4統計學分析采用SPSS 17.0軟件進行統計學的數據分析,組間率采用χ2檢驗進行比較,P<0.05為差異有統計學意義。
2 結果
2.1 3年抗-HCV ELISA檢測,A、B試劑之間差異無統計學意義,結果見表1。

表1 2種HCV- ELISA試劑檢測結果
2.2 125份單試劑不合格的樣本確證試驗有103份為陰性,22份為陽性或不確定。22份的結果及S/CO值的分布見表2、表3。

表2 22份確證陽性(不確定)結果
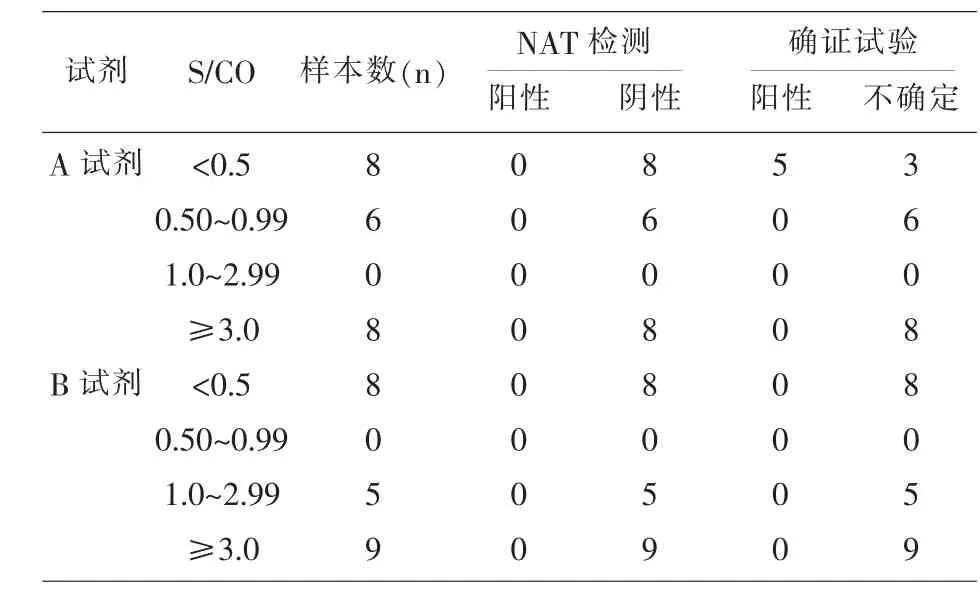
表3 22份確證陽性(不確定)樣本S/CO值分布
3 討論
用抗-HCV ELISA試劑檢測131179份樣本,不合格樣本232份,不合格率0.18%,低于浙江溫州0.27%[5]和河北承德0.42%[6]。雖然ELISA檢測試劑具有價格便宜,操作簡單,穩定性好,可自動化進行檢測和結果分析等諸多的優點[7],但在實際工作中,導致ELISA檢測結果假陽性的因素較多,如不同廠家試劑敏感性和特異性有差異、所選用的抗原或抗體組合不完全相同、內源性物質以及樣本溶血等[8]。表1數據顯示兩種試劑不相符率達53.88%(125/232),低于河南安陽58.5%[9],但2種試劑無統計學差異。丙肝由于其病毒結構的特殊性,兩種試劑的不相符率遠高于梅毒ELISA法14.99%[10],因此筆者認為國產丙肝檢測試劑的質量還有待于進一步的提高。隨著核酸檢測技術的推廣和應用,使經血液傳播疾病標志物的檢測窗口期大為縮短,因此核酸檢測在一些發達國家已經用于常規獻血者血液篩查,我國部分地區也已經開展核酸檢測[11,12]。125份丙肝單試劑陽性的樣本進行核酸檢測,未檢出陽性,分析原因,可能有以下幾方面:⑴本地區處于HCV的低流行區;⑵HCV是RNA病毒,對溫度的變化較敏感,相對穩定性不夠好,較易降解;⑶檢測系統本身的靈敏度、樣本病毒載量較低、病毒在樣本中呈不規則的分布和核酸檢測抓取病毒的隨機性;⑷試驗樣本數量達不到足夠的大等等。
有相關研究顯示,ELISA檢測丙肝抗體,單一試劑陽性的樣本確證試驗多為陰性[13,14],125份單試劑陽性的樣本進行重組免疫印跡確證試驗,僅有5份陽性,陽性率4.0%,低于河南安陽8.3%[9]。表2,3數據顯示,確證試驗為陽性的標本,ELISA檢測1種試劑S/CO均在2.5以上,另1種試劑S/ CO均在0.5以上,提示如果用單試劑檢測丙肝抗體存在漏檢的風險,雖然大部分的血站實驗室為了更好地保證血液安全,ELISA法檢測都設置了灰區,但筆者建議乙肝、丙肝、艾滋和梅毒的灰區應分別設置,應結合本實驗室近年的試驗數據來確定,既最大限度地保證血液安全,同時減少不必要的血液資源浪費。
試驗數據顯示,丙肝單試劑陽性的樣本假陽性高,這樣既造成獻血者對自己身體狀況的擔憂,還使其成為永久的淘汰者,不能再參加無償獻血,剝奪了他們為社會奉獻愛心的權利,造成了固定獻血者的流失和血液資源的不必要浪費。針對血液篩查假陽性的問題,國外除了對血液篩查反應性結果做確證試驗外,還制定了關于獻血者假陽性回歸的相關政策,對某些獻血者部分血液篩查不合格的,經過一段時間的屏蔽后進行再次檢測,檢測合格的獻血者可以重新參加獻血[15]。郭永健、葛紅衛等國內專家也為我們提供了相應的回歸策略[16,17],但由于確證試劑價格較高,一般血站難以長期開展,但我們可以結合本站工作實際和核酸試驗,制定反應性獻血者屏蔽和回歸的方案,讓假陽性者重新回歸到獻血者隊伍中。
參考文獻
[1]胡麗華.臨床輸血學檢驗[M].第3版.北京:人民衛生出版社,2013:222.
[2]衛生部.血站技術操作規程[S].衛醫政發[2012]1號. 2012:13.
[3]衛生部.全血及成分血質量要求[S]. GB18469-2012. 2012:13.
[4]葉應嫵,王毓三,申子瑜.全國臨床檢驗存在規程[M].第3版.南京:東南大學出版社,2006:623-628.
[5]朱紫苗.溫州地區2007-2012年無償獻血者血液感染性指標檢測結果分析[J].中國輸血雜志,2014,27(1):71-73.
[6]王天恒,董志偉,王淑香.承德地區無償獻血人群HBV、HCV、HIV感染情況調查[J].中國輸血雜志,2013,26(1):68-69.
[7]田華. 4394例新生兒HIV、HCV、HBV、TP檢測結果分析[J].實驗與檢驗醫學,2013,31(5):480-481.
[8]陳景芬,張員梅,劉殿香. ELISA檢測抗HCV影響因素分析[J].中華醫學實踐雜志,2007,2(6):152.
[9]武麗娟.反應性獻血者屏蔽與歸隊的探討[J].臨床輸血與檢驗,2015,17(2):153-155.
[10]陳紅.無償獻血者TP-ELISA檢測不合格標本分析[J].實驗與檢驗醫學,2015,33(4):473-475.
[11]Stramer SL,Glynm SA,Kleinman SH,et al. Detection of HIV-1 and HCV infections among antibody-negative blood donors by nucleic acid-amplification testing [J]. N Engl J Med,2004,351(8):760-768.
[12]Soldan K,Davison K,Dow B. Estimates of the frequency of HBV,HCV,and HIV infectious donations entering the blood supply in the United Kingdom,1996-2003[J]. Euro Surveil,2005,10(2):17-19.
[13]Wu S,Liu Y,Cheng L,et al. Clinical evaluation of the signal-tocutoff ratios of hepatitis C virus anti-body screening tests used in China[J]. J Med Virol,2011,83(11):1930-1937.
[14]李雪梅,楊茂春,楊春晴,等.獻血者HBsAg、抗-HCV、抗-HIV、抗-TP ELISA檢測陽性與確證試驗的對比研究[J].中國輸血雜志,2013,26(6):541-543.
[15]Zou S,Musavi F,Notari EP,et al. Donor deferral and resulting donor loss at the American Red Cross Blood Services,2001 throuˉ gh 2006[J]. Transfusion,2008,48(12):2531-2539.
[16]郭永健,姚鳳蘭,林授,等譯. HIV-1和HCV核酸檢測、血液處置和獻血者屏蔽與歸隊指引(上)[J].中國輸血雜志,2011,24 (1):79-84.
[17]葛紅衛,林授,汪德海,等譯. HIV-1和HCV核酸檢測、血液處置和獻血者屏蔽與歸隊指引(下)[J].中國輸血雜志,2011,24 (2):172-176.
(收稿日期2016-01-27;修回日期2016-02-15)
DOI:10.3969/j.issn.1674-1129.2016.02.045
中圖分類號:R193.3,R457.1+2
文獻標識碼:A
文章編號:1674-1129(2016)02-0248-03

