5-Aza-dC在肺癌細胞系中去甲基化作用機制
童波 鐘進生 梁瑩 吳西雅 肖祖克 周洪 郭玲玲
5-Aza-dC在肺癌細胞系中去甲基化作用機制
童波 鐘進生 梁瑩 吳西雅 肖祖克 周洪 郭玲玲
目的 研究5-Aza-dC對肺癌細胞系中的去甲基化的作用。方法 對正常肺細胞以及5-Aza-dC分組處理的A549、NCI-H520甲基化特異性PCR和RT-PCR定量檢測。結果 未處理的A549和NCI-H520細胞中TFPI-2表現出完全甲基化特異性。而經過5-Aza-dC處理過的肺癌細胞系細胞則表現出不完全甲基化狀態,并呈現出量效關系。A549和NCI-H520細胞在經5-Aza-dC處理后TFPI-2基因mRNA表達均明顯高于未處理組,差異具有統計學意義(P<0.05);并呈現出量效關系。結論 5-Aza-dC對肺癌細胞中的TFPI-2基因具有去甲基化作用,并具有量效關系。
5-Aza-dC;TFPI-2;甲基化;A549;NCI-H520
肺癌是一種死亡率較高的呼吸系統惡性腫瘤[1]。雖然對肺癌所采用的治療方案在不斷的改善,患者5年生存率卻未獲得提高[2]。惡性腫瘤的侵襲和轉移是造成肺癌臨床治療失敗和患者死亡的主要原因[3]。早期治療生存率明顯高于晚期治療的患者[4]。基因甲基化是腫瘤分子生物學研究的熱點[5]。在腫瘤發生發展中通過去甲基化處理可恢復抑癌基因的表達,從而達到防治腫瘤的目的[5-6]。
組織因子信號通路抑制因子TFPI-2,是一種31kD大小的Kunitz 型絲氨酸蛋白酶抑制劑,分泌到細胞外基質(ECM)中,被認為是一種抑癌基因。因為TFPI-2可抑制血纖維蛋白溶解酶的活性,參與基質金屬蛋白酶(MMP)的激活[2],調控ECM的降解和腫瘤細胞浸潤。大部分惡性腫瘤,例如神經膠質瘤、胰腺癌、肝細胞癌TFPI-2表達下調。在細胞中穩定轉染或通過融合腺病毒導入TFPI-2后,可降低了癌細胞的浸潤性[3],但目前,還沒有研究觀察TFPI-2恢復表達、高表達以及去甲基化對肺癌所造成的影響。
5-氮雜-2’-脫氧胞苷(5-Aza-dC)可能通過使甲基化后的抑癌基因再次活化[7-10]。5-Aza-dC作為治療惡性腫瘤的去甲基化藥物已被美國食品藥品管理局批準[11]。
1 材料與方法
1.1 材料 人肺癌細胞系A549、NCI-H520及正常肺細胞系細胞均購自上海拜力生物科技有限公司。使用購自美國FBS公司的濃度為10%的胎牛血清培養基(Thermo fisher, 美國)。DNA提取以及修飾試劑盒購自TOYOBO,從Takara公司購買Taq DNA聚合酶,dNTPs。引物由大連寶生生物工程有限公司合成。RNA提取,RT-PCR試劑盒均購自TOYOBO。
1.2 細胞培養以及分組藥物處理 對照組:同期培養不加藥培養96h,只換液;A549、NCI-H520細胞株分別分為藥物1組:將濃度為1×10-7mol/L的5-Aza-dC加入到DMEM培養液中培養96h;藥物2組:將濃度為5×10-7mol/L的5-Aza-dC加入到DMEM培養液中培養96h;藥物3組:將濃度為1×10-6mol/L的5-Aza-dC加入到DMEM培養液中培養96h。
1.3 甲基化特異性PCR 引物為,F:5′-TTTCGTATAAA GCGGGTATTC-3′,R: 5′-ACGACCCGCTAATCAAAACG-3’,非甲基化:F:5′-GGATGTTTG TTTTGTATA-3′;R:5′-AAA CATCCAAAAAAACACCTAAC-3′。反應控制條件為:20min 95℃;30s 94℃;30s 52℃;45s 72℃循環40次后在72℃保溫10min,以100V的電壓進行40min的電泳,進行成像。
1.4 RT-PCR定量檢測 TFPI-2引物:F:5’-CAGAATT CTATGGACCCCGCTCGCCCC-3’;R:5’-CAGTCGACTTAAAATTGCTTCTTCCG-3’,以β-action作為內參。以100V的電壓進行40min的電泳,在成像系統中進行成像并攝像,對比表達強度。
1.6 Western blot分析各細胞中TFPI-2蛋白表達 對各組中TFPI-2蛋白表達水平進行測定。
1.7 統計學方法 本次研究采用SPSS19.0統計學軟件包進行納入與分析,所計量資料采用“x±s”表示,采用ANOVA并t檢驗進行統計學分析。
2 結果
2.1 肺癌細胞系細胞TFPI-2基因甲基化影響 未處理的A549和NCI-H520細胞中TFPI-2表現出完全甲基化特異性。而經過5-Aza-dC處理過的肺癌細胞系細胞則表現出不完全甲基化狀態,并呈現出量效關系。見圖1。
2.2 肺癌細胞系細胞TFPI-2基因mRNA表達對比 A549和NCI-H520細胞在經5-Aza-dC處理后TFPI-2基因mRNA表達均明顯高于未處理組,差異具有統計學意義(P<0.05);并呈現出量效關系。見表1。
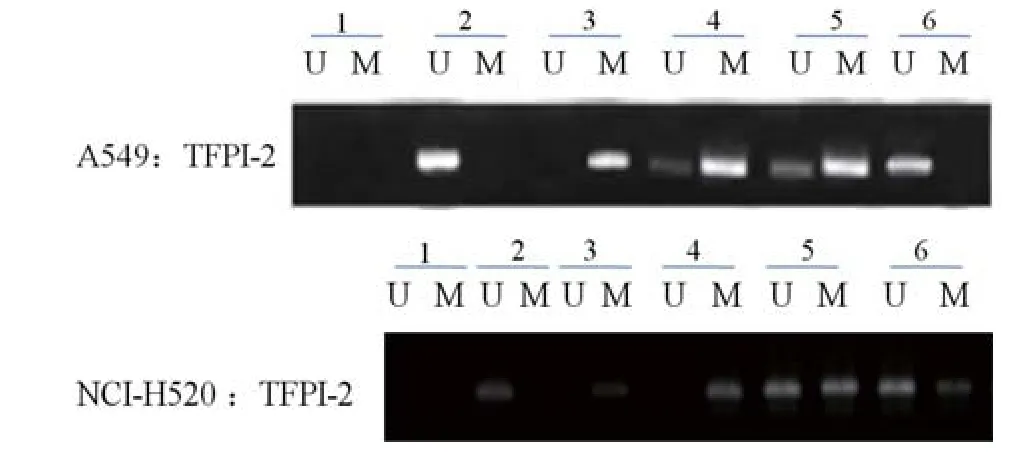
圖1 5-Aza-dC不同濃度對肺癌系細胞處理對TFPI-2甲基化水平的作用

表1 肺癌細胞系細胞TFPI-2基因mRNA表達對比(x±s,倍)
3 討論
腫瘤的發生發展涉及多種機制,包括細胞增殖和凋亡,細胞遷移和浸潤。在這個過程中包含了ECM被一系列的諸如MMP 蛋白酶的降解。在胰腺癌、食管癌、鼻咽癌、前列腺癌中發現TFPI-2的表達能夠抑制腫瘤細胞的增殖。一些研究對其機制進行了研究[9],發現TFPI-2可降低了細胞的增殖能力,將細胞阻斷在G1/S期,這同細胞周期依賴的激酶抑制因子p15和p27有關。p27(通過調控CDK2將細胞阻斷在G1/S期)在細胞周期中的調控作用,例如在胰腺癌和纖維肉瘤中,都已經有報道[10]。有研究通過腺病毒,將p27轉入NSCLC細胞中,使細胞停滯在G1/S期,并抑制了裸鼠移植瘤的增長。說明p27的低表達同病人預后差有關,在NSCLC中,p27表達高,病人生存期長。這也是TFPI-2腫瘤制效應的機制之一[11]。腫瘤細胞的浸潤和進展也需要ECM降解,主要是通過蛋白酶,特別是MMP。研究報道[12],TFPI-2是一種MMP活性的抑制因子,主要通過抑制纖溶酶來抑制MMP-1、-2、-3、-9。另外,除直接抑制外,TFPI-2也抑制MMP-1和-3的表達,來抑制腫瘤的增殖。SCLC手術切除標本稀少,主要是支氣管鏡和縱隔鏡檢查標本,因此僅僅夠用于免疫組織化學分析。
TFPI-2是一種潛在的血纖維蛋白溶解酶抑制因子,可以通過激活MMPs參與腫瘤進展的蛋白酶,因此,TFPI-2是一種潛在的腫瘤浸潤和轉移的抑制因子。在諸如神經膠質瘤、黑色素瘤、肝細胞癌、非小細胞肺癌的惡性腫瘤中低表達。TFPI-2作為一種抑癌基因,基因啟動子區甲基化發生率明顯高于正常肺組織,且能抑制TFPI-2基因的表達,可促進肺癌的發生發展。我們前期研究亦表明TFPI-2基因在非小細胞肺癌中呈低表達,基因甲基化與該基因表達沉默以及下降存在密不可分的相關性,并且其與TNM和淋巴結轉移之間呈負相關性。因此TFPI-2的表達與肺癌的侵襲轉移密切相關,其基因啟動子區CpG島高甲基化是TFPI-2低表達的可能機制之一,對于腫瘤的侵襲轉移具有促進作用。那么,通過去甲基化治療可促進肺癌TFPI-2基因表達,可能是肺癌治療的新方向,可作為肺癌基因治療的新靶點。
通過基因檢測后發現TFPI-2基因在染色體7q22上,此種蛋白是一種較絲氨酸蛋白酶跟家具有抑制纖溶酶作用,并可以對多種蛋白酶起到抑制性作用。腫瘤的轉移以及侵襲主要是通過使細胞外基質(ECM)降低來實現,而對ECMT的降解FPI-2具有抑制性的作用,由于此種機制使得腫瘤的生長得到控制,并對腫瘤細胞的浸潤以及轉移起到抑制性的作用[12]。
本次研究發現5-Aza-dC對肺癌細胞系細胞的甲基化具有一定的抑制性作用,同時還發現5-Aza-dC存在劑量依賴性。
[1] Jemal A,Siegel R,Ward E,et al.Cancer Statistics,2009[J].CA Cancer J Clin,2009,59(4):225-249.
[2] Crivaux M,Zureik M,Marsal L,et al.Five year survival for lung cancer patients managed in general hospital[J].Rev Mal Respir,2011,28(7):31-38.
[3] Makale M.Cellular mechanobiology and cancer metastasis[J].Birth Defects Res C Embryo Today,2007,81(4):329-343.
[4] Etzioni R,Urban N,Ramsey S,et al.The case for early detection[J].Nat Rev Cancer,2003,3(4):243-252.
[5] Novik KL,Nimmrich I,Genc B,et al.Epigenomics:genome-wide study of methylation phenomena[J].Curr Issues Mol Biol,2002,4(4):111-128.
[6] Herman JG,Baylin SB.Gene silencing in cancer in association with promoter hypermethylation[J].N Engl J Med,2003,349(21):2042-2054.
[7] Pinto A,Zagonel V.5-Aza-2’deoxycytidine and 5-Aza-cytidine in the treatment of acute myeloid leukemias and myelodysplastic syndromes:past,present,and future trends[J].Leukemia,1993,1:51-60.
[8] Kantarjian H,Oki Y,Garcia-manero G,et al.Results of a randomized study of 3 schedules of low-dose decitabine in higher-risk myelodysplastic syndrome and chronic myelomonocutic leukemia[J]. Blood,2007,109(1):52-57.
[9] Yang AS.Doshi KD,choi SW,et al.DNA methylation changes after 5-Aza-2’-deoxycytidine therapy in patients with leukemia[J].Cancer Res,2006,66(10):5495-5503.
[10] Mund C,Hackanson B,Stresemann C,et al.Characterization of DNA demethylation effects induced by 5-Aza-2’-deoxycytidine in patients with myelodysplastic syndrome[J].Cancer Res,2005,65(16):7086-7090.
[11] Issa JP,Kantarjian HM,Kirkpatrick P.Azacitidine[J].Nat Rev Drug Discov,2005,4(4):275-276.
[12] Du X,Chand HS,Kisiel W.Human tissue factor pathway inhibitor-2 does not bind or inhibit activated matrix metalloproteinase-1[J].Biochim Biophys Acta,2003,1621(3):242-245.
Objective To study the effect of 5-Aza-dC on the methylation of lung cancer cell lines. Methods Quantitative detection of A549, NCI-H520 methylation specific PCR and RT-PCR in normal lung cells and 5-Aza-dC group. Results TFPI-2 in untreated A549 and NCI-H520 cells showed complete methylation specificity. The 5-Aza-dC treated lung cancer cell lines showed incomplete methylation status, and showed a dose effect relationship. After 5-Aza-dC treatment, A549 and NCI-H520 cells were significantly higher than the untreated group, the difference was statistically significant (P<0.05), and showed a dose effect relationship. Conclusion 5-Aza-dC has a role in the methylation of TFPI-2 gene in lung cancer cells, and has dose effect relationship.
5-Aza-dC;TFPI-2;Methylation;A549;NCI-H520
10.3969/j.issn.1009-4393.2016.29.006
江西 330006 江西省人民醫院呼吸內科 (童波 梁瑩 吳西雅肖祖克 周洪 郭玲玲) 333200 婺源縣人民醫院內二科 (鐘進生)
梁瑩 E-mail:anlixia002@163.com

