苓桂術(shù)甘湯治療代謝綜合征的配方顆粒與傳統(tǒng)飲片隨機(jī)對照盲態(tài)評價臨床研究方案
趙 陽 付 靜 陸 芳 李 博 趙迎盼 李 睿 李慶娜 曹唯儀 高 蕊
(1 中國中醫(yī)科學(xué)院西苑醫(yī)院臨床藥理所,北京,100091; 2 北京康仁堂藥業(yè)有限公司,北京,101301)
?
苓桂術(shù)甘湯治療代謝綜合征的配方顆粒與傳統(tǒng)飲片隨機(jī)對照盲態(tài)評價臨床研究方案
趙陽1付靜2陸芳1李博1趙迎盼1李睿1李慶娜1曹唯儀1高蕊1
(1 中國中醫(yī)科學(xué)院西苑醫(yī)院臨床藥理所,北京,100091; 2 北京康仁堂藥業(yè)有限公司,北京,101301)
目的:評價苓桂術(shù)甘湯配方顆粒與傳統(tǒng)飲片治療代謝綜合征的有效性和安全性。方法:采用隨機(jī)、對照、盲態(tài)評價、等效性臨床研究設(shè)計方法,擬將280例受試者隨機(jī)分為配方顆粒劑組和傳統(tǒng)飲片水煎劑組,通過16周的治療,觀察胰島素抵抗指數(shù),空腹血糖、代謝綜合征指標(biāo)組分及安全性指標(biāo)等在組間的分布差異,評價苓桂術(shù)甘湯配方顆粒與傳統(tǒng)飲片治療代謝綜合征的療效和安全性是否相同。結(jié)論:本研究采用隨機(jī)對照、盲態(tài)評價、等效性設(shè)計的方法,同時規(guī)范合并用藥與飲食鍛煉的要求,能夠較好的控制患者個體因素和不同醫(yī)生診療差異的影響,提高臨床研究的規(guī)范性和科學(xué)性,保證研究結(jié)果的可靠性和可信性,驗證配方顆粒的療效及安全性,為配方顆粒的臨床合理應(yīng)用提供依據(jù)。
苓桂術(shù)甘湯;配方顆粒;代謝綜合征
代謝綜合征(Metabolic Syndrome,MS)是以肥胖、高血糖、血脂異常、高血壓等代謝相關(guān)危險因素的組合[1],這些因素能夠促進(jìn)動脈粥樣硬化性心血管疾病的發(fā)生,增加2型糖尿病的發(fā)生風(fēng)險,嚴(yán)重影響機(jī)體健康[2,10]。MS的發(fā)病機(jī)制尚未完全闡明,多數(shù)學(xué)者認(rèn)為胰島素抵抗(Insulin Resistence,IR)是MS病理生理發(fā)展過程中的核心環(huán)節(jié)[3],超重和肥胖是IR的標(biāo)志[4,11-12]。
隨著MS發(fā)病率的逐年上升[6-7],中醫(yī)藥在治療MS方面的作用越來越得到重視[5,8]。通過查閱文獻(xiàn),苓桂術(shù)甘湯能夠顯著降低MS模型大鼠的血清抵抗素、胰島素水平和胰島素抵抗指數(shù)[14]。在臨床上,苓桂術(shù)甘湯常被應(yīng)用于治療肥胖、糖脂代謝異常[15,18],但目前缺少高質(zhì)量的臨床研究證據(jù)證實中醫(yī)藥改善MS的臨床療效[22-23],值得進(jìn)一步研究。中藥配方顆粒是由符合炮制規(guī)范的中藥飲片經(jīng)過現(xiàn)代工藝制成。與傳統(tǒng)飲片相比,配方顆粒雖然具有質(zhì)量穩(wěn)定、使用方便、便于攜帶和存儲等優(yōu)點[16],但配方顆粒與傳統(tǒng)飲片在臨床療效、成分含量的等效性方面仍存在爭議[17]。因此,擬通過多中心、隨機(jī)對照、盲態(tài)評價的臨床研究方法,評價苓桂術(shù)甘湯配方顆粒與傳統(tǒng)飲片治療MS的有效性和安全性,為中藥配方顆粒在臨床上的推廣使用提供科學(xué)依據(jù)。
1 研究目的
采用隨機(jī)對照、盲態(tài)評價的臨床研究方法,評價苓桂術(shù)甘湯配方顆粒與傳統(tǒng)飲片治療MS的有效性和安全性。
2 研究方案
本研究采用隨機(jī)、陽性藥對照、盲態(tài)評價、等效性臨床研究設(shè)計。
2.1病例納入標(biāo)準(zhǔn)1)符合MS診斷標(biāo)準(zhǔn);根據(jù)中國2型糖尿病防治指南(2013年版)對MS的診斷標(biāo)準(zhǔn),具體如下:a.中心性肥胖:腰圍男性≥90 cm,女性≥85 cm。b.高血糖:空腹血糖≥6.1 mmol/L(110 mg/dL)或糖負(fù)荷后2 h血糖≥7.8 mmol/L(140 mg/dL)和/或已確診為糖尿病并治療者。c.高血壓:血壓≥130/85 mmHg和/或已確認(rèn)為高血壓病治療者。d.空腹TG≥1.70 mmol/L(150 mg/dL)。e.空腹HDL-C<1.04 mmol/L(40 mg/dL)。以上具備3項或更多項即可診斷。2)具備中醫(yī)辨證為脾虛濕盛證者[9];形體肥胖、胸脅脹滿、頭暈?zāi)垦!⒕氲》αΑ⑸噘|(zhì)淡,苔白,脈沉緊[13]。3)入組前4周的檢查符合MS診斷標(biāo)準(zhǔn),然后進(jìn)入為期4周的導(dǎo)入期,進(jìn)行飲食控制和生活方式干預(yù),目的為保持均衡的飲食及生活習(xí)慣,且原藥物治療方案維持不變,導(dǎo)入期結(jié)束后復(fù)查仍符合MS診斷標(biāo)準(zhǔn)者。4)年齡在18~65歲之間。5)簽署知情同意書。
2.2病例排除標(biāo)準(zhǔn)1)已確診為糖尿病的受試者,在生活方式干預(yù)及藥物治療后,空腹血糖≥7 mmol/L(126 mg/dL)或糖化血紅蛋白≥8%;2)TC≥6.22 mmol/L(240 mg/dL)或LDL-C≥4.92 mmol/L(190 mg/dL)或TG≥3.39 mmol/L(300 mg/dL);3)收縮壓≥160 mmHg和/或舒張壓≥100 mmHg;4)惡性腫瘤、嚴(yán)重心臟疾病、血液系統(tǒng)疾病、腦血管意外、嚴(yán)重創(chuàng)傷或重大手術(shù)后患者;5)腎病綜合征、甲狀腺功能減退、急性或慢性肝膽疾病、痛風(fēng)等患者;6)由藥物(吩噻嗪類、β-阻滯劑、腎上腺皮質(zhì)類固醇等)引起的血脂異常;7)肝、腎功能異常,ALT>1.5N或Cr>N(N為正常值上限);8)過敏體質(zhì)者、已知對試驗藥物過敏者;9)有藥物或乙醇濫用者;10)活動性肝病,精神病患者;11)3個月內(nèi)參加過其他臨床試驗者;12)妊娠或準(zhǔn)備妊娠的婦女及哺乳期婦女;13)研究者認(rèn)為不宜參加臨床研究者。
2.3剔除、脫落和中止試驗的標(biāo)準(zhǔn)
2.3.1剔除標(biāo)準(zhǔn)1)試驗開始后發(fā)現(xiàn)受試者不符合病例納入標(biāo)準(zhǔn)或符合排除標(biāo)準(zhǔn),即本不應(yīng)當(dāng)進(jìn)行隨機(jī)化入組的病例。2)在隨機(jī)化之后沒有記錄任何數(shù)據(jù)。3)未曾使用試驗用藥。4)使用了禁用的藥物以致有效性和安全性無法判定的病例。
2.3.2脫落標(biāo)準(zhǔn)所有填寫過知情同意書并篩選合格進(jìn)入試驗的受試者,無論何時何故退出,只要沒有完成規(guī)定的觀察周期的受試者,均應(yīng)為脫落病例。脫落的原因可能有如下方面:1)受試者依從性差中途自行換藥或加用其他藥物者。2)觀察中自然脫離、失訪者,包括治療有效但不能完成整個療程,以致臨床資料不全等影響療效和安全性判斷者。
2.3.3中止標(biāo)準(zhǔn)已經(jīng)入選的受試者在試驗期間出現(xiàn)了不宜繼續(xù)進(jìn)行試驗的情況,導(dǎo)致該病例不能按照研究方案完成試驗為研究病例的中止。一般出現(xiàn)以下情況時應(yīng)采取中止措施:1)受試者在試驗期間病情急劇惡化,并且不能排除其病情與試驗無關(guān),應(yīng)考慮中止該研究病例;中止該病歷后研究者對患者對癥治療。2)受試者在研究期間出現(xiàn)了嚴(yán)重不良反應(yīng)事件,應(yīng)中止該研究病例;3)在研究過程中,受試者在藥物的使用、接受訪視、隨訪等方面不能依從臨床試驗方案執(zhí)行,經(jīng)研究者判斷有可能影響研究結(jié)果的真實性時應(yīng)考慮中止該研究病例。
病例中止后應(yīng)保留其病例記錄表,并以最后1次檢測結(jié)果為最終結(jié)果,對其進(jìn)行療效和不良反應(yīng)數(shù)據(jù)分析。
2.3.4全面終止臨床試驗的標(biāo)準(zhǔn)1)試驗中發(fā)現(xiàn)嚴(yán)重安全性問題。2)試驗中發(fā)現(xiàn)藥物治療效果太差,甚至無效,不具有臨床價值。3)發(fā)現(xiàn)臨床試驗方案有重大失誤,難以評價藥物療效;或在實施中發(fā)生了重要偏差。4)申辦者因經(jīng)費(fèi)原因、管理原因要求終止試驗。
2.4干預(yù)措施試驗組:常規(guī)給予飲食、運(yùn)動等基本療法,根據(jù)受試者的具體情況制定飲食和運(yùn)動方案。服用苓桂術(shù)甘湯中藥配方顆粒,2次/d,1袋/次,餐后1 h服用。對照組:常規(guī)給予飲食、運(yùn)動等基本療法,根據(jù)受試者的具體情況制定飲食和運(yùn)動方案。服用苓桂術(shù)甘湯飲片水煎劑,1劑/d,水煎分2次服用,餐后1 h服用。試驗藥物均由北京康仁堂藥業(yè)有限公司提供。保證制備配方顆粒的飲片與傳統(tǒng)湯劑的飲片來源一致。
2.5合并用藥規(guī)定如患者同時患有其他疾病,如:高血壓、高血脂等必須服用的治療藥物以及治療方法,可以繼續(xù)使用,但應(yīng)保持試驗期間藥物的用法用量不變。試驗期間不可使用計劃外的與本病治療相關(guān)的其他中、西藥制劑。所有的合并用藥都必須詳細(xì)記錄在原始記錄和CRF中,包括藥物的通用名稱、使用劑量和給藥方法、用藥起始時間及使用的原因。所有的合并用藥都必須詳細(xì)記錄在原始記錄和CRF中,包括藥物的通用名稱、使用劑量和給藥方法、用藥起始時間及使用的原因。
2.6試驗療程導(dǎo)入期:本試驗導(dǎo)入期為4周,為MS受試者隨機(jī)入組之前的準(zhǔn)備期,允許進(jìn)行MS患者教育,優(yōu)化飲食和運(yùn)動的依從性,考慮受試者代謝控制參數(shù)的穩(wěn)定性,以便能夠最準(zhǔn)確的估算藥物的有效性,避免過度夸大真正的治療效果,同時篩除依從性比較差的受試者。治療期:療程為16周。
2.7觀測指標(biāo)
2.7.1人口統(tǒng)計學(xué)資料年齡、性別、民族、職業(yè)、吸煙及飲酒情況等。
2.7.2病史目前合并疾病或其他潛在的危險因素(高血壓、高脂血癥等)及飲食控制、運(yùn)動鍛煉、用藥治療情況、重要既往史、藥敏史。
2.7.3體格檢查身高、體重、生命體征(體溫、心率、呼吸、血壓),需要在靜息狀態(tài)下測量,血壓統(tǒng)一取坐位血壓。
2.7.4療效性指標(biāo)1)主要指標(biāo):胰島素抵抗指數(shù)HOMA-IR。2)次要指標(biāo):空腹血糖、MS指標(biāo)組分測量值:腰圍、體重、血脂(TC、TG、HDL-C、LDL-C)、血壓、糖化血紅蛋白、中醫(yī)癥狀消失率。
2.7.5安全性指標(biāo)實驗室檢查可接受篩選前7天內(nèi)的檢查結(jié)果,安全性指標(biāo)主要包括以下內(nèi)容:1)心電圖檢查;2)血常規(guī);3)尿常規(guī);4)便常規(guī)+OB;5)血生化;6)妊娠試驗;7)不良事件的觀察與記錄,本研究中需要密切關(guān)注胃腸道不適癥狀和低血糖的發(fā)生情況。
2.7.6依從性觀察觀察期間研究者或指定人員應(yīng)做好藥物發(fā)放回收的記錄工作。受試者在每次回訪時應(yīng)歸還未使用的藥物和已使用過的藥物包裝,由研究者或指定人員進(jìn)行藥物數(shù)量清點,對丟失、未歸還的研究藥物做好記錄。研究者應(yīng)記錄受試者是否按時按量服用研究藥物、是否在研究期間自行服用其他藥物。藥物依從性=實服藥量/應(yīng)服藥量×100%,依從性在80%~120%范圍內(nèi)視為依從性良好。如受試者依從性不好,應(yīng)查找原因并記錄在案。
2.7.7成本效果分析本研究將從衛(wèi)生經(jīng)濟(jì)學(xué)角度進(jìn)行2組成本-效果分析比較,統(tǒng)計治療組及對照組的成本(元)及效果(%),計算成本效果比(C/E)。由于間接成本和隱形成本包含很多不確定因素,本研究從受試者治療產(chǎn)生的直接成本角度出發(fā),考慮每位受試者治療所產(chǎn)生的藥物費(fèi)、檢查費(fèi)、因不良反應(yīng)進(jìn)行治療的費(fèi)用及住院費(fèi)等,作為成本指標(biāo)。效果指標(biāo)采取MS治愈率。考慮到藥品價格及用藥劑量的變動,將進(jìn)行敏感度分析。
2.8療效判定標(biāo)準(zhǔn)
2.8.1主要療效指標(biāo)評價胰島素抵抗指數(shù)(HOMA-IR)相對基線的組內(nèi)和組間變化。計算方法:胰島素抵抗指數(shù)=空腹血糖水平×空腹胰島素水平/22.5(HOMA-IR=FPG×FINS/22.5);空腹血糖測量值相對基線的組內(nèi)和組間變化。
2.8.2次要療效指標(biāo)評價MS指標(biāo)組分測量值相對基線的組內(nèi)和組間變化。
2.9試驗訪視流程圖見表1。
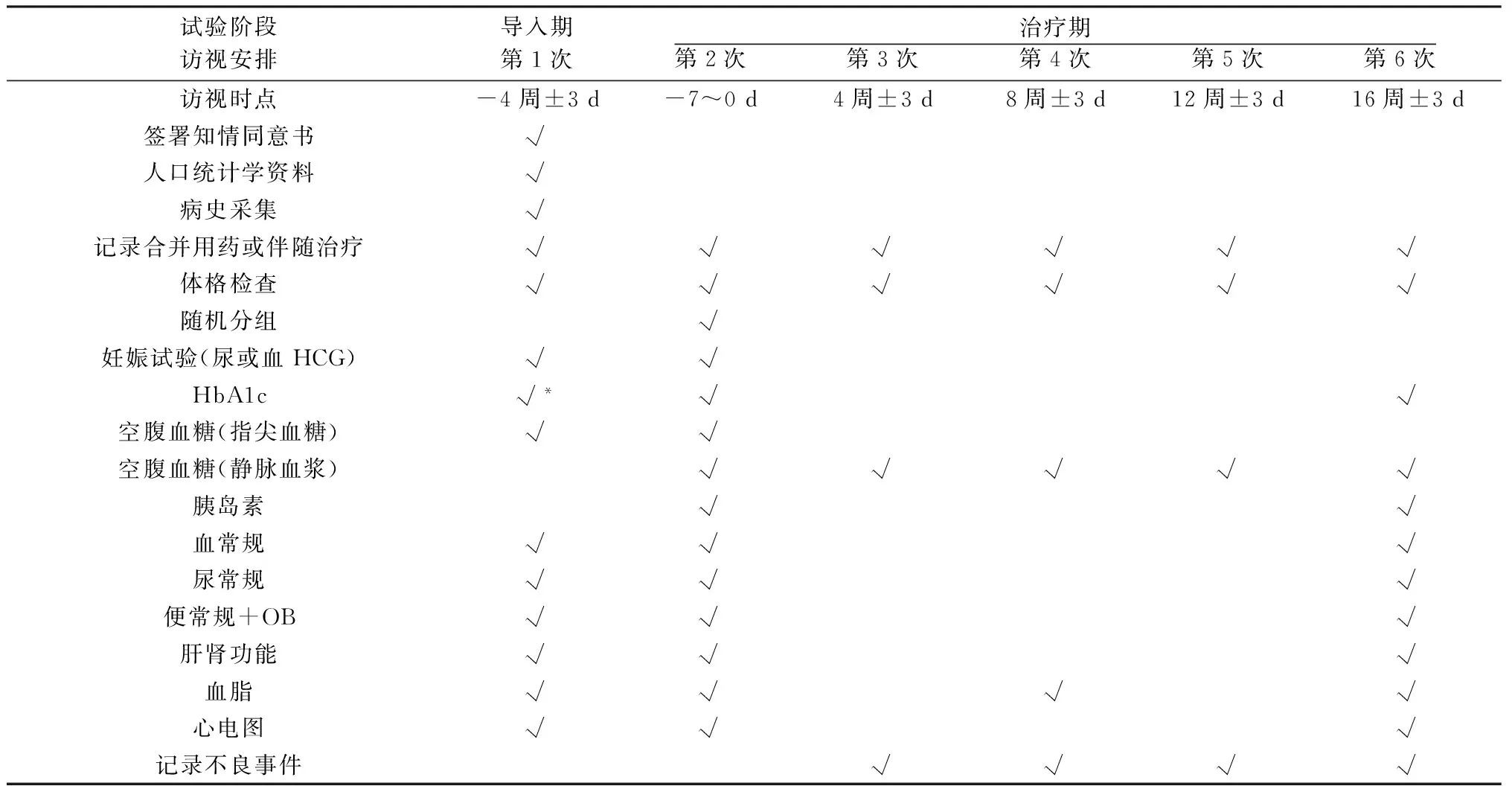
表1 試驗訪視流程圖
2.10樣本量采用定量指標(biāo)成組等效性試驗設(shè)計,根據(jù)文獻(xiàn)顯示中藥改善胰島素抵抗的效果平均為)(2.77±0.78),設(shè)定等效界值(L=-0.3,,U=0.3),α=0.025(單側(cè)),β=0.20,試驗組與對照組=1∶1,應(yīng)用PASS 11軟件進(jìn)行樣本量計算,每組117例,考慮20%脫落率,整體研究總計280例。試驗組140例,對照組140例[20]。
2.11隨機(jī)、分配、盲法采用區(qū)組隨機(jī)設(shè)計,利用SAS軟件程序生成隨機(jī)數(shù)字及分組,具體設(shè)計方法見隨機(jī)化方案。藥物管理員嚴(yán)格依據(jù)隨機(jī)化方案給受試者發(fā)藥。采用盲態(tài)評價方法進(jìn)行藥物療效和安全性評價。因研究藥物劑型不同無法實施雙盲,因此本試驗的研究數(shù)據(jù)將委托第3方對研究結(jié)果進(jìn)行評估,接受委托的第3方數(shù)據(jù)分析人員不參與臨床試驗的實施工作及任何可能對評估產(chǎn)生偏倚的工作。盲態(tài)評價的主要工作內(nèi)容包括:對試驗數(shù)據(jù)進(jìn)行審核、劃分統(tǒng)計分析數(shù)據(jù)集、對統(tǒng)計分析計劃書進(jìn)行修改和確認(rèn)、對審核后的已鎖定的數(shù)據(jù)庫進(jìn)行統(tǒng)計分析。
3 數(shù)據(jù)管理和統(tǒng)計分析方法
本研究采用中國中醫(yī)科學(xué)院西苑醫(yī)院藥物臨床試驗電子化數(shù)據(jù)管理系統(tǒng)進(jìn)行數(shù)據(jù)管理,在研究啟動之前,將由數(shù)據(jù)管理員撰寫數(shù)據(jù)管理計劃,該計劃將作為數(shù)據(jù)管理過程的指導(dǎo)性文件,臨床試驗數(shù)據(jù)管理工作所需的步驟和信息均以數(shù)據(jù)管理計劃為準(zhǔn)。統(tǒng)計軟件采用SAS 9.2,詳細(xì)的統(tǒng)計方法將在統(tǒng)計分析計劃中提供。
4 技術(shù)路線
見圖1。
5 質(zhì)量控制措施
由課題負(fù)責(zé)單位成立專家顧問組、數(shù)據(jù)管理組及質(zhì)量控制組,對臨床研究的全過程進(jìn)行質(zhì)量控制。在研究過程中,由課題組委派臨床監(jiān)查員定期對研究單位進(jìn)行現(xiàn)場監(jiān)查,以保證臨床試驗的實施能夠嚴(yán)格遵從研究方案。臨床試驗藥品應(yīng)由專人負(fù)責(zé)保存、制作及發(fā)放。質(zhì)控工作的具體內(nèi)容將在質(zhì)量控制計劃中提供。
6 討論
本研究通過開展苓桂術(shù)甘湯配方顆粒與傳統(tǒng)飲片對照治療MS的隨機(jī)、對照、盲態(tài)評價、多中心臨床試驗,從多靶點、方位對比分析苓桂術(shù)甘湯顆粒和傳統(tǒng)飲片的有效性和安全性;采用的隨機(jī)對照、盲態(tài)評價的方法能夠更好的控制患者個體因素和不同醫(yī)生診療差異的影響,提高臨床研究的規(guī)范性和科學(xué)性;同時規(guī)范合并用藥與飲食鍛煉的要求,完善復(fù)雜干預(yù)下隨機(jī)對照試驗和盲態(tài)評價的質(zhì)控體系,保證研究結(jié)果的可靠性和可信性,能夠更嚴(yán)謹(jǐn)?shù)膶Ρ葍煞N不同劑型的有效性和安全性。采用飲片與顆粒劑療效的等效性設(shè)計,驗證配方顆粒臨床使用上的療效及安全性,為配方顆粒的臨床合理應(yīng)用提供依據(jù)。
[1]中華醫(yī)學(xué)會糖尿病學(xué)分會.中國2型糖尿病防治指南(2013年版)[S].中國糖尿病雜志,2014.
[2]K George MM Albertiemail,Paul Zimmet,Jonathan Shaw.The metabolic syndrome-a new worldwide definition[J].The Lancet,Volume 366,No.9491,p1059-1062.
[3]Nele Pattyn.The effect of exercise on the cardiovascular risk factors constituting the metabolic syndrome:a meta-analysis of controlled trials[J].Sports Med,2013 Feb,43(2):121-33.
[4]Dieli-Conwright CM.Effects of a 16-week Resistance and Aerobic Exercise Intervention on Metabolic Syndrome in Overweight/Obese Latina Breast Cancer Survivors[J].Cancer Epidemiol Biomarkers Prev.2015,24(4):763.
[5]張慧,郭宏敏.中醫(yī)藥治療代謝綜合征研究進(jìn)展[J].中醫(yī)藥臨床雜志,2006,18(1):91-92.
[6]顧東風(fēng).中國成年人代謝綜合征的患病率[J].中華糖尿病雜志,2005,13(3):181-186.
[7]陶然.江蘇省成年人代謝綜合征流行特征及其不同診斷標(biāo)準(zhǔn)的對比研究[J].吉林大學(xué)學(xué)報:醫(yī)學(xué)版,2015,41(1):181-189.
[8]徐業(yè),李斌,吳敏.中藥復(fù)方治療代謝綜合征隨機(jī)對照試驗的Meta分析[J].新中醫(yī),2015,42(2):235-237.
[9]陳淑嬌,李燦東,賴新梅,等.160例代謝綜合征患者中醫(yī)證候特點研究[J].中華中醫(yī)藥雜志,2015,30(3):689-692.
[10]Liira H.Exercise intervention and health checks for middle-aged men with elevated cardiovascular risk:a randomized controlled trial[J].Scand J Prim Health Care,2014 Dec,32(4):156-62.
[11]Balducci S.Anti-inflammatory effect of exercise training in subjects with type 2 diabetes and the metabolic syndrome is dependent on exercise modalities and independent of weight loss[J].Nutr Metab Cardiovasc Dis,2010,20(8):608-17.
[12]宋桉,趙家軍.肥胖致胰島素抵抗的機(jī)制研究新進(jìn)展[J].中國老年學(xué)雜志,2013,33(17):4359-4361.
[13]張海慶.代謝綜合征中醫(yī)病機(jī)探討[J].中醫(yī)研究,2013,26(10):9-10.
[14]黃江榮,李祥華,杜亞明,等.加味苓桂術(shù)甘湯對代謝綜合征大鼠糖代謝的影響[J].中藥藥理與臨床,2013,25(3):167-169.
[15]張麗娜.加味苓桂術(shù)甘湯治療奧氮平導(dǎo)致的肥胖以及對血清甘油三酯和脂聯(lián)素等指標(biāo)的影響[J].中華中醫(yī)藥學(xué)刊,2013,33(11):2583-2585.
[16]肖龍泉.傳統(tǒng)中藥湯劑與中藥配方顆粒劑比較研究[J].中醫(yī)藥臨床雜志,2014,26(7):729-731.
[17]吳敏.康仁堂參附“全成分”配方顆粒治療老年人肺心病并冠心病療效觀察[J].中西醫(yī)結(jié)合心血管病電子雜志,2014,10(9):35-36.
[18]宋清武,李慧臻.加味苓桂術(shù)甘湯對非酒精性脂肪肝患者血清NO水平的干預(yù)研究[J].內(nèi)蒙古中醫(yī)藥,2014,33(10):3-4.
[19]高伯正.《傷寒論》苓桂術(shù)甘湯證條新解[J].光明中醫(yī),2015,30(3):459.
[20]劉紅蕓,王曉良.苓桂術(shù)甘湯加減治療痰飲病舉隅[J].中國中醫(yī)急癥,2014,23(8):1574.
[21]趙一舉,王晞星,王晞星.運(yùn)用苓桂術(shù)甘湯治療痰飲病驗案3則[J].中醫(yī)臨床研究,2013,5(13):87.
[22]張雪.中藥(二甲雙胍對照)干預(yù)糖尿病前期的系統(tǒng)評價[D].成都:成都中醫(yī)藥大學(xué),2015.
(2015-10-10收稿責(zé)任編輯:徐穎)
Effects of Linggui Zhugan Granules in the Treatment of Metabolic Syndrome:A Randomized Controlled Clinical Trial
Zhao Yang1,Fu Jing2,Lu Fang1,Li Bo1,Zhao Yingpan1,Li Rui1,Li Qingna1,Cao Weiyi1,Gao Rui1
(1ClinicalPharmacologyInstituteofChinaAcademyofChineseMedicalScienceofXiyuanHospital,Beijing100091,China;2BeijingKangrentangPharmaceutialCo.LTD,Beijing101301,China)
Objective:To evaluate the efficacy and safety of Linggui Zhugan granules and slices in the treatment of metabolic syndrome.Methods:A randomized,controlled research were conducted with 280 subjects who are randomly divided into Linggui Zhugan granules group and Linggui Zhugan slices group.During16 weeks of treatment,insulin resistance index,fasting blood glucose,metabolic syndrome components and safety indicators are observed,and the safety differences were concluded between the two groups.Conclusion:By adopting a randomized,controlled,evaluation on grouping unknown,equivalence clinical study,as well as standardized drug combination and exercise with diet,the standardization and scientificity of the research can be ensured.This can guarantee the reliability and credibility of outcomes and verify the clinical effect and safety of traditional Chinese medicine (TCM) granules.It provides evidence for the clinical application of TCM granules.
Linggui Zhugan decoction; Traditional Chinese Medicinal Granules; Metabolic Syndrome
國家中醫(yī)藥管理局中醫(yī)藥科學(xué)技術(shù)研究專項(編號:國中醫(yī)藥科2016ZX10)
趙陽(1987.02—),女,醫(yī)學(xué)碩士,助理研究員,生物統(tǒng)計員,藥物臨床試驗統(tǒng)計學(xué),zhaoyang@xygcp.com
高蕊(1966.05—),女,醫(yī)學(xué)博士,主任醫(yī)師,藥物臨床試驗機(jī)構(gòu)辦公室主任,臨床藥理,E-mail:gaorui@xygcp.com
R242
A doi:10.3969/j.issn.1673-7202.2016.07.055

