基于光熱效應的沙門氏菌試紙條檢測方法研究
邴欣,劉靜靜,高盧翔,張震,劉兆臣,賈敏,*(.山東省產品質量檢驗研究院,山東濟南500;.山東師范大學生命科學學院,山東濟南5004)
基于光熱效應的沙門氏菌試紙條檢測方法研究
邴欣1,劉靜靜2,高盧翔2,張震2,劉兆臣2,賈敏2,*
(1.山東省產品質量檢驗研究院,山東濟南250012;2.山東師范大學生命科學學院,山東濟南250014)
建立一種基于氧化石墨烯-金復合物的光熱效應沙門氏菌滲濾試紙條的檢測方法。制備了石墨烯-金納米復合物,并將其與抗體偶聯,在傳統滲濾試紙條方法的基礎上,優化了滲濾試紙條的各項試驗條件以及激光照射時長。采用目測法及光熱效應溫差法檢測沙門氏菌的最低檢測限分別為2.4×104CFU/mL及2.4×103CFU/mL。繪制了石墨烯-金納米復合物光熱效應滲濾試紙條方法檢測沙門氏菌的標準曲線,并得到線性回歸方程:y=0.754x-2.09,R2=0.971。
試紙條;石墨烯納米復合物;光熱效應;沙門氏菌
沙門氏菌是引起食物中毒的食源性致病菌之一,由沙門氏菌引起的食物中毒在各國的細菌性食物中毒中位居首位[1],在我國細菌性食物中毒病例中,沙門氏菌引起的食物中毒病例約占40%[2]。沙門氏菌是我國眾多食品標準中的檢測項目,且要求不得檢出[3-5]。
傳統沙門氏菌檢測方法需經增菌、分離培養、生化反應和血清學鑒定等繁瑣檢驗程序,需4 d~7d才能得到明確診斷結果,耗時費力[6]。分子生物學檢測方法需要精密儀器及昂貴試劑,不適宜大范圍推廣使用[7]。沙門氏菌免疫學檢測方法有酶聯免疫吸附測定法(ELISA)、熒光免疫分析法(FIA)、免疫磁性分離法(IMS)等,但ELISA法檢測結果易出現假陽性,FIA法靈敏度低且成本較高,IMS法靈敏度低[8]。因此,價格低廉、操作簡單、檢測快速的沙門氏菌檢測方法的研究迫在眉睫。
近年來,免疫膠體金試紙條因其簡便、快速、靈敏度高等優點得到廣泛的應用,但此類檢測方法通常采用目測或者讀卡器區分顏色深淺來判斷檢測結果[9-11],其靈敏度與其他分子檢測方法仍然偏低,且無法實現準確的定量檢測。因此如何提高試紙條檢測方法的靈敏度,實現定量或半定量檢測已成為試紙條檢測方法的主要發展方向。近年來,研究者從諸多方面致力于提高試紙條檢測方法的靈敏度,例如將其與熒光技術[12-13]、電化學技術[14-15]相結合來實現精確的定量檢測。
Qin等[16]利用納米金(AuNPs)的光熱效應顯著提高了層析式試紙條的檢測靈敏度,AuNPs與待測物偶聯后用激光照射,AuNPs可產生熱量并引起溫度變化,且AuNPs的溫度變化與待測物濃度成線性關系,待測物濃度可通過標準曲線計算得到。已有文獻報道通過AuNPs與氧化石墨烯(GO)的偶聯可增強光熱效應的轉化[17]。本研究用氧化石墨烯-納米金復合物替代傳統免疫膠體金試紙條上的納米金,并利用氧化石墨烯-納米金復合物的光熱效應來進行沙門氏菌的檢測以提高靈敏度。
1 材料與方法
1.1材料與試劑
LB培養基、牛肉膏蛋白胨培養基:北京奧博星生物技術有限公司;氯金酸:國藥集團化學試劑有限公司;碳酸鉀(K2CO3)、檸檬酸三鈉、甲醇、吐溫20:天津市華特化研科技有限公司;牛血清白蛋白(BSA):Sigma,Roche738328;氧化石墨烯:南京先豐納米材料科技有限公司;PBS:賽默飛世爾生物化學制品(北京)有限公司;抗鼠傷寒沙門氏菌抗體:博奧森生物有限公司;鼠傷寒沙門氏菌(ATCC14028):中國醫學菌種保藏中心。
1.2儀器與設備
MOV-112電熱鼓風恒溫干燥箱:三洋電機國際貿易有限公司;HZQ-X100搖床培養箱:哈爾濱市東聯電子技術開發有限公司;IRS紅外熱像儀:上海熱像機電科技股份有限公司;OX-R301-1近紅外燈:OXLASERS。
1.3方法
1.3.1石墨烯-金納米復合物的制備與電鏡表征
采用檸檬酸鈉還原法[18]制備膠體金:取1 mL 0.1%的氯金酸(HAuCl4)水溶液,用雙蒸水稀釋定容至100mL后轉移到250 mL圓底燒瓶中。將圓底燒瓶置于電熱套上加熱直至溶液沸騰。保持煮沸1 min后,劇烈攪拌下一次性迅速加入3.5 mL 1%的檸檬酸三鈉,持續攪拌,溶液由最初的淺黃色逐漸變為黑色再變為藍色最后變為紅色,待顏色保持不變后繼續煮沸并攪拌10min~15 min,關閉電熱套停止加熱,使溶液自然冷卻,所得溶液即為膠體金溶液,4℃冰箱儲存待用。
在制備膠體金溶液的基礎上,對比并結合多項研究[19-20],最終采用如下方法合成石墨烯-金納米復合物:當膠體金溶液在持續的攪拌下變為紅褐色時,一次性迅速加入3.5 mL的氧化石墨烯溶液,繼續攪拌至溶液顏色保持不變后,繼續煮沸并攪拌10 min~15 min,停止加熱,使溶液自然冷卻。8 000 r/min離心10 min除去多余的石墨烯,沉淀物用雙蒸水復溶即得石墨烯-金納米復合物。
將制備好的石墨烯-金納米復合物進行電鏡掃描,在電鏡下觀察膠體金顆粒的形態及其在石墨烯表面的分布情況,驗證復合物是否合成成功。
1.3.2石墨烯-金納米復合物標記抗沙門氏菌抗體的制備
0.1 mol/L K2CO3調節石墨烯-金納米復合物pH至9.0,取1 mL石墨烯-金納米復合物置于2 mL的EP管中,加入1 mL 0.6 μg/mL的沙門氏菌抗體,室溫振搖反應4 h~8 h,4℃過夜保存。將上述石墨烯-金-抗沙門氏菌抗體復合物分裝到EP管中,4℃10 000 r/min離心30 min,棄上清,二次水復溶沉淀,即得石墨烯-金-抗沙門氏菌抗體復合物。
1.3.3沙門氏菌的培養及樣品前處理
1.3.3.1沙門氏菌的培養
鼠傷寒沙門氏菌ATCC 14028置于LB液體培養基中,37℃搖床培養,待細菌生長至對數生長期(OD600=0.3)時收集待用。
1.3.3.2沙門氏菌的前處理
沙門氏菌ATCC 14028在使用之前需要處理,以去除多余的培養基及細菌代謝物對試驗結果的干擾。待細菌生長至對數生長期時,收集一定量的菌液,4℃,3 000 r/min離心5 min,棄上清,二次水復溶后再離心。重復上述離心操作,棄上清,0.01 mol/L PBS緩沖液將離心沉淀溶解后待用。
1.3.4包被液的優化
將1 μg抗鼠傷寒沙門氏菌的抗體分別溶于含有0%、2%、4%、6%、8%、10%甲醇的0.01 mol/LPBS溶液,滴加到Whatman AE 99硝酸纖維素膜上的加樣區內,37℃干燥箱中包被1 h。滴加10 μL 3%的BSA封閉液于37℃干燥箱中封閉30 min。然后用0.4%PBST沖洗液沖洗1 min,晾干后滴加10 μL石墨烯-膠體金-抗體復合物,滲入后于0.4%PBST溶液中沖洗1 min,晾干后觀察背景顏色較低的為最佳包被液。
1.3.5封閉液的優化
1.3.5.1封閉液中BSA濃度的優化
將1 μg抗鼠傷寒沙門氏菌抗體用甲醇含量為6%的包被液包被,滴加到Whatman AE 99硝酸纖維素膜上的加樣區內,于37℃干燥箱中包被1 h。然后分別滴加10 μL 0%、1%、2%、3%、4%、5%封閉液于37℃干燥箱中封閉30 min,于0.4%PBST沖洗液中沖洗1 min。晾干后滴加10 μL石墨烯-膠體金-抗體復合物,滲入后于0.4%PBST沖洗液中沖洗1 min,晾干后觀察背景較低的為封閉液中最佳BSA濃度。
通過設置微課程上傳至教學平臺,教師課上可將重點微課程加入教學中,學生課下根據自身情況反復觀看微課,便于課前預習、課后復習[2][3]。
1.3.5.2封閉液中Tween-20的優化
將1 μg抗鼠傷寒沙門氏菌的抗體用甲醇含量為6%的包被液包被,滴加到Whatman AE 99硝酸纖維素膜上的加樣區內,37℃干燥箱中包被1 h。滴加10 μL含有0%、0.2%、0.4%、0.6%、0.8%、1.0%Tween-20的封閉液于37℃干燥箱中封閉30 min,于0.4%PBST沖洗液中沖洗1 min。晾干后滴加10 μL石墨烯-膠體金-抗體復合物,滲入后于0.4%PBST沖洗液中沖洗1 min,晾干后觀察背景較低的為封閉液中最佳Tween-20的量。
1.3.6沖洗液優化
將1 μg抗鼠傷寒沙門氏菌抗體用甲醇含量為6%的包被液包被,包被結束后滴加10 μL 4%BSA+0.6% Tween-20的封閉液于37℃干燥箱中封閉30 min,于0.4%PBST沖洗液中沖洗1 min。晾干后滴加10 μL石墨烯-膠體金-抗體復合物,滲入后,分別用含有0%、0.2%、0.4%、0.6%、0.8%、1.0%Tween-20的沖洗液沖洗1 min,晾干后觀察背景較低的為最佳沖洗液。
1.3.7照射時長的優化
制作完成石墨烯-膠體金-抗體復合物試紙條后,用甲醇含量為6%的包被液將1 μg抗鼠傷寒沙門氏菌的抗體包被到Whatman AE 99硝酸纖維素膜上的加樣區內,37℃包被1 h,滴加10 μL 4%BSA+0.6% Tween-20的封閉液于37℃干燥箱內封閉30 min,于最佳沖洗液中沖洗1 min,晾干后分別滴加10 μL石墨烯-膠體金-抗體復合物與相同數量的鼠傷寒沙門氏菌沉淀的混合物,滲入后,于0.4%Tween-20沖液洗中沖洗1 min,晾干后,808 nm紅外光照射加樣區1 min,熱像儀測量并記錄加樣區不同時間點(0、10、20、30、40、50、60 s)的溫度并計算溫差,觀察溫差情況選擇最佳的照射時長。
1.3.8石墨烯-膠體金復合物光熱效應滲濾試紙條的靈敏度測試
用甲醇含量為6%的包被液將1 μg抗鼠傷寒沙門氏菌的抗體滴加到Whatman AE 99硝酸纖維素膜上的加樣區內,37℃包被1 h,滴加10 μL 4%BSA+0.6% Tween-20的封閉液于37℃干燥箱內封閉30 min,于0.4%Tween-20沖液洗中沖洗1 min,晾干后,分別加入10 μL石墨烯-膠體金-抗體復合物與不同細菌數鼠傷寒沙門氏菌沉淀的混合物,滲入后,于0.4%Tween-20沖洗液中沖洗1 min,晾干后,808 nm紅外光照射加樣區最優時長,熱像儀測量并記錄加樣區的溫度并計算溫差。多次試驗確定最低檢測限,繪制標準曲線。
2 結果與分析
2.1石墨烯—金納米復合物的制備與電鏡表征石墨烯—金納米復合物的電鏡表征見圖1。

圖1 石墨烯-金納米復合物透射電鏡圖片Fig.1 The TEM image of GO-Au nanocomposite
綜合試驗條件、制備的難易程度及所需時間、制備的復合物的穩定性等多方面因素,本試驗將目前多種石墨烯-金納米復合物制備法的優點進行融合,得到了如下所述的制備方法。首先利用檸檬酸三鈉還原法制備膠體金,在此基礎上加入氧化石墨烯溶液并通過加熱進行原位還原。該方法用時短,制備的石墨烯-金納米復合物穩定性高。利用透射電鏡(TEM)對制備的石墨烯-金納米復合物進行表征,電鏡結果顯示,本研究所制備的復合物,金顆粒呈現球形,平均粒徑約20 nm且大小均一,較好地結合在石墨烯片層上,證明本試驗所用方法可應用于合成石墨烯-金納米復合物。
2.2最佳包被液的選擇
包被液通過靜電力可以將抗體牢固的包被到Whatman AE 99硝酸纖維素膜上,本試驗探究了0.01 mol/L的PBS緩沖液中不同甲醇含量對抗體固定的影響,結果見圖2。如圖2所示,結果表明:甲醇含量為6%時背景明顯比不加甲醇及其它濃度甲醇的背景顏色淺。由于背景顏色深淺直接影響試紙條的升溫情況,因此選擇甲醇含量為6%的PBS緩沖液。

圖2 不同包被液對滲濾試紙條方法的影響Fig.2 Dot immune-graphene-gold filtration assay with different coating buffers
2.3最佳封閉液的選擇
2.3.1封閉液中BSA濃度的選擇
封閉液可以占據Whatman AE 99硝酸纖維素膜上的非特異性位點,降低非特異性結合,增強信噪比,常見的封閉液主要有BSA和脫脂牛奶兩種,脫脂牛奶相對BSA成分復雜,因此本試驗選擇BSA作為封閉液,結果見圖3。如圖3所示,BSA含量為4%時背景明顯較其它BSA含量的背景顏色淺,因此本試驗選擇BSA含量為4%的封閉液。

圖3 封閉液中不同BSA含量對滲濾試紙條方法的影響Fig.5 Dot immune-graphene-gold filtration assay with different concentration BSA blocking buffers
2.3.2封閉液中Tween-20的選擇
Tween-20有復性抗原的作用,可提高特異性的識別能力,因此本試驗優化了封閉液中Tween-20的量,結果見圖4。如圖4所示,結果表明:Tween-20含量為0.6%時背景較低。因為背景顏色深淺直接影響試紙條的升溫情況,因此本試驗選擇添加0.6%Tween-20的封閉液。

圖4 添加不同Tween-20的封閉液對滲濾試紙條方法的影響Fig.4 Dot immune-graphene-gold filtration assay with different concentration Tween-20 blocking buffers
2.4最佳沖洗液的選擇
過量的封閉液除結合非特異性位點外還有可能結合特異性位點,過量的待檢測鼠傷寒沙門氏菌及未結合的石墨烯-膠體金-抗體復合物也會對滲濾試紙條的靈敏度產生影響,Tween-20為表面活性劑,可以減少背景和非特異性條帶,故優化沖洗液中Tween-20的量。本試驗用0.01 mol/L PBS添加Tween-20作為沖洗液結果見圖5。如圖5所示,結果表明:Tween-20含量為0.4%時背景較低,因此選用0.01 mol/L PBS+ 0.4%Tween-20作為沖洗液。

圖5 不同沖洗液對滲濾試紙條方法的影響Fig.7 Dot immune-graphene-gold filtration assay with different washing buffers
2.5最佳照射時長的選擇
石墨烯-膠體金復合物在808 nm紅外光照射下產熱產生溫差,適宜的照射時長可以節約試驗時間同時提高測試穩定性。試驗結果如圖6所示。結果表明:隨著照射時間的增加,溫差不斷增加,但10 s之后增加趨勢不明顯,為節約試驗時間并減小試驗誤差,本試驗選擇20 s為最佳照射時間。
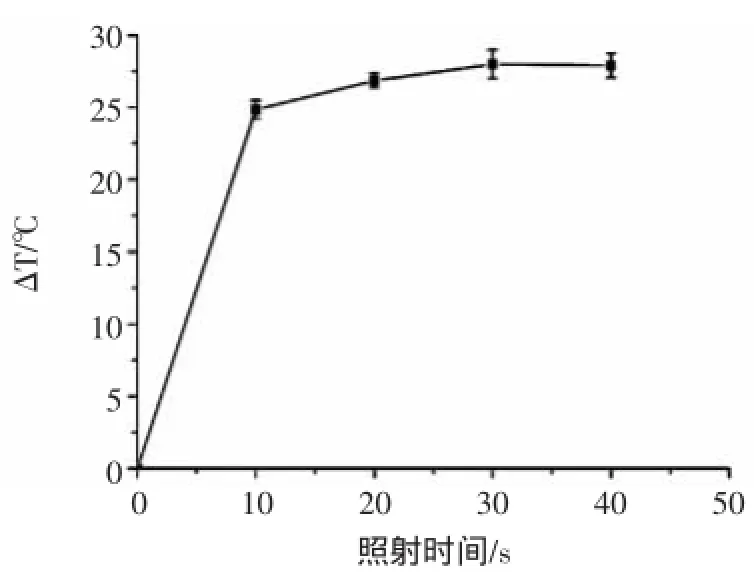
圖6 照射時長的優化Fig.6 Optimization of the irradiation time
2.6石墨烯-膠體金復合物光熱效應滲濾試紙條靈敏度測試
光熱效應滲濾試紙條方法在傳統滲濾試紙條方法定性檢測的基礎上根據石墨烯-膠體金的良好熱效應建立,通過808 nm紅外光照射加樣區得出溫差定量測定鼠傷寒沙門氏菌。激光照射前對照組的溫度為T01,808 nm激光照射20 s后熱像儀測得的溫度為T02,滴加沙門氏菌的試驗組激光照射前的溫度為T1,808 nm激光照射20 s后熱像儀測得的溫度為T2,溫差ΔT=T2-T1-(T02-T01)。
以鼠傷寒沙門氏菌的個數(CFU/mL)為橫坐標,溫差(ΔT)為縱坐標繪制標準曲線,得出鼠傷寒沙門氏菌的個數與溫差的線性關系。結果如圖7所示。結果表明:隨著鼠傷寒沙門氏菌的個數的增加,溫差不斷增加。該試驗所得標準曲線線性公式為:y=0.754x-2.09,R2=0.971,說明鼠傷寒沙門氏菌的個數與溫差呈良好的線性相關。當信噪比=3∶1時,鼠傷寒沙門氏菌的個數為2 400 CFU/mL,鼠傷寒沙門氏菌的最低檢測限為2 400 CFU/mL。
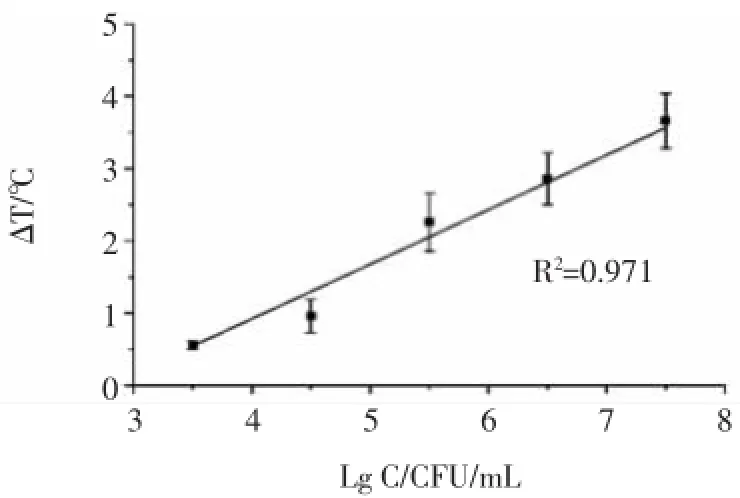
圖7 沙門氏菌數目與溫差的線性標準曲線Fig.7 The linear relation of the number of Salmonella and ΔT
3 結論
本研究利用檸檬酸三鈉還原制備膠體金,在此基礎上加入氧化石墨烯溶液,通過加熱法進行原位還原,確定了石墨烯-金納米復合物的制備方法與條件。利用該方法制備的石墨烯-金納米復合物對抗沙門氏菌抗體進行標記,制備了石墨烯-金-抗沙門氏菌抗體復合物。采用雙抗夾心法,建立了檢測沙門氏菌的基于石墨烯-金納米復合物光熱效應的滲濾試紙條方法。該滲濾試紙條方法采用目測法檢測沙門氏菌時,在沙門氏菌數目為2.4×104CFU/mL時出現可與空白區分開的紅斑,而采用溫差法檢測時,可以將檢測限降低到2.4×103CFU/mL。相比基于膠體金光熱效應的滲濾試紙條方法,該方法對沙門氏菌檢測的靈敏度提高了10倍。本研究通過大量試驗數據計算繪制出沙門氏菌數目與溫度差的標準曲線,得到線性回歸方程:y=0.754x-2.09,R2=0.971。試驗結果證明,基于光熱效應的滲濾試紙條方法較傳統滲濾試紙條方法靈敏度更高,該方法可應用于鼠傷寒沙門氏菌的檢測。
[1]王毳,閆磊,曾慶祝.沙門氏菌的檢測技術與方法[J].現代食品科技,2007,23(5):82-85
[2] Yang B,Qu D,Zhang X,et al.Prevalence and characterization of Salmonella serovars in retail meats of marketplace in Shaanxi,China [J].International journal of food microbiology,2010,141(1):63-72
[3]中華人民共和國衛生部,中國國家標準化管理委員會.GB 2726—2005熟肉制品衛生標準[S].北京:中國標準出版社,2005
[4]中華人民共和國衛生部,中國國家標準化管理委員會.GB 7099—2003糕點、面包衛生標準[S].北京:中國標準出版社,2003
[5]中華人民共和國衛生部,中國國家標準化管理委員會.GB 9678.1—2003糖果衛生標準[S].北京:中國標準出版社,2003
[6]孫園園,趙鵬,劉駿,等.沙門氏菌檢測方法研究進展[J].中國畜牧獸醫,2011,38(1):218-221
[7]李小玲,劉斌,但現龍,等.沙門氏菌內標PCR快速檢測試劑盒的研制與應用[J].中國農業科學,2011,44(16):3395-3402
[8]劉喆,張書蕭,王少輝,等.沙門氏菌的檢測技術進展[J].中國動物傳染病學報,2012,20(2):81-86
[9]Liu C,Jia Q,Yang C,et al.Lateral flow immunochromatographic assay for sensitive pesticide detection by using Fe3O4nanoparticle aggregates as color reagents[J].Anal Chem,2011,83(17):6778-6784
[10]Kim Y A,Lee E H,Kim K O,et al.Competitive immunochromatographic assay for the detection of the organophosphorus pesticide chlorpyrifos[J].Anal chimacta,2011,693(1):106-113
[11]Zhou Y,Pan F G,Li Y S,et al.Colloidal gold probe-based immunochromatographic assay for the rapid detection of brevetoxins in fishery product samples[J].BiosensBioelectron,2009,24(8):2744-2747
[12]Xu W,Chen X,Huang X,et al.Ru(phen)3 2+doped silica nanoparticle based immunochromatographic strip for rapid quantitative detection of β-agonist residues in swine urine[J].Talanta,2013,114:160-166
[13]Li Z,Wang Y,Wang J,et al.Rapid and sensitive detection of protein biomarker using a portable fluorescence biosensor based on quantum dots and a lateral flow test strip[J].Anal Chem,2010,82(16):7008-7014
[14]Wang L,Lu D,Wang J,et al.A novel immunochromatographic electrochemical biosensor for highly sensitive and selective detection of trichloropyridinol,a biomarker of exposure to chlorpyrifos[J]. BiosensBioelectron,2011,26(6):2835-2840
[15]Nian H,Wang J,Wu H,et al.Electrochemical immunoassay of cotinine in serum based on nanoparticle probe and immunochromatographic strip[J].Anal ChimActa,2012,713:50-55
[16]Qin Z,Chan W C W,Boulware D R,et al.Significantly improved analytical sensitivity of lateral flow immunoassays by using thermal contrast[J].AngewChemInt Ed,2012,124(18):4434-4437
[17]Zedan A F,Moussa S,Terner J,et al.Ultrasmall gold nanoparticles anchored to graphene and enhanced photothermal effects by laser irradiation of gold nanostructures in graphene oxide solutions[J].ACS nano,2012,7(1):627-636
[18]Frens G.Controlled nucleation for the regulation of the particle size in monodisperse gold suspensions[J].Nature,1972(241):20-22
[19]馮曉苗,閆真真.石墨烯-金納米復合材料:水熱合成及在生物傳感器中的應用[J].無機化學學報,2013,29(5):1051-1056
[20]Hu J,Li F,Wang K,et al.One-step synthesis of graphene-AuNPs by HMTA and the electrocatalytical application for O2and H2O2[J].Talanta,2012,93:345-349
A Paper-based Detection Method of Salmonella Using the Photo-thermal Effect
BING Xin1,LIU Jing-jing2,GAO Lu-xiang2,ZHANG Zhen2,LIU Zhao-chen2,JIA Min2,*
(1.Shandong Product Quality Inspection Research Institute,Jinan 250012,Shandong,China;2.College of Life Science,Shandong Normal University,Jinan 250014,Shandong,China)
A novel paper-based dot immune-graphene-gold filtration assay for the detection of Salmonella was developed based on the photothermal effect of graphene oxide(GO)-Au nanocomposite.First of all,the GO-Au nanocomposite and anti-Salmonella antibody modified GO-Au nanocomposite were synthesized.Based on the traditional strip test method,experimental conditions such as the buffer solutions and the irradiation time were optimized.The limit of naked eye detection was as low as 2.4×104CFU/mL and could be increased to 2.4×103CFU/mL by the use of temperature contrast.The standard curve of dot immune-graphene-gold filtration assay for detecting Salmonella was established,and the linear regression equation:y=0.754x-2.09,R2=0.971.
strip;graphene nanocomposites;photo-thermal effect;Salmonella
2016-05-06
國家質量監督檢驗檢疫總局科技計劃項目(2014QK122)作者簡介:邴欣(1977—),男(漢),高級工程師,博士,研究方向:產品質量安全。

