加溫濕化高流量鼻導(dǎo)管吸氧聯(lián)合枸櫞酸咖啡因治療早產(chǎn)兒呼吸暫停
左曉曉,薛愛梅,那 利
早產(chǎn)兒呼吸暫停(apnea of prematurity,AOP)是目前新生兒重癥監(jiān)護(hù)中面臨的主要臨床問題之一,是早產(chǎn)兒呼吸管理中較為常見的問題。對于AOP,臨床多采用甲基黃嘌呤類藥物聯(lián)合無創(chuàng)輔助呼吸治療[1-2]。無創(chuàng)呼吸支持國內(nèi)以往多采用經(jīng)鼻持續(xù)氣道正壓通氣(nasal continuous positive airway pressure,nCPAP),療效確切,但存在著不足之處。近些年將加溫濕化高流量鼻導(dǎo)管吸氧(heated humidified high-flow nasal cannula,HHFNC)技術(shù)應(yīng)用在AOP的治療上,取得了良好效果,現(xiàn)報(bào)道如下。
1 資料與方法
1.1一般資料采用前瞻性隨機(jī)對照研究方法,按照入院單雙次序,并征得患兒家屬知情同意,將我院新生兒/兒童重癥監(jiān)護(hù)病房自2014年10月至2016年10月收治的64例AOP患兒分為觀察組和對照組,每組32例。納入標(biāo)準(zhǔn):①出生胎齡小于37周;②頻發(fā)呼吸暫停:1 h內(nèi)呼吸暫停發(fā)作超過2~3次。排除標(biāo)準(zhǔn):①生后重度窒息;②嚴(yán)重呼吸窘迫綜合征(需要?dú)夤懿骞軝C(jī)械通氣支持者);③重度高膽紅素血癥(總膽紅素大于340 μmol·L-1);④吸吮與吞咽不協(xié)調(diào);⑤吸吮與呼吸不協(xié)調(diào)。觀察組給予HHFNC,對照組給予nCPAP。觀察組32例,男性20例,女性12例,胎齡(31.5±3.3)周、體質(zhì)量(1.56±0.42) kg、呼吸暫停發(fā)作起始日齡(6.5±4.3) d;對照組32例,男性18例,女性14例,胎齡(32.1±4.0)周、體質(zhì)量(1.66±0.48) kg、呼吸暫停發(fā)作起始日齡(7.1±5.3) d。兩組一般情況比較,差異均無統(tǒng)計(jì)學(xué)意義(P>0.05)。
1.2方法
1.2.1治療方法兩組均監(jiān)測心率、呼吸、血氧飽和度等生命體征,同時(shí)給予保暖,保持呼吸道通暢,腸內(nèi)喂養(yǎng)(腸內(nèi)喂養(yǎng)量不足時(shí)給予部分腸道外營養(yǎng)支持治療)等,枸櫞酸咖啡因注射液首劑20 mg·kg-1·d-1,維持量5 mg·kg-1·d-1應(yīng)用等治療。觀察組采用斐雪派克MR810(Fisher & Paykel,新西蘭)加溫濕化器,設(shè)置:體質(zhì)量1 000~1 999 g時(shí)氣體流量為3 L·min-1,體質(zhì)量2 000~2 999 g時(shí)為4 L·min-1,每組氣體流量在基線水平最大可增加3 L·min-1;利用空氧混合儀吸氧濃度控制在21%~40%之間,目標(biāo)使血?dú)夥治鲋醒醴謮涸谡7秶鷥?nèi)或經(jīng)皮血氧飽和度在90%~94%之間;對照組采用Sophie新生兒呼吸機(jī)(Stephan,德國)nCPAP治療。觀察兩組臨床癥狀改善[3](顯效:治療后24 h內(nèi)未再出現(xiàn)呼吸暫停;有效:治療后72 h內(nèi)未再出現(xiàn)呼吸暫停;無效:治療后72 h仍出現(xiàn)呼吸暫停或病情加重),氧暴露時(shí)間(排除治療中轉(zhuǎn)為有創(chuàng)機(jī)械通氣病例),胃潴留(胃殘余超過上次喂養(yǎng)量的1/3,或24 h胃殘余量超過喂養(yǎng)總量的1/4,或持續(xù)喂養(yǎng)時(shí)超過1 h的量),鼻中隔及鼻部局部皮膚損傷和氣胸發(fā)生率,患兒舒適度(觀察呼吸支持時(shí)患兒有無煩躁及抗拒動(dòng)作)和患兒家屬接受度(出院前設(shè)計(jì)一個(gè)針對患兒父母的統(tǒng)計(jì)表,內(nèi)容主要介紹HHFNC和nCPAP兩種呼吸支持方案:包括適應(yīng)證、優(yōu)點(diǎn)及不良反應(yīng)等,由患兒父母對自己患兒所選方案做一次再選擇,在面對兩種方案時(shí)依舊認(rèn)可并愿意選擇原方案者,投認(rèn)可票,會(huì)選擇另一種方案者投否定票,然后計(jì)算出認(rèn)可票在本組總例數(shù)中的構(gòu)成比,作為其接受度)。

2 結(jié)果
2.1兩組治療效果比較觀察組臨床癥狀改善較對照組比較無明顯差異(Z=-0.330,P=0.741)。觀察組氧暴露時(shí)間(16.30±2.98) d與治療組的(16.30±2.98) d比較,差異無統(tǒng)計(jì)學(xué)意義(P>0.05),見表1。
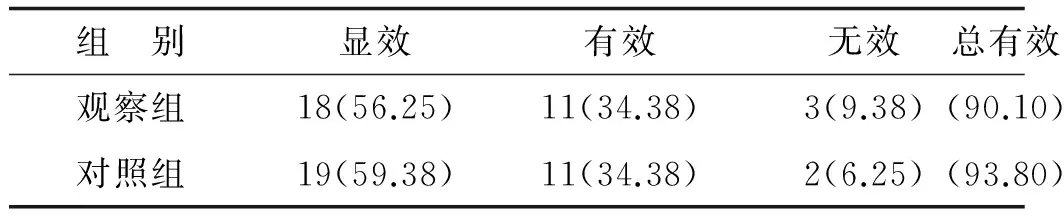
表1 臨床癥狀改善情況比較(n=32) 例(%)
2.2兩組并發(fā)癥情況比較觀察組胃潴留、鼻中隔及鼻部局部皮膚損傷發(fā)生率明顯低于對照組,兩組均無氣胸出現(xiàn),見表2。
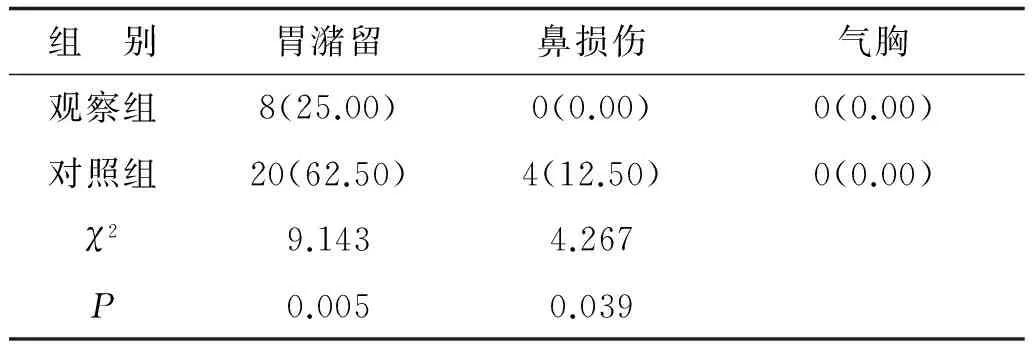
表2 兩組并發(fā)癥情況比較(n=32) 例(%)
2.3兩組舒適度及家屬接受度比較觀察組舒適度及家屬接受度明顯高于對照組,見表3。
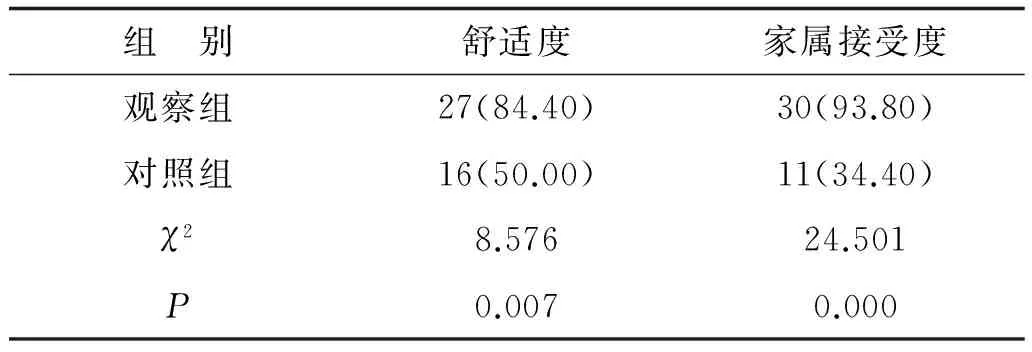
表3 兩組舒適度及家屬接受度比較(n=32) 例(%)
3 討論
呼吸暫停是呼吸停止時(shí)間>20 s,伴有心率減慢(<100次·min-1),或出現(xiàn)青紫、血氧飽和度降低和肌張力低下,是早產(chǎn)兒的常見癥狀;AOP發(fā)病機(jī)制仍不清楚,胎齡越小發(fā)病率越高,胎齡<30周發(fā)生率>80%,胎齡30~31周為50%,如不及時(shí)發(fā)現(xiàn)和處理,可致腦缺氧損傷,甚至猝死[4]。AOP治療除給氧和藥物治療外,很多學(xué)者還發(fā)明了其他一系列治療方法。姚仁芬等[5]自行設(shè)計(jì)制作的振動(dòng)式水囊床,以及金淑芹[6]等提出的簡易水床及體位護(hù)理等,通過這種特殊設(shè)計(jì)的治療床產(chǎn)生的機(jī)械振動(dòng)波,達(dá)到興奮呼吸中樞和刺激呼吸肌的效應(yīng)。
在藥物和無創(chuàng)輔助呼吸應(yīng)用方面,早期國內(nèi)多采用氨茶堿+nCPAP方案。但氨茶堿使用時(shí)有效血藥濃度與中毒濃度接近,需嚴(yán)密監(jiān)測,且臨床療效欠佳[7]。咖啡因的作用機(jī)制主要是通過興奮呼吸中樞,其脂溶性高,滲透入腦脊液更迅速,早產(chǎn)兒易于耐受,咖啡因的臨床效應(yīng)濃度為5~20 mg·L-1,低于50 mg·L-1時(shí)很少出現(xiàn)不良反應(yīng)。nCPAP是減少呼吸暫停發(fā)作頻率的一種有效的氣道支持方法,其原理為給氧時(shí)通過持續(xù)氣流產(chǎn)生的氣道正壓,使肺泡保持開放,防止肺不張、改善肺換氣及提高氧合能力的作用,同時(shí)增加跨肺壓和氣道直徑、減少氣道阻力,更有利于自主呼吸,從而減少呼吸暫停的發(fā)生[8-9]。但其也存在一些較常見的并發(fā)癥,如:鼻中隔損傷及鼻部局部皮膚損傷等。由于咖啡因的不良反應(yīng)發(fā)生率較氨茶堿相對低,在AOP治療上逐漸替代氨茶堿,取得良好療效。HHFNC在國外較廣泛應(yīng)用,但國內(nèi)應(yīng)用尚不太多[10]。本研究顯示HHFNC聯(lián)合枸櫞酸咖啡因在AOP治療方面,療效滿意,與nCPAP聯(lián)合枸櫞酸咖啡因療效相當(dāng),在鼻中隔及鼻部局部皮膚損傷、胃潴留、患兒舒適度及家屬認(rèn)可度等方面,均明顯優(yōu)于后者。
HHFNC是把加溫濕化的空氧混合氣體通過特制雙孔鼻導(dǎo)管直接經(jīng)鼻輸入,可產(chǎn)生類似于nCPAP的氣道正壓,從而幫助肺容量恢復(fù)[11],也可減少nCPAP所致的分泌物聚集、氣道變冷和水分流失等情況。減輕或避免對患兒鼻部的刺激,從而減輕鼻前庭受壓、鼻中隔損傷,同時(shí)減少死腔、減低鼻咽阻力、降低呼吸功、利于肺復(fù)張。另外,HHFNC固定簡單,無需像nCPAP需借助特殊固定帽將管道固定于頭部患兒,患兒舒適度提高,便于護(hù)理。Osman等應(yīng)用早產(chǎn)兒的疼痛評估項(xiàng)目觀察了60例患兒,結(jié)果顯示HHFNC組疼痛評分明顯低于nCPAP組[12]。本研究中采取問卷調(diào)查法,結(jié)果顯示患兒家屬的接受度與nCPAP相比具有明顯優(yōu)勢。
本研究兩組中均無氣胸發(fā)生,這與Campbell的研究相吻合[13],但HHFNC氣道壓力不恒定,是否會(huì)增加氣胸的發(fā)生,還需大樣本臨床觀察。有報(bào)道HHFNC混合氣體在輸出時(shí)已按需要的濃度進(jìn)行稀釋,吸入氧濃度不隨患者呼吸狀態(tài)改變,氧濃度可控,不加重早產(chǎn)兒視網(wǎng)膜病和支氣管肺發(fā)育不良的發(fā)生[14]。綜上所述,HHFNC聯(lián)合枸櫞酸咖啡因治療AOP效果滿意,方法簡單易行,便于基層醫(yī)院開展,并發(fā)癥較nCPAP減輕或減少,是一種較好的治療方法,值得推廣。
[1] 趙婧,母得志.早產(chǎn)兒呼吸暫停診療進(jìn)展[J].臨床兒科雜志,2012,30(3):291-294.
[2] Schoen K,Yu T,Stockmann C,et al.Use of methylxanthine therapies for the treatment and prevention of apnea of prematurity[J].Paediatr Drugs,2014,16(2):169-177.
[3] 楊慶南,朱建幸,謝利娟,等.不同PEEP水平的鼻塞持續(xù)正壓通氣對早產(chǎn)兒反復(fù)呼吸暫停的療效觀察川[J].上海交通大學(xué)學(xué)報(bào)(醫(yī)學(xué)版),2010,30(7):871-873.
[4] 邵肖梅,葉鴻瑁,丘小汕.實(shí)用新生兒學(xué)[M].4版.北京:人民衛(wèi)生出版社,2011:245-247.
[5] 姚仁芬,金慧珠,胡婷,等.簡易自制振動(dòng)式水囊床在早產(chǎn)兒呼吸暫停中的應(yīng)用[J].中外醫(yī)療,2010,29(31):186.
[6] 金淑芹,劉金秀,杜占彩,等.簡易水床及體位護(hù)理對早產(chǎn)兒呼吸暫停的干預(yù)效果分析[J].全科護(hù)理,2014,12(29):2710-2711.
[7] Abu-Shaweesh JM,Martin RJ.Neonatal apnea:what’s new[J].Pediatr Pulmonol,2008,43(10):937-944.
[8] De Paoli AG,Davis PG,Lemyre B.Nasal continuous positive airway pressure versus nasal intermittent positive pressure ventilation for preterm neonates: a systematic review and meta-analysis[J].Acta paediatrica,2003,92(1):70-75.
[9] De Paoli AG,Morley CJ,Davis PG,et al.In vitro comparison of nasal continuous positive airway pressure devices for neonates[J].Arch Dis Child Fetal Neonatal Ed,2002,86(17):42-45.
[10]武榮,封志純,劉石.新生兒診療技術(shù)進(jìn)展[M].北京:人民衛(wèi)生出版社,2016:138-142.
[11]Corley A,Caruana LR,Barnett AG,et al. Oxygen delivery through high-flow nasal cannulae increase end-expiratory lung volume and reduce respiratory rate in post-cardiac surgical patients[J].Br J Anaesth,2011,107(6):998-1004.
[12]Osman M,Elsharkawy A,Abdel-Hady H.Assessment of pain during application of nasal-continuous positive airway pressure and heated,humidified high-flow nasal cannulae in preterm infants[J].J Perinatol,2015,35(4):263-267.
[13]Campbell DM,Shah PS,Shah V,et al.Nasal continuous positive airway pressure from high flow cannula versus infant flow for preterm infants[J].J Perinatol,2006,26(9):546-549.
[14]Poets CF.Apnea of prematurity:what can observational studies tell us about pathophysiology[J].Sleep Med,2010,11(7):701-707.

