腦缺血再灌注大鼠局灶性腦缺血預處理后Nogo-A及NgR的表達
焦義明 何健玲 何勝男
(鄭州大學第二附屬醫院體檢中心,河南 鄭州 450014)
腦缺血再灌注大鼠局灶性腦缺血預處理后Nogo-A及NgR的表達
焦義明 何健玲 何勝男1
(鄭州大學第二附屬醫院體檢中心,河南 鄭州 450014)
目的 觀察局灶性腦缺血預處理干預后大鼠腦內Nogo-A、NgR表達的情況。方法 建立腦缺血再灌注及預處理模型,將健康雄性SD大鼠隨機分為假手術組、缺血再灌注組和缺血預處理組,每組又分為1、2、7 d 3個亞組,預處理時間為10 min,免疫組化法檢測大鼠缺血海馬區Nogo-A、NgR的表達,RT-PCR方法檢測大鼠缺血海馬區NgR mRNA的表達。結果 與假手術組比較,缺血再灌注組在1、2、7 d 3個時間點Nogo-A及NgR表達均增高;腦缺血預處理干預后,Nogo-A及NgR在各個時間點的表達較缺血再灌注組均明顯降低(P<0.05)。結論 局灶性腦缺血預處理的干預可以降低大鼠腦內Nogo-A及NgR的表達而提高腦缺血耐受的神經保護作用。
局灶性腦缺血預處理;Nogo-A;NgR
給予一次或多次非致死量的腦缺血預預處理能夠誘導腦缺血耐受,從而可以減輕腦缺血再灌注引起的腦損傷。隨著對這一作用認識的加深,其分子保護機制被提出許多種。但其通過何種具體的機制發揮作用,目前仍然不清楚〔1〕。Nogo-A是一種重要的神經生長抑制因子,其作用是抑制神經元的再生,而腦缺血后功能損傷程度則與神經元再生的難易存在一定關系。由此表明,腦缺血后功能損傷輕重一定程度上取決于Nogo-A的作用。NgR是Nogo-A的受體,而Nogo-A 往往通過與之結合來發揮作用。為此,本實驗擬通過制備腦缺血預處理模型,觀察腦組織中Nogo-A、NgR表達的情況,來探討腦缺血耐受的保護機制。
1 材料與方法
1.1 動物分組 成年健康雄性SD大鼠,體重(250±30)g,由河南省實驗動物中心提供,隨機分為3組,假手術組;缺血再灌注組:假手術3 d后給予2 h大腦中動脈栓塞(MCAO),再分別灌注1、2、7 d 3個時間點后處死;缺血預處理組:缺血預處理10 min再灌注3 d后給予2 h MCAO,再灌注1 d、2 d及7 d 3個時間點后處死。
1.2 缺血預處理及模型制作 本實驗參照Longa等〔2〕線栓法并加以改進進行。在腹腔注射10%的水合氯醛(0.3 ml/100 g)麻醉,采取頸正中部切口,鈍性依次分離右側頸總、頸外、頸內動脈,將右側頸外動脈結扎并切斷,在殘端距分叉約5 mm處,剪一切口,插入約0.26 mm直徑的釣魚線,沿頸內動脈輕柔推進距分叉處約19 mm遇有輕微阻力即行,結扎頸外動脈殘端,10 min后抽出釣魚線至分叉處,形成第一次再灌注,縫合切口,完成腦缺血預處理。3 d后再次用同樣方法造成MCAO 2 h,各組分別再灌注1 d、2 d、7 d后檢測大鼠神經功能情況,然后處死取出腦組織用于指標測定。假手術組僅分離右側頸總動脈及分叉處,不插入線栓阻斷MCAO。動物蘇醒后爬行時向左劃圈,提尾時左前肢內收屈曲為模型制備成功的標志,術中用白熾燈使大鼠肛溫保持在37℃左右。
1.3 神經功能缺損評分 采用Longa等〔2〕的神經功能標準評分:無任何神經功能障礙為0分;不能伸展左側前肢為1分;向左側劃圈為2分;向左側傾倒為3分;無自主活動且伴有意識障礙為4分。
1.4 免疫組化分別檢測大鼠大腦缺血海馬區Nogo-A 和NgR的表達 每個亞組大鼠處死后斷頭取腦,固定、石蠟包埋后切片,取前鹵后6 mm部分進行連續性冠狀切片,片厚5 μm,分別按Nogo-A和NgR的免疫組化說明書依次進行染色、 DAB顯色、封片,光鏡下觀察細胞質內呈棕色者為Nogo-A和NgR陽性細胞。每張切片分別選取10個具有代表性的高倍視野,平均計算Nogo-A和NgR陽性細胞數。
1.5 RT-PCR檢測大鼠缺血海馬區NgR mRNA的表達 每個亞組在右側腦缺血組織區取100 g研磨粉碎,加入1.4 ml Trizol 試劑勻漿,經過分離、沉淀、洗滌、溶解后即可提取總RNA。用瓊脂糖凝膠電泳鑒定總RNA 質量,用Transgene 公司提供的RT試劑盒將總RNA逆轉錄為cDNA,用 NgR上游引物(5'CAGTGACTTAGAGGGTTGTGCT3')及下游引物(5'CCATTGCCTGGTGGAGTGT3')建立PCR 反應體系,擴增DNA長度為210 bp;然后對產物DNA進行電泳,用D-140 圖像記錄系統對目的條帶分析,以NgR 的DNA 條帶和內參GPADH(上游引物5'CAGTGCCAGCCTCGTCTCAT3',下游引物5'AGGGGCCATCCACAGTCTTC3',擴增片段595 bp)的DNA 條帶灰度值比值計算目的基因NgR mRNA的表達量。
1.6 統計學方法 采用SPSS13.0軟件進行t檢驗及多因素方差分析。
2 結 果
2.1 神經功能缺損評分 假手術組在各個時間點均無神經功能缺損,缺血再灌注組均有不同程度的神經功能缺損,而缺血預處理組神經功能評分在各時間點均明顯低于缺血再灌注組(P<0.05)。見表1。
2.2 免疫組化方法檢測大鼠右側海馬區Nogo-A表達 缺血再灌注組在右側海馬區可見較多的胞質染色深的Nogo-A陽性細胞,與假手術組相應時間點比較差異顯著(P<0.05);實施預處理干預后,右側海馬區Nogo-A陽性細胞數有所降低,與缺血再灌注組比較差異顯著(P<0.05)。見表2。
2.3 免疫組化方法檢測大鼠右側海馬區NgR表達 缺血再灌注組右側海馬區可見有較多的胞質染色深的NgR陽性細胞,與假手術組相應時間點比較差異顯著(P<0.05);實施預處理干預后,右側海馬區 NgR陽性細胞有所降低,與缺血再灌注組相應時間點比較差異顯著(P<0.05)。見表3。
2.4 RT-PCR檢測大鼠右側海馬區NgR mRNA表達 缺血再灌注組右側海馬區可見有較多的NgR mRNA表達,與假手術組相應時間點比較差異顯著(P<0.05);實施預處理干預后,右側海馬區NgR mRNA表達有所降低,與缺血再灌注組相應時間點比較差異顯著(P<0.05)。見表4。
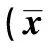
表1 各組神經功能缺損評分的比較±s,n=10)
與假手術組比較:1)P<0.05;與缺血再灌注組比較:2)P<0.05,下表同

表2 各組右側海馬區Nogo-A表達的比較

表3 各組右側海馬區NgR表達的比較

表4 各組右側海馬區NgR mRNA表達的比較
3 討 論
缺血預處理后的腦組織可對隨后發生的缺血產生保護性的耐受現象〔3〕。腦缺血耐受的保護機制是一個復雜的多機制參與的過程,包括細胞因子的參與、興奮性和抑制性神經遞質動態平衡的改變等,但其具體的內源性保護機制仍不明確。Moncayo等〔4〕對2 492例腦梗死患者研究發現,發生過短暫性腦缺血(TIA)的腦梗死患者預后較好,未發生過TIA的患者預后較差,且神經功能缺損較重。由此可知,TIA一定程度上類似于腦缺血預處理,因而研究腦缺血預處理的分子保護機制又具有一定的臨床意義。有研究表明,缺血10 min作為預處理,再灌注3 d后產生的腦保護作用最強,且時間持續約為7 d〔5〕。因此,本實驗設計采用缺血10 min作為預處理時間,3 d作為再灌注時間,同時設置了1 d、2 d、7 d 3個時間點,其符合預處理腦保護作用的持續時間。
本實驗發現,局灶性腦缺血預處理可通過降低Nogo-A的表達來起到神經保護作用。也有研究證實,應用Nogo-A抗體IN-1可使腦缺血損傷后的神經元軸突生長和功能恢復〔6〕。由此可見,腦缺血損傷后的受損程度和功能恢復情況與Nogo-A有很大關系。本文結果推測Nogo-A與NgR相結合來發揮腦損傷作用,而至于二者如何結合的,還有待進一步研究。通過腦缺血預處理后,二者表達較缺血再灌注組而言均降低,大鼠的神經功能評分也是降低的,因此我們進一步推測腦缺血預處理可能通過降低Nogo-A與NgR的表達這一途徑來提高腦缺血耐受的,從而對腦缺血損傷起保護作用。這對缺血性腦血管疾病的防治作用具有一定的臨床意義。
1 Durukan K,Tatlisumak T.Preconditioning-induced ischemic tolerance:a window into endogenous gearing for cerebroprotection〔J〕.Exp Transl Stroke Med,2010;2(1):2.
2 Longa EI,Weinstein PR,Carlson S,etal.Reversible middle cerebral artery:occlusion without craniotomy in rats〔J〕.Stroke,1989;20(1):84-91.
3 Murry CE,Jennings RB,Reimer KA.Preconditioning with ischemia:a delay of lethal cell injury in ischemic myocardium〔J〕.Circulation,1986;74(5):1124-36.
4 Moncayo J,de Freitas GR,Bogousslaky J,etal.Do transient ischemic attacks have a neural protective effect〔J〕?Neurology,2000;54(11):2089-90.
5 Zhou C,Li Y,Nanda A,etal.HBO suppresses Nogo-A,NgR,or RhoA expression in the cerebral cortex after global ischemia〔J〕.Biochem Biophys Res Commun,2003;309(2):368-76.
6 趙 紅,高曉玉,王得新.腦缺血再灌注模型大鼠神經生長抑制因子Nogo-A的表達變化〔J〕.中風與神經疾病雜志,2009;26(1):4-7.
〔2015-08-12修回〕
(編輯 曹夢園)
焦義明(1984-),男,碩士,醫師,主要從事腦血管疾病的基礎研究。
R743.3
A
1005-9202(2017)02-0299-03;
10.3969/j.issn.1005-9202.2017.02.017
1 河南中醫藥大學肝膽脾胃二科

