腦惡性膠質瘤手術及放化療后腫瘤復發及預后因素分析
劉先進
河南駐馬店市中心醫院 駐馬店 463000
腦惡性膠質瘤手術及放化療后腫瘤復發及預后因素分析
劉先進
河南駐馬店市中心醫院 駐馬店 463000
目的 分析腦惡性膠質瘤手術及放化療后腫瘤的復發及預后因素。方法 選取2010-03—2016-03間收治的52例腦惡性膠質瘤術后放化療腫瘤復發再手術的患者作為觀察對象。記錄兩次手術時間間隔,術前KPS評分、切除程度以及腫瘤體積等多項預后因素,分別采用Kaplan-Meier生存曲線和Cox風險比例模型對預后因素進行單因素、多因素分析,研究各預后因素對患者生存狀況的影響。結果 單因素Kaplan-Meier生存分析發現,術前KPS評分≥70分、行腫瘤全切術以及腫瘤體積<50cm3,能夠延長患者的術后生存時間(P<0.05);多因素Cox風險比例模型分析發現,KPS評分<70分、腫瘤體積≥50cm3,是腫瘤復發再手術的高危預后因素(P<0.05)。結論 腦惡性膠質瘤是發病率和病死率最高的顱內惡性腫瘤。術前KPS評分能對治療效果進行有效的評估;而腫瘤的體積、切除程度均會影響到患者的生存時間。
腦惡性膠質瘤;放化療;腫瘤復發;再手術治療
腦惡性膠質瘤大都生長在腦神經組織內,細胞分化不良,迅速復制,難以根治[1-2]。僅40%的患者能實施全切除術,且原發部位仍會有腫瘤細胞殘存,3個月~2 a就可復發[3]。2010-03—2016-03間,我們對52例腦惡性膠質瘤手術及放化療后腫瘤復發的患者,再次給予手術治療,現對腫瘤的復發及預后因素進行分析,報告如下。
1 資料與方法
1.1 一般資料 選本組52例患者中,男27例、女25例;年齡19~64歲,平均43.1歲。按照WHO 2 000年中樞神經系統分類標準,原發腫瘤Ⅲ級32例,Ⅳ級20例,腫瘤復發后Ⅲ級27例,Ⅳ級25例。
1.2 方法 在不影響神經功能的前提下,對患者實施顯微切除手術,最大程度將腫瘤細胞切除。術后進行放療化療并定期進行經頭顱CT檢測以及MRI檢查,監測腫瘤復發情況。一旦復發即應選擇適當的時機再次行切除手術。記錄兩次手術時間間隔,術前KPS評分、切除程度以及腫瘤體積等多項預后因素,分別采用Kaplan-Meier生存曲線和Cox風險比例模型對預后因素進行單因素、多因素分析,觀察各預后因素對患者生存狀況的影響。
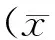
2 結果
2.1 單因素Kaplan-Meier生存分析 原發性腦惡性膠質瘤患者進行手術后,輔以放療和化療治療。腫瘤復發后再次進行手術,存活時間6.2~36.5個月,中位生存期為15.1個月,95%可信區間為11.52~19.03。運用Kaplan-Meier生存曲線對預后因素進行單因素分析發現,術前KPS評分≥70分、行腫瘤全切術以及腫瘤體積<50cm3,能夠延長患者的術后生存時間(P<0.05),見表1。
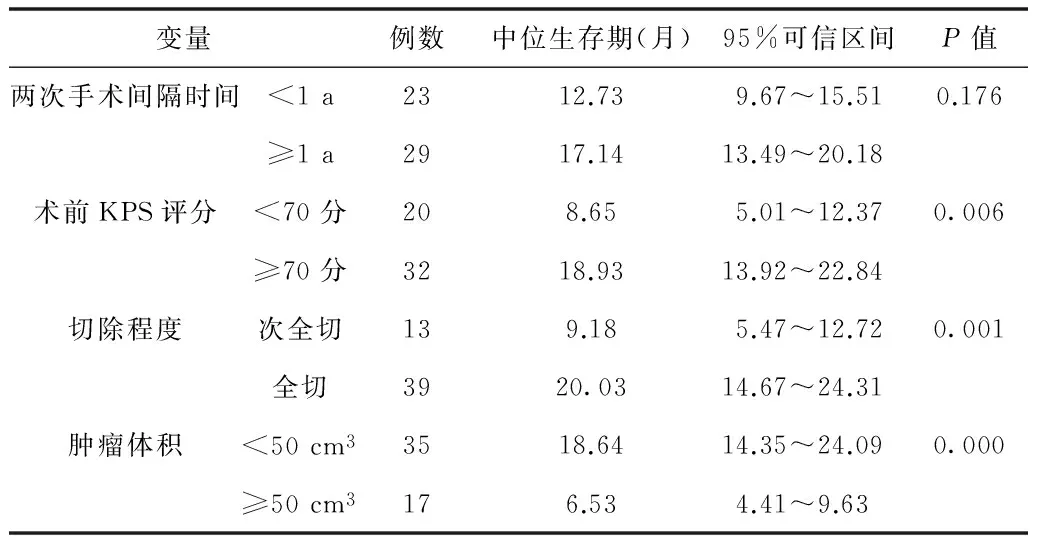
表1 腦惡性膠質瘤術后放化療復發腫瘤預后因素單因素分析
2.2 多因素Cox風險比例模型分析 采用Cox風險比例模型對患者的獨立預后因素(包括KPS評分、腫瘤體積以及切除程度)等進行綜合分析,發現KPS評分<70分、腫瘤體積≥50 cm3,是腫瘤復發再手術的高危預后因素(P<0.05),見表2。
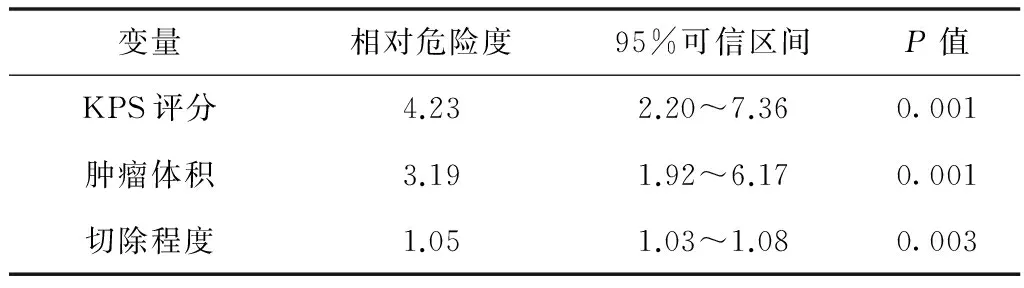
表2 腦惡性膠質瘤術后放化療復發腫瘤預后因素多因素Cox回歸分析
3 討論
腦惡性膠質瘤是發病率和病死率最高的顱內惡性腫瘤,隨著醫療技術水平的提高,雖然患者的生存時間有所延長,但仍無法有效遏制腫瘤的復發。在WHO的腦膠質瘤分類標準中,Ⅲ級(間變星形細胞瘤)到Ⅳ級(多形性膠質母細胞瘤)型腫瘤起病驟然、發展迅速,多位于大腦半球,腫瘤中心可見多處壞死及出血,頭顱CT及MRI均明顯強化,腫瘤周圍腦組織大范圍水腫[4-5]。由于其浸潤性生長及腫瘤組織與正常腦組織無明顯界限,故只有在早期腫瘤較小又位于適當部位者,可爭取全部切除[6]。
腦惡性膠質瘤大都生長在腦神經組織內,細胞分化不良、生長迅速、病程短、為浸潤性生長,與正常腦組織無明顯界限,多數不限于一個腦葉,呈指狀向腦組織外深入破壞腦組織[7]。其治療效果與腫瘤的體積及位置關系密切。若腫瘤體積大且與重要神經組織關系密切,只能實施次全切手術,無法將腫瘤組織徹底切除,術后容易復發而威脅患者的生命安全。
在腫瘤復發機理的研究中,腫瘤干細胞假說是可信度最高的一種。腦膠質瘤的組織中含有膠質瘤干細胞,對于術后輔助放療化療具有一定的抵抗性,最終導致腫瘤復發[8]。
本組結果顯示,原發性腦惡性膠質瘤患者實施切除術后,輔以放療、化療治療,短時間內復查頭顱CT及MRI檢查,無腫瘤復發跡象。但部分患者3個月即發生復發,表明惡性膠質瘤對放化療的敏感度極差。我們在對52例手術及放化療后腫瘤復發再手術的腦惡性膠質瘤患者治療期間,記錄每次頭顱CT以及MRI的檢查結果,以及兩次手術時間間隔、術前KPS評分、切除程度以及腫瘤體積等多項預后因素,采用Kaplan-Meier生存曲線對預后因素進行單因素分析。發現術前KPS評分≥70分、行腫瘤全切術以及腫瘤體積<50 cm3,能夠延長患者的術后生存時間。采用Cox風險比例模型對預后因素進行多因素分析,發現KPS評分<70分、腫瘤體積≥50 cm3,是腫瘤復發再手術的高危預后因素。由此可見,術前KPS評分能夠對患者的臨床治療效果進行有效的評估,而腫瘤的體積、切除程度都會影響到患者的生存時間。
[1] 步星耀,郭曉鶴,丁玉超,等.腦惡性膠質瘤術后放化療腫瘤復發再手術治療的臨床研究[J].中華臨床醫師雜志(電子版),2012,5(12):1 135-1 139.
[2] 鐘鳴谷,牟永告,張湘衡,等.復發腦膠質瘤再手術療效的影響因素分析[J].中國神經精神疾病雜志,2012,42(19):36-39.
[3] 邱俊,易勇.腦惡性膠質瘤術后放化療腫瘤復發再手術治療的臨床研究[J].環球中醫藥,2015,8(13):55.
[4] 周志龍,步星耀,閆兆月,等.腦惡性膠質瘤術后會師化療同步適形放療的臨床觀察[J].腫瘤防治研究,2014,41(15):374-378.
[5] 李萬湖,胡旭東,徐亮,等.膠質瘤治療后假性進展的MR波譜分析[J].中國輻射衛生,2014,23(6):112-114.
[6] 丁玉超,步星耀,張懷亮,等.顯微手術聯合敏感藥物間質化療治療復發性腦惡性膠質瘤[J].醫藥論壇雜志,2011,32(11):10-12.
[7] 王媛,張成輝.分析影響Ⅲ、Ⅳ級腦膠質瘤術后放化療的因素及處理方法[J].中國醫學工程,2015,23(7):35.
[8] 魏方,錢立庭,蔡樹華,等.血清TGF-β、GFAP在腦惡性膠質瘤中的表達及與預后的關系[J].廣東醫學,2015,36(18):3 184-3 186.
(收稿 2016-09-22)
R739.41
B
1077-8991(2017)02-0016-02

