核苷(酸)類似物治療慢性乙型肝炎患者HBV逆轉錄酶區變異的研究
李健,曾文興,方穎慧,曾小平
(1、南昌大學基礎醫學院免疫學教研室,江西南昌330006;2、宜春市人民醫院檢驗科,江西宜春336000)
核苷(酸)類似物治療慢性乙型肝炎患者HBV逆轉錄酶區變異的研究
李健1、2,曾文興2,方穎慧2,曾小平1
(1、南昌大學基礎醫學院免疫學教研室,江西南昌330006;2、宜春市人民醫院檢驗科,江西宜春336000)
目的分析核苷(酸)類似物治療的慢性乙型肝炎患者HBV逆轉錄酶區耐藥相關變異位點、變異位點組合模式、HBV DNA水平和HBeAg等特征,為臨床應用核苷(酸)類似物抗乙肝病毒治療提供參考。方法納入研究的141例慢性乙型肝炎患者,使用NAs治療的107例為治療組,未使用藥物抗病毒治療的34例為對照組。采用線性探針反向雜交法(PCRRLP)檢測HBV逆轉錄酶區耐藥相關變異位點,實時熒光定量PCR法檢測乙型肝炎病毒DNA水平,酶聯免疫吸附試驗檢測乙肝免疫標記物,并對耐藥相關變異的特點和研究病例的臨床資料進行統計學分析。結果核苷(酸)類似物治療效果不佳組耐藥相關變異檢出率(82.5%)明顯高于未治療的對照組(5.9%)和抗病毒治療有效組(有效組10例未檢出耐藥相關變異)(P<0.01)。97例核苷(酸)類似物抗病毒效果不佳的病例中80例檢出140個耐藥相關變異位點,包括rtM204I 45個、rtM204V 32個、rtA181V 28個、rtL180M 25個、rtN236T 10個;變異位點組合模式主要有:rtL180M+rtM204I、rtM204V、rtM204I+rtM204V、rtA181V+rtM204V、rtM204I、rtA181V+rtN236T等;51個對NAs應答不佳病例耐藥變異檢出率70.59%,46個病毒學突破病例耐藥變異檢出率95.65%,差異明顯(P<0.01)。NAs單藥治療病例早于多藥治療病例檢出耐藥相關位點(P<0.01);NAs治療時間越長,耐藥變異檢出率越高(P<0.01);病例HBV-DNA水平等級越高,耐藥變異檢出率也越高(P<0.01)。結論⑴NAs治療慢性乙型肝炎可導致HBV逆轉錄酶區變異,NAs抗乙型肝炎病毒效果不佳與HBV逆轉錄酶區變異密切相關;⑵不同NAs藥物導致慢性乙肝患者HBV逆轉錄酶區變異位點、變異模式特點不同;⑶NAs治療慢性乙型肝炎的用藥種類與方式、治療時長,患者HBV-DNA水平等對HBV逆轉錄酶區發生耐藥變異均可能產生重要影響。提示在NAs治療前、治療過程合適時間點檢測NAs耐藥相關變異位點和HBV DNA水平,可為臨床慢性乙型肝炎的抗病毒治療提供重要參考。
核苷(酸)類似物;慢性乙型肝炎;耐藥;HBV逆轉錄酶區;基因變異
乙型肝炎病毒(Hepatitis B virus,HBV)是引起慢性乙型肝炎(Chronic hepatitis B,CHB)的病原體,在全球流行。世界衛生組織報道,全球約20億人曾感染HBV,其中2.4億人為慢性HBV感染者[1];全球有30%的肝硬化、45%的肝癌由乙肝病毒感染而引起;HBV感染導致的肝功能衰竭、肝硬化和肝細胞癌患者中每年有約65萬人死亡[2-4]。在我國60%肝硬化和80%HCC患者由HBV感染引起[4,5]。我國10年前乙型肝炎血清流行病學調查表明,我國一般人群HBsAg攜帶率為7.18%[6-8],推算我國現有約有9300萬慢性HBV感染者,約有2000萬例CHB患者[9,10]。乙型肝炎病毒感染和治療是我國也是全球嚴重的公共衛生問題之一,長期危害人民健康、阻礙經濟發展、影響社會和諧。因此,加強乙型病毒性肝炎檢測、預防、診斷、治療和預后的相關研究,具有重要意義。
目前除干擾素外,應用于乙型肝炎抗病毒治療的主要藥物是核苷(酸)類似物(nucleoside analogues,NAs)。我國批準的核苷(酸)類似物包括拉米夫定(Lamivudine,LAM)、阿德福韋酯(Adefovir dipivoxil,ADV)、恩替卡韋(Entecavir,ETV)、替比夫定(Telbivudine,LdT)等[11]。LAM和LdT為L-核苷類藥物;ETV為脫氧鳥苷類藥物;ADV為五環磷酸鹽類藥物。NAs進入人體內可形成磷酸鹽活性成分,作為HBV DNA聚合酶的競爭性抑制劑與人體內天然的脫氧三磷酸核苷(dNTP)競爭結合到HBV DNA聚合酶上,使HBV的DNA鏈合成終止,這是NAs抑制HBV復制的機制[12,13]。NAs口服給藥、價格較低、抗病毒效果較好因而目前廣泛應用于抗乙肝病毒。用藥依從性好的HBeAg陽性CHB患者,LAM治療一年內HBV DNA的轉陰率可達30%~40%[14,15];ADV治療一年內HBV DNA的轉陰率可達10%~25%[16];ETV治療一年內HBV DNA的轉陰率可達67%[14];LdT治療一年內HBV DNA的轉陰率可達60%[16];對HBeAg陰性CHB患者,單用NAs治療一年內HBV DNA的轉陰率更好,可達50%~90%[17-19]。
HBV是變異率較高的病毒之一,發生在HBV逆轉錄酶區的基因變異,如果與HBV聚合酶有關就可導致HBV聚合酶與NAs結合力降低,使得NAs對變異的HBV抑制能力下降,野生株病毒因對藥物敏感而被抑制,變異株對核苷(酸)類似物不敏感繼續復制增殖甚至代替野生株從而導致NAs抗病毒效果不佳甚至導致耐藥的產生[20]。
NAs不能完全清除體內病毒,目前用藥患者數巨大且患者長期服用NAs,對NAs耐藥問題在臨床上越發嚴重,往往導致患者病情反復甚至加重[21]。本文中將病毒學突破和病毒學復發的病例統歸為病毒學突破組;應答不佳和原發性無應答病例統歸為應答不佳組;病毒學突破、病毒學復發、應答不佳和原發性無應答的病例統歸為抗病毒效果不佳組;有病毒學應答病例歸為抗病毒有效組;NA+NA為NAs聯合或序貫用藥[22]。
1 材料與方法
1.1 研究對象
1.1.1 納入標準慢性乙型肝炎(chronic hepatitis B,CHB)患者診斷符合《慢性乙型肝炎防治指南(2015年版)》,即患者血清HBsAg陽性,HBeAg陽性或陰性,HBV DNA陽性;ALT持續或反復升高,或肝組織學檢查有肝炎病變。未合并其它病毒性肝炎。使用核苷(酸)類似物治療的病例(NAs治療組)抗病毒治療時間大于6個月;對照組慢性乙型肝炎患者未使用任何抗病毒藥物進行治療。
1.1.2 研究對象一般資料據納入標準共選取2014年至2016年宜春市人民醫院門診或住院CHB患者共141例,病例平均年齡39.43±12.66,最大76歲,最小14歲。
NAs治療CHB患者(以下稱治療組)107例,其中男87例、女20例,均使用一種或多種NAs進行抗病毒治療,且未使用過其它抗病毒藥物。其中,NAs治療CHB患者效果不佳者97例(即出現病毒學無應答、應答不佳、病毒學反彈、病毒學突破的四種情況之一):單NAs治療的共61例(單用過LAM治療的31例,單用過ADV治療的20例,單用過EDV治療的15例,單用過LdT治療的5例);曾經用過多種NAs治療的36例(用過LAM、ADV、ETV治療的11例;用過LAM、ADV治療的患者14例;用過LAM、ETV治療的10例;用過ADV、ETV治療的1例)。NAs治療慢性乙型肝炎患者有效者10例。
對照組慢性乙型肝炎患者34例,其中男28例、女6例;均未使用任何抗病毒藥物進行治療。
1.2 方法
1.2.1 HBV-DNA定量檢測HBV-DNA熒光定量PCR檢測試劑盒購自中山大學達安基因股份有限公司,用一對乙型肝炎病毒特異性引物和一條乙型肝炎病毒特異性熒光探針,配以PCR反應液、耐熱DNA聚合酶(Taq酶)、核苷酸單體(dNTPs)等成分,用PCR體外擴增法定量檢測乙型肝炎病毒DNA。本試劑盒的檢出限度為1.0×102IU/ml,線性范圍為1.0×102~1.0×108IU/ml。
1.2.2 HBV逆轉錄酶區耐藥相關變異位點測定乙型肝炎病毒核酸檢測試劑盒購自亞能基因股份有限公司,使用BIO-RAD基因擴增儀對提取的HBV-DNA進行PCR擴增,PCR擴增產物在FYY3醫用核酸分子快速雜交儀上與設計的探針進行特異性雜交,雜交后洗膜、顯色,根據膜條特定位置顯色(藍色)與否來判斷HBV逆轉錄酶區相關耐藥變異位點。
1.2.3 乙肝血清免疫標記物購自中山生物工程有限公司乙肝五項ELISA檢測試劑盒,檢測乙肝五項(HBsAg、抗-HBs、HBeAg、抗-HBe、抗-HBc)。乙型肝炎病毒表面抗原(HBsAg)、乙型肝炎病毒e抗原(HBeAg)是采用ELISA雙抗體夾心法檢測;乙型肝炎病毒表面抗體(抗-HBs)是采用ELISA雙抗原夾心一步法檢測;乙型肝炎病毒e抗體(抗-HBe)和乙型肝炎病毒核心抗體(抗-HBc)是采用ELISA競爭抑制法原理檢測。使用Anthos2010酶標儀測定樣本和陰性、陽性和空白對照的吸光度值并判斷結果。
1.3 統計學方法應用SPSS 19.0統計軟件進行統計。兩樣本均數的比較采用t檢驗。兩樣本率的比較采用χ2檢驗,根據情況選擇Pearson卡方檢驗、Yates卡方檢驗;兩個樣本率的比較選擇四格表,兩個樣本構成比的比較選擇2×C表。P<0.05為差異有統計學意義。
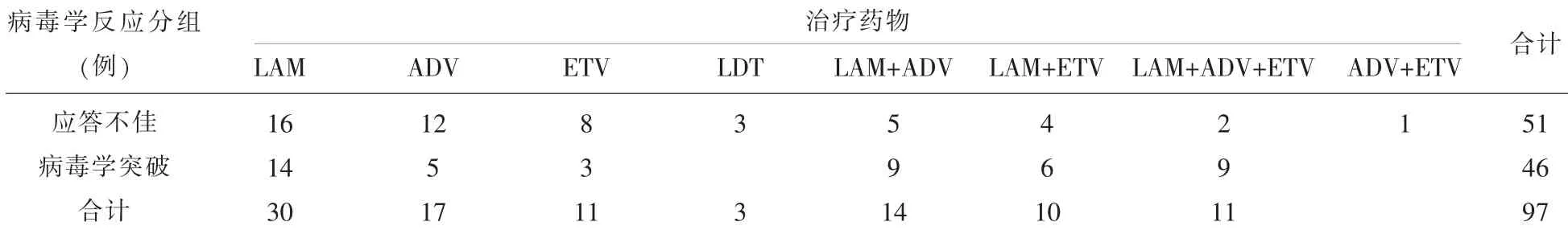
表1 97例不同NAs治療CHB療效不佳患者的病毒學反應
2 結果
2.1 資料情況對照組與NAs治療組在性別、年齡比較均無顯著性差異(P=0.877,P=0.093),具有可比性。
2.2 不同NAs治療CHB效果不佳患者的病毒學反應分布情況NAs治療CHB效果不佳的97個病例,其中51例出現對NAs應答不佳,46例出現病毒學突破,見表1。
2.3 不同NAs治療CHB效果不佳者病毒學突破的比較
2.3.1 單LAM與單ADV治療病例效果不佳者病毒學突破比較單LAM治療發生病毒學突破在療效不佳患者中占比46.67%,與單ADV治療發生病毒學突破(在療效不佳患者中占比29.41%)比較,無統計學差別(χ2=1.34,P>0.05),見表2。
2.3.2 單LAM與含LAM多藥治療病例效果不佳者病毒學突破比較單LAM治療發生病毒學突破占療效不佳患者46.67%,與LAM聯合或序貫應用其它藥物治療組(占比68.57%)比較,差異無統計學意義(χ2=3.19,P>0.05),見表2。
2.3.3 單LAM與單ETV治療病例應答不佳者病毒學突破比較單LAM治療發生病毒學突破在療效不佳患者中占比46.67%,與單ETV治療發生病毒學突破(在療效不佳患者中占比27.27%)比較,統計學無差別(χ2=1.28,P>0.05),見表2。
2.3.4 單NAs與多NAs治療病例應答不佳者病毒學突破比較單NAs治療發生病毒學突破在療效不佳患者中占比36.07%,與多NAs聯合或序貫應用其它藥物治療發生病毒學突破(在療效不佳患者中占比66.67%),差異有統計學意義(χ2=12.41,P<0.01),見表2。
2.4 HBV逆轉錄酶區耐藥相關變異檢測結果
2.4.1 對照組與NA治療效果不佳組HBV逆轉錄酶區耐藥變異檢出情況對照組(未治療組)34個病例中檢出HBV逆轉錄酶區耐藥相關變異2例,檢出率5.9%。NAs治療效果不佳組97例中檢出HBV逆轉錄酶區耐藥相關變異80例,檢出率82.5%。NAs治療效果不佳組HBV逆轉錄酶區耐藥相關變異檢出率明顯高于未治療組(χ2=63.078,P<0.01),即明顯高于自然變異,見表3。
2.4.2 NAs抗病毒治療有效組與效果不佳組HBV逆轉錄酶區耐藥變異檢出率比較治療組中有10個病例使用NAs抗病毒治療有效,未檢出HBV逆轉錄酶區耐藥相關變異;97例使用NAs抗病毒治療效果不佳,80例檢出HBV逆轉錄酶區耐藥相關變異,檢出率82.5%。抗病毒效果不佳組變異檢出率明顯高于抗病毒有效組(χ2=32.68,P<0.01),見表3。
2.4.3 NA治療效果不佳患者應答不佳組與病毒學突破組病例HBV逆轉錄酶區耐藥變異檢出情況治療組97個病例中檢出HBV逆轉錄酶區耐藥相關變異80例,其中對NAs應答不佳的51個病例中36例檢出耐藥變異,病毒學突破46個病例中44例檢出耐藥變異。兩組耐藥變異檢出率差異顯著(χ2=10.51,P<0.01),見表3。
2.5 耐藥相關變異位點與分布對照組兩病例檢出變異位點兩個:rtM204V和rtN236T。治療組80個病例檢出變異位點140個:rtL180M25個、rtM204V32個、rtM204I45個、rtA181V28個、rtN236T10個。變異位點詳細分布見圖1。

圖1 耐藥相關變異位點在不同NAs治療下的分布

表2 不同NAs治療CHB效果不佳者病毒學突破的比較

表3 不同分組耐藥相關變異的比較
2.5.1 變異位點rtM204V rtM204V在單LAM治療組占總變異位點數的40.0%,與rtM204V在其它單NAs治療組占總變異位點數的11.1%比較有統計學意義(χ2=7.826,P=0.005);與rtM204V在含LAM其聯合或序貫用藥組變異位點數的20.9%比較有統計學意義(χ2=4.213,P=0.04),見表4。
2.5.2 變異位點rtM204I rtM204I占單LAM治療組變異位點數的37.1%。與rtM204I在其它單NAs治療組占總變異位點數的19.4%比較差異沒有統計學意義(χ2=2.747,P=0.097;與rtM204I在含LAM聯合或序貫用藥組變異位點數的37.31%比較沒有統計學意義(χ2=0.0003,P=0.987),見表5。
2.5.3 變異位點rtA181V rtA181V占單ADV治療組變異位點數的57.9%。與rtA181V在其它單NAs治療組占總變異位點數的4.0%比較有統計學意義(χ2=23.68,P=0.000);與rtA181在含ADV其聯合或序貫用藥組變異位點數的27.27%比較差異有統計學意義(χ2=5.509,P=0.025),見表6。
2.5.4 變異位點rtN236T rtN236T占單ADV治療組變異位點數的31.58%,與rtA181V在其它單NAs治療組變異位點數為0比較有統計學意義(χ2=14.087,P=0.002);與rtN236T在含ADV其聯合或序貫用藥組變異位點數的7.8%比較差異有統計學意義(χ2=5.210,P=0.023),見表7。
2.5.5 NAs單藥與多藥治療CHB患者變異位點構成比較單NAs治療組比較多NAs聯合或序貫治療組各變異位點構成比比較(χ2=2.49,P=6.646),差異無統計學意義,單藥治療和多藥治療各變異位點構成比總體沒有差別,見表8。

表4 不同NAs治療CHB療效不佳患者HBV逆轉錄酶區rtM204V變異情況的比較

表5 不同NAs治療CHB療效不佳患者HBV逆轉錄酶區rtM204I變異情況的比較

表6 不同NAs治療CHB療效不佳患者HBV逆轉錄酶區rtA181V變異情況

表7 不同NAs治療CHB療效不佳患者HBV逆轉錄酶區rtN236T變異情況

表8 單藥與多藥治療變異位點構成比較
2.6 主要耐藥相關變異模式與分布檢出11種變異位點組合模式,按檢出頻次由多到少排列分別為:16例rtL180M+rtM204I、12例rtM204V、9例rtM204I+rtM204V、8例rtA181V+rtM204V、7例rtM204I、7例rtA181V+rtN236T、6例rtA181V+ rtM204I、5例rtL180M、4例rtL180M+rtM204I+ rtA181V。3例rtM204V+rtM204I+rtN236T、3例rtA181V。變異模式詳見圖2。
2.7 NAs治療CHB患者HBV逆轉錄酶區耐藥變異相關因素分析
2.7.1 耐藥變異與用藥時長的關聯性單NAs治療檢出耐藥相關變異病例(單藥治療耐藥變異+組)的用藥時間長于未檢出NAs耐藥相關變異病例(單藥治療耐藥變異-組)(P<0.01),提示,用藥時間越長,耐藥相關變異發生率越高;多藥治療檢出耐藥變異病例(多藥治療耐藥變異+組)的用藥時間長于單藥治療檢出耐藥變異病例(單藥治療耐藥變異+組)(P<0.01),提示單藥治療比多藥聯合更易發生耐藥變異。見表9。

圖2 主要的主要耐藥相關變異模式的分布
2.7.2 耐藥變異與用藥方式的關聯性本研究NAs治療CHB療效不佳患者中,單藥治療的病例耐藥變異檢出率為59.15%,而多藥治療病例耐藥變異檢出率為97.2%,兩種用藥方式療效不佳的患者耐藥變異病例檢出率差異顯著(χ2=17.157,P<0.01),見表10。
2.7.3 耐藥變異與患者攜帶HBeAg的關聯性HBeAg陰性組病例與HBeAg陽性組病例耐藥變異檢出率差異無統計學意義(χ2=3.233,P>0.05),見表10。
2.7.4 耐藥變異與NAs治療后病毒學反應NAs治療CHB療效不佳患者中,應答不佳組耐藥變異檢出率(70.59%)明顯低于病毒學突破組(95.65%)(χ2=8.85,P<0.01),見表10。
2.7.5 耐藥變異與HBV DNA水平的關聯性NAs治療組在檢測耐藥變異位點的同時,有81個病例檢測了HBV-DNA水平,將HBV DNA劃分為三個等級,分別統計每個等級區間耐藥變異的檢出例數并進行構成比的比較(χ2=9.455,P<0.01),差異具有統計學意義,即HBV DNA水平越高,耐藥變異檢出率越高,見表10。

表9 耐藥變異與用藥時長的關聯性
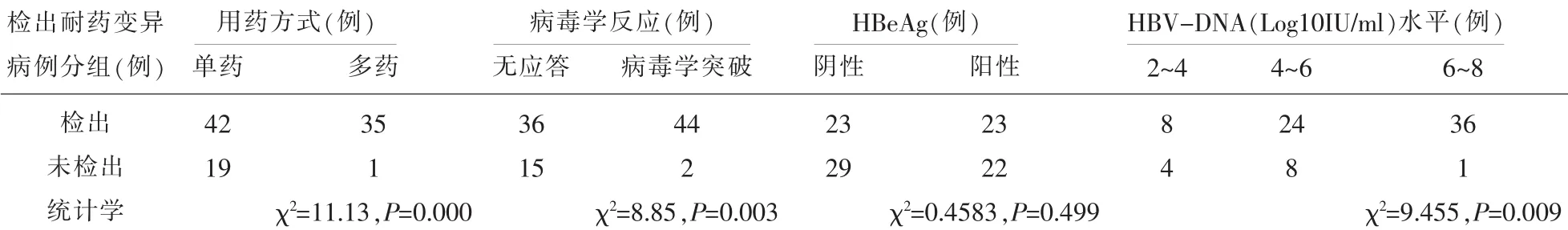
表10 各種因素下檢出耐藥變異的比較
3 討論
3.1 乙肝病毒逆轉錄酶區的自然變異與耐藥HBV是最容易變異性的病毒之一,基因變異如果發生在逆轉錄酶區且影響編碼HBV DNA聚合酶就可以導致對核苷(酸)類似物的耐藥[23]。本研究對照組未使用NAs治療的34例中,有2例檢出了耐藥相關變異,檢出率5.9%,2個變異位點為rtM204V和rtN236T;rtM204V是LAM耐藥相關變異位點,rtN236T是ADV耐藥相關位變異位點。這說明乙肝病毒自然變異可導致較高的NAs耐藥,在使用NAs藥物之前檢測NAs藥物相關變異位點可以指導臨床選擇NAs用藥[24]。有專家提出需要實現有效的耐藥管理,把耐藥監測點置于用藥之前也就是監測自然耐藥變異。
3.2 乙肝病毒逆轉錄酶區主要變異位點和變異模式的分布LAM治療病例主要的變異位點是rtM204I、rtM204V,也檢出了rtL180M和rtA181V;rtM204V占LAM治療病例的變異位點總數的40%,高于其他用藥方式病例的檢出率;rtM204I占LAM治療病變異位點總數的37.1%,但與其他用藥方式的檢出率沒有統計學差別,這兩個位點都是最重要的LAM耐藥相關的變異位點[25,26],本研究分析單LAM治療組與其它單NAs治療組、LAM+其它單NAs治療組比較rtM204I的檢出率沒有差別,說明rtM204I可能是出現頻率較高的交叉耐藥位點;而單LAM治療組rtM204V的檢出率高于其它單NAs治療組和LAM+其它單NAs治療組下,說明rtM204V主要是LAM的耐藥相關變異位點[27]。
ADV治療病例主要的變異位點是rtA181V、rtN236T,兩位點分別占單ADV治療組變異位點數的57.9%、31.58%,本研究分析單ADV治療組rtA181V、rtN236T的檢出率顯著高于其它單NAs治療組和ADV+其它單NAs治療組,說明rtA181V、rtN236T是ADV主要耐藥相關位點[25,27],檢出ADV耐藥變異模式主要為rtA181V+rtN236T[26]。ETV治療病例檢出rtM204I、rtL180M,有報道表明要對ETV耐藥,需要rtM204I+rtL180M位點變異,還需要合并rtT184G/S/A等位點同時變異[25],本研究中未檢測rtT184G/S/A變異的位點,推測rtM204I、rtL180M應該是LAM與ETV耐藥相關變異的交叉位點[28,29]。針對多NAs耐藥變異的組合模式更為復雜,本研究中簡單總結了耐藥模式,多藥治療效果不佳組的主要變異模式rtL180M+ rtM204I、rtA181V+rtM204V、rtA181V+rtM204I,這與相關報道對LAM和ADV耐藥檢出rtL180M+ rtA181V+rtM204V變異模式有一致性[30]。
本研究中單藥治療病例與多藥治療病例在耐藥變異位點的構成上沒有統計學差別,可能與多藥治療組所用藥物一般包含單藥組用藥有關;多藥治療如果是序貫治療那么可能導致的耐藥變異將包含所有用過藥物的耐藥相關變異位點[31],聯合用藥可以提高基因屏障[28],減少耐藥變異的產生。另外本研究的樣本量不夠大、檢測的變異位點有限,對單藥治療和多藥治療患者耐藥相關變異位點的構成比也有一定的影響。
3.3 耐藥變異的相關因素應用NAs藥治療慢性乙型肝炎時,藥物的選擇(如選用單藥的種類、幾種NAs藥物聯合或序貫用藥的選擇),用藥劑量與方法,治療時間長短,患者本身的HBV DNA水平和攜帶乙肝標記物情況等對乙肝病毒逆轉錄酶區發生耐藥變異均可能產生重要影響。
本研究觀察單NAs治療檢出變異組用藥時間明顯長于未檢出變異組,說明運用NAs藥物治療CHB會對病毒產生選擇性壓力,治療時間越長出現耐藥變異的變異株被篩選出來的幾率就越大[32,33];而單藥治療病例早于多藥治療病例檢出耐藥相關位點可推測單藥治療可能比多藥治療更容易導致耐藥變異的產生,而多藥聯合可以提高基因屏障[28]。但本研究中多藥物治療耐藥變異的檢出率卻明顯高于單藥治療,看起來與基因屏障理論相矛盾,可能是因本研究中多藥治療中采用聯合用藥的病例少而采用序貫用藥的病例多,序貫用藥是在對前者藥物產生耐藥變異而失去抗病毒藥效再改變藥物種類,后種藥物又可引起新的變異,前后變異疊加因而使得變異檢出率反而更高。比較HBeAg陰性和陽性組耐藥變異檢出情況,兩者沒有統計學意義。而在HBV-DNA水平分等級比較耐藥變異檢出情況時發現,研究病例HBV-DNA水平等級越高,耐藥變異檢出率也越高。這與國內多位學者的研究結果一致[34,35],說明在使用NAs治療CHB時,如果不能有效抑制病毒復制,病毒復制仍然處于較高的水平,NAs治療反而有利于耐藥變異的產生。
3.4 NAs治療CHB效果NAs抗乙肝病毒治療口服給藥方法簡單且價格經濟,目前在臨床廣泛應用[36],但隨之而來的就是對NAs耐藥率的提高[37,38]。NAs抗病毒用藥時間的延長,使得耐藥變異增加最終導致耐藥的發生[39,40]。用藥方法是影響NAs治療效果重要因素,單用LAM治療后,往往有著很高的耐藥突變率[41],且常出現與LAM耐藥相關的突變位點rtM204I、rtM204V,rtL180M和rtA181V,如出rtL180M+rtM204I、rtA181V也可導致對ADV耐藥[42],rtL180M也是LAM和ETV的交叉耐藥位點。所以開始抗病毒治療時就要選擇合適的藥物,新版防治指南建議初次使用ETV或者替諾福韋酯[22],另一方面聯合用藥可以提高基因屏障從而降低耐藥變異的產生。再者在使用NAs抗乙肝病毒治療時,迅速有效降低HBV-DNA水平很重要,如果短時間內藥物能有效抑制病毒復制,那么依賴較高基因復制水平的變異就難以產生。本研究發現病毒學應答不佳和病毒學突破病例耐藥變異檢出率非常高,說明在治療過程中,必須監測重要的耐藥相關變異位點和HBV DNA水平等相關指標,一旦患者檢出耐藥相關變異位點且病毒學應答不佳或病毒學突破,則需要更換NAs進行挽救性治療,如不及時進行挽救性治療,可產生嚴重的后果包括肝功能失代償、急性肝功能衰竭甚至死亡[43]。
4 結論
4.1 NAs治療慢性乙型肝炎可導致HBV逆轉錄酶區變異,NAs抗乙型肝炎病毒效果不佳與HBV逆轉錄酶區變異密切相關,即HBV耐藥變異是NAs抗病毒治療效果不佳甚至失敗的主要原因。
4.2 不同NAs藥物導致慢性乙肝患者HBV逆轉錄酶區變異位點、變異模式特點不同:⑴LAM常見耐藥相關變異位點為rtM204I、rtM204V、rtL180M,變異模式多為rtM204V、rtM204I+rtM204V、rtM204I+rtL180M。⑵ADV常見耐藥相關變異位點為rtA181V、rtN236T,變異模式多為rtA181V+ rtN236T。
4.3 NAs治療CHB用藥種類與方式,治療時長,患者HBV-DNA水平等對HBV逆轉錄酶區發生耐藥變異均可能產生重要影響。一般單藥治療出現耐藥變異早于多藥治療;治療時間越長出現耐藥變異的變異株被篩選出來的幾率越大;患者HBVDNA水平等級越高,耐藥變異檢出率越高。
4.4 本研究的臨床建議在使用NAs抗乙肝病毒治療前,應檢測常見的耐藥相關變異位點,從而選擇正確的藥物,盡量減少耐藥變異的產生,保護敏感的變異位點。在治療中,選擇合適的時間點監測重要的變異位點和HBV-DNA水平,特別是開始治療后的早期評價病毒學反應,看藥物的治療效果,如果出現耐藥變異或者早期治療病毒學應答不佳應及時調整挽救性用藥方案,避免病情的反復和惡化。長期使用NAs應該堅持監測變異位點和HBV-DNA水平[33]。總之耐藥變異位點的檢測和用藥期間的監測,可以指導臨床選擇和調整NAs藥物[34,35],具有非常重要的臨床價值。
[1]Ott JJ,Stevens GA,Groeger J,et al.Global epidemiology of hepatitis B virus infection:new estimates of age-speci?c HBsAg seroprevalence and endemicity[J].Vaccine,2012,30(12):2212-2219.
[2]Lozano R,Naghavi M,Foreman K,et al.Global and regional mortality from 235 causes of death for 20 age groups in 1990 and 2010:a systematic analysis for the Global Burden of Disease Study 2010 [J].Lancet,2012,380(9859):2095-2128.
[3]Hou J,Liu Z,Gu F.Epidemioiogy and Prevention of HepatitisB Virus Infection[J].Int J Med Sci,2005,2(1):50-57.
[4]Goldstein ST,Zhou F,Hadler SC,et al.A mathematical model to estimate global hepatitis B disease burden and vaccination impact [J].Int J Epidemiol,2005,34(6):1329-1339.
[5]Wang FS,Fan JG,Zhang Z,et al.The global burden of liver disease:The major impact of China[J].Hepatology,2014,60(6):2099-2108.
[6]Hang X,Bi S,Yang W,et al.Epidemiological serosurvey of Hepatitis B in China-declining HBV prevalence due to Hepatitis B vaccination[J].Vaccine,2009,27(47):6550-6557.
[7]Fung J,Seto W-K,Lai C-L,et al.Profiles of HBV DNA in a large population of Chinese patients with chronic hepatitis B:Implications for antiviral therapy[J].J Hepatol,2011,54(2):195-200.
[8]Liang X,Bi S,Yang W,et al.Epidemiological serosurvey of hepatitis B in China-declining HBV prevalence due to hepatitis B vaccination[J].Vaccine,2009,27(47):6550-6557.
[9]Liang X,Bi S,Yang W,et al.Evaluation of the impact of hepatitis B vaccination among children born during 1992-2005 in China[J]. J Infect Dis,2009,200(1):39-47.
[10]Lu FM,Zhang H.Management of hepatitis B in China[J].Chin Med J(Ensl),2009,122(1):3-4.
[11]乙型肝炎病毒耐藥專家委員會.乙型肝炎病毒耐藥專家共識:2009年更新[J].中華實驗和臨床感染病雜志(電子版),2009,3(1):69-79.
[12]杜冠華.病毒與抗病毒藥物[J].食品與藥品,2006,2006(3B):32-32.
[13]Fung J,Lai CL,Seto WK,et al.Nucleoside/nucleotide analogues in the treatment of chronic hepatitis B[J].J Antimicrobial Chemotherapy,2011,66(12):2715-2725.
[14]Chang TT,Gish RG,de Man R,et al.A comparison of entecavir and lamivudine for HBeAg-positive chronic hepatitis B[J].N Eng J Med,2006,354(10):1001-1010.
[15]Lai CL,Shouval D,Lok As,et al.Entecavir versus lamivudine for patients with HBeAg-negative chronic hepatitis B[J].N Engl J Med,2006,354(10):10l1-1020.
[16]Marcellin P,Chang TT,Lim SG,et al.Adefovir dipivoxil for the Treatment of hepatitis B e antigen-positive chronic hepatitis B[J].N Engl J Med,2003,348(9):808-816.
[17]Lai CL,Gane E,Liaw Y,et al.Telbivudine versus lamivudine in patients with chronic hepatitis B[J].N Engl J Med,2007,357(25):2576-2588.
[18]Marcellin P,Heathcote EJ,Buti M,et al.Tenofovir disoproxil fumarate versus adefovir dipivoxil for chronic hepatitis B[J].N Engl J Med,2008,359(23):2442-2455.
[19]Lau GK,Piratvisuth T,Luo KX,et al.Peginterferon A1fa-2b,lamivudine,and the combination for HBeAg-positive chronic hepatatis B[J].N Engl J Med,2005,352(26):2682-2695.
[20]Fung J,Seto WK,Lai CL,et al.Extrahepatic effects of nucleoside and nucleotide analogues in chronic hepatitis B treatment[J].J Gastroenterol Hepatol,2014,29(3):428-434.
[21]張玲,吳昊鶴.核苷類似物耐藥后乙型肝炎治療的研究進展[J].臨床醫學,2011,31(1):104-105.
[22]中華醫學會肝病學分會.慢性乙型肝炎防治指南(2015年更新版)[J].中華傳染病雜志,2015,33(11):219-240.
[23]婁紅梅,鐘細濤,李志國,等.乙型肝炎病毒基因自然變異耐藥性的研究[J].中華肝臟病雜志,2011,19(11):868-869.
[24]婁紅梅,劉洪海.乙型肝炎病毒基因自然變異耐藥性與HBV DNA、HBeAg、ALT及AST相關因素分析[J].廣東醫學,2012,33 (9):1279-1281.
[25]古麗娣,張丹,曾惠玲,等.核苷(酸)類似物治療引起乙肝病毒耐藥相關基因位點突變的總結分析[J].現代檢驗醫學雜志,2013,28(1):122-123.
[26]金怡,魏飛力,馬麗娜,等.PCR產物直接測序法檢測乙肝病毒耐藥位點的臨床研究[J].北京醫學,2011,33(12):961-965.
[27]薛彩花,吳瑋,安俊麗,等.987例乙型肝炎患者HBV-DNA P區多位點耐藥突變分析及臨床意義[J].胃腸病學和肝病學雜志,2014,23(10):1187-1190.
[28]王潔,金生.乙型肝炎病毒耐藥變異及其檢測研究進展[J].現代醫藥衛生,2014(24):3711-3713.
[29]曹靈芝,樊正勤,趙耘.慢性乙型肝炎患者基因耐藥變異特征分析[J].中國實用醫藥,2016,11(14):53-55.
[30]鄭金梅.HBV核苷(酸)類似物多藥耐藥的檢測和分析[D].太原:山西醫科大學,2013.
[31]郝建宏,胡憶玲,林愛清.慢性乙型肝炎患者HBV基因耐藥突變分析[J].實用肝臟病雜志,2016,19(4):473-475.
[32]榮海燕,張朝霞.乙型肝炎病毒耐藥突變與HBV-DNA量和HBeAg之間的相關性研究[J].實用醫學雜志,2013,29(3):404-406.
[33]楊璞葉,劉山紅,馮彪.阿德福韋酯聯合拉米夫定治療拉米夫定耐藥患者療效觀察[J].醫學爭鳴,2008,29(2):155-157.
[34]李金明,謝南,熊德琴,等.基因芯片法檢測乙肝病毒多位點變異的臨床應用[J].實驗與檢驗醫學,2009,27(6):615-616.
[35]許瑞元,王爾莉,曹霜,等.乙型肝炎病毒耐藥突變基因檢測在臨床中的應用[J].實驗與檢驗醫學,2014,32(2):179-180.
[36]廖艷霞,楊光.乙型肝炎病毒基因耐藥變異的研究現狀[J].廣東醫學,2011,32(16):2214-2216.
[37]張小曼,肖子鴻,張純瑜,等.核苷(酸)類藥物引起HBV基因突變的危險因素與模式分析[J].中華實驗和臨床感染病雜志(電子版),2015,9(5):92-96.
[38]趙建強,劉加法.山東省濰坊市慢性乙型肝炎患者HBV P區基因耐藥突變檢測及相關因素分析[J].病毒學報,2015(1):14-17.
[39]趙帥.LAM和ETV聯合治療慢性乙肝患者對乙肝病毒耐藥基因多位點變異研究[D].石家莊:河北醫科大學,2015.
[40]Chen CH,Lin CL,Hu TH,et al.Entecavir vs.lamivudine in chronichepatitis B patients with severe acute exacerbation and hepatic decompensation[J].J Hepatol,2014,60(6):1127-1134.
[41]Lampertico P,Vigano M,Manenti E,et al.Low resistance to adefovir combined with lamivudine:a 3-year study of 145 lamivudine-resistant hepatitis B patients[J].Gastroenterology,2007,133:1445-1451.
[42]Yao GB,Zhu M,Cui ZY,et al.A 7-year study of lamivudine therapy for hepatitis B virus e antigen-positive chronic hepatitis B patients in China[J].J Dig Dis,2009,10:131-137.
[43]Sun J,Hou JL,Xie Q,et al.Randomised clinical trial:efficacy of Peginterferon alfa-2a in HBeAg positive chronic hepatitis Bpatients with lamivudine resistance[J].Aliment Pharmacol Ther,2011,34(4):424-431.
Study on the Variation of HBV Reverse Transcriptase Gene Region in Patients with Chronic Hepatitis B Treated with Nucleoside Analogues
LI Jian1,2,ZENG Wenxing2,FANG Yinghui2,ZENG Xiaoping1.1.Department of Immunology,Basic Medical College of Nanchang University,Nanchang 330006,China;2.Clinical laboratory,The People's Hospital of Yichun City,Yichun Jiangxi 336000,China.
Objective To analyze the drug-resistant related mutation loci in HBV reverse transcriptase region,the combination mode of the mutation loci,the levels of HBV DNA and hepatitis Be antigen(HBeAg)in chronic HBV infected patients treated with NAs provides references for the anti-HBV therapy of NAs.Methods One hundred and forty-one patients with chronic HBV infection were selected in the study,of which the 107 cases with NAs treatment were set as the treatment group,and the rest 34 patients receiving no antiviral treatment were set as the control group.Drug-resistant related mutation loci in HBV reverse transcriptase region was determined by the reverse linear probe hybridization PCR(PCR-RLP).The level of HBV DNA was detected by real-time fluorescence quantitative PCR.And immune markers of HBV were examined by Enzyme-linked immunosorbent assay (ELISA).Finally,the characteristics of drug resistance-related mutations and the clinical data of the study cases were analyzed statistically.Results The detection rate of drug-resistant related mutation loci in the poor effective treatment group(82.5%)was significantly higher than that in the untreated control group(5.9%)and the effective group(0%)(P<0.01).There were 97 cases
NAs showing the poor antiviral effect in the treatment group,of which 80 ones possessed 140 drug-resistant mutation loci. The major mutation sites included 45 rtM204I,32 rtM204V,10 rtN236T,25 rtL180M and 28 rtA181V.Main combination modes of the mutation loci were rtL180M+rtM204I,rtM204V,rtM204I+rtM204V,rtA181V+rtM204V,rtM204I and rtA181V+rtN236T,etc. Mutation detection rate in the 51 cases with poor NAs response was 70.59%,with 95.65%in the 46 virological breakthrough cases (P<0.01).Mutation in those who received monotherapy was usually detected much earlier than that in multi-drug treated ones(P<0. 01).The longer treatment time of NAs,the higher rate of drug-resistance mutation sites were detected(P<0.01).The higher level ofHBV-DNA,the higher the detection rate of drug-resistance was detected(P<0.01).Conclusions 1.NAs treatment of chronic hepatitis B can lead to mutations in HBV reverse transcriptase region,and NAs anti-hepatitis B virus ineffective is closely related to mutations in HBV reverse transcriptase region.2.Different NAs drugs result in different characteristics of mutation loci and combination modes of the mutation loci in HBV reverse transcriptase region of chronic hepatitis B patients.3.Selection of NAs,treatment time,the level of HBV-DNA in patients may all have an important impact to drug-resistance related mutations in HBV reverse transcriptase region.It is suggested that NAs drug resistance-related mutations and level of HBV-DNA in patients should be detected before treatment or be monitored during treatment,which can provide important references for clinical antiviral therapy of chronic hepatitis B.
∶Nucleoside analogues;Chronic hepatitis B;Drug resistance;Gene mutation in HBV reverse transcriptase region;Gene mutation
R512.6+2,R446.62
A
1674-1129(2017)04-0466-09
10.3969/j.issn.1674-1129.2017.04.005
2017-03-16;
2017-05-30)
李健,1983年生,學士學位,主管檢驗師;南昌大學基礎醫學院免疫學教研室同等學歷申請碩士學位研究生;研究方向:乙肝病毒基因耐藥變異。
曾小平,1973年生,南昌大學基礎醫學院免疫學教研室副教授、碩士生導師。

