洗滌紅細胞容量控制問題分析
王姣杰,單泓,段艷麗,張玉紅,李建斌
(河南省紅十字血液中心,河南鄭州50012)
洗滌紅細胞容量控制問題分析
王姣杰,單泓,段艷麗,張玉紅,李建斌
(河南省紅十字血液中心,河南鄭州50012)
目的分析由2U懸浮紅細胞制備洗滌紅細胞的容量變化,為更加規范合理血液成分制備提供理論依據。方法2016.6-2016.12期間,隨機抽取100袋2U懸浮紅細胞為起始血液制備洗滌紅細胞,按照《血站技術操作規程》(2015)和《全血及成分血質量要求》(GB18469-2012)制備并檢測按國標控制容量前后洗滌紅細胞的容量、血紅蛋白含量、上清蛋白含量、溶血率,比較容量控制前后各項指標的變化。結果按照制《血站技術操作規程》(2015)制備洗滌紅細胞在未進行容量控制前測得洗滌紅細胞容量323±16.7ml,血紅白白含量51.5±6.68g;容量按國標控制后,洗滌紅細胞容量為272±2.11ml,血紅蛋白含量為43.2±4.38g,洗滌紅細胞容量控制前后對比,容量及血紅白白含量差別均有統計學意義(P<0.01),但容量控制后血紅蛋白含量均在國標范圍內。而上清蛋白含量及溶血率前后無明顯變化。結論按照《血站技術操作規程》(2015)制備的洗滌紅細胞,在未按國標進行容量控制前,容量明顯高于國家標準,容量控制后雖然各項指標均符合國標,但血紅蛋白含量相對偏低,為更加充分利用血源、提高洗滌紅細胞質量,建議適當提高洗滌紅細胞容量范圍。
洗滌紅細胞;容量;國家標準
洗滌紅細胞屬于常用紅細胞制品之一,是由全血或懸浮紅細胞經生理鹽水洗滌去除幾乎全部血漿成分,及部分非紅細胞成分的血液制品。臨床主要用于血漿蛋白過敏患者、自身免疫性溶血性貧血、腎功能不全等患者的輸血,近年來臨床需求呈相對增多趨勢[1,2]。新國標即《全血及成分血質量要求》(GB18469-2012)對洗滌紅細胞的質量控制要求包括外觀、容量、血紅蛋白含量、上清蛋白含量、溶血率及無菌實驗幾個方面[3]。新版國標自2012年7月1日實施以來,我們嚴格按照要求制備洗滌紅細胞,每批次抽檢質量均符合國標要求,但在制備過程中筆者發現,由2U懸浮紅細胞為原料血制備洗滌紅細胞時,洗滌至第三遍后盡可能去除上清及白膜后,留下的濃縮紅細胞再添加100ml生理鹽水或紅細胞保養液后常常超出國標所示的容量要求,而為達到國標容量質控要求,不可避免會丟棄一些紅細胞,造成血液資源浪費。針對洗滌紅細胞容量這一質控指標,我們自2016年6月-2016年12月隨機分析了100袋洗滌紅細胞,檢測按照《血站技術操作規程》(2015)制備的洗滌紅細胞容量數據,及按照國標容量控制前后血紅蛋白含量等指標變化,期望為更加規范合理進行血液成分制備提供依據。現將我們的結果報告如下。
1 材料與方法
1.1 材料2016年6月-2016年12月期間檢驗合格的2U懸浮紅細胞,四聯袋生理鹽水耗材(威高),含紅細胞添加液的五聯袋洗滌耗材(費森)。
1.2 洗滌紅細胞制備方法將四聯袋生理鹽水耗材或含紅細胞添加液的五聯袋洗滌耗材與母袋懸浮紅細胞用無菌接駁機對接,打開管路將生理鹽水加入紅細胞內,邊加邊輕輕混勻,加入約200ml后,卡住止流夾,離心力1977g,離心5min,溫度4℃,離心后輕輕取出并將母袋血置于分漿夾中,將上清及白膜層全部轉移至廢液袋內,再將生理鹽水約200ml加入母袋血內,重復上述步驟。依次洗滌三次后,依據要求加入生理鹽水或紅細胞保養液約100ml[4]。
1.3 洗滌后紅細胞質量測定用電子秤稱量洗滌紅細胞重量并計算血容量,檢測每袋洗滌紅細胞定容前后血紅蛋白含量、上清蛋白含量、溶血率等指標[5]。
1.4 統計學處理采用SPSS 12.0軟件進行統計分析,數值變量以均值±標準差(x±s)表示,比較洗滌紅細胞定容前后各檢測指標變化,采用配對t檢驗,以P<0.05為差異有統計學意義。
2 結果
我們統計分析了100袋洗滌紅細胞,按照操作規程制備洗滌紅細胞在未進行容量控制前測得洗滌紅細胞容量323±16.7ml,血紅蛋白含量51.5± 6.68g;容量按國標控制后,洗滌紅細胞容量為272±2.11ml,血紅蛋白含量為43.2±4.38g,洗滌紅細胞容量控制前后對比,容量及血紅蛋白含量差別均有統計學意義(P<0.01),但容量控制后血紅蛋白含量均在國標范圍內。而上清蛋白含量及溶血率前后無明顯變化。具體結果見表1。
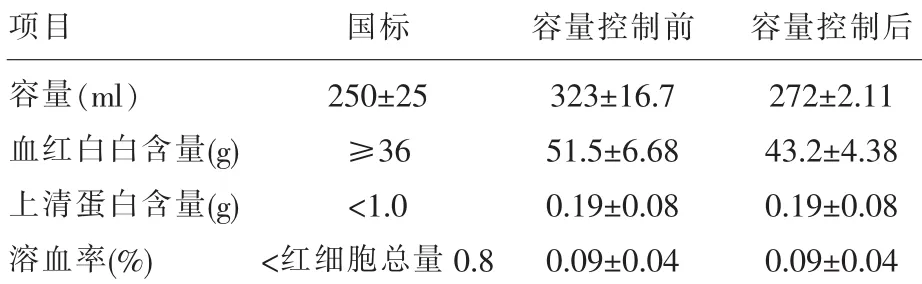
表1 洗滌紅細胞定容前后質檢結果(n=100)
3 討論
洗滌紅細胞為臨床常用血液制品之一,主要用于血漿蛋白過敏患者、自身免疫性溶血性貧血、腎功能不全等貧血患者的輸血,近年來臨床需求呈相對增多趨勢。《血站技術操作規程》(2015)明確要求用合格的紅細胞懸液為起始血液,使用無菌接合機將待洗滌的紅細胞懸液袋導管和洗滌溶液聯袋進行無菌接合連通,1U紅細胞加入液體量約100ml,混勻后,離心,離心后把上清轉移至空袋內,按此步驟洗滌三次,最后將適量(每單位紅細胞中加入約50ml)保存液(生理鹽水或紅細胞保存液)移入已完成洗滌的紅細胞,混勻,熱合,即為成品洗滌紅細胞[4]。
新版國標與舊版《全血及成分血質量要求》(GB18469-2001)相比,對洗滌紅細胞質量要求有較大變化,舊版的紅細胞回收率和血漿蛋白清除率變為成品洗滌紅細胞的血紅蛋白含量和上清蛋白質含量,取消了舊版的白細胞去除率要求,增加了溶血率<紅細胞總量0.8%的規定,對于容量的要求未作修改,新舊版均要求400ml全血制備的洗滌紅細胞容量為250ml±10%。與舊版相比,新版國標更加注重洗滌紅細胞成品的質量控制,操作起來相對簡單、科學。
影響洗滌紅細胞質量因素有多種,起始血液的質量、離心力大小、溫度、操作人員的手法等[6-10]。我們在實踐中發現,離心力1977g,離心時間5min,離心溫度4度時的離心條件更有利于制備出高質量的洗滌紅細胞制品。通過加強對操作人員的反復培訓,嚴格按照操作規程,注重細節,從我們的檢測結果可以看出,100袋成品洗滌紅細胞均符合《全血及成分血質量要求》(GB18469-201)對洗滌紅細胞的質量控制要求。但是在實際工作中,我們發現按照《血站技術操作規程》制備的洗滌紅細胞容量常常高于國標要求,我們隨機統計了100袋規格為2U的洗滌紅細胞,未按國標控制前容量為323±16.7ml,遠高于國標對容量的要求。而為達到國標容量質控要求,不可避免會丟棄一些紅細胞,盡管如此,我們其他各項指標質控結果仍然符合國標要求。但是洗滌紅細胞的血紅蛋白含量相對偏低。因此,為提高血液質量,是否對洗滌紅細胞容量要求適當放寬,期待同仁們進一步考證。
[1]曹陽.洗滌紅細胞的臨床應用分析[J].臨床血液學雜志(輸血與檢驗版),2007,8(4):171-172.
[2]朱同華.洗滌紅細胞在自身免疫溶血性貧血患者中的應用[J].中國輸血雜志,2013,26(4):379-380.
[3]GB18469-2012.全血及成分血質量要求[S].2012.8.
[4]國家衛生計生委.血站技術操作規程[S].2015版:11-12.
[5]安蓬蓬,李浩瀧,劉春燕,等.新國標實施后的洗滌紅細胞質檢結果分析[J].臨床輸血與檢驗,2016,18(2):158-160.
[6]危燕芬,林麗娟,朱仕清.洗滌紅細胞質量檢查情況分析[J].實驗與檢驗醫學,2012,30(3):262-264.
[7]張西春,曹麗,王曉華.不同離心條件對制備洗滌紅細胞質量的影響[J].臨床輸血與檢驗,2005,7(3):213.
[8]Basu D,Kulkarni R.Overview of blood components and their preparation[J].Indian J Anaesth,2014,58(5):529-537.
[9]Acker JP,Hansen AL,Yi QL,et al.Introduction of a closed-system cell processor for red blood cell washing:postimplementation monitoring of safety and efficacy[J].Transfusion,2016,56(1):49-57.
[10]李美霖,段錦,麻靜敏,等.不同儲存時間血液制備洗滌紅細胞效果分析[J].河北醫藥,2015,37(18):2754-2756.
R457.1+2,R193.3
A
1674-1129(2017)04-0621-02
10.3969/j.issn.1674-1129.2017.04.060
2017-03-06;
2017-05-31)

