血清胃蛋白酶原聯合胃泌素-17對胃癌篩查的價值研究
胡鵬 ,朱長才,汪薇 ,黃萍
(1.武漢科技大學醫學院,武漢 湖北 430081;2.武漢市紅十字會醫院檢驗科,武漢 湖北 430015;3.解放軍武漢總醫院檢驗科,武漢 湖北 430070)
胃癌是常見消化道惡性腫瘤,病死率占惡性腫瘤第3位[1]。早期胃癌患者經合理治療后5年生存率>90%[2],但胃癌進展期患者經治療后的5年生存率只有約30%[3],所以胃癌的早期診斷對患者的治療尤為關鍵。目前我國早期胃癌的平均檢出率<10%[4],由于胃癌早期多無明顯特征性臨床表現,所以多數胃癌確診時已為進展期。目前臨床公認的診斷胃癌的金標準為胃鏡聯合病理學檢查,但由于其屬侵入性檢查且費用較高,會給患者帶來生理和心理上的壓力,難以用于大面積篩查。因此血清學腫瘤標志物:胃蛋白酶原Ⅰ(pepsinogenⅠ,PGⅠ)、胃蛋白酶原Ⅱ(pepsinogenⅡ,PGⅡ)、胃蛋白酶原Ⅰ/Ⅱ比值(pepsinogen ratio,PGR)、胃泌素-17(gast rin-17,G-17)成為胃癌篩查的研究熱點。本研究就上述各項指標進行回顧性分析,現報道如下。
1 資料與方法
1.1 臨床材料 收集武漢市紅十字會2016年1月~2017年1月患者資料87例,臨床資料見表1。

表1 患者臨床資料
1.2 排除及入選標準 無嚴重心腦血管疾病等胃鏡檢查禁忌證;近1個月未使用抗生素、抑酸劑、非甾體抗炎藥、胃黏膜保護劑。排除合并全身其他系統及器官惡性腫瘤、排除嚴重肝腎功能不全。所有病例均經由胃鏡及活檢病理組織學檢查確診,分為3組:胃癌組、良性胃病組(包含淺表胃炎、十二指腸潰瘍等良性胃病)、正常對照組。
1.3 方法
1.3.1 胃鏡檢查 按固定部位活檢組織2~5塊做病理組織學診斷,標本要求達到黏膜肌層。
1.3.2 血清PGⅠ、PGⅡ、PGR(PGⅠ/PGⅡ)、G-17測定 清晨空腹采集受試者靜脈血3ml,迅速分離血清后于-20℃冰箱中冷凍待測。PGⅠ、PGⅡ、G-17均采用芬蘭Biohit公司酶聯免疫吸附測定(enzyme linked immunosorbent assay,ELISA)試劑盒,嚴格按照說明書操作。使用CHROMATE酶標儀對檢測結果進行定量分析。PGR為PGⅠ與PGⅡ的比值。
1.4 靈敏度、特異度、準確度計算方法 靈敏度=真陽性數/篩檢人數×100%;特異度=真陰性數/篩檢人數×100%;準確率=(真陽性數+真陰性數)/篩檢人數×100%。
1.5 統計學方法 采用SPSS 19.0軟件進行數據統計、分析。以Kolmogorov-Smirnov檢驗測定變量的分布。計量資料呈偏態分布,用中位數(M)和四分位數(P25~P75)表示。兩組間比較采用Mann-Whitney U檢驗。采用受試者工作曲線(receriver operating characteristics,ROC)計算每個變量的曲線下面積(area under the curve,AUC)、診斷臨界值、診斷敏感度和特異度。P<0.05為差異有統計學意義。
2 結果
2.1 3組之間血清PGⅠ、PGⅡ、PGR、G-17水平比較 胃癌組PGⅠ、PGR、G-17與良性胃病組、正常對照組比較,差異有統計學意義(P<0.05);而胃癌組PGⅡ與良性胃病組、正常對照組比較,差異無統計學意義,見表2。

表2 胃癌組、良性胃病組、正常對照組血清PGⅠ、PGⅡ、PGR、G-17水平比較M(P25~P75)
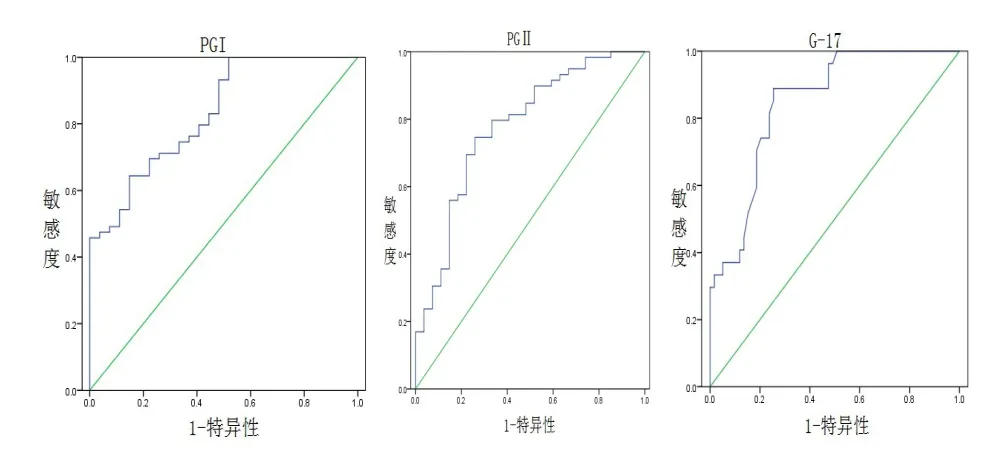
圖1 血清PGⅠ、PGR、G-17 ROC曲線
2.2 血清PGⅠ、PGR、G-17在胃癌中的診斷價值評估 因胃癌組PGⅡ與良性胃病組、正常對照組比較差異無統計學意義,所以將PGⅠ、PGR、G-17水平做ROC曲線。ROC曲線顯示PGⅠ診斷胃癌的曲線下面積為(0.831±0.045),最佳臨界值為86.95μg/L、敏感度為0.644、特異性為0.852;PGR曲線下面積為(0.776±0.055),最佳臨界值為5.80、敏感度為0.746、特異性為 0.741;G-17曲線下面積為(0.847±0.041),最佳臨界值為8.15 pmol/L、敏感度為0.889、特異性為0.746,見表2,表3。
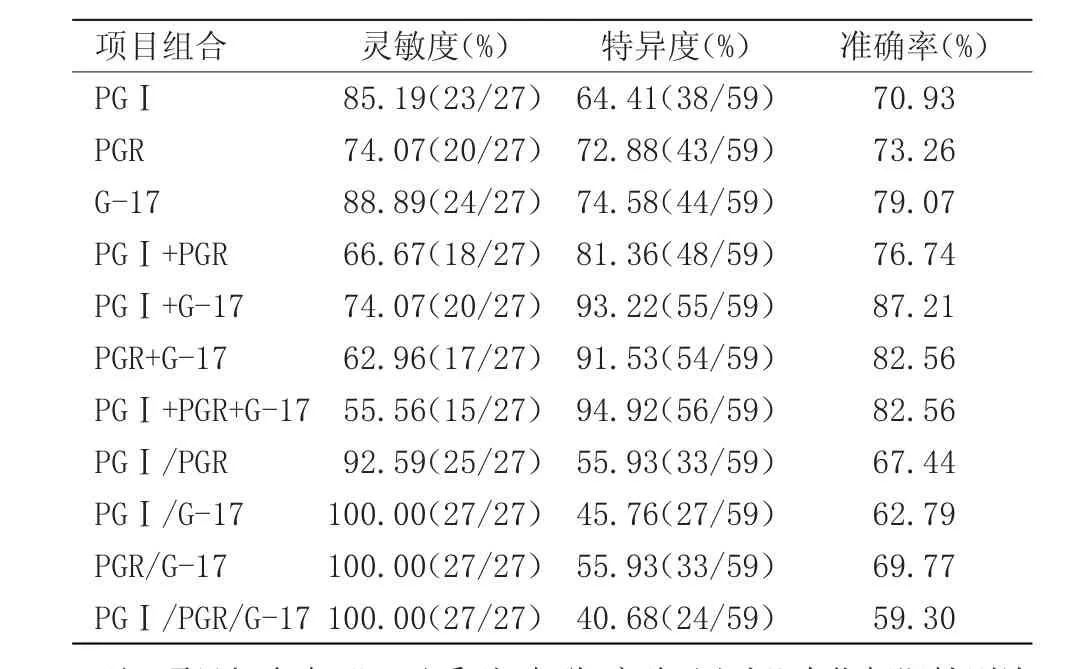
表3 血清PGⅠ、PGR、G-17單項及聯檢對肝癌的診斷價值比較
3 討論
胃蛋白酶原(pepsinogen,PG)是胃蛋白酶的前體,根據免疫原性將其分成PGⅠ和PGⅡ兩種亞型。PGⅠ主要由胃底的主細胞和頸黏液細胞分泌,PGⅡ除此之外還由賁門腺、胃竇幽門腺和十二指腸Brunner腺分泌。PG大部分進入胃腔,在酸性胃液作用下活化成胃蛋白酶,僅約1%透過胃黏膜毛細血管進入血液循環。血清PGⅠ、PGⅡ、PGR是胃黏膜狀態的指標,對胃黏膜的損傷較敏感[5],可反映胃黏膜腺體和細胞的數量,也間接反映胃黏膜不同部位的分泌功能和病變嚴重程度,是篩查胃癌的參考指標[6-7]。
G-17主要由胃竇部G細胞合成和分泌,它通過激活ECL細胞刺激胃酸分泌,從而釋放組織胺并刺激胃腸道上皮細胞增殖。隨著研究的進一步深入,G-17被發現與胃癌的浸潤及轉移密切相關[8-9],同時G-17的水平升高還與胃底和胃體癌的形成與發展有關。研究還指出萎縮性胃炎伴隨的高胃泌素狀態對胃黏膜癌變有促進作用[10]。
本研究結果顯示,胃癌組相對良性胃病組、正常對照組,PGⅠ、PGR明顯降低(P<0.05),G-17明顯升高(P<0.05),同時通過ROC曲線分析,PGⅠ、PGR、G-17曲線下面積分別為0.831、0.776、0.847,證實了以上各項指標在胃癌篩查方面的有效作用。同時,本研究提出了本院最佳診斷臨界值分別為:PGⅠ86.95μg/L、PGR 5.80、G17 8.15 pmol/L。依據最佳臨界值,單項指標中G-17的特異度和特異度最高為88.89%和74.58%。
每一種血清學標志物在診斷上均有其自身的價值,也會有一定的局限性。多種血清標志物的聯合檢測可相互彌補單一檢測的不足,從而提高胃癌篩查的效能。本研究探討了PGⅠ、PGR、G-17之間聯合檢測對胃癌篩查的篩查價值。串聯實驗可以提高特異性,PGⅠ+PGR+G-17檢測后特異度高達94.92%,故可認為三項聯合檢測是一個有效的用于判斷胃癌病情的血清學指標。PGⅠ、PGR、G-17聯合平行實驗中PGⅠ/G-17、PGR/G-17、PGⅠ/PGR/G-17靈敏度可高達100%,可作為排除胃癌或者篩查胃癌較好的組合標志物。
總體而言,本研究表明PGⅠ、PGR、G-17是胃癌篩查的有效血清學標志物,聯合檢測對胃癌檢測的診斷有較高價值,可作為胃鏡病理學檢查的有效補充,是可疑患者、健康體檢的有效篩查或排除胃癌的檢測項目。但為排除在研究方法、試劑使用、患者個體差異情況及區域群體差異[11-13]等情況,仍需要進一步臨床大數據佐證。
[1] Wong RK,Jang R,Dar ling G.Postoperative chemoradio-therapy vs.preoperative chemoradiotherapy for local ly ad-vanced(operable)gast ric cancer:Clarifying the role and technique of radiotherapy[J].J Gast rointest Oncol,2015,6(1):89-107.
[2] Isobe Y,Nashimoto A,Akazawa K,et al.Gast ric cancer t reatment in Japan:2008 annual repor t of the JGCA na-tionwide regist ry[J].Gast ric Cancer,2011,14(4):301-316.
[3] Ajani JA,Bent rem DJ,Besh S,et al.Gast ric cancer,ver-sion 2.2013: Featured updates to the NCCN Guidelines[J].J Nat l Compr Canc Netw,2013,11(5):531-546.
[4] 中華醫學會消化內鏡學分會.中國早期胃癌篩查及內鏡診治共識意見(2014年,長沙)[J].中華消化雜志,2014,34(7):433-448.
[5] 陳美珍,張民樂,岑國禎.血清胃蛋白酶原含量測定在胃疾病中的應用價值[J].當代醫學,2012,18(33):34-35.
[6] 張衛東,孫曉,牛愛軍.血清胃蛋白酶原檢測在胃部疾病應用價值[J].醫學檢驗與臨床,2013,24(4):12-14.
[7] 黃語嫣,陳衛昌,高楠,等.血清胃蛋白酶原I、Ⅱ在胃癌及癌前病變診斷中的價值[J].中華內科雜志,2013,52(4):332-333.
[8] Kim YM,Kim IM,Nam TJ.Capsosiphon fulvescens glycoprotein reduces AGS gast ric cancer cel l mingration by downregulating t ransforming groth factor-β 1 and integrin expression[J].Int J Oncol,2013,43(4):1059-1065.
[9] Misha P, Senthivnayagam S, Rangasamy V, et al.Mixedlineage kinase-3/JNKL axispromotes migration of humangast ric cancer cel ls fol lowing gastrin stimulation[J].Molen docrinol,2010,24(3):598-607.
[10]Kikuchi R,Abe Y,Ii jima k,et al.Low serum levels of pepsinogen and gastrin 17 are predictive of extensive gas-t ric at rophy with high-risk of ear ly gast ric cancer[J].To-hoku J Exp Med,2011,223(1):35-44.
[11]李海英,左燦,王艷蘭,等.長沙地區健康成年居民胃蛋白酶原參考范圍的建立[J].國際檢驗醫學雜志,2014,35(12):1575-1579.
[12]程清.血清胃蛋白酶原對胃癌早期診斷的意義[J].現代檢驗醫學雜志,2013,28(1):67-69.
[13]孫濤,袁媛,李兆申.早期胃癌非創傷性檢查進展與現狀[J].中國實用內科雜志,2014,34(4):421-427.

