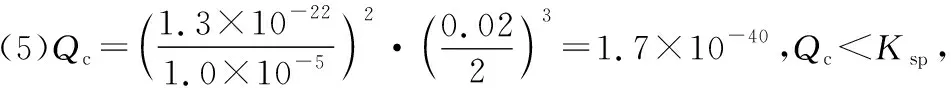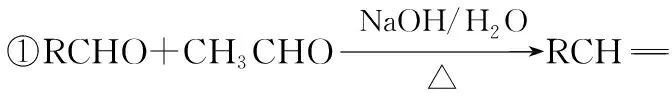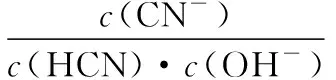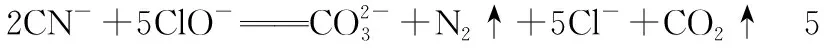淺談化學原創試題的命題原則與策略
欒厚福
黑龍江
縱觀歷年高考試題和各地聯考題會發現化學試卷中有較多設計精巧的原創試題。任何考生都沒有見過和做過這些原創試題,對學生來說很公平,也體現了考試的客觀公平性。
所謂的原創試題就是命題教師根據自己的智慧和教學經驗自主設計、首創的用于考查學生知識和能力的試題。由于原創試題的命題形式或所涉及的材料等都很新穎,而且對中學化學教學和高三學生備考都具有良好的導向作用,備受廣大師生的青睞。我們作為高中化學教師,要結合現有資源和自己的教學經驗,學會命制高水平的原創試題。教師命制原創試題不僅能體現教師的業務水平,而且有助于教師對《課程標準》和《考試大綱》的理解,也有助于提高教師的鉆研能力,更有助于提高教師的社會價值。
接下來筆者結合十余年的命題經驗闡述關于原創試題的命題原則和命題策略,希望對命題教師有借鑒意義或參考價值。
一、原創試題的命題原則
1.依據《考試大綱》,避免偏難偏怪
作為一名命題教師,要針對哪部分知識命題、命制什么題型,怎樣的難度,做到心中有數,要熟悉最新的《考試大綱》,明確“考綱”對這部分知識的能力層次要求,這是命題最基本的原則。還要注意掌握命題的難易程度和深廣度,要與“考綱”要求的知識點和能力要求相吻合。在平常的教學中會發現有些資料中偶爾出現偏題、難題、怪題等,用高中化學知識很難解釋,命題教師命制原創試題都屬于有目的的創設,命題時要避開偏題、難題、怪題的出現,這樣的試題既耗時又不能達到預期的訓練目的。

2.命題科學準確,經得起推敲
命題需使用真實的化學情境、素材,拉近化學與生產生活的距離,并保證命題的科學準確性,這是衡量命題質量的重要指標。整個試題命制過程都應自始至終地貫徹科學性原則,尊重客觀事實,切忌主觀臆斷,否則命制的試題起不到訓練選拔的作用,甚至會誤導學生等。命題還需要做到知識的遷移運用、體現活學活用,避免死記硬背,受定式思維影響等。
原創試題最終用于學生訓練,以檢測學生對知識的掌握情況,由于教師命題經驗不足或水平有限等,所命原創試題有可能出現漏洞、有差錯或有爭議,為了減少由此引發的影響,教師要根據學生做題情況或同仁的交流反饋,進行反復研究、修改并使之完善,使試題經得起推敲。即命題要做到題意清楚、表述準確、內容完整,知識準確無誤、內容不超綱、導向正確、答案準確等。
如某試卷中出現“下列關于電離平衡常數(K)說法正確的是( )A.電離平衡常數(K)越小,表示弱電解質的電離能力越弱B.……”,試題答案為A。一般來說,電離平衡常數(K)的大小能表示弱電解質的電離能力,但需有限定條件,即“在相同溫度下”或“同一條件下”,而本題題干中,沒有給出限定條件,顯然該題命題不夠科學準確,因此命制原創試題后要反復研究、檢測反饋,確保無任何異議。
3.與教學有關聯,基礎而創新
有個別的原創試題為了追求創新,題干中設置了較冗長的背景信息,甚至與學科內容無關,雖有創意,但會誤導學生、干擾學生的正常思維,不能為了原創而去刻意創新;命題形式和內容都要與教學實際有關聯。命題時還要借助情境信息等對基礎知識、基本技能、基本化學思想方法的考查,并促進學生長期學習和發展;命題時既要立足基礎,又要貴在創新,即盡量做到內容創新、情境創新、問題創新、題型創新等,富有時代氣息,有令人耳目一新的感覺。
二、原創試題的命題策略
1.教材內容拓展延伸
有些原創試題內容源于教材,是教材內容的拓展或延伸等,學生看到這些題有似曾相識的感覺,因此引導學生還要重視對教材知識的挖掘,尤其是教材中的資料卡片、科學視野、科學探究、某些典型習題等都可以作為原創題的切入點;還可以對教材多個知識點的整合處理進行綜合命題,某些實驗試題可能改編于教材實驗或原理的探究延伸等,都要給予高度重視。
例1(2016·卷Ⅰ·13題)短周期元素W、X、Y、Z的原子序數依次增加。m、p、r是由這些元素組成的二元化合物,n是元素Z的單質,通常為黃綠色氣體,q的水溶液具有漂白性,0.01 mol·L-1r溶液的pH為2,s通常是難溶于水的混合物。上述物質的轉化關系如圖所示。下列說法正確的是
( )
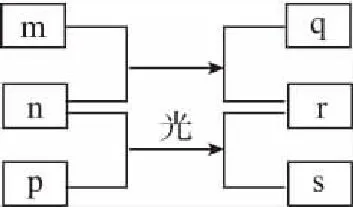
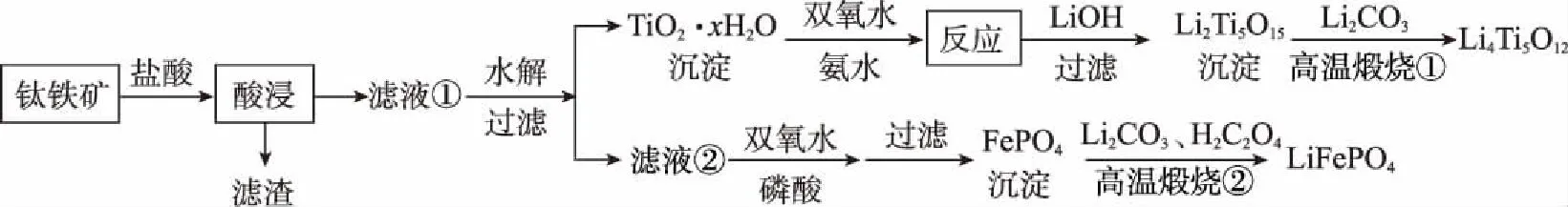
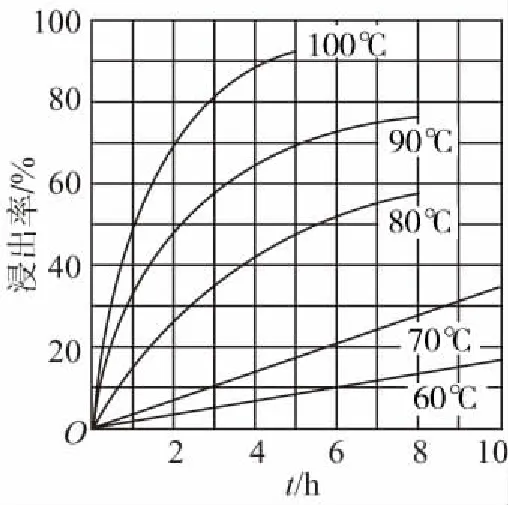
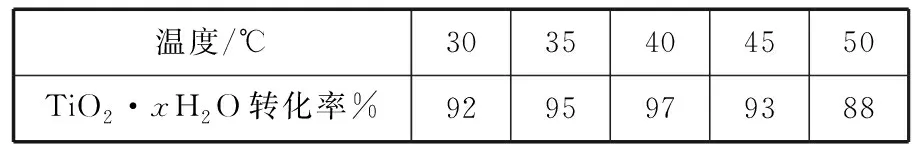
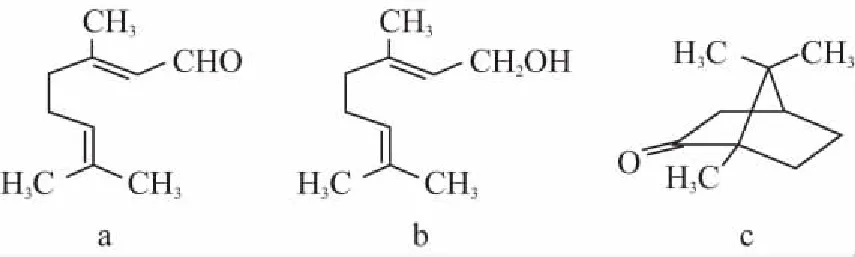
A.原子半徑的大小W B.元素的非金屬性Z>X>Y C.Y的氫化物常溫常壓下為液態 D.X的最高價氧化物的水化物為強酸 【參考答案】C 【分析】本題命題新穎獨特,能結合元素推斷和框圖推斷將元素化合物性質與元素周期表、周期律知識整合進行綜合命題,在以前的考試卷中幾乎沒有出現過。試題以教材內容為切入點命題,多個知識點進行整合,拉近了與教材的距離。根據“n是元素Z的單質……s通常是難溶于水的混合物”確定n為Cl2,根據0.01mol·L-1r溶液的pH為2可知r為強酸HCl,結合m為二元化合物和q水溶液有漂白性可確定m、q分別為H2O和HClO,再根據二元化合物p能與Cl2在光照時反應生成HCl和難溶于水的混合物s,可確定p為CH4。題中反應條件看起來也似曾相識,教材中學過的能和Cl2光照的反應僅有2個,即Cl2分別與H2、CH4的反應,根據其他信息可完成推斷作答。 再如2015年天津卷第10題結合明礬的凈水原理和氧化還原反應等考查FeCl3的凈水原理、氧化還原反應的配平、影響鹽類水解的因素等;2014年課標卷Ⅱ第27題根據碳、鉛同主族進行命題;還有很多聯考卷結合Cl2、SO2的制備等綜合探究其性質。這些高考題或聯考卷中很多試題是以教材內容為切入點進行綜合命題,也是原創題最常見的命題方式。 2.結合生產實際命題 有些原創試題往往結合化工生產實際進行命題,讓學生做到理論聯系實際、關注生產生活,注重知識和能力的全面考查。化學反應原理命題一般都結合特定工業生產實際或環境保護等信息載體,結合圖象、表格數據信息等確定最適宜的反應條件、考查化學平衡移動、轉化率的計算等。歷年的高考卷中的工藝流程題往往也都是結合化工生產流程信息綜合考查元素化合物和化學理論、分離提純等知識的應用,也是原創命題教師比較青睞的命題形式。 例2(2017·卷Ⅰ·27題)Li4Ti5O12和LiFePO4都是鋰離子電池的電極材料,可利用鈦鐵礦(主要成分為FeTiO3,還含有少量MgO、SiO2等雜質)來制備,工藝流程如下: 回答下列問題: (1)“酸浸”實驗中,鐵的浸出率結果如上圖所示。由圖可知,當鐵的浸出率為70%時,所采用的實驗條件為___________________。 (3)TiO2·xH2O沉淀與雙氧水、氨水反應40 min所得實驗結果如下表所示: 溫度/℃3035404550TiO2·xH2O轉化率%9295979388 分析40℃時TiO2·xH2O轉化率最高的原因:___________________________。 (4)Li2Ti5O15中Ti的化合價為+4,其中過氧鍵的數目為___________________。 (5)若“濾液②”中c(Mg2+)=0.02 mol·L-1,加入雙氧水和磷酸(設溶液體積增加1倍),使Fe3+恰好沉淀完全即溶液中c(Fe3+)=1.0×10-5mol·L-1,此時是否有Mg3(PO4)2沉淀生成? (列式計算)。FePO4、Mg3(PO4)2的Ksp分別為1.3×10-22、1.0×10-24。 (6)寫出“高溫煅燒②”中由FePO4制備LiFePO4的化學方程式:_________________。 【參考答案】(1)90℃加熱5h或100℃加熱2h (3)40℃前,未達到平衡狀態,隨著溫度升高,轉化率變大;40℃后,H2O2分解加劇,轉化率降低 (4)4 【分析】本題結合生產工藝流程考查Ti、Fe及其化合物間的轉化,并配有圖象根據限定條件考查實驗條件的選擇,根據表格數據信息分析40℃時TiO2·xH2O轉化率最高的原因,這些命題都源于圖象、數據信息判斷;(5)還突出對溶度積常數及其應用這一高考高頻考點的考查;(2)(6)側重結合生產流程考查化學用語的正確書寫;有的試題中還可能涉及生成物產率的計算,有的試題結合侯氏制堿法綜合考查化學實驗等。如2016年課標卷Ⅱ第27題。這種命題形式也比較常見,所選工藝流程或生產原理等要符合學生的認知水平,尤其涉及實際生產,要保證所選取材料的客觀性。設問盡量新穎(可配圖表、數據等分析),考查的知識面要廣,這類試題涉及工藝流程、反應原理等信息,表面看起來難度較大,但在設置問題時難度適中即可。 3.結合大學知識命題 某些工藝流程中涉及部分Ni、Co、Pb及其化合物的信息,化學實驗方案設計中經常涉及氧化還原滴定原理的考查與計算,如2017年江蘇卷第18題等。還有很多高考題或聯考卷中部分試題中均涉及大學《無機化學》《有機化學》和《分析化學》教材內容。在命制原創題時可以適當參考大學內容作為資源,并結合學生已有知識進行綜合命題,這樣命制的原創試題能考查學生接受、處理信息和運用所學知識的能力,試題也具有較高的區分度。 4.競賽聯考試題改編 教師剛開始命制原創試題,會有一定難度,可以根據全國化學競賽或聯考卷等為載體進行深度改編,這樣也能命出較高質量的原創試題。 例3(2017·全國高中化學競賽初賽·12題)下列化合物均為天然萜類化合物: 對這些萜類化合物敘述錯誤的是 ( ) A.三種化合物中只有a和c互為同分異構體 B.三種化合物中b的沸點最高 C.三種化合物均易被氧化 D.三種化合物均可催化氫化 【參考答案】C 【分析】若對該題進行深度改編,可給出3種天然萜類化合物的結構簡式,避開原題的命題角度,可以從有機物的結構、性質、同分異構體、分子式和官能團種類的判斷、鑒別方法等角度進行命題,這樣的考題也很新穎,如果題干再進行適當處理,似乎找不出原題的影子,就能命出較高質量的原創試題。 5.網絡資源整合加工 教師命制原創試題,可對網絡資源進行整合或加工,也可作為原創題命制的載體。如根據360百科中氫氰酸(HCN)和氰化鉀(KCN)的信息并結合電離平衡、水解平衡、氧化還原反應、物質分離提純鑒別等角度可進行綜合命題。根據上述信息可命出如下原創試題。 【原創】氫氰酸(HCN)是一種常見的弱酸。氰化鉀(KCN)是有劇毒的鹽,可用于照相、蝕刻、石印和電鍍業等。 回答下列問題: (3)KCN溶液露置于空氣中吸收CO2轉化成HCN和K2CO3,該反應的化學方程式為___________________。 (4)已知KCN和KCl都是白色晶體,在外觀上無明顯區別;AgCN是淡灰色固體,但見光后易變成褐色的固體。在實驗室中檢驗KCN和KCl可將其分別配制成溶液,分別取少量溶液滴入AgNO3溶液,可觀察的實驗現象是 ___________________,得出的結論是___________________。 (4)分別產生白色沉淀和淡灰色沉淀(或棕色固體),得到淡灰色(或棕色)沉淀的溶液是KCN 【分析】本題既結合網絡資源信息又結合課內知識進行綜合命題,所命制試題新穎獨特且有創意。高考中每年都涉及對弱電解質溶液的考查,往往這類物質都是以最新的科技信息或前沿知識進行命題。命題教師可以適當整合網絡資源或科技前沿知識進行命題。