肝硬化患者行保留部分膽囊后壁的腹腔鏡膽囊切除術的臨床研究*
周曉鋒,金錦春,王先鋒,王方平
(新昌縣人民醫院,浙江 紹興,312500)
肝硬化患者膽囊結石發生率是普通人群的兩倍,為9.5%~13.7%,無肝硬化患者膽囊結石發病率為5.2%[1]。對國外文獻中約4 895例尸檢資料進行回顧性分析,發現肝硬化患者膽囊結石發生率為29.4%,無肝硬化者為12.8%[2]。以往為此類患者行膽囊切除術時,需行開腹手術[3]。然而,肝硬化患者行開腹膽囊切除術較腹腔鏡膽囊切除術(laparoscopic cholecystectomy,LC)術中出血量更多,手術時間更長,住院時間更長[4]。肝硬化患者行開腹膽囊切除術的并發癥發生率高達5%~23%[5]。這些不良后果主要由失血過多、術后肝功能衰竭、敗血癥等原因造成。雖然LC已成為治療膽囊結石的金標準,但最初肝硬化曾認為是相對禁忌證[6]。自1993年報道首例肝硬化患者行LC后[7],大量文獻表明經過不斷的改進與完善,LC對于Child A級、B級肝硬化患者是安全的[8]。但肝硬化患者行LC,術中、術后出血風險仍是困擾著外科醫生的難題,現回顧分析為肝硬化患者行保留膽囊床部分膽囊后壁的LC的臨床療效,將結果報道如下。
1 資料與方法
1.1 臨床資料 采用隨機數生成器隨機選取2014年7月至2017年7月收治的40例肝硬化合并膽囊結石患者(觀察組),男26例,女14例,37~68歲。隨機選取40例不合并肝硬化患者為對照組,男19例,女21例,42~73歲。兩組患者均無腹部手術史,術前經腹部B超確診。入選標準:(1)膽囊結石合并慢性膽囊炎的擇期手術;(2)合并肝硬化Child A級;(3)患者要求行LC。排除標準:(1)嚴重心、腦、肺、肝、腎功能異常,無法耐受手術及麻醉;(2)合并膽總管結石;(3)急性膽囊炎、磁化膽囊、膽囊解剖變異;(4)凝血功能嚴重異常。手術均由同一團隊完成。術前患者均簽署知情同意書,本研究獲得醫院倫理委員會批準。兩組患者術前一般資料差異無統計學意義(P>0.05),見表1。
1.2 手術方法 觀察組:全麻成功后,患者取仰臥位,手術床頭高腳低15°,左傾15°,常規三孔法施術。探查腹腔有無腹水及肝臟硬化情況,見圖1。由于肝硬化患者多伴有靜脈曲張,分離膽囊與周圍組織粘連、膽囊三角區時應用超聲刀分離解剖出膽囊管及膽囊動脈后結扎切斷。切開膽囊壺腹部,向膽囊底部方向切除膽囊,同時將膽囊床區域的膽囊后壁保留于膽囊床位置,切除膽囊后電凝燒灼保留的膽囊后壁黏膜,見圖2,充分止血。取出膽囊,放置腹腔引流管,縫合各切口。對照組手術過程同觀察組,但術中完整切除膽囊,不保留膽囊床區域的膽囊后壁,常規放置腹腔引流管,以觀察是否存在術后出血、膽漏,并引流膽囊床區滲液。


組別例數(n)年齡(歲)性別(n)男女BMI(kg/m2)觀察組4054.2±13.6261425.3±4.1對照組4049.1±12.5192123.8±9.2t/χ2值1.3321.2570.925P值0.1870.220.358

圖1 術中觀察肝臟硬化程度 圖2 切除膽囊后電凝燒灼保留的膽囊后壁黏膜
1.3 觀察指標 觀察兩組手術時間、術中出血量、術后腹腔引流時間、術后住院時間、住院費用及術后并發癥。術后隨訪3~24個月,平均(12.5±5.6)個月。

2 結 果
兩組均順利完成手術,無一例中轉開腹,無術中、術后出血及死亡病例。兩組手術時間、術中出血量、術后腹腔引流時間、術后住院時間、住院費用及術后并發癥發生率差異無統計學意義(P>0.05)。觀察組術后1例患者膽囊床區積液伴感染,加強抗感染治療后治愈;對照組1例患者術后出現轉氨酶升高,予以保肝治療后治愈。兩組患者手術相關指標見表2。
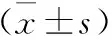

組別例數(n)手術時間(min)術中出血量(ml)術后腹腔引流時間(d)術后住院時間(d)住院費用(萬元)術后并發癥[n(%)]觀察組4042.11±25.2315.72±5.692.42±1.314.30±1.180.92±0.231(2.5)對照組4037.24±19.6712.33±12.151.92±0.873.67±1.220.89±0.151(2.5)t/χ2值1.3090.7831.0331.4220.6580.000P值0.1940.4360.3050.1590.5121.000
3 討 論
根據美國國家衛生研究院1993年發表的共識聲明,LC在肝硬化患者中的應用是禁忌與受限的[9]。但同年有學者報道了為首例肝硬化患者行LC,自此LC在肝硬化患者中的應用出現了大幅增長[7]。隨著腹腔鏡操作技能及器械的改進,也逐漸允許LC應用于肝硬化患者中。越來越多的研究表明,有癥狀的膽石癥合并Child A級患者可安全施行LC,其發病率、死亡率并無顯著增加[10]。但肝硬化患者肝纖維化的改變、繼發的門靜脈高壓癥會增加手術創面出血風險,雖然并未達到難以控制、危及生命的程度,但必然會引起術中出血量增加,此類出血對于無肝硬化的患者影響較小,但可引起肝硬化患者術后肝功能異常,甚至肝衰竭、肝性腦病等并發癥。
傳統LC術中處理膽囊與周圍組織的粘連、膽囊三角區時,精細分離并結扎膽囊動脈后并不會出現額外的出血,但由于肝硬化多伴有靜脈曲張,傳統電刀容易出血,控制此處出血也是減少LC術中、術后出血的重要措施。超聲刀直接離斷3~5 mm的血管是安全的,因此應用超聲刀分離是較為安全的,同時出血較少,本研究結果也證明了這一點。另一個容易出血的位置是順行切除膽囊的膽囊床。此處出血對于肝硬化患者而言,處理較困難,會造成額外出血,并對手術的連續性及流暢性產生不良影響,必然延長手術時間,同時更容易對術者心理造成不良影響,尤其手術經驗較少的術者,會因慌亂造成術中、術后并發癥發生率增加。因此尋找使術中出血變得可控的方法成為肝硬化患者行LC的迫切需要。本研究提出的保留膽囊床區域膽囊后壁的LC,使術中出血量大大減少,且更具可控性。
傳統LC術中盡量完整切除膽囊是手術成功的標志之一,因膽囊大部切除往往引起術后殘余膽囊,從而繼發殘余膽囊結石,引起反復發作的炎癥,甚至惡變[11]。但我們選擇性地保留膽囊床區域膽囊后壁,因切斷結扎了膽囊管,并不會造成上述不良反應,同時術中燒灼殘余膽囊壁黏膜,破壞了其分泌功能,理論上并不存在發生殘余膽囊及包裹性積液的可能,而且可減少膽囊床毛細膽管漏的發生。本研究中1例患者術后并發膽囊床區積液感染,考慮與患者膽囊為肝內膽囊,膽囊床位置深在,電凝燒灼殘余膽囊黏膜不全有關;余者術后近、遠期腹部B超隨訪未見殘余膽囊、膽囊床積液及毛細膽管漏發生。本研究中兩組患者均于術后第2天常規復查腹部B超,如膽囊床區無大量積液,腹腔引流液少于10 ml/d,則拔除腹腔引流管。
術中自肝硬化的膽囊床上剝離膽囊時很容易損傷,引起大量出血。保留膽囊床區域膽囊后壁的LC,術中常規應用超聲刀處理膽囊與周圍組織的粘連、膽囊三角區內的曲張血管,被證明在控制出血方面是有效、安全的,減少了術中膽囊床止血的操作,縮短了手術時間,同時降低了術后出血、殘余膽囊、膽漏等并發癥發生率,術后可早期安全地拔除腹腔引流管,減輕了患者痛苦,減少了外源性感染的發生,患者可早期出院,極大地降低了醫療成本,使患者可更早地投入正常工作與生活中,本研究結果亦表明了此術式的安全性與可行性。當然本研究也存在一定局限性。首先,本研究未納入Child B級、C級患者,研究表明,這些患者也是膽囊結石高發人群;第二,未納入肝硬化合并急性結石性膽囊炎患者,此類患者行保留膽囊床區域膽囊后壁的LC是否安全、有效仍待進一步研究證明。
相較非肝硬化患者,肝硬化患者由于具有肝纖維化、肝硬變及繼發門靜脈高壓癥等危險因素,必然導致并發癥發生率增高。隨著腹腔鏡操作技能的提高、設備的改進及經驗的積累,明智地選擇LC,合理的選擇患者,充分的術前準備,適當的手術技巧,會使并發癥發生率、死亡率明顯降低。總之,LC術中保留膽囊床區域膽囊后壁,常規應用超聲刀處理膽囊與周圍組織粘連、膽囊三角區內的曲張血管,對于膽囊結石合并Child A級肝硬化的患者具有術中出血量少、手術安全、創傷小、康復快、術后并發癥少等優勢,是可行、安全、有效的,適于臨床推廣。

