生長激素在卵巢儲備功能低下患者IVF-ET中的應用
王雪梅,劉迎春,黃靜,胡玉琴,宋小敏,劉穎,姜宏
(中國人民解放軍第105醫院生殖醫學中心,合肥 230031)
卵巢儲備功能低下(Diminished ovarian reserve,DOR)是指卵巢產生卵子能力減弱,卵母細胞質量下降,可導致生育能力下降。由于DOR患者的基礎竇卵泡數少,且對促排卵藥物的反應性低,可導致體外受精-胚胎移植過程(IVF-ET)中獲卵數及可利用胚胎數明顯減少、周期取消率增高、累計妊娠率降低[1]。有研究報道,生長激素(Growth hormone,GH)能增強顆粒細胞對促性腺激素的反應性,促進卵泡生長發育及雌激素合成[2-4],但其是否能夠改善DOR患者的IVF-ET臨床結局尚存爭議。本研究通過分析在促排卵過程中添加GH者的臨床和實驗室結局,旨在探討GH對DOR患者IVF-ET臨床結局的影響。
資料與方法
一、研究對象
回顧性分析2011年3月至2017年4月在我院生殖中心行體外受精-胚胎移植(IVF-ET)的173例患者的臨床資料。
納入/排除標準:所有患者年齡均<40歲;基礎FSH水平≥10 U/L但<20 U/L,或FSH/LH≥3,或E2≥293 pmol/L;基礎竇卵泡數≤7個;獲卵數≤5個;移植胚胎均為卵裂胚,且至少移植一枚優質卵裂胚;所有患者均為第一周期IVF-ET,并排除內分泌疾病(甲狀腺功能亢進、糖尿病、高泌乳素血癥等)、子宮畸形、宮腔粘連、宮腔占位、子宮內膜異位癥、子宮腺肌癥等。
共納入173例患者。根據促排卵過程中是否添加重組人生長激素(r-hGH),分為GH組(71例)和對照組(102例)。
二、診療回顧
控制性促排卵方案包括拮抗劑方案、短方案及長方案。71例患者于促性腺激素(Gn)啟動當日開始使用r-hGH(安蘇盟,安科藥業)4 IU/d至HCG日(GH組);102例患者在Gn過程中不添加r-hGH(對照組)。
根據卵泡生長情況調整Gn用量,當2~3個卵泡直徑≥18 mm時,給予重組HCG(rhCG,艾澤,默克雪蘭諾,德國)250 μg皮下注射,36~38 h后在陰道超聲引導下穿刺取卵,常規IVF/ICSI授精,18 h觀察受精情況,72 h進行胚胎評分[5]。將6細胞Ⅰ級或7細胞Ⅱ級以上的胚胎定義為優質胚胎,5細胞Ⅲ級以上胚胎定義為可利用胚胎。
選擇2~3枚胚胎移植(至少含1枚優質胚胎)。移植后肌肉注射黃體酮60 mg/d進行黃體支持,5周后行陰道超聲檢查,宮腔內見妊娠囊為臨床妊娠。妊娠12周內胚胎停止發育或自然流產者判定為早期流產。
三、觀察指標及判定標準
患者基礎資料:年齡、體重指數(BMI)、不孕年限、基礎激素水平、基礎竇卵泡計數(AFC);控制性促排卵及體外受精資料:控制性促排卵方案、受精方式及體外培養結果;胚胎移植及妊娠結局。
受精率=受精數/獲卵數;卵裂率=卵裂數/受精數;臨床妊娠率=臨床妊娠周期數/移植周期數;胚胎種植率=著床胚胎數/移植胚胎數;早期流產率=妊娠12周前流產周期數/臨床妊娠周期數。
四、統計學方法
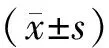
結 果
一、患者一般資料
兩組間患者平均年齡、不孕年限、BMI、基礎性激素水平(FSH、LH、E2)、基礎AFC均無顯著性差異(P>0.05)(表 1)。

表1 兩組患者一般資料比較(-±s)
二、控制性促排卵及體外受精結局
GH組中拮抗劑方案21例、短方案24例、長方案26例,對照組中拮抗劑方案32例、短方案35例、長方案35例,兩組間方案構成比無顯著性差異(P>0.05);GH組和對照組間IVF及ICSI受精占比分別為[83.1%(59/71) vs. 83.3%(85/102)]和[16.9%(12/71) vs. 16.7%(17/102)],兩組間無顯著性差異(P>0.05)。
兩組間Gn天數和劑量、HCG日內膜厚度和激素水平(LH、E2、P)、獲卵數、成熟卵數、受精率、卵裂率、可移植胚胎數、優質胚胎數、冷凍胚胎數均無顯著性差異(P>0.05)(表 2)。
三、胚胎移植及妊娠結局
兩組間移植胚胎數及早期流產率均無顯著性差異(P>0.05);但GH組的臨床妊娠率及胚胎種植率顯著高于對照組(P<0.05)(表3)。

表2 兩組控制性促排卵及體外受精結果比較[(-±s),%]
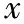
表3 兩組胚胎移植及妊娠結局比較[(-±s),%])
注:與對照組比較,*P<0.05
討 論
卵巢儲備功能與女性的年齡及生育能力密切相關,且隨年齡增長逐漸下降,37歲以后下降速度尤為明顯,且不可逆[6]。2016年美國疾病控制與預防中心全國輔助生殖技術數據顯示,DOR女性占助孕人群的30%左右[7],并與IVF-ET中的卵巢低反應、高周期取消率及不良妊娠結局相關[1],如何改善DOR患者的IVF-ET結局是近年學者們研究的熱點。
生長激素是腦垂體前葉嗜酸粒細胞分泌的一種肽類激素,可直接作用于靶細胞表面的生長激素受體(GHR)或通過IGF-1等生長介質的間接作用調節機體的生長發育和代謝。人卵巢的顆粒細胞、卵母細胞、黃體細胞及子宮內膜均存在GHR,GH可通過下丘腦和垂體增加Gn分泌,直接作用于卵巢提高其對Gn的反應性,與Gn有協同效應。而GH的繼發介質IGF-1可直接作用于卵巢顆粒細胞和膜細胞,促進類固醇激素合成和卵泡發育。此外,GH可通過與子宮內膜GHR結合增加腺體密度和內膜厚度,增強分泌功能和乳蛋白分泌,使胚胎更加易于黏附于內膜,改善子宮內膜的容受性。1988年GH被首次應用于低促性腺性性腺功能減退癥(HH)對HMG不敏感患者,發現GH可增加卵巢對HMG的反應性,減少HMG用量。2015年國內專家共識明確,在IVF周期中加用GH可以提高卵母細胞質量,改善卵泡的選擇和成熟[8]。目前GH多用于低反應患者,Meta分析證實,POR患者的IVF促排卵過程中添加GH可提高臨床妊娠率和活產率,且不良事件無明顯增加[9-11]。Kyrou等[3]通過對22項RCT的薈萃分析發現,在15項POR的干預措施中,添加GH是唯一有效的干預措施。
近年有學者發現,DOR患者的促排卵過程中添加GH可以降低Gn用量,提高 HCG日雌激素水平和卵子質量、增加獲卵數、可利用胚胎數及優質胚胎數,但并不能顯著提高臨床妊娠率[12-14]。本研究的結果顯示,40歲以下DOR患者在Gn同時添加小劑量r-hGH后,Gn用量和天數、HCG日子宮內膜厚度、激素水平、獲卵數、成熟卵數、優質胚胎數、冷凍胚胎數、受精率、卵裂率與對照組間并無顯著性差異(P>0.05),但臨床妊娠率及胚胎種植率均顯著高于對照組(P<0.05),表明在控制性促排卵中同時添加GH,并不能改善DOR患者的卵子數量及質量,但可通過改善子宮內膜容受性,提高DOR患者胚胎種植率和臨床妊娠率。Meta 分析結果顯示,子宮內膜發育不良患者在促排卵過程中添加 r-hGH,Gn 的用量和天數、獲卵數、優質胚胎數、HCG 注射日 E2值均無明顯變化,但子宮內膜容受性和臨床妊娠率均顯著提高[15]。我們的前期研究也證實,r-hGH可通過提高IGF-1、VEGF水平及子宮內膜血流灌注,改善子宮內膜容受性和凍融胚胎移植(FET)周期的臨床妊娠率及活產率[16]。
綜上所述,在IVF-ET促排卵過程中添加r-hGH可提高DOR患者的胚胎種植率及臨床妊娠率,從而改善妊娠結局。但GH在DOR患者中的最佳劑量、應用時間及確切應用價值尚有待擴大樣本量以及前瞻性隨機對照研究進一步證實。

