芹菜根中一種具有抗癌活性的雙氨基甲酸酯
楊曉軍,高 霞,趙 敏,李文惠,張越誠,湯江江
1延安大學化學與化工學院;2延安大學附屬醫院,延安 716000;3西北農林科技大學,楊凌 712100
芹菜ApiumL.為傘形科植物,是食藥同源品種,全世界各地均有栽培[1]。芹菜中富含有黃酮、氨基酸、香豆素等多種物質[2],具有抗菌、抗腫瘤和抗心血管等疾病的作用[3,4]。目前對芹菜化學成分的研究主要集中在其莖、葉和籽上,對其根部化學成分的研究較少。為挖掘芹菜根中的抗腫瘤活性成分。本實驗通過采用多種色譜分離技術,對陜西蒲城縣種植的旱芹根乙醇提取物進行了分離純化,得到3個單體化合物,利用其光譜數據及其文獻比對法確定3個單體化合物的結構分別為:雙氨基甲酸酯AG-01 (1)、佛手柑內酯 (2)和芹菜素 (3)。同時采用MTT法對化合物1進行了體外抗腫瘤細胞實驗,結果表明化合物1對肝癌細胞BEL-7402和胃癌細胞SGC7901均具有較好的細胞毒活性。
1 儀器與材料
1.1 儀器
X-4型顯微熔點儀(上海科學儀器有限公司);IR Prestige-21紅外光譜儀(日本島津公司) ;AV-500 型核磁共振儀 (瑞士Bruker公司),TMS為內標;MAT-711型質譜儀(美國Thermo公司); Vario EL 有機元素分析儀(德國Elementar公司); JP600型超聲波提取器(武漢嘉鵬電子有限公司)。
1.2 材料
Sephadex LH-20(Pharmacia產品);柱層析色譜和薄層色譜用硅膠(青島海洋化工廠產品);四甲基偶氮唑鹽溶液(MTT)試劑(Sigma公司);陽性對照品紫杉醇(紫杉醇江蘇紅豆杉藥業有限公司);人肝癌細胞株BEL-7402(上海美軒生物科技有限公司)、人肺癌細胞株A549(上海繼和生物科技有限公司),人胃癌細胞株SGC-7901(上海研生生化試劑有限公司);旱芹根于2017年11月采集自陜西省蒲城縣,經延安大學生命科學院白重炎研究員鑒定為傘形科芹屬ApiumL.的根,標本存放于延安大學天然產物化學實驗室,標本編號為YD20171109。
2 實驗方法
2.1 提取和分離
稱取芹菜根2.0 kg(干重),用粉碎機粉碎成粉末,將此粉末在超聲波輔助提取下,用50%的乙醇提取3次,每次1 h,將所得提取液減壓濃縮后得黃色浸膏,將此浸膏混懸于水中后,用石油醚萃取,將石油醚萃取液減壓濃縮后得石油醚萃取物21 g。將此萃取物首先經硅膠柱層析分離,以氯仿-丙酮梯度洗脫(100∶0→1∶1),洗脫餾分根據薄層板點板情況進行合并,共分得3段(P1-3)。第1段硅膠柱色譜(石油醚∶氯仿=20∶1)分得化合物1(13 mg)。第2段硅膠柱色譜(石油醚∶氯仿=15∶1),再根據薄層板點板情況合并相同部分,將此合并部分再經Sephadex LH-20純化得化合物2(105 mg)。第3段硅膠柱色譜(石油醚∶氯仿=9∶1)分得化合物3(51mg)。
2.2 化合物1的體外細胞毒活性
采用MTT法對化合物1進行體外細胞毒活性測定。取處于對數生長期的3株人體腫瘤細胞(人肝癌細胞BEL-7402、人肺癌細胞A549和人胃癌細胞SGC-7901),用含10%小牛血清的 RPMI 1640 細胞培養液調整細胞濃度,以3 000~4 000個/孔接種于96孔板上,置于37 ℃、5%CO2恒溫培養箱中培育24 h后加藥。設陰性對照組(DMSO溶劑對照組)、陽性對照組(紫杉醇)和化合物1實驗組,每組設立3個復孔,受試化合物1的終濃度分別為75.83、37.91、18.96、9.48、4.74 μM,培育48 h后,每孔加入10 μL MTT溶液(0.012M),繼續孵育反應4 h,棄去上清液,加入DMSO 100 μL /孔,振蕩均勻后用酶標儀在570 nm處測定每孔光密度值(OD值),計算對細胞增殖抑制率,并用Origin7.0軟件計算其 IC50值。細胞增殖抑制率(%)=[(對照組OD平均值-給藥組OD平均值)÷對照組OD平均值]×100%
3 結果與分析
3.1 結構鑒定
化合物1淺灰色粉末固體(丙酮),mp.222.1~223.4 ℃;與三氯化鐵反應呈陽性,提示含有酚羥基;HR-ESI-MS:m/z221.1431[M]+(C10H7NO5,計算值221.142 3),確定相對分子質量為221,不飽和度為8。IR (KBr) νmax3 327~3 485 cm-1(酚OH),3 014 cm-1苯環C-H伸縮振動吸收峰,1 683 cm-1(酰胺羰基C=O伸縮振動吸收峰)、2 962 cm-1和 2 835cm-1處有強吸收峰為亞甲基C-H不對稱伸縮振動和對稱伸縮振動吸收峰,1 604、1 576、1 492 cm-1為苯環的骨架伸縮振動吸收峰;13C NMR(125 MHz,CDCl3)共顯示6條譜線,DEPT譜顯示有1條芳香次甲基碳信號δc:110.6 (d),1條sp3雜化亞甲基碳信號δc:67.8(t),4條季碳信號δc:165.8(s,酰胺C=O),145.3(s,芳香季碳),130.1(s,芳香季碳),154.6(s,連接氧原子芳香季碳);1H NMR(500 MHz,CDCl3)共顯示有3種類型氫,由各類型氫的積分面積和分子式可以確定該化合物為一對稱分子,δH:6.76(2H,s,2個芳香CH),5.19(4H,s,2個sp3雜化-CH2),9.51(1H,br s,-OH);在HMBC相關譜圖中觀察到δ:5.19的亞甲基氫分別與酰胺羰基季碳δc:165.8、芳香季碳δc:130.1以及芳香次甲基δc:110.6相關。該化合物的其它C-H相關及其所有1H NMR和13C NMR數據見表1所示。綜合以上的分析化合物1可被推定為一新的雙氨基甲酸酯化合物。
化合物2白色針晶(甲醇);mp.189.6~190.3 ℃。EI-MS:m/z217[M+H]+,239[M+Na]+,元素分析得知碳、氫的百分含量分別為:66.39和4.11;質譜和元素分析提示該化合物的分子式為C12H8O4。IR (KBr) νmax1 728,1 637,1 612,1 472,1 408 cm-1;1H NMR (CDC13,500 MHz)δ: 6.31(1H,d,J=8.8 Hz,H-3),8.06(1H,d,J=8.8 Hz,H-4),7.14(1H,s,H-8),7.58(1H,d,J=8.6 Hz,H-12),6.97 (1H,d,J=8.6 Hz,0.8 Hz,H-13),4.46 (3H,s,5-OCH3);13C NMR(CDCl3,125 MHz)δ: 164.2 (C-2),113.2 (C-3),139.6(C-4),151.2 (C-5),112.9(C-6),156.3(C-7),94.7(C-8),153.3(C-9),105.8(C-10),144.6(C-12),106.2(C-13),61.7(5-OCH3)。以上數據與文獻[5,6]對照,確定該化合物為佛手柑內酯。
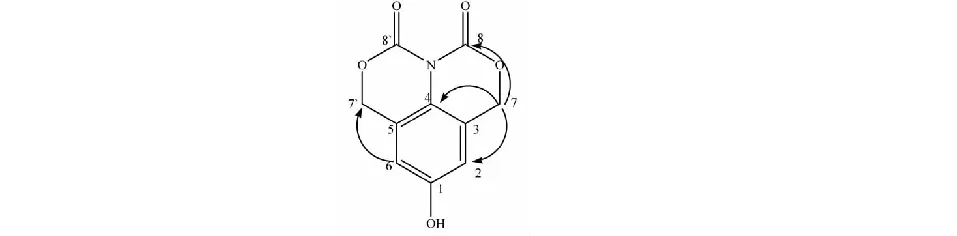
圖1 化合物1的主要HMBC相關Fig.1 The key HMBC of compound 1

PositionδH(mult.,JHH Hz)δc1H-1HCOSYHMBC1154.6 (s)2,66.76 (CH,s)110.6 (d)C-7,C-43,5145.3 (s)4130.1 (s)7,7`5.19 (s)67.8 (t)C-2,C-4,C-8,8`8,8`165.8 (s)1-OH9.51 (br s)
化合物3淺黃色針狀結晶(甲醇);1H NMR (500 MHz,DMSO-d6) δ:6.83 (1H,s,H-3),6.24(1H ,s,H-6),6.52(1H,s,H-8),7.79(2H,d,J= 8.6,H-2′,6′),6.91(2H,d,J= 8.6 Hz,H-3′,5′),12.04(1H,br.s,5-OH),10.67(1H,br.s,7-OH),10.43(1H,br.s,4′-OH);13C NMR (125 MHz,DMSO-d6) δ:164.8(C-2),104.7(C-3),181.9(C-4),161.3(C-5),98.7(C-6),165.1(C-7),94.1(C-8),161.7(C-9),102.9(C-10),121.5(C-1′),128.6(C-2′,6′),117.1 (C-3′,5′),157.6(C-4′)。以上數據與文獻[7,8]對照,確定該化合物為芹菜素。
3.2 化合物1的體外細胞毒活性
采用MTT法對化合物1進行體外細胞毒活性測試,結果表明化合物1對人胃癌細胞SGC-7901和人肝癌細胞BEL-7402均具有較強的細胞毒活性,具體活性結果見2。

表2 化合物1的細胞毒活性
4 結論
目前從芹菜根中分離得到具有較強抑制腫瘤細胞生長的化學成分主要為芹菜素和佛手柑內酯[9,10]。本文首次報道從陜西產旱芹根中分離得到一個新的雙氨基甲酸酯化合物,并研究了該化合物對人體腫瘤細胞的體外毒活性,研究表明該化合物對人胃癌細胞SGC-7901和人肝癌細胞BEL-7402具有較強的細胞毒活性,IC50分別為29.6和32.4μM。這一研究結果為進一步對陜西產旱芹根的開發利用提供了科學依據。

