ACDF中應用零切跡雙插片自穩型椎間融合器與鎖定鈦板內固定聯合椎間融合器的效果比較
朱俊,袁峰,彭琨翔,陳鵬宇,張弛,鄧斌
(1徐州醫科大學研究生學院,江蘇徐州221000;2徐州醫科大學附屬醫院)
頸椎退行性病變的特征在于頸椎間盤退變。頸椎間盤退變是頸部疼痛的常見病因,退變引起的椎間盤損傷可致椎間隙塌陷、椎間盤突出、椎管狹窄、脊髓及神經根受壓,從而引起走路不穩及雙上肢的神經根性疼痛[1]。頸椎前路減壓融合術(ACDF)是治療頸椎退行性病變的經典手術方式[2]。ACDF術中使用鈦板內固定可提高植骨融合率,療效較好,但仍可出現鈦板及螺絲的松動、軟組織損傷、食管穿孔、吞咽困難及相鄰節段退變加速等并發癥[3]。近年來流行的零切跡設計可避免由于鋼板內置物對于椎前周圍軟組織的壓迫而引起相關術后并發癥。2016年11月~2018年3月,我們對45例單節段頸椎間盤退行性病變患者行ACDF治療,其中19例采用頸椎零切跡雙插片自穩型椎間融合器(ROI-C),26例采用普通椎間融合器聯合前路鈦板,均取得較好效果。現報告如下。
1 資料與方法
1.1 臨床資料 選取2016年11月~2018年3月徐州醫科大學附屬醫院收治的單節段退行性頸椎病患者45例。病例納入標準:患者具有頸肩部疼痛或四肢麻木乏力或走路不穩等典型脊髓及神經根受壓癥狀;MRI檢查結果回報存在單節段頸椎椎間盤突出并壓迫脊髓或神經根;經保守治療(牽引、藥物等)2個月以上無明顯好轉。排除標準:頸椎骨折脫位、病變累及2個或2個以上多節段頸椎病變;先天性或黃韌帶肥厚及后縱韌帶鈣化導致的椎管狹窄;存在骨質疏松、全身或局部感染、惡性腫瘤等影響手術的合并癥。根據手術治療方式不同將45例患者分為ROI-C組19例和鈦板組26例,ROI-C組男11例、女8例,年齡(55.42±8.03)歲。對照組男11例、女15例,年齡(59.15±8.04)歲。兩組性別、年齡差異無統計學意義(P>0.05)。本研究獲醫院倫理委員會批準,患者均知情同意。
1.2 手術方法與術后處理 45例患者的手術均由徐州醫科大學附屬醫院脊柱外科1名經驗豐富主任醫師完成。全身麻醉完全后留置導尿管,患者取仰臥位于手術臺,雙肩下墊以軟枕使頭頸后呈仰伸位,治療巾卷成圓柱狀置于頸后,頸兩側以沙袋固定,并軟頭圈墊于枕部下,患者額前貼以長膠帶并固定于手術臺兩側。常規消毒鋪巾后根據影像學資料確定病變節段并取頸前右側胸鎖乳突肌內緣橫切口,分離軟組織至椎體前緣,并顯露椎間隙。于C臂機透視下再次確認具體病變節段后,使用Caspar撐開器將病變的椎間隙撐開。充分清除病變的椎間盤、椎體邊緣的骨贅并處理上下終板軟骨至骨面滲血,神經剝離子探查脊髓及神經根減壓是否滿意。ROI-C組:探查脊髓及神經根,減壓后進行試模,根據病變的椎間隙情況選擇合適的融合器,將自體左髂骨松質骨填塞其中。于病變椎間隙距離椎體前緣約2 mm處放置融合器。使用專用弧形嵌片沖擊器將自鎖嵌片沿凹槽插入上下位椎體內。經透視確認雙插片及融合器位置良好后,常規負壓引流,關閉傷口。鈦板組:同樣方法減壓植骨后將融合器植入病變的椎間隙,C臂機透視下達到理想位置后進行加壓,根據患者椎間隙情況選擇合適的鈦板固定于病變椎間隙的上下位椎體前緣,經透視確認鈦板及融合器位置良好后,常規負壓引流,關閉傷口。兩組術后均常規予抗感染及營養神經等對癥處理,術后第2天視引流情況拔除引流管,囑患者佩戴頸托在家人陪同下下地活動及功能鍛煉,術后1周根據切口情況予以拆線,出院后1、2、3、6個月至徐州醫科大學附屬醫院門診復查,視結果確定摘除頸托時間,一般為12周左右。
1.3 觀察指標與方法 ①手術一般情況及術后并發癥:記錄每例患者手術時間及術中出血量。術后第6個月行頸椎三維CT檢查,觀察融合情況。比較兩組術后并發癥情況。②臨床功能恢復情況:采用日本骨科學會頸椎病評分表(JOA)和疼痛視覺模擬評分 (VAS)對比評價患者臨床功能恢復情況[4]。術后手術部位的吞咽困難根據Bazaz的標準進行分級評估[5]。③頸椎曲度、融合節段高度、病變椎間融合情況:頸椎的曲度選用Cobb′s角測量法當中的四線法即于頸椎側位X線延長C1、C7兩椎體下終板直線,再分別作出兩延長線的垂線,其兩垂線交叉所形成的銳角即為頸椎曲度[6]。融合節段的高度選用王良意等[7]頸前柱高度的測量方法,即測量自融合節段的上位椎體的前上緣至下位椎體的前下緣之間距離作為前柱高度。依據Vaccraro標準[8]于X線或CT三維重建進行評價病變椎間融合的情況:過伸過屈位X線片上頸椎有無不穩現象;椎間融合器與病變椎體上下終板之間有無明顯的透亮影;椎間融合器與病變椎體上下終板之間有無連續的骨小梁連接;與上一次檢查相比融合器有無移位。
2 結果
2.1 兩組手術一般情況及術后并發癥比較 45例患者均順利完成手術。ROI-C組、鈦板組手術時間分別為(129±25)、(172±29)min,術中出血量分別為(88±29)、(151±33)mL,兩組比較,P均<0.05。兩組圍手術期間生命體征平穩,術后經透視觀察兩組內固定裝置系統均在位良好且無嚴重并發癥出現。術后麻醉清醒后1周,ROI-C組14例出現不同程度的吞咽不適感,鈦板組18例出現不同程度的吞咽不適感,未予特殊處理,約2周后癥狀基本消失;ROI-C組1 例出現聲音嘶啞,鈦板組3例出現聲音嘶啞,3周后癥狀消除。住院期間45例患者的手術切口均Ⅰ期/甲級愈合,左側髂骨區無疼痛,感覺無異常,切口無感染等并發癥出現。
2.2 兩組臨床功能恢復情況 手術后兩組JOA評分、VAS評分分別較術前提高,差異均有統計學意義(P均<0.05);術后同時間點兩組JOA評分比較差異均無統計學意義(P均>0.05),見表1、表2。
2.3 兩組頸椎曲度、融合節段高度、病變椎間融合情況比較 兩組術后頸椎Cobb′s角比較差異均有統計學意義(P<0.05),見表3。兩組手術前后椎間隙高度比較差異均無統計學意義(P均>0.05),見表4。兩組末次隨訪時均植骨融合。
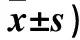
表1 兩組手術前后JOA評分比較(分,
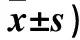
表2 兩組手術前后VAS比較(分,

表3 兩組手術前后Cobb′s角比較

表4 兩組手術前后手術節段椎間隙高度比較
3 討論
ACDF自Robinson于1955年首次報道以來,已獲得不斷改進和發展,越來越受到脊柱外科醫生推崇,成為前路椎間融合的金標準[9]。近年來,研究者們開發了新的替代穩定裝置,即零切跡雙插片自穩融合器,由兩個固定嵌片與一個融合器組成的裝置系統。理想的頸椎椎間融合器應做到提供即時穩定性,保持脊柱對齊和椎間孔高度,達到相等或者更高的融合成功率,并且減少自體移植物所帶來的并發癥等[10]。鈦或碳素纖維籠已廣泛用于頸椎椎間融合術,但有報道顯示易發生沉陷、遷移和結構破壞[11]。聚醚醚酮(PEEK)是不可吸收的生物聚合物應被應用于各行業。PEEK籠具有生物相容性,射線可透過性,且其彈性模量與人體骨骼相近。與帶有鈦板螺釘的ACDF相比較,ROI-C的置入可以避免患者體內存留較多的手術硬件,此外與鈦板的ACDF相比,ROI-C不僅是更小的手術切口,還可使椎間隙前的暴露范圍減小,這樣可減少解剖對椎間隙前的組織損傷[10]。鈦板的安裝需要延長手術的顯露范圍,因而增加了損傷肌肉、血管與神經的風險,尤其在長節段固定過程中。因此,ACDF最常見的并發癥之一是術后慢性吞咽困難,雖然ACDF術后慢性吞咽困難的原因尚未明確,但提出幾種機制。麻醉時的氣管插管損傷,在手術過程中過分的牽拉椎前組織,術后鈦板及瘢痕組織對食管與氣管的損傷等,甚至有報道食管穿孔的事件[12]。食管吞咽困難絕大部分患者在術后3個月緩解,對于癥狀長時間不緩解或緩解不明顯的情況則有可能是鈦板與食道反復摩擦或與周圍軟組織粘連形成等[13]。本研究ROI-C組吞咽困難發生率遠低于鈦板組,只有1例患者術后6個月感到中度吞咽困難,并在術后半年的回訪中癥狀已消失。Yamagata等[14]報道,ACDF后早期吞咽困難發生率在2%~67%,有可能是術后軟組織腫脹或者鈦板的直接導致。
在ACDF術中應用ROI-C,手術步驟得到了簡化,無需經前路對鋼板螺釘進行鉆孔、攻絲等步驟,縮短了手術時間,避免了術中長時間的牽拉喉返神經,同時避免了進行減壓植骨融合內固定的操作空間相對較小的問題,從而不需要顯露較大的操作范圍及牽拉較多的軟組織。因此,能縮短手術時間并減少術中出血,本研究結果顯示,ROI-C組手術時間及術中出血量均明顯低于鈦板組。
Lee等[15]報道了運用零切跡自鎖式頸椎融合器的融合率為93.6%。本組手術患者術后6個月的融合率為95.48%。至末次隨訪時,患者影像學資料均顯示已達到骨性融合標準,并未發現存在融合器及固定嵌片松動或塌陷的情況。高融合率與融合器獲得可靠的穩定性有關,已有生物力學研究證實自鎖式頸椎融合器的穩定性能與聯合鋼板內固定在生物力學強度方面無明顯統計學差異[16]。
前入路頸椎減壓植骨融合內固定術后改善并維持頸椎生理曲度和椎間隙高度有利于良好臨床療效的獲得。生理曲度和椎間高度的丟失會引起頸椎生物力學的異常,進而導致頸部后方軟組織的勞損,并加速相鄰節段退變。嚴重的頸椎后凸會造成脊髓神經損害。有研究觀察了ACDF頸椎曲度及節段序列與預后的關系,結果表明頸椎曲度及節段序列的維持或改善能明顯改善手術預后,同時有學者研究證實最大限度地改善頸椎曲度并維持正常的椎間隙高度可顯著降低患者術后軸性癥狀的發生[17]。本研究兩種術后頸椎生理曲度與手術節段椎間隙高度較術前均明顯改善,至末次隨訪時,患者的頸椎生理曲度與手術節段椎間隙高度得到維持,均獲得滿意的早期臨床效果。但術后鈦板組Cobb′s角低于ROI-C組,且兩組間差異有統計學意義。究其原因可能是鈦板的曲度很難完全與椎體前緣貼合,且鈦板長度一定程度上限制了頸椎前屈及后伸,從而影響到椎體曲度。
ACDF遠期并發癥主要是鄰近節段的退行性病變。有調查顯示,ACDF中不使用鎖定鈦板比使用鎖定鈦板鄰近節段退變發生率低。目前尚未明確其機制,有關研究發現生物力學的改變加速了退變的發生,與ACDF后鄰近節段活動度增加,導致相鄰節段應力分布改變以及與椎間盤負荷增加等相關[16]。同時鈦板亦會損傷其后方的前縱韌帶與纖維環前方的軟組織,導致鄰近節段骨化,從而加快鄰近節段退變的進程。且隨著融合節段的增加,鎖定鋼板的應力阻擋將會導致融合率下降并可能導致假關節形成[18],易致鋼板的松動,甚至發生螺釘進入椎間隙等情況。
綜上所述,ACDF中應用ROI-C安全有效,具有操作簡便、術中出血少等優勢,有助于改善頸椎曲度和椎間隙高度,圍手術期患者吞咽不適和聲音嘶啞發生率較低。但本研究的隨訪時間短,病例數較少。ROI-C的遠期療效和并發癥需進一步大規模前瞻性對照研究驗證。

