μ-T圖解析及其對(duì)依數(shù)性和二元相圖的分析
陳 平,李 睿,吳振玉,古莉娜,李 村
(安徽大學(xué)化學(xué)化工學(xué)院,安徽合肥230601)
狹義的化學(xué)勢(shì)概念是等溫等壓下體系不做非體積功時(shí)一切相平衡與化學(xué)平衡的判據(jù)[1-4],以相平衡為例,必須所有物質(zhì)在所分布的所有相中化學(xué)勢(shì)都相等。抓住了相平衡的本質(zhì),可以用化學(xué)勢(shì)關(guān)于溫度作圖的圖解法分析討論二組分在定壓下溫度-組成圖以及稀溶液依數(shù)性的一些問(wèn)題,結(jié)論直觀,對(duì)理解和學(xué)習(xí)化學(xué)勢(shì)、依數(shù)性以及相圖很有幫助。
1 μ-T關(guān)系及其相關(guān)結(jié)論
1.1 研究模型
設(shè)物質(zhì)A與B能形成混合物。純物質(zhì)A與B及其混合物滿(mǎn)足以下條件:(1)能夠被明確地區(qū)分出固、液、氣三態(tài)。(2)研究所涉及到的相變均為一級(jí)相變。(3)當(dāng)混合物具體到某一相態(tài)時(shí),在所研究的濃度范圍內(nèi)為均勻單相并且混合物至少有一種物質(zhì)的化學(xué)勢(shì)能夠以μ(T,P,x)=μ*(T,P)+RTlnx的形式表達(dá),其中μ(T,P,x)是指在溫度(T)、壓強(qiáng)(P)、摩爾分?jǐn)?shù)為x時(shí),該物質(zhì)在該相態(tài)的化學(xué)勢(shì),μ*(T,P)是指該物質(zhì)處于同相態(tài)時(shí)的純物質(zhì)在溫度(T)和壓強(qiáng)(P)下的化學(xué)勢(shì)。
1.2 相關(guān)結(jié)論
1.2.1 相關(guān)結(jié)論一
1.2.2 相關(guān)結(jié)論二
由于溫度升高,SA,m變大,則-SA,m減小,得到結(jié)論:定壓下純物質(zhì)A的化學(xué)勢(shì)關(guān)于溫度的函數(shù)圖像的斜率隨溫度升高而減小。
1.2.3 相關(guān)結(jié)論三
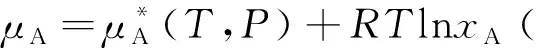
1.3 μ-T圖示
根據(jù)結(jié)論一與結(jié)論二先作某一相態(tài)純物質(zhì)A的定壓下化學(xué)勢(shì)關(guān)于溫度的函數(shù)圖像,如圖1(a)可見(jiàn),函數(shù)圖像隨溫度單調(diào)遞減并且斜率隨溫度升高而下降,即溫度升高曲線變陡,這里為了便于說(shuō)明問(wèn)題特意將曲線畫(huà)得較為陡峭,以下圖示也是這樣。
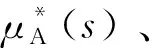
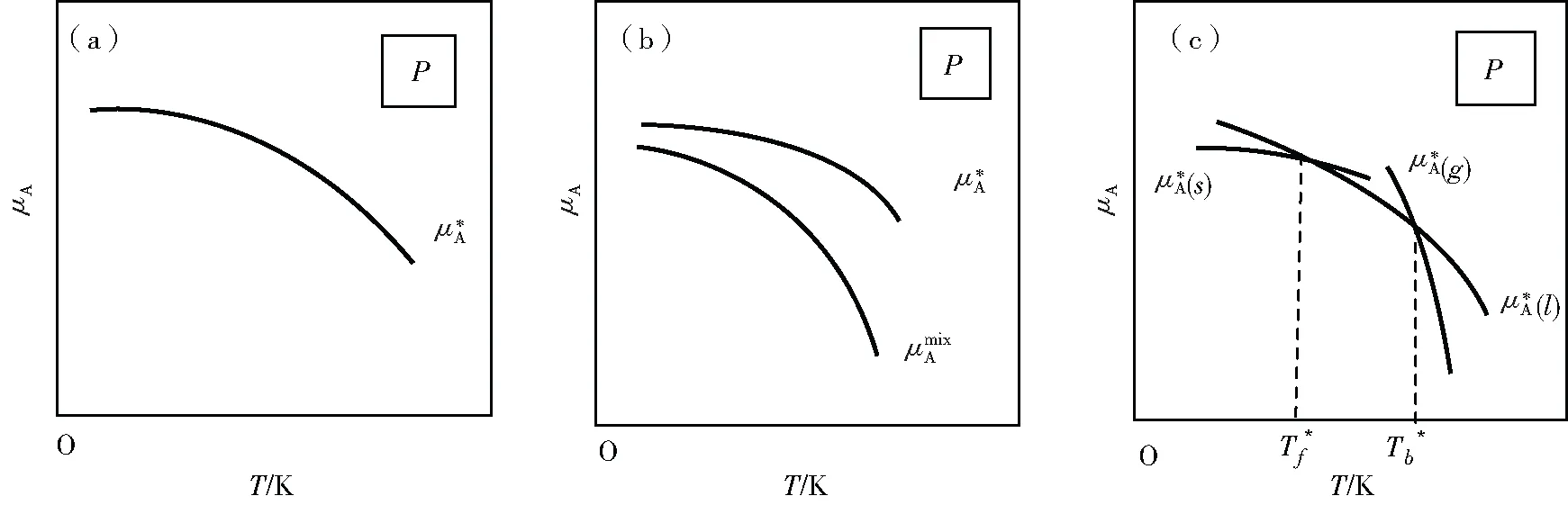
圖1 物質(zhì)A的化學(xué)勢(shì)與溫度關(guān)系圖
2 μ-T圖解析和應(yīng)用討論
2.1 μ-T圖解法對(duì)稀溶液依數(shù)性的解釋
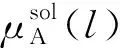
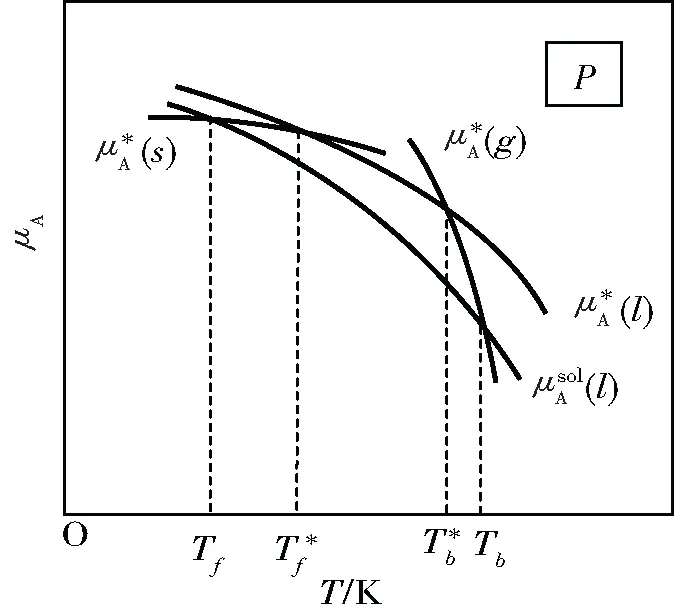
圖2 稀溶液中溶劑的凝固點(diǎn)降低和沸點(diǎn)升高與溶劑的化學(xué)勢(shì)關(guān)系示意圖
2.2 μ-T圖解法對(duì)二組分理想溶液T-x相圖(氣液兩相)的分析
首先,研究的模型是物質(zhì)A與物質(zhì)B組成理想溶液,以及A與B組成的理想氣體達(dá)到了相平衡,也就是說(shuō)A與B的化學(xué)勢(shì)都能以μ(T,P,x)=μ*(T,P)+RTlnx形式表達(dá)。化學(xué)勢(shì)圖像法在這里解釋了氣相與液相組成的大小情況與沸點(diǎn)之間的聯(lián)系。
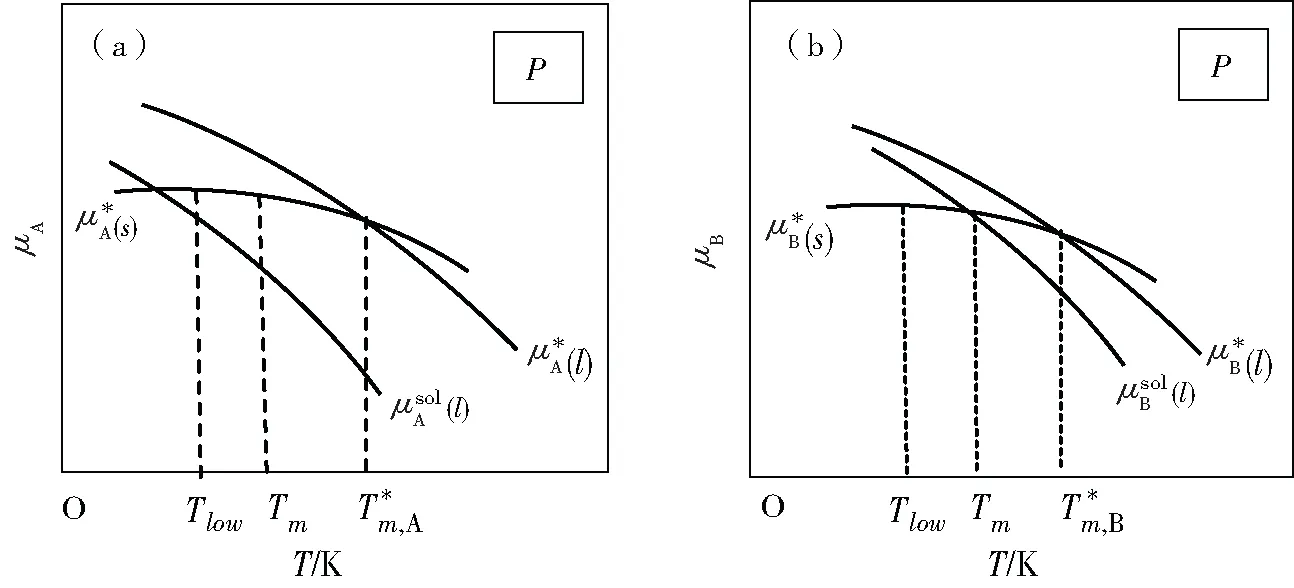
設(shè)在A與B的混合溶液中A的含量為xA,那么在壓強(qiáng)P時(shí)可以分別將溶液中的A、純液態(tài)A、純氣態(tài)A的μ-T曲線作在同一圖上,如圖3所示。
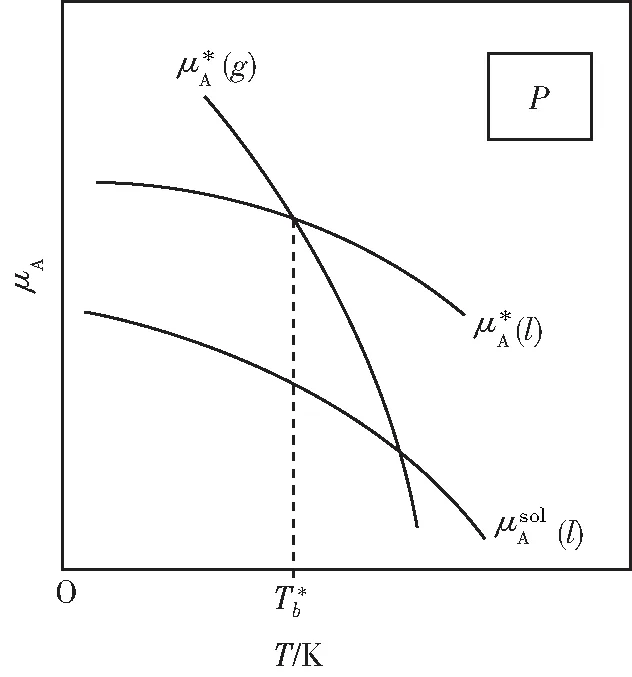
圖3 物質(zhì)A在溶液相中和純A固相、氣相的化學(xué)勢(shì)與溫度關(guān)系圖
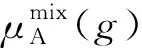
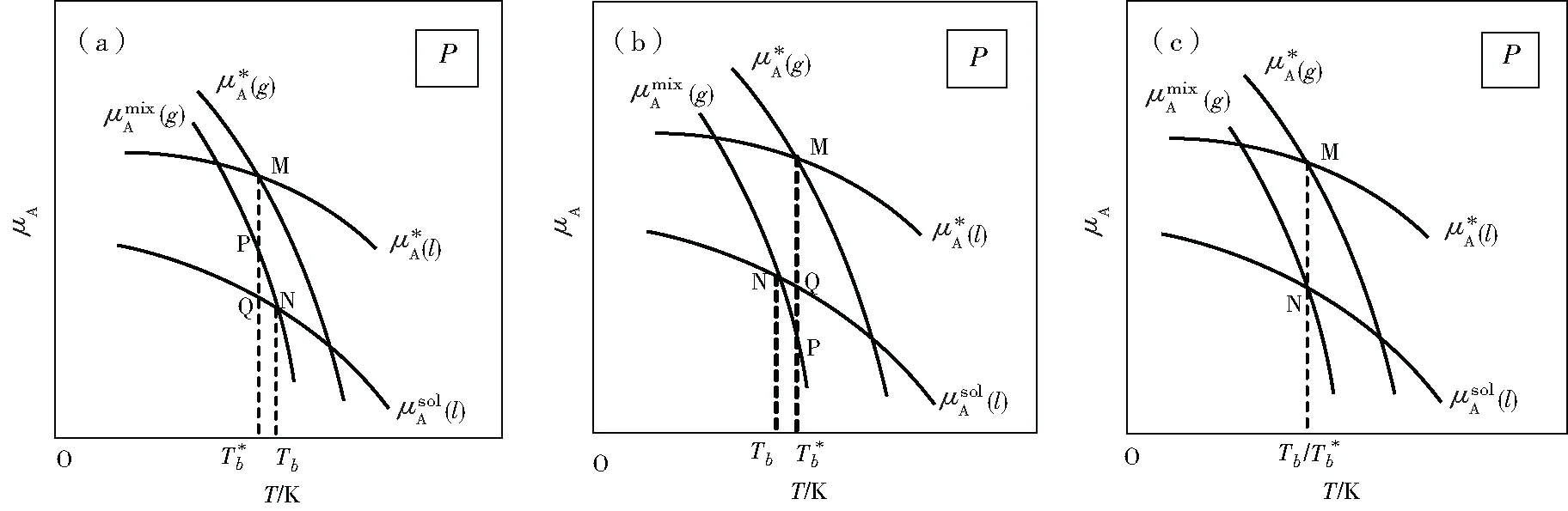
圖線由上自下移動(dòng)出現(xiàn)的三種情況
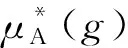
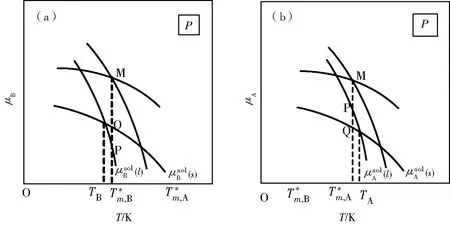
第一種情況如圖4(a):B組分飽和蒸氣壓較小,B在氣相中的摩爾分?jǐn)?shù)yB較小,使yA下降幅度較小,導(dǎo)致混合氣體中A的化學(xué)勢(shì)下降幅度較小。P點(diǎn)化學(xué)勢(shì)高于Q點(diǎn),出現(xiàn)沸點(diǎn)升高現(xiàn)象。

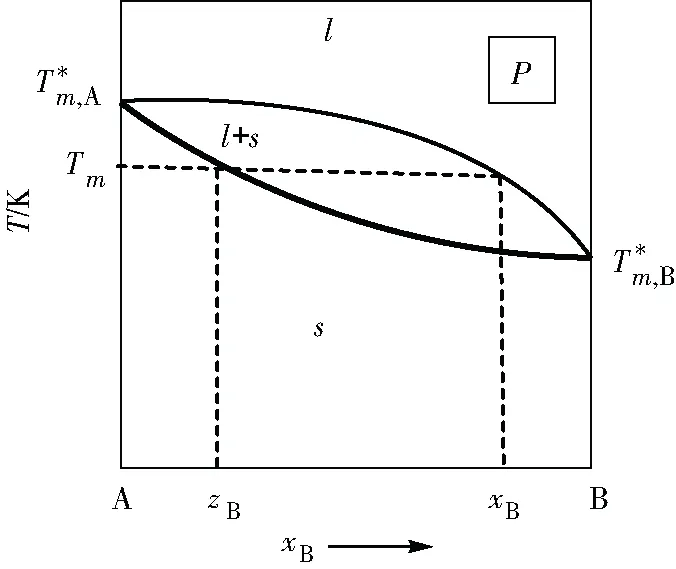
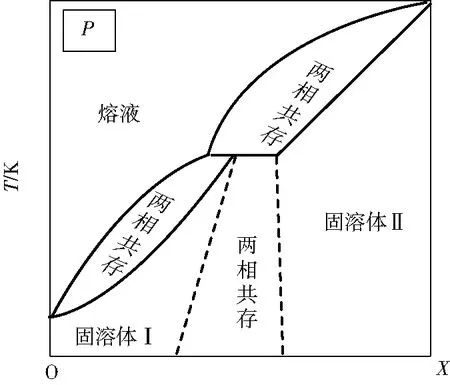
第二種情況如圖4(b):B組分飽和蒸氣壓較大,B在氣相中的摩爾分?jǐn)?shù)yB較大,使yA下降幅度較大,導(dǎo)致混合氣體中A的化學(xué)勢(shì)下降幅度較大。P點(diǎn)化學(xué)勢(shì)低于Q點(diǎn),出現(xiàn)沸點(diǎn)降低現(xiàn)象。同理可以得到:yA 第三種情況如圖4(c):A在氣相中與液相中化學(xué)勢(shì)下降數(shù)值相同,沸點(diǎn)不變。此時(shí)在相平衡點(diǎn)N上氣液兩相yA=xA。如果是一對(duì)旋光異構(gòu)體能形成理想溶液且沸點(diǎn)相同就會(huì)出現(xiàn)圖4(c)的情況。 以上分析結(jié)果在理想液態(tài)混合物的T-x相圖中都有體現(xiàn),如圖5(a)。 圖5 理想液態(tài)混合物的T-x相圖 圖6 簡(jiǎn)單低共熔二元相圖及其組成與化學(xué)勢(shì)關(guān)系示意圖 圖7 低共熔點(diǎn)溶液中A與B化學(xué)勢(shì) 同理,此時(shí)因?yàn)樵赥m時(shí)純固體B已經(jīng)和溶液中B化學(xué)勢(shì)相等,而純固體A化學(xué)勢(shì)高于溶液相A的化學(xué)勢(shì),因此在熔點(diǎn)Tm時(shí)只有純B固相與溶液相達(dá)到相平衡。綜合上述用化學(xué)勢(shì)圖像法解釋了液相為什么只有在組成xB為a時(shí)才與純物質(zhì)A固相、純物質(zhì)B固相達(dá)到相平衡,而在其他組成只與純物質(zhì)A固相或純物質(zhì)B固相達(dá)到相平衡,這個(gè)例子同時(shí)也強(qiáng)調(diào)了相平衡條件指的是所有分布了這種物質(zhì)的相里,該物質(zhì)化學(xué)勢(shì)要在各相中相等,并不是指所有物質(zhì)在所有相中化學(xué)勢(shì)相等。 圖8 xB介于a到1時(shí)溶液中A與B化學(xué)勢(shì)關(guān)系示意圖 圖9是理想二組分液固兩相都完全互溶的相圖。 圖9 理想二組分液固兩相都完全互溶的T-x相圖 設(shè)有相平衡B(s,zB=a+δ)+A(s,zA=1-a-δ)B(l,xB=a)+A(l,xA=1-a),讓低熔點(diǎn)的B在固溶體中含量高于熔液中含量δ,讓高熔點(diǎn)的A在固溶體中低于熔液中含量δ,這里a與δ都為正數(shù)且兩數(shù)之和小于1。將B純固體化學(xué)勢(shì)純液體化學(xué)勢(shì)固溶體中化學(xué)勢(shì)熔液中化學(xué)勢(shì)關(guān)于溫度的關(guān)系曲線作在一張圖上,如圖10(a)所示;將A純固體化學(xué)勢(shì)純液體化學(xué)勢(shì)固溶體中化學(xué)勢(shì)熔液中化學(xué)勢(shì)關(guān)于溫度的關(guān)系曲線作在一張圖上,如圖10(b)所示。 圖10 各相中A與B化學(xué)勢(shì)情況 在熔液與固溶體都是理想的混合物的情況下,相平衡時(shí)高熔點(diǎn)組分固溶體含量大于熔液中含量,產(chǎn)生凝固點(diǎn)下降現(xiàn)象;低熔點(diǎn)組分熔液中含量大于固溶體中含量,產(chǎn)生凝固點(diǎn)升高現(xiàn)象。如圖11是固態(tài)部分部分互溶的二組分相圖(具有一轉(zhuǎn)熔溫度),兩類(lèi)固溶體與熔液的相平衡的兩個(gè)部分中把固溶體和熔液近似看成是理想混合物,那么上述結(jié)論仍然成立。 圖11 固態(tài)部分部分互溶的二組分T-x關(guān)系示意圖 為了加強(qiáng)對(duì)化學(xué)勢(shì)、稀溶液的依數(shù)性、相圖等知識(shí)點(diǎn)的學(xué)習(xí)理解,本文根據(jù)化學(xué)勢(shì)的定義推導(dǎo)出相關(guān)結(jié)論,得到了化學(xué)勢(shì)與溫度關(guān)系的圖示,并根據(jù)相關(guān)圖示分析和解釋了依數(shù)性和幾類(lèi)簡(jiǎn)單的二組分相圖,使相圖的教學(xué)、學(xué)習(xí)和分析不僅僅局限于課本的表述,也可以從化學(xué)勢(shì)的理論上進(jìn)行分析,為從理論分析繪制相圖提供了一種思路,使教學(xué)和學(xué)習(xí)更有意義。
2.3 μ-T圖解法對(duì)簡(jiǎn)單的低共熔二元相圖分析
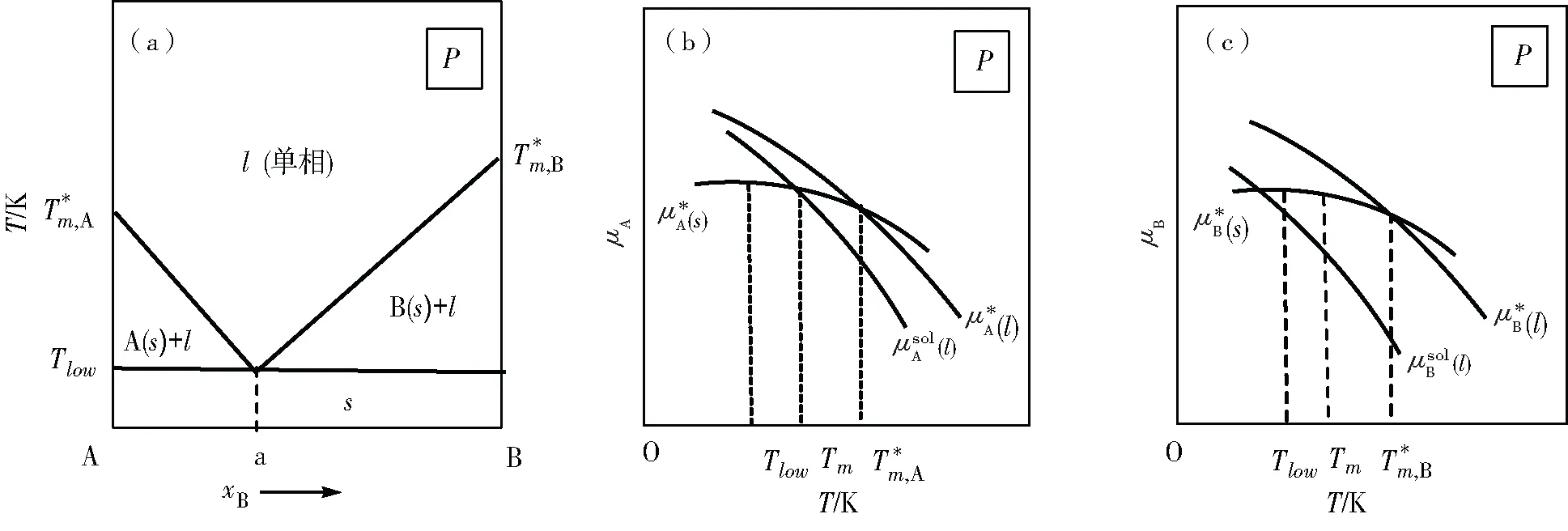
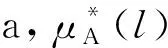
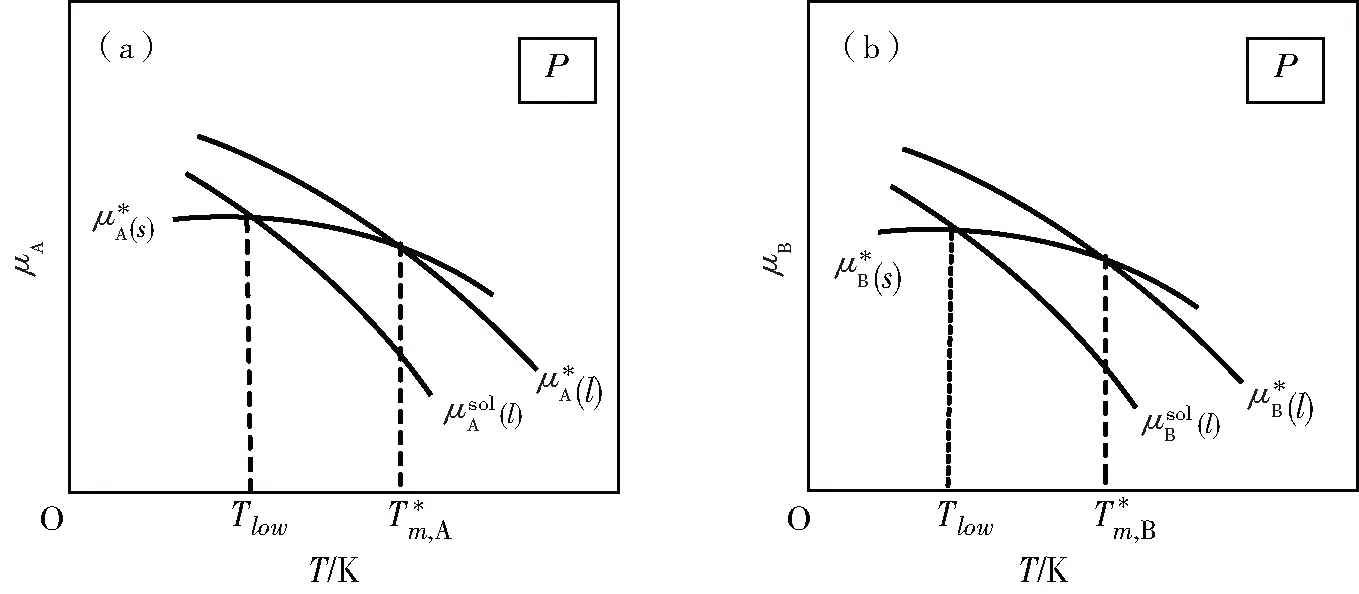
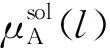
2.4 理想的二組分液相與固溶體相平衡的分析
3 結(jié)語(yǔ)

