lncRNAs在糖尿病大鼠肺纖維化中的作用機制及利拉魯肽對其防治作用
周蕾 張雅中 房輝 秦江媛
(唐山市工人醫院內分泌二科,河北 唐山 063000)
近年來,糖尿病(DM)肺纖維化越來越受到重視。DM肺纖維化的患者存在肺彌散功能障礙及通氣功能障礙〔1〕。長鏈非編碼(lnc)RNAs參與多種器官纖維化的生物學過程,在DM肺纖維化的發病過程中起重要的調控作用〔2〕。異常表達的 lncRNAs可能成為新的治療靶點。本實驗通過觀察lncRNAs在DM大鼠肺組織的表達及利拉魯肽的干預作用,研究lncRNAs在DM肺纖維化中的發生作用及利拉魯肽對其新的作用機制。
1 材料與方法
1.1實驗動物 選用6~8周齡健康SPF(無特定病原體動物)級Sprague-Dawley(SD)雄性大鼠60只,體重(BW)180~220 g,由河北聯合大學附屬醫院實驗動物中心提供(使用證明編號:MY06DXK07)。
1.2主要實驗試劑及儀器 利拉魯肽注射液(北京諾和諾德(中國)制藥有限公司),鏈脲佐菌素(STZ,美國Sigma公司),兔抗大鼠轉化生長因子(TGF)-β1多克隆抗體、兔抗大鼠Wnt3a多克隆抗體、兔抗大鼠β-catenin多克隆抗體、SABC試劑盒、二氨基聯苯胺(DAB)顯色試劑盒(美國Abcam公司),逆轉錄試劑盒(美國Invitrogen公司),血糖儀及血糖檢測試紙條(德國羅氏公司)。
1.3動物分組與處理 取雄性 SD大鼠(河北聯合大學實驗動物中心)50只。其中40只腹腔單次注射STZ 60 mg/kg誘導建立DM模型,對照(NC)組腹腔注射等量上述枸櫞酸緩沖液,72 h后尾靜脈采血測定空腹血糖(FPG),FPG≥16.7 mmol/L視為造模成功,將造模成功的30只大鼠隨機分為DM組、DM+利拉魯肽低劑量組〔400 μg/(kg ·d),DM+LL組〕、DM+利拉魯肽高劑量組〔800 μg/(kg·d),DM+HL組〕,治療8 w(腹腔注射利拉魯肽0.225 μg/g體重,2 次 /d)〔3〕。
1.4標本收集與處理 在禁食12 h后,取大鼠尾末梢毛細血管全血測定FPG;天平稱重大鼠BW,均為1次/w。殺檢前1天空腹尾靜脈取血測定糖化血紅蛋白(HbA1c)、動脈取血測定氧分壓(PaO2)、血氧飽和度(SaO2)及二氧化碳分壓(PaCO2)。麻醉大鼠取肺組織,標記后放置-80℃保存。
1.5免疫組化染色 按照SP試劑盒說明檢測各組TGF-β1、Wnt3a、β-catenin蛋白表達情況。免疫組化染色后半定量分析采用 Imag proplus5.0 圖像分析系統進行光密度分析,棕黃色顆粒為陽性信號。
1.6RT-PCR法檢測lncRNAs-H19 mRNA表達 取新鮮冰凍組織,重量約100 mg,按照Trizol一步法提取RNA,測定RNA濃度和純度。取等量RNA逆轉錄得到cDNA,進行擴增。
1.7統計學方法 采用SPSS17.0軟件進行單因素方差分析。
2 結 果
2.1各組FPG、HbA1c、BW及血氣比較 與NC組比較,DM組FPG、HbA1c、BW差異有統計學意義(P<0.05)。DM+LL、DM+HL組FPG及HbA1c水平顯著低于DM組,PaO2及SaO2顯著高于DM組,PaCO2顯著低于DM組(P<0.05),且DM+HL組血糖降低效果更明顯,見表1。

表1 各組血糖、HbA1c、BW及血氣比較
與NC組比較:1)P<0.05;與DM組比較:2)P<0.05;與DM+LL組比較:3)P<0.05
2.2肺組織病理學變化 蘇木素-伊紅(HE)染色顯示,與NC組比較,DM組肺組織結構紊亂,肺泡間質及毛細血管基底膜增厚,部分肺泡腔萎縮甚至塌陷。見圖1。
2.3免疫組化結果 TGF-β1、Wnt3a、β-catenin在肺間質中呈間斷不連續分布表達于肺間質及血管上皮細胞核周圍的胞質。DM組TGF-β1、Wnt3a、β-catenin表達的平均光密度值顯著高于NC組(P<0.01),DM+LL、DM+HL組顯著低于DM組(P<0.01),DM+HL組顯著低于DM+LL組(P<0.01),見表2,圖2。

表2 各組TGF-β1、Wnt3a、β-catenin比較
與NC組比較:1)P<0.01;與DM組比較:2)P<0.01;與DM+LL組比較:3)P<0.01
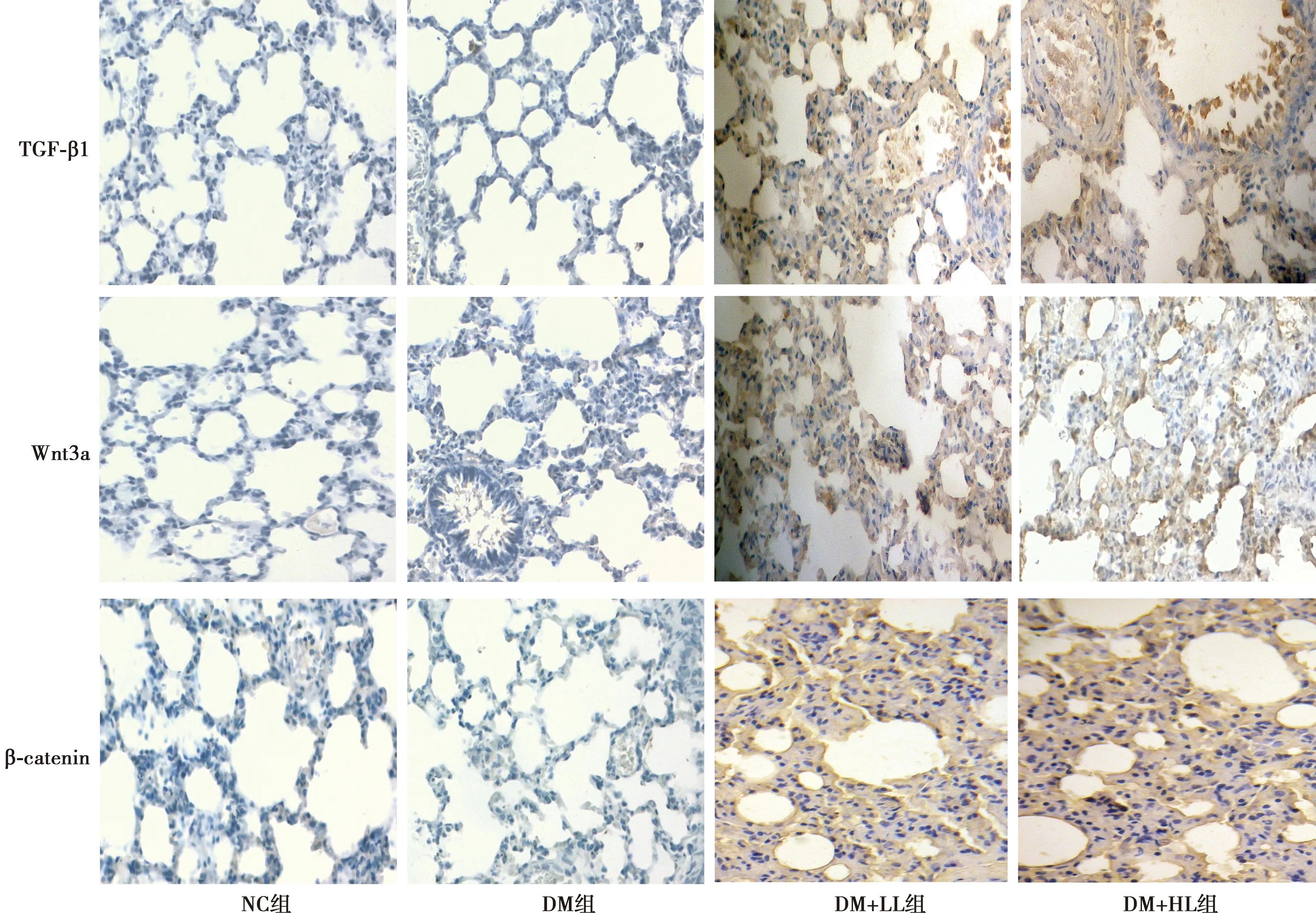
圖2 各組免疫組化檢測TGF-β1、Wnt3a、β-catenin在肺組織中的表達(免疫組化,×40)
2.4lncRNAs-H19在各組肺組織中mRNA表達比較 與NC組相比較,lncRNAs-H19 mRNA的表達在DM組增高2.95倍;與DM組比較,DM+LL組下降1.21倍,DM+HL組下降2.0倍,差異有統計學意義(P<0.05),見圖3。

1~4:NC組、DM組、DM+LL組、DM+HL組圖3 各組肺組織中lncRNAs-H19 mRNA表達
3 討 論
血糖代謝在不同組織和器官有不同且復雜的生物化學過程,研究表明,DM肺纖維化是DM慢性并發癥中另一個重要的組織病變〔4〕。而lncRNAs在高糖環境下發揮關鍵作用〔5〕,研究證實lncRNAs參與了眾多病理生理學過程,如細胞分化與個體發育、腫瘤的發生與遷移及器官與組織纖維化等〔6,7〕。lncRNAs-H19是最先被報道的lncRNAs 之一〔8〕,高濃度H19在器官和組織纖維化的形成中發揮了重要作用。lncRNA-H19能夠通過調控TGF-β蛋白的表達來影響其下游相關信號傳導通路的相關表達。TGF-β1是各個器官和組織中最重要的致纖維化因子〔9,10〕。
Wnt信號通路是一條含有高度保守的堿基序列的信號通路,由 Wnt 相關蛋白及下游的靶基因組成。研究顯示,抑制 Wnt/β-catenin 信號通路可降低肺纖維化的發生發展〔11〕。Wnt蛋白是細胞中重要的調控者,Wnt3a是Wnt蛋白家族一員,主要通過旁分泌、 自分泌方式釋放于胞外,并結合細胞表面受體,激活下游信號產生級聯效應〔12〕。
本研究通過基因和蛋白水平驗證,DM肺纖維化可能與lncRNAs-H19過度表達有關。同時DM大鼠肺組織TGF-β1、Wnt、β-catenin蛋白活性增加,提示lncRNAs-H19的過多表達激活TGF-β1上調 Wnt/βcatenin 信號通路增加了DM肺組織纖維化的進程。而經過利拉魯肽治療后,lncRNAs-H19表達量下降,繼之通過TGF-β1下調 Wnt/βcatenin 信號通路,并隨治療濃度的增大效果更為顯著。
綜上,DM大鼠肺組織中異常表達的 lncRNAs可能是導致DM肺纖維化的重要途徑,而利拉魯肽能降低其表達,且呈濃度依賴性。

