SUZ12過表達及敲減惡性外周神經鞘瘤穩定細胞株的建立及其意義
張 靜 ,高 雅 ,李新宇 ,朱香熹 ,孫碩遙 ,肖 可 ,王 靜 ,劉嘉岳 ,趙玉龍 ,李光明 ,朱 澤
(1.天津醫科大學病原生物學系,天津300070;2.天津醫科大學基礎醫學院,天津300070;3.遵義醫科大學珠海校區臨床醫學系,珠海519090;4.多倫多大學圣喬治校區,多倫多ONM5S)
惡性外周神經鞘瘤(malignant peripheral nerve sheath tumor,MPNST)是一類具有高度惡性,發展迅速,易轉移復發且預后差的侵襲性軟組織肉瘤,約占所有軟組織肉瘤的5%~10%,其中將近50%的MPNST與NF1基因相關,NF1的病人一生中有10%~15%的風險轉變成MPNST[1-4]。另外,腫瘤抑制因子(TP53和p16INK4A)的喪失和生長因子受體信號(例如EGFR或PDGFR)過度激活在神經纖維瘤的惡性轉化中也起著重要作用。因此,基于這種關聯,MPNST最經典基因學研究大多集中在NF1基因的缺失以及TP53和CDKN2A/p16基因的缺失上[5]。然而最近的一些對MPNST病人的組織標本進行二代測序的研究結果顯示,在MPNST中PRC2的組成單元SUZ12和EDD的突變失活也屬頻發事件[5-9]。PRC2可以調節組蛋白H3的27位點上的酪氨酸三甲基化,而SUZ12作為PRC2復合體的重要組分,可以通過穩定PRC2復合體保證H3K27me3在表觀遺傳修飾過程中功能正常發揮。
CRISPR/Cas9是在細菌和古細菌中發現的一種獲得性免疫系統,通過crRNA識別、Cas蛋白裂解來抵抗病毒和噬菌體的入侵,因其敲除效率高,脫靶率低,敲除效果穩定的優點被用于替代傳統的TALEN技術和ZEN技術,已成為一種主流的基因編輯工具[10-11]。因此,為了進一步研究SUZ12基因在MPNST中的作用,筆者使用慢病毒載體構建SUZ12過表達及CRISPR/Cas9敲減的MPNST穩定細胞株,為針對SUZ12在MPNST中的生物學功能、作用機制和疾病診斷治療的進一步研究提供了實驗基礎。
1 材料與方法
1.1 主要材料和試劑 ST88-14細胞株由天津醫科大學腫瘤醫院楊吉龍教授饋贈;293T細胞和大腸桿菌由本實驗保存;胎牛血清、DMEM培養基購自美國Gibco公司;慢病毒載體系統(GV492、GV371、pHelper1.0、pHelper2.0),Lenti-CAS9-puro 慢病毒購自上海吉凱公司;質粒抽提試劑盒購自Promega公司;TOP10感受態細胞購自Genechem公司;FastQuant RT Kit、SuperRealPreMix Plus購自天根公司;SUZ12引物由北京索真公司合成;MTT試劑盒購自索萊寶公司。
1.2 細胞培養 MPNST細胞系ST88-14在含10%的胎牛血清和1%的雙抗的DMEM完全培養基中培養,37℃,7.5% CO2溫箱中孵育。
1.3 SUZ12基因過表達載體的構建
1.3.1 SUZ12目的基因PCR擴增 SUZ12基因PCR擴增引物,正向引物:5′-AGGTCGACTCTAGA GGATCCCGCCACCATGGCGCCTCAGAAGCACGGC GGTG-3′,反向引物:5′-TCCTTGTAGTCCATACCG AGTTTTTGTTTTTTGCTCTGTTTTG-3′,擴增產物為2 261bp。PCR 體系反應條件:98℃ 5 min,98℃ 10 s,55 ℃ 10 s,72 ℃ 90 s,循環 30次,72 ℃ 8 min。擴增完成后,1.5%瓊脂糖凝膠電泳測定結果。
1.3.2 過表達載體的構建 將GV492載體用BamHI/AgeI酶切,PCR產物與載體進行交換,構建重組質粒(設置一組不含SUZ12片段的質粒作為對照組)。重組質粒轉化入感受態細胞,將其涂布在含有氨芐青霉素的平板上,在37℃培養箱中培養過夜,之后進行菌落PCR的鑒定,正義鏈:5′-GATGTTAATGAAGGAGAGAAAG-3′,反義鏈:5′-CCTTATAGTCCTTATCATCGTC-3′。產物經1.5%瓊脂糖凝膠電泳,選取陽性克隆進行轉化,挑菌,質粒抽提,進行測序鑒定。
1.4 SUZ12敲減載體的構建
1.4.1 sgRNA靶位點的設計與合成 在NCBI中明確SUZ12基因的CDS外顯子區域,使用麻省理工學院的CRISPR設計工具(http//crispr.mit.edu/)設計3對SUZ12基因的sgRNA序列,并在其兩端加入BbsⅠ位點,序列見表1。引物退火形成帶有粘性末端的雙鏈,稀釋200倍后使用。
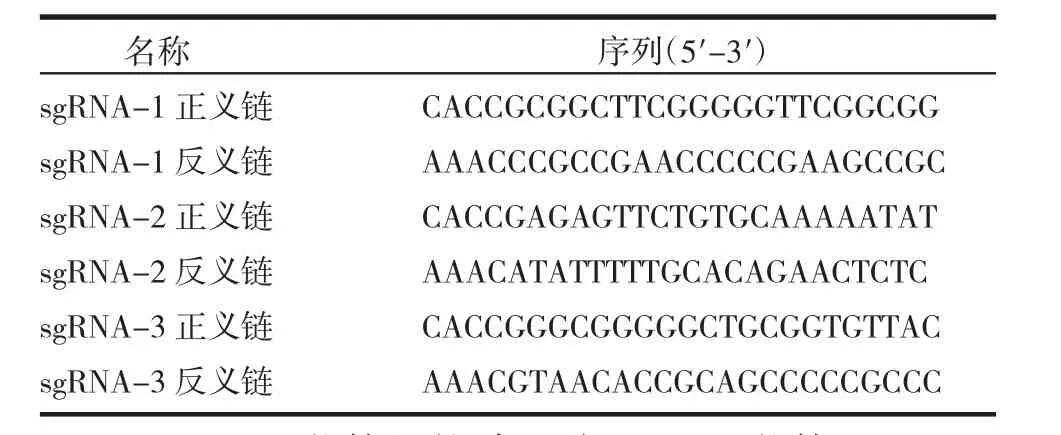
表1 3對特異性sgRNA序列Tab 1 3 pairs of specific sgRNA sequences
1.4.2 sgRNA載體的構建 將GV371載體用BbsⅠ酶切,與退火形成雙鏈的sgRNA混合,配置酶切連接反應體系進行連接,酶切體系:Vector plasmid(100 ng/μL)1 μL,Oligo 雙鏈 DNA(0.089 μmol/L)2 μL,10×Buffer Tango 2 μL,DTT(10 mmol/L)1 μL,ATP (10 mmol/L)1 μL,T7 DNA Ligase 0.5 μL,BbsI 1 μL,H2O 11.5 μL;將上述反應物置于 PCR 儀,37 ℃5 min,21 ℃ 5 min,16 ℃ 30 min,共 6 個循環。將連接產物轉化至TOP10感受態細胞中,接種到含Amp抗性的LB固體培養基上,37℃培養箱中過夜。挑菌,質粒抽提,進行測序鑒定。
1.5 慢病毒包裝與滴度測定
1.5.1 慢病毒包裝 將GV載體質粒、pHelper1.0載體質粒、pHelper 2.0載體質粒按照一定比例(20 μg∶15 μg∶10 μg) 加到 2.4 mL 的 Opti-MEM 和 100 μL的Lipofectamine2000中,共同轉染293T細胞,37℃、5% CO2培養箱中培養。48 h后收集293T細胞上清液,超速離心去除上清,加入病毒保存液,充分溶解后,高速離心,分裝上清,-80℃保存。
1.5.2 慢病毒的滴度檢測 測定前24 h,接種293T細胞到96孔板(4×104個/孔):在EP管中加入90 μL的無血清培養基,取待測的病毒原液10 μL加入到EP管中,倍比稀釋到最后一管;棄去293T細胞培養基,加入90 μL稀釋好的病毒溶液,37℃培養箱培養;24 h后加入完全培養基,96 h后觀察綠色熒光蛋白的表達情況。
1.6 確定慢病毒感染的最適MOI,以及嘌呤霉素(Puro)篩選的最適劑量
1.6.1 感染預實驗 ST88-14細胞在病毒感染前一天鋪板,至細胞匯合度為20%~30%;病毒于冰上融化,依次將病毒稀釋至滴度 1×108TU/mL,1×107TU/mL,1×106TU/mL,吸棄培養液加入病毒及相應感染增強液,混勻,繼續培養,12 h后換回常規培養基,繼續培養;感染72 h后,用熒光顯微鏡觀察感染效率。
1.6.2 確定嘌呤霉素的最適劑量 將ST88-14細胞接種于48孔板中,48 h后加入Puro進行篩選,Puro 濃度梯度設置為 0、0.5、1、2、4、6 μg/mL;Puro處理48 h后細胞全部死亡的最低藥物濃度作為篩選穩定株的藥物濃度。
1.7 慢病毒感染ST88-14細胞及穩定細胞株的建立1.7.1 過表達穩定株的構建 制備密度為3~5×104個/mL的ST88-14細胞懸液,每孔100 μL接種到96孔板中,37℃培養24 h;病毒冰上融化,根據預實驗MOI值進行稀釋;吸棄培養液加入病毒及相應感染增強液,在37℃、7.5% CO2溫箱中培養,12h后換回常規培養基,繼續培養;感染72 h后,加入2 μg/mL的Puro篩選48 h以上。之后降低Puro濃度到1 μg/mL,繼續對細胞進行篩選和擴增,同時收集細胞行下游RT-qPCR檢測。
1.7.2 CRISPR/Cas9敲除穩定株的構建 制備密度為 3~5×104個/mL 的細胞懸液,每孔 100 μL 接種到96孔板中,37℃培養24 h;Cas9病毒冰上融化,根據預實驗MOI值適當稀釋;吸棄培養液加入病毒及相應感染增強液,在37℃,7.5% CO2溫箱中培養,12 h后換回常規培養基,繼續培養;感染72 h后,加入2 μg/μL的 puromycin篩選至少 48 h以上,得到ST88-14-Cas9細胞。將ST88-14-Cas9細胞鋪6孔板,用含1 μg/mL劑量的Puro的完全培養基培養至30%,按照預實驗感染條件分別感染3個sgRNA的Lenti-sgRNA-GFP病毒,12 h后換回常規培養液,感染48~72 h后,在熒光顯微鏡下觀察綠色熒光的表達情況。用含1 μg/mL的Puro的完全培養基擴大培養,繼續傳代、擴增進行鑒定。
1.8 SUZ12過表達和敲減穩定株的鑒定
1.8.1 熒光顯微鏡觀察 用含1 μg/mL Puro篩選兩周后,用倒置熒光顯微鏡觀察綠色熒光蛋白的表達效率,并拍照。
1.8.2 RT-qPCR鑒定 用TRIzol提取SUZ12過表達組和敲減組總RNA,反轉錄得到cDNA,進行RT-qPCR 檢測,SUZ12 引物序列為:SUZ12-F:AGAAAACGAAATCGTGAGGATGG;SUZ12-R:GCAC GTAGGTCCCTGAGAAA。PCR反應體系為:cDNA template 4 μL,Primer F (20 μmol/L)2 μL,Primer R(20 μmol/L)2 μL,SYBR qPCR Master Mix 10 μL,Rox Dye 0.04 μL,加水至 20 μL;PCR 反應條件:98℃ 2 min,98℃ 10 s,68 ℃ 30 s,循環 40次,95 ℃ 15 s,60℃1 min,99℃15 s。每組實驗獨立重復3次。
1.9 SUZ12過表達和敲減組細胞增殖活性的測定 胰酶消化各組細胞,調整細胞濃度為1×104個/mL,每孔200 μL接種到96孔板;分別在 24、48、72 h后棄上清,加入90 μL完全培養基和10 μL MTT溶液,孵箱內繼續培養4 h;棄上清,每孔加入110 μL DMSO溶液,避光震蕩10 min,490 nm處測吸光度,繪制增長曲線。每組實驗獨立重復3次。
1.10 統計學處理 采用SPSS20.0處理數據,多組間均數比較采用方差分析。P<0.05有統計學意義。
2 結果
2.1 過表達重組質粒的鑒定結果 過表達重組質粒SUZ12的PCR產物經瓊脂糖凝膠電泳檢測后得到一個2 261bp的特異性條帶,與預期大小一致,見圖1。GV492載體經BamHI/AgeI酶切后與SUZ12基因構建重組質粒,轉化、涂板、挑菌后進行PCR鑒定,經瓊脂糖凝膠電泳分析,得到469bp的陽性轉化子,見圖2。酶切鑒定陽性的克隆經過測序,結果與NCBI中的人SUZ12基因(ID:23512)進行比對,序列一致,表明過表達重組載體構建成功。
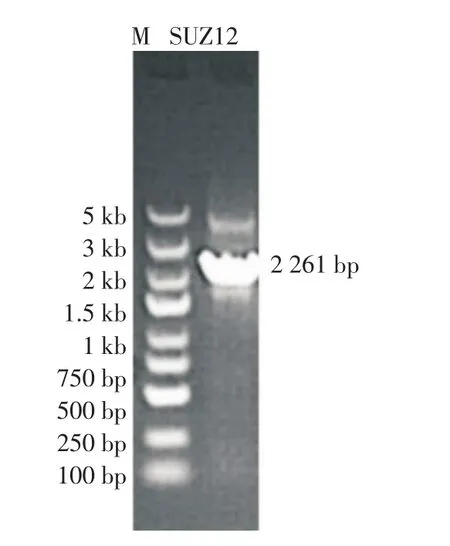
圖1 SUZ12基因擴增電泳圖Fig 1 PCR amplification of SUZ12
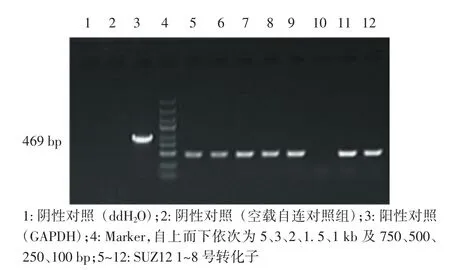
圖2 重組載體PCR產物鑒定及瓊脂糖凝膠電泳圖Fig 2 Identification of recombinant vector and agarose gel electrophoresis
2.2 CRISPR/Cas9表達載體的構建 為了提高敲除效率,設計并合成了3條sgRNA靶向序列,載體GV371(U6-sgRNA-SV40-EGFP)BbsⅠ酶切后,分別與退火獲得的3個目的片段sgRNA連接過夜,轉化TOP10感受態細胞、涂板、挑菌、質粒抽提、送測序鑒定。測序結果表明插入的片段序列與設計合成的靶向SUZ12序列一致,見圖3。
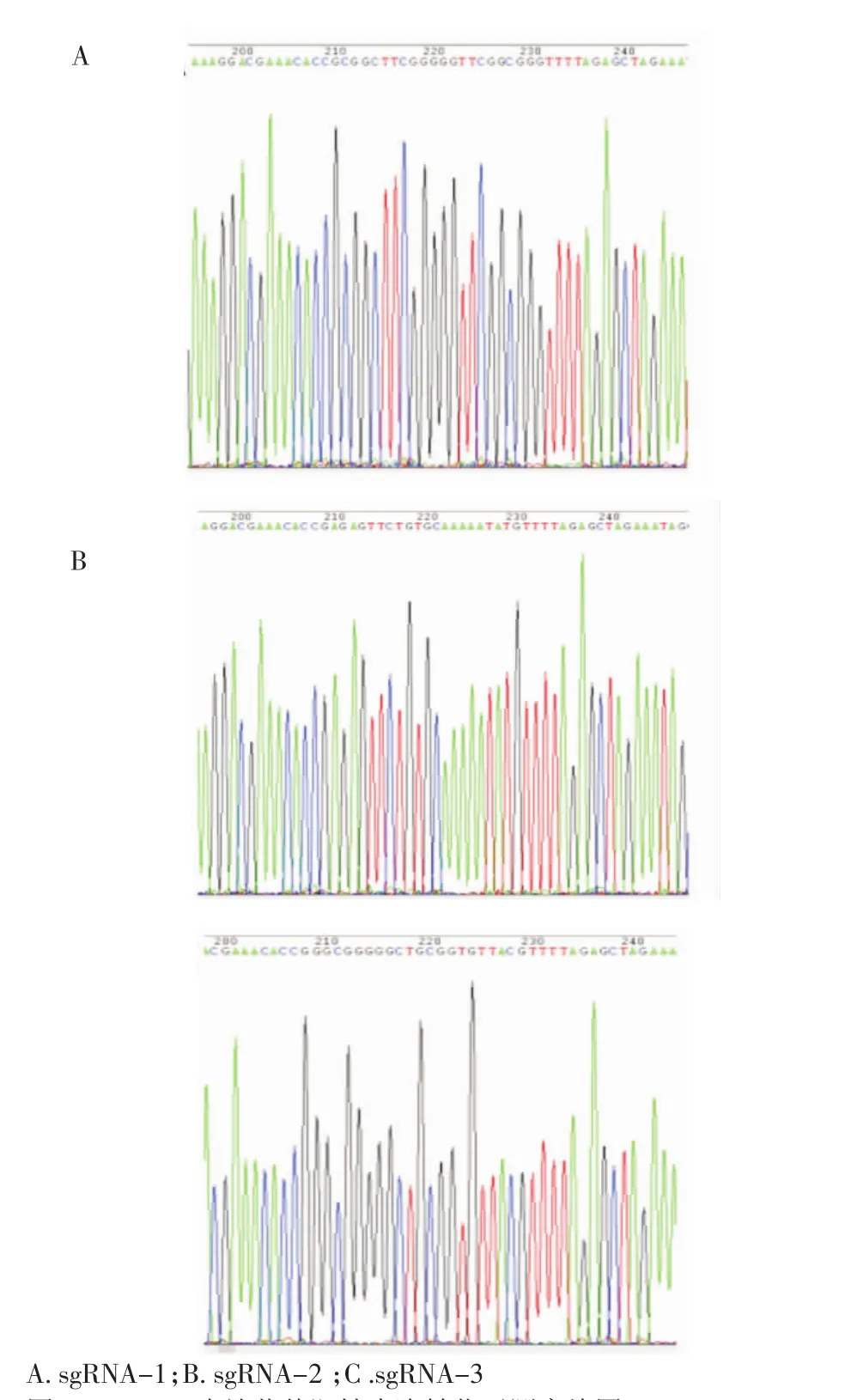
圖3 sgRNA表達載體陽性克隆轉化子測序峰圖Fig 3 sgRNAexpressionvectorpositiveclonetransformantsequencing peak map
2.3 病毒滴度的測定 在倒置熒光顯微鏡下觀察加入不同稀釋倍數病毒原液的293T細胞熒光表達情況顯示,熒光細胞的數目隨病毒稀釋倍數的增加而逐漸減少,估算過表達慢病毒和3種Lenti-sgRNA的病毒滴度分別為 5×108TU/mL、1×109TU/mL、1×109TU/mL 和 1.5×109TU/mL,見圖 4。
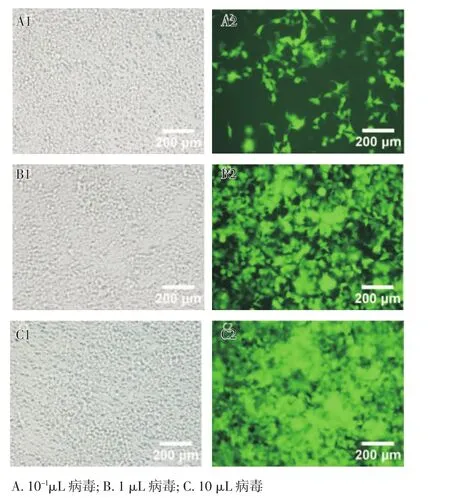
圖4 不同稀釋倍數的慢病毒感染293T細胞的熒光表達情況(×200)Fig 4 Fluorescenceexpressionsof293Tcellsinfectedwithlentiviruses at different dilutions(×200)
2.4 慢病毒感染的最適MOI及嘌呤霉素篩選的最適劑量 在不同濃度病毒感染ST88-14細胞72 h后,用顯微鏡觀察熒光表達豐度,感染效率80%左右,細胞生長良好的組所對應的MOI值即可作為后續感染實驗的依據,確定MOI=10為CRISPR/Cas9慢病毒的最佳感染條件,MOI=100為過表達慢病毒的最佳感染條件,見圖5。待ST88-14細胞生長至70%~80%時加入不同濃度的Puro,篩選48 h以上,當Puro的濃度大于等于2 μg/mL時,ST88-14細胞全部死亡,因而確定Puro最適劑量為2 μg/mL,見圖6。
2.5 慢病毒轉染ST88-14細胞的結果 慢病毒轉染ST88-14細胞2周后,用倒置熒光顯微鏡進行觀察,鏡下均可見大量綠色熒光蛋白,并且熒光隨著細胞傳代可持續表達(圖7)。
2.6 穩定株細胞的篩選及鑒定 構建好的SUZ12過表達及敲減慢病毒分別感染ST88-14細胞后,經Puro篩選獲得穩定細胞株,提取RNA進行RT-qPCR檢測。PT-qPCR結果顯示過表達組SUZ12 mRNA表達量明顯較對照組高(P<0.05),敲減組SUZ12 mRNA表達量相比對照組明顯減少(P<0.05)。由此說明,SUZ12過表達和敲減的ST88-14穩定細胞株構建成功,見圖8。
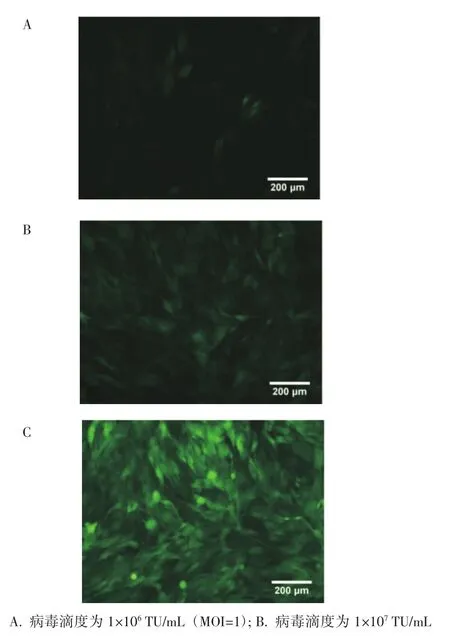
圖5 過表達組相同感染條件下不同濃度病毒感染效率比較(×200)Fig 5 Comparison of virus infection efficiency at different concentrations in the same infection conditions(×200)
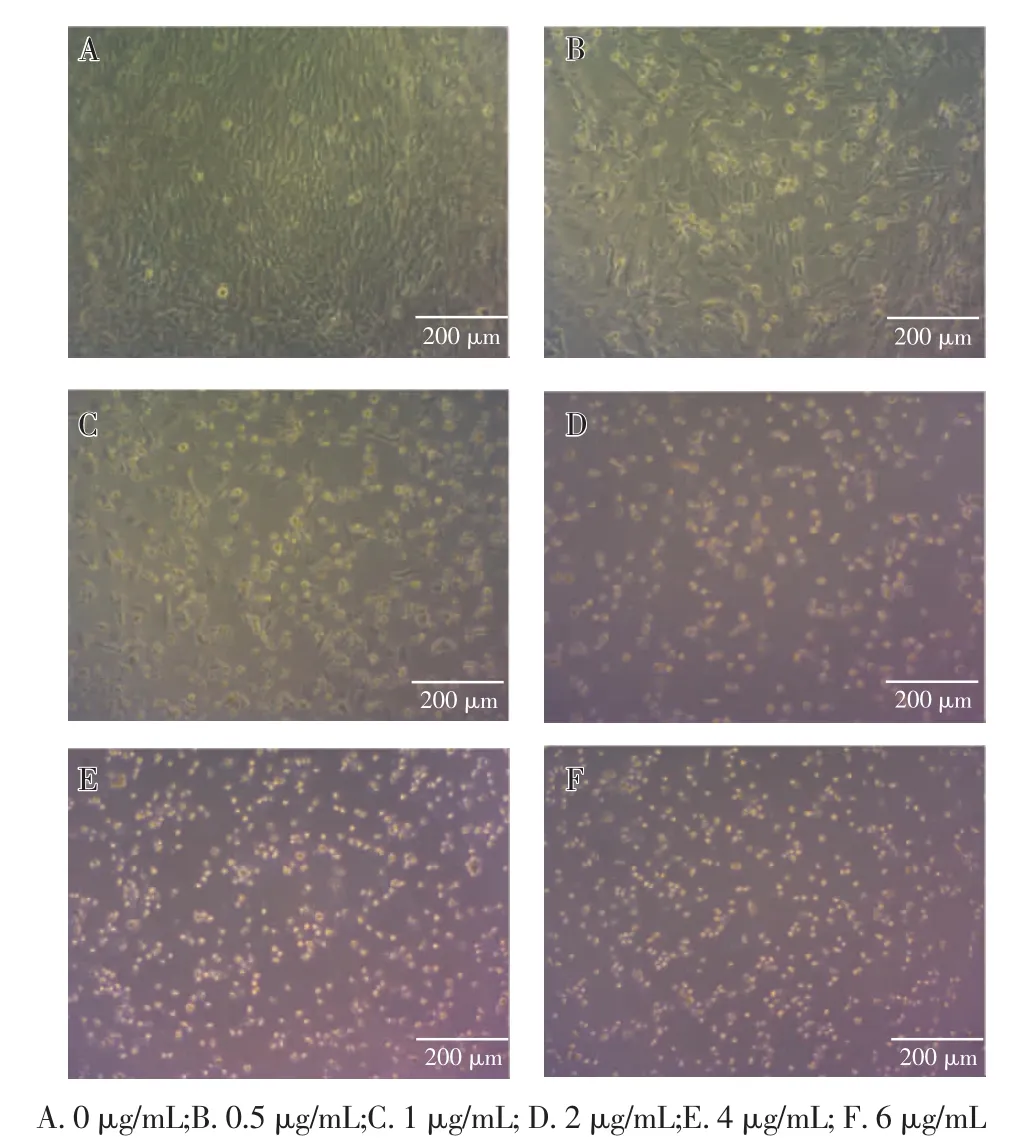
圖6 不同濃度嘌呤霉素篩選48 h后ST88-14的細胞狀態Fig 6 Cell state of ST88-14 after 48 hours at different concentrations of puromycin
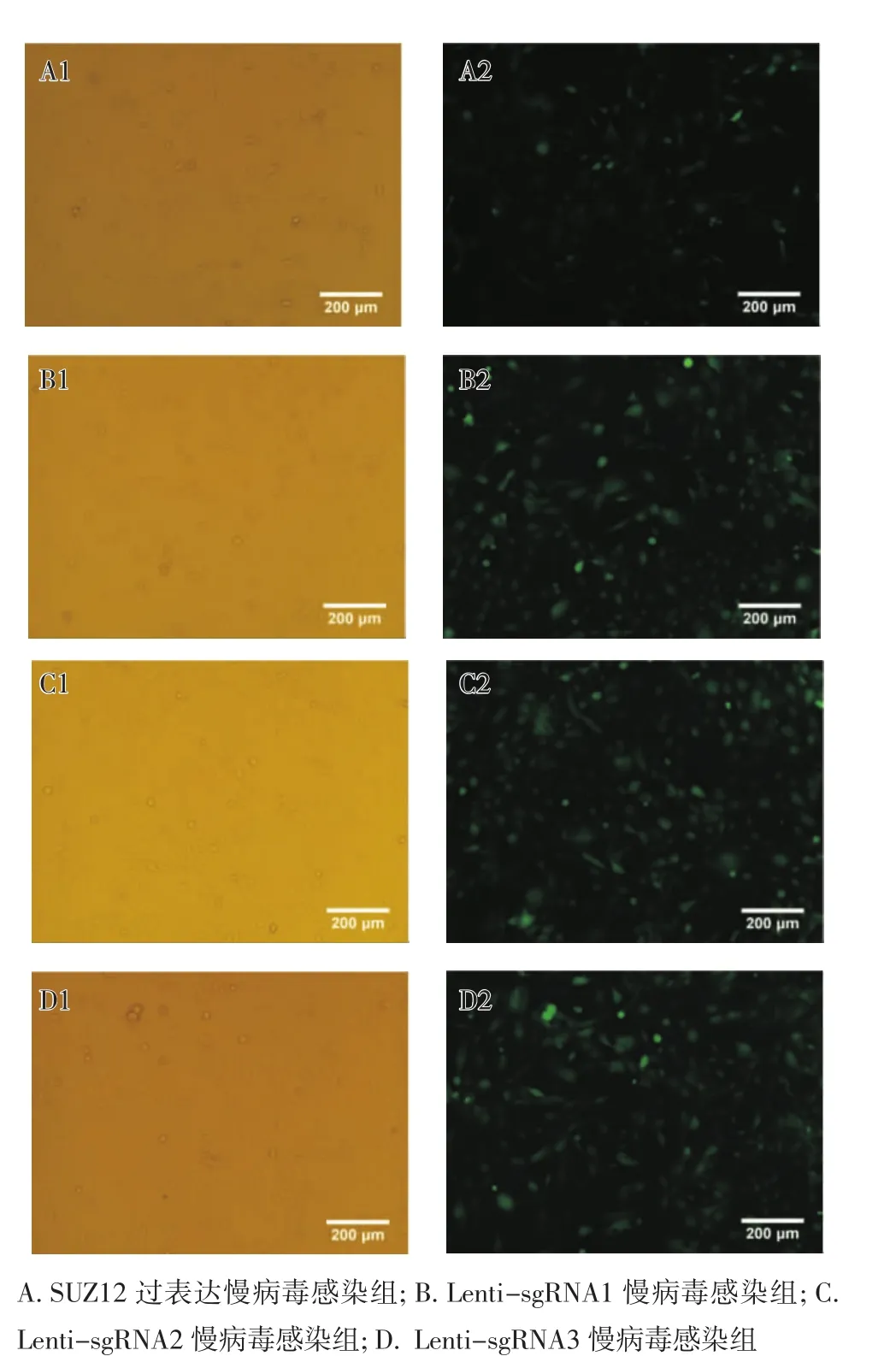
圖7 慢病毒轉染ST88-14細胞后穩定表達綠色熒光蛋白(×200)Fig 7 Stable expression of green fluorescent protein after transfection of ST88-14 cells with lentivirus(×200)
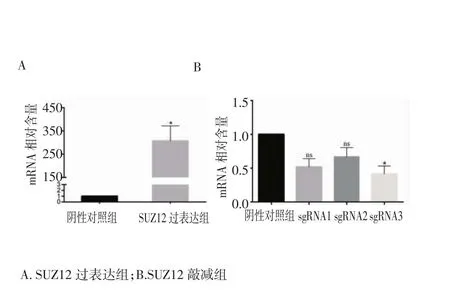
圖8 過表達和敲減組SUZ12 mRNA相對表達情況Fig 8 Relative expression of SUZ12 mRNA in overexpressed and knockdown groups
2.7 SUZ12基因過表達抑制MPNST細胞增殖 SUZ12過表達和敲減穩定株構建完成后,用MTT法測定各組細胞增殖活性的改變。MTT結果顯示,過表達組的細胞增殖活性與陰性對照組相比明顯降低(P<0.05),敲減組的細胞增殖活性與陰性對照組相比明顯升高(P<0.05)。表明SUZ12基因過表達抑制MPNST細胞增殖。見圖9。
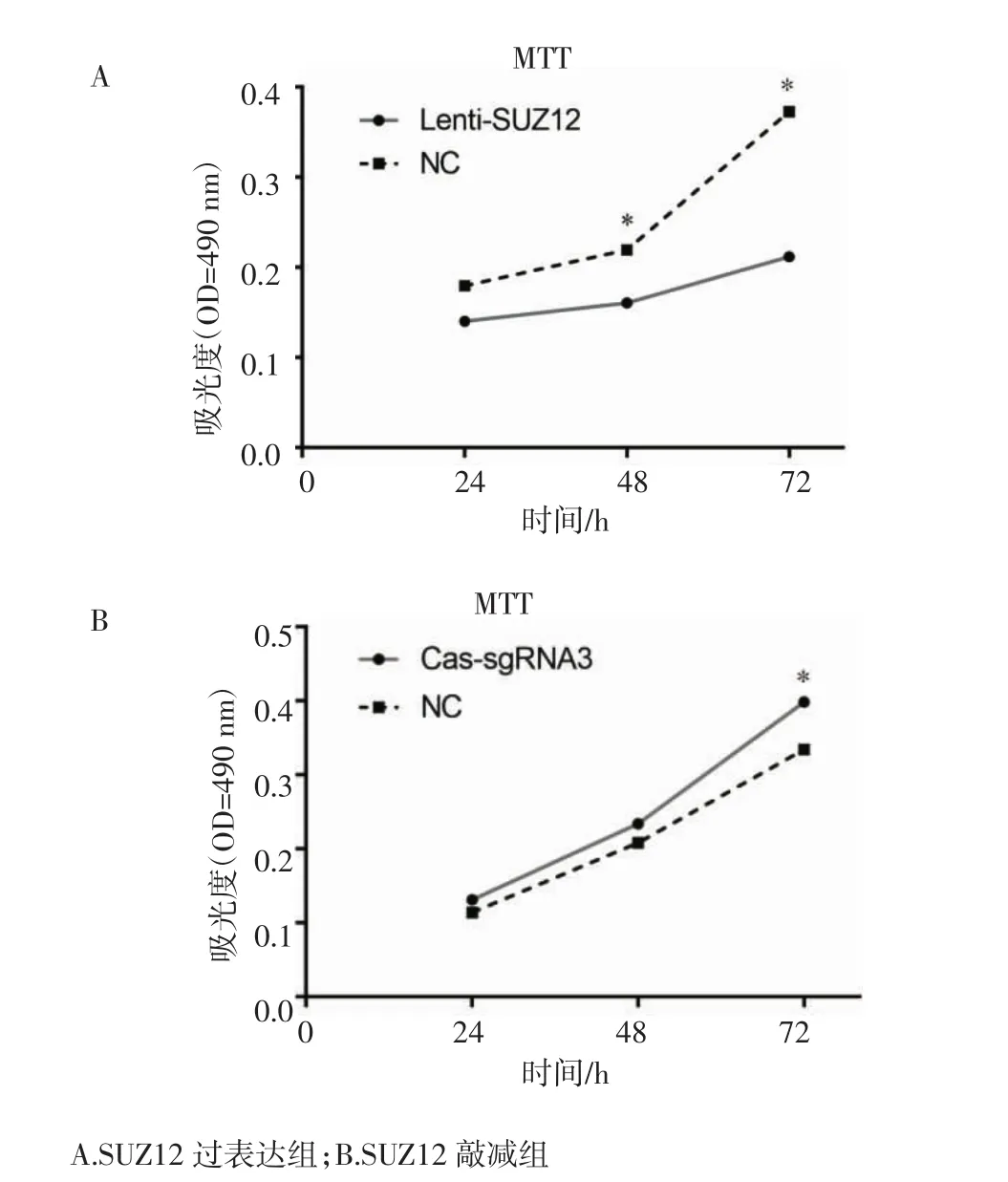
圖9 過表達和敲除組細胞增殖活性的測定Fig 9 Determination of cell proliferation activity in overexpression and knockout groups
3 討論
SUZ12是多疏抑制復合物2(PRC2)必不可少的組成部分,它可以通過調控組蛋白和DNA甲基化修飾轉錄過程,借此以穩定PRC2,使PRC2的功能正常發揮[12],除此之外,SUZ12還可以影響組蛋白三甲基化的活性,參與EED-EZH2復合物的功能沉默過程[13]。有研究表明SUZ12在胃癌、結腸癌、卵巢癌、子宮內膜癌、乳腺癌、套淋巴細胞癌等腫瘤中表達明顯高于癌旁組織,并且,SUZ12表達量的增加提高了腫瘤細胞無限增殖、轉移及侵襲的能力,影響了患者的預后[14-18]。SUZ12在上述腫瘤中表達量增加,促進了腫瘤的發展,然而其在血液系統腫瘤、神經膠質瘤等腫瘤中的表達量明顯低于癌旁組織,這表明SUZ12表達量的減少也促進了腫瘤的發展,同時具有抑癌的作用[19-20],因而,SUZ12在腫瘤的發生發展過程中發揮了雙向功能。
本研究組在對12例MPNST全基因組進行深度測序后發現,在NF1陰性的散發性MPNST中,SUZ12基因往往呈現缺失狀態[3],這提示我們SUZ12可能在散發性MPNST的發生發展過程中起到了關鍵作用。Andrew等結合了全外顯子測序隊列的分析、TCGA提供的公開數據,以及對該疾病的前幾代測序研究的回顧,分析計算出了MPNST特異性基因突變率,分別為 NF1(56/64=87.5%),SUZ12(69/123=56.1%),EED(40/123=32.5%),TP53(29/72=40.3%),CDKN2A(54/72=75.0%)[5-9],也證實在 MPNST 中大多存在SUZ12基因的缺失。研究發現大多數MPNST患者中存在PRC2不同組分功能喪失性突變,而SUZ12和EED的缺失性突變又阻斷了H3K27me3的甲基化進程,導致H3K27me3缺失,引起PRC2染色質調節信號通路失活[21]。研究者在10%~25%的腎癌、肺癌、胃癌和神經膠質瘤中發現了H3K36me3的缺失[22-25],而H3K36me3的缺失與細胞周期檢查點相關基因存在協同致死效應,WEE1抑制劑AZD1775對H3K36me3缺失的細胞更加敏感[26],本課題組之前對43例MPNST的組織標本進行免疫組化染色,發現H3K27me3在65.11%的MPNST患者中均缺失[27],而H3K36me3缺失可以作為用藥靶點也為由PRC2組分突變所致H3K27me3缺失的腫瘤提供了一個表觀遺傳學的治療策略。
本課題組所用的腫瘤細胞系屬于神經細胞,而神經細胞具有不可分裂的特性,使外源片段的導入比較困難,慢病毒載體是由人類免疫缺陷病毒(HIV-1)改造后產生,具有感染效率高、基因片段容量大、持續穩定表達且可感染分裂和非分裂細胞的特點,因此選用慢病毒載體作為基因操作的工具。CRISPR/Cas9是一項新興的基因編輯技術,自問世以來,已廣泛應用于腫瘤領域的科學研究,而且有研究表明,CRISPR/Cas9即使不進行單克隆篩選,也可永久顯著敲低目的基因的表達水平[28]。本實驗通過慢病毒包裝系統制備了SUZ12過表達和CRISPR/Cas9敲減慢病毒,分別轉染ST88-14細胞后,成功獲得了能穩定表達綠色熒光蛋白的SUZ12過表達和敲減穩定細胞株,RT-qPCR的結果也證明過表達組SUZ12 mRNA表達量明顯較對照組高(P<0.05),敲減組SUZ12 mRNA表達量相比對照組明顯減少(P<0.05)。MTT結果顯示,過表達組的細胞增殖活性與陰性對照組相比明顯降低(P<0.05),敲減組的細胞增殖活性與陰性對照組相比明顯升高(P<0.05)。由此說明,SUZ12基因過表達抑制MPNST細胞增殖。
綜上所述,筆者通過本課題組和其他實驗室的研究數據確定了SUZ12基因在MPNST中處于缺失狀態,而H3K36me3缺失可以作為治療靶點也為PRC2組分缺失突變所致的H3K27me3缺失提供了治療策略,因此筆者構建了SUZ12過表達和敲減的MPNST穩定細胞株,初步探索SUZ12基因表達狀態的變化所引起細胞增殖的改變,本課題組將進一步在體內和體外實驗中探索細胞侵襲遷移、周期等功能的改變,以闡明PRC2功能失活在MPNST的發病演進中的作用及其分子機制,并為MPNST的治療提供了一個基于表觀遺傳學的治療策略。

