計劃性再手術在嚴重腹腔感染患者救治中的地位
楊學武,田偉軍
(天津醫科大學總醫院普通外科,天津300052)
腹部手術患者術后出現消化道瘺,極易繼發嚴重腹腔感染,死亡率極高,有效控制瘺出量和感染程度是避免患者術后死亡的關鍵[1]。計劃性再手術清理腹腔感染灶,術中瘺口及感染灶周圍放置雙套管,術后給予生理鹽水持續沖洗負壓吸引,減少毒素吸收,促進瘺口愈合,降低全身炎癥反應程度。部分患者應用一次性封閉負壓引流材料(VSD)行暫時性腹腔關閉,維持腹膜腔封閉性、完整性,大大降低了患者腹膜腔壓力,促進胃腸功能恢復,應用術中所放置的空腸營養管給予腸內營養,保證充足的熱量供給。我院普通外科于2015年9月-2018年11月對16例嚴重腹腔感染的危重癥患者進行了計劃性再手術,顯著降低了死亡率。
1 資料與方法
1.1 一般資料 回顧分析2015年9月-2018年11月天津醫科大學總醫院普通外科腹部手術后出現消化道瘺(腸瘺、膽瘺、胰瘺)繼發嚴重腹腔感染的16例患者,其中男性11例,女性5例,平均年齡(54.2±16.9)歲,其中 8例腸瘺、4例膽瘺、2例胰瘺、2例多源瘺并存,13例行2次手術,3例行多于2次手術并應用VSD暫關腹技術,平均住院時間(50.1±21.8)d,雙套管持續沖洗(17.9±9.9)d,應用腸內營養共14例,開始時間(2.0±1.3)d。
1.2 制作方法
1.2.1 雙套管制作方法 本文所用的雙套管均自制,外套管用的是醫用乳膠引流管作為外管,用一次性吸痰管作為內管,在外管距離管端2 cm處打孔,插入內管,前端平齊,外管前端打孔2~3處。內管沖洗出生理鹽水,稀釋消化道瘺出液及壞死組織,外管接負壓持續吸引,外管與內管之間要有足夠空間,0.2~0.3 cm間距,以利于壞死組織及液體吸出,該雙管套可在嚴格無菌操作要求下現做現用,也可以用環氧乙烷消毒后備用。制作成品見圖1。

圖1 雙套管Fig 1 Double cannula
1.2.2 雙套管使用方法 手術當日即開始使用雙套管。原則是持續沖洗,保證引流管通暢引流。沖洗量平均約為3 000 mL/d。沖洗液使用無菌生理鹽水,無需加入抗生素[3],持續低負壓吸引,負壓值維持在10~20 KPa(約 75~150 mmHg)較為適宜[4]。根據引流的具體情況隨時調整沖洗速度,必要時可在超聲引導下調整管路深度。
1.3 實際操作
1.3.1 VSD暫關腹技術 多次手術腹腔清理患者使用VSD暫關腹技術,切口下方使用紗布墊保護胃腸道,外敷一次性封閉負壓引流材料(VSD),常用材料為黑色聚氨酯泡沫海綿,單片規格為15cm×10cm,修剪處理成傷口面積的80%,間斷縫合固定覆蓋傷口,以無菌3M膜封閉,生理鹽水持續沖洗,封閉負壓吸引,計劃性手術清理更換VSD,每周1~2次[5]。本文多次手術患者最多手術次數為18次。VSD暫關腹術后見圖2。

圖2 VSD暫關腹術后Fig 2 Postoperation of VSD temporary abdominal closure
1.3.2 根據腹腔感染引流液培養結果選用敏感抗生素。并給于奧曲肽或生長抑素等減少消化液分泌配合治療。
1.3.3 觀察指標 每次術前術后24 h內均測定血常規、血氣分析、腎功能、生化等血化驗指標,監測生命體征變化,如體溫、心率、平均動脈壓等,并進行APACHE II評分。
1.4 統計學分析 采用Graphpad prism 7.0軟件進行統計分析。術前、術后數據對比采用配對t檢驗。P<0.05認為具有統計學意義。
2 結果
2.1 術前、術后APACHE II評分對比 如圖3所示,APACHE II評分術后(5.5±4.3)較術前(9.1±4.5)顯著下降,差異具有統計學意義(P<0.01)。

圖3 16例患者術前、術后急性生理學及慢性健康狀況評分對比Fig 3 Comparison of acute physiology and chronic health scores of 16 patients before and after operation
2.2 術前、術后最高體溫對比 如圖4所示,術后最高體溫(36.9±0.36)℃較術前最高體溫(38.4±0.42)℃顯著下降,差異具有統計學意義(P<0.01)。

圖4 術前、術后最高體溫對比Fig 4 Comparison of the highest body temperature before and after operation
2.3 術前術后血常規白細胞數對比 如圖5所示,監測血常規白細胞指標術后[(10.4±4.9)×109/L]較術前[(14.8±6.0)×109/L]顯著下降,差異具有統計學意義(P<0.01)。
2.4 是否應用VSD暫關腹技術患者術前、術后APACHE II評分對比 本研究中應用VSD暫關腹技術患者(4例),術后 APACHE II評分(6.3±2.6)較術前(9.5±4.1)下降(P<0.05),差異具有統計學意義。相同治療方法未應用VSD暫關腹技術患者(12例)術后 APACHE II評分(5.3±4.8)較術前(8.9± 4.8)下降,差異均具有統計學意義(P<0.05),見圖6。
2.5 不同類型消化道瘺患者術前術后APACHE II評分對比 膽瘺患者術后APACHEII評分(6.0±4.9)較術前(9.0±6.0)下降,腸瘺患者術后評分(3.6±2.0)較術前(7.5±1.5)下降,二者差異具有統計學意義(P<0.05)。胰瘺患者術后評分(12.5±4.5)較術前(16.5±3.5)下降,多源瘺患者術后評分(5.0±4.2)較術前(8.0±5.7)下降,二者差異不具有統計學意義(P>0.05),見圖7。
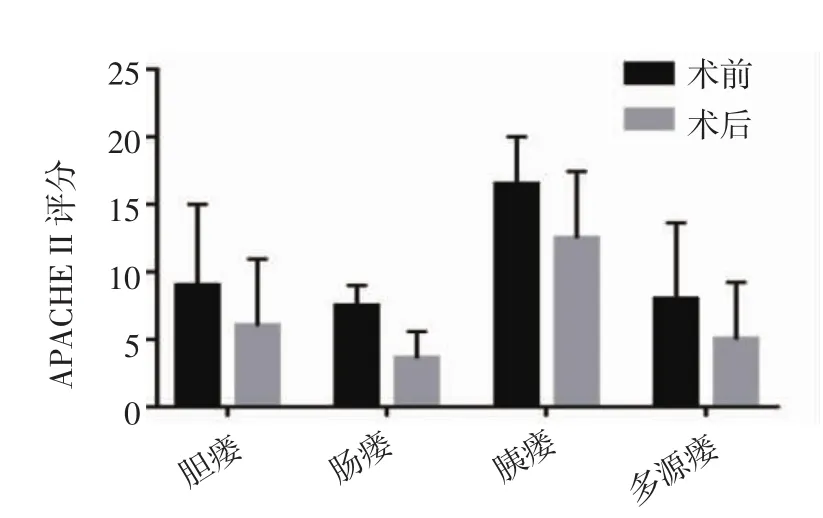
圖7 不同類型疾病術前、術后APACHE II評分對比Fig 7 Comparison of APACHE II scores before and after operation for different diseases
全組患者通過計劃性再手術,術后腹腔感染均逐漸控制,(APACHEⅡ)評分系統中年齡、慢性健康狀況術前術后對比無顯著變化,差異主要體現在手術前后急性生理學評分(APS)的變化上,而APS中最主要表現在血常規WBC及體溫的變化。通過對比,其差異具有統計學意義(P<0.01)。同時,計劃性再手術治療方法對于是否應用VSD技術均有效(P<0.05)。16例患者中,1例患者因肝破裂術后多臟器功能衰竭死亡,余15例患者均腹腔感染消退,瘺口愈合,好轉出院。相關文獻報道,包括C級胰瘺在內的消化道瘺合并嚴重腹腔感染死亡率高達25%~33%[6-7,30],本組死亡率為6.3%,病死率顯著下降。
3 討論
腹部手術后出現的消化道瘺絕大部分為吻合口瘺,部分患者可同時出現多種類型消化道瘺,其危害主要在于消化液對腹腔組織的腐蝕導致局部感染和繼發出血,不可控制的腹腔感染是導致患者死亡的主要原因[8]。原有的腹腔被動引流管術后很快被膿血塊、脫落壞死組織或纖維素阻塞,不能有效引流感染壞死組織及液體[9]。腹腔感染持續加重,出現感染性休克、多臟器功能衰竭,最終可導致患者死亡。所以,早期徹底的腹腔清理沖洗和充分有效的腹腔引流是控制腹腔感染和促進瘺口愈合的關鍵[2]。
計劃性再手術最核心的一點就是計劃性,即根據病情,可以時間為計劃,可以病情需求為計劃,一般情況下24~48 h進行一次,最長不超過72 h,避免腹腔感染加重再次損害機體,在毒素尚未形成更大的危害的時候及時清理。趙允召等[10]認為計劃性再手術的優勢在于:對于血液動力學不穩定的腹腔嚴重感染患者,進行有效、快速、微創、計劃性的多次手術清理腹腔感染灶,對于防止全身感染持續加重,出現多臟衰竭,效果顯著,明顯降低了病死率。納入本研究16例患者,均存在嚴重腹腔感染,伴有消化道液持續漏出,單純通過被動引流管及影像學引導的穿刺置管沖洗,已不能滿足清除腹腔感染的需要。姜朝暉等[11]對46例消化道瘺患者分期手術治療進行分析,認為早期再手術治療的益處是:腹腔感染尚局限,消化道液對組織的腐蝕較輕,周圍組織間的粘連易于分離,瘺口組織較新鮮,及時中止因瘺發生對患者全身情況的再次打擊,全身內環境紊亂尚處于可調控范疇等。因此,在患者全身狀況允許的前提下計劃性的再手術,及時清理腹腔感染灶,沖洗腹腔各間隙,可更有效、更快速地緩解腹腔感染,最大程度地減少毒素吸收、穩定血液動力學指標。
黎介壽等[12]認為“有明顯腹腔感染時不進行腸切除吻合或縫合”。而計劃性再手術的主要目的并不是要修補消化道瘺口,而是要在瘺口周圍的腹腔間隙建立有效、確定、充分的引流機制,清理瘺口周圍滲漏積聚的膽汁、腸液、胰液、膿血塊等,減少機體吸收腹腔感染灶產生的炎癥因子及毒素,降低消化液對周圍臟器組織的進一步腐蝕損害[13-14]。但瘺口局部條件允許的情況下可適當縫合暫時性的封閉瘺口,減少短期內的消化液瘺出量,爭取術后控制感染、改善全身狀況的寶貴時間窗。本研究中有3例患者因其高腹壓、感染重、腹腔臟器嚴重水腫,強行關腹勢必造成腹膜腔壓力急劇上升,出現腹腔間隔室綜合征。因而采用了一次性封閉負壓引流材料(VSD)輔助的暫時性腹腔關閉(TAC)。計劃性的手術清理腹腔感染灶,并更換VSD關腹材料。Navsaria等[15]與Bertelsen等[16]共報道121例VSD材料輔助完成TAC,認為該技術安全有效。VSD具有多重優勢:(1)高效的引流促進感染的控制;(2)延展腹壁面積,有效保持腹腔封閉性;(3)減輕消化液對組織的腐蝕[17-20],腹腔感染控制、組織水腫消退后,每次更換VSD材料時逐漸縮小使用面積、長(每次1~3cm)、寬(每次3~5cm),最后當材料寬度縮小至5cm以內時,腹壓<12 mmHg可直接關腹,若>12 mmHg或腹壁缺損,繼續治療至傷口合攏,再植皮封閉創面形成人工疝,6~12月再行腹壁確定性重建[5,21]。
計劃性再手術的第二個目的即清理腹腔感染灶后在瘺口周圍放置1~2根雙套管,雙套管旁留置多孔乳膠引流管一根伴隨,術后持續由內管滴入生理鹽水,外管開放的負壓吸引能將感染腔隙中的細菌分泌物及消化液漏出物及時吸出,降低腔隙中的細菌量,減輕局部炎癥反應,促進瘺口的新生血管生成和肉芽組織的形成[22-23]。經臨床驗證,當腹腔引流液達150 mg/kg時,細菌量由108/mL降至102/mL[24]。總之,持續雙套管沖洗負壓引流的特點是變以往的被動引流為主動吸引,可及時、徹底地排出膿腔積液及壞死組織,使創面及膿腔保持高效引流,一般使用3~5 d后,沖洗液中絮狀物明顯減少,轉為清亮,感染控制后可采用間斷沖洗及低負壓吸引,引流量下降至<20 mL/d后,逐步往外退出雙套管,竇道自然愈合。
再手術的第3個目的即留置空腸營養管。“腸道有功能且能安全使用時就應使用腸道”已經成為目前公認的營養支持治療的原則,只要腹膜腔壓力降低、腸蠕動恢復,應盡早試行腸內營養,這樣有利于減少腸漏等消化道瘺的進一步加重,并促進瘺口的愈合[25-26]。本文所研究患者均為腹腔重大手術后創傷應激、腫瘤消耗,機體處于高度分解代謝狀態,營養狀況差。充足、合理的營養支持可使機體從分解代謝轉為合成代謝狀態,促進組織器官修復,改善臨床結局,尤其在重癥感染情況下,營養治療尤為關鍵[27-28]。研究[29-30]表明長期腸外營養PN可導致腸黏膜功能及腸內生態異常并損傷免疫功能,腸內營養EN的眾多優點可彌補PN的不足之處,只有當其無法滿足機體需要時(<60%機體需要量)應考慮結合PN,可EN+PN聯合供能。此外,EN在促進胃腸道供能恢復和縮短住院時間方面有顯著效果[31]。本文除2例小腸第4組腸瘺患者給予腸內營養后漏出液增多,停用EN改以PN供能,其余高位或低位腸瘺及其他類型消化道瘺均主要依靠腸內營養,營養支持效果滿意。
綜上所述,對于消化道瘺伴腹腔感染的危重癥患者,計劃性再手術清理腹腔感染灶,可在最短的時間力挽狂瀾,避免患者腹腔感染急劇加重出現膿毒血癥、感染性休克、多重感染等感染不可控的情況,挽救患者進入多臟器功能不全,甚至衰竭、死亡的結局。再配合雙套管持續負壓沖洗吸引、VSD暫關腹技術、腸內營養支持等方法,可以顯著降低死亡率,因此證實計劃性再手術療法對于腹腔感染的危重癥患者切實有效。

