基于UbD理論培養學考生化學核心素養的教學設計
李世媛 支二娟

摘要:以UbD理論為導向,運用逆向教學設計法對高一化學必修1《鐵及其重要化合物》單元的“Fe2+、Fe3+的性質及其轉化”一課進行了教學設計和實踐,發現這一方法可以幫助教師創設真實的問題情境,激發化學學考生的學習興趣,促進學生對概念的理解,提高課堂教學的有效性,且為學生的表現性評價提供有力的依據。
關鍵詞:UbD理論;元素化合物;逆向教學設計;補鐵劑;真實問題情境
文章編號:1008-0546( 2019)07-0081-03
中圖分類號:G633.8
文獻標識碼:B
doi: 10.3969/j .issn.1008-0546.2019.07.024
在新中考改革背景下化學成為了中考的一門選考科目,因此,許多初中沒有深入學習過化學的學生在高一需要繼續學習化學,參加高中化學學業水平考試,甚至是三年后的高考。對于需要通過高一一年時間來學習化學并通過學業水平考試的學考生而言,必修模塊的學習任務重且時間緊張。那么如何在有限的時間內提升化學學考生的核心素養,使他們成為具有化學素養的合格公民呢?美國學者格蘭特·威金斯和杰伊·麥克泰格提出了UbD( Understanding by De-sign)理論,即“通過教學設計,使更多的學生真正理解他們所要學習的知識[1]”,倡導教師幫助學生理解學科大概念,并在學生的表現中找到其理解的證據。筆者以這一理論為導向,對《必修l》模塊《鐵及其化合物》單元的“Fe2+、Fe3+的性質及其轉化”進行了逆向教學設計的探索與實踐。
一、逆向教學設計法在《鐵及其化合物》單元教學中的應用
格蘭特·威金斯和杰伊·麥克泰格提出了幫助教師實現UbD理念的逆向教學設計法,這包括以下三個階段(如圖1):
1.確定預期的學習結果
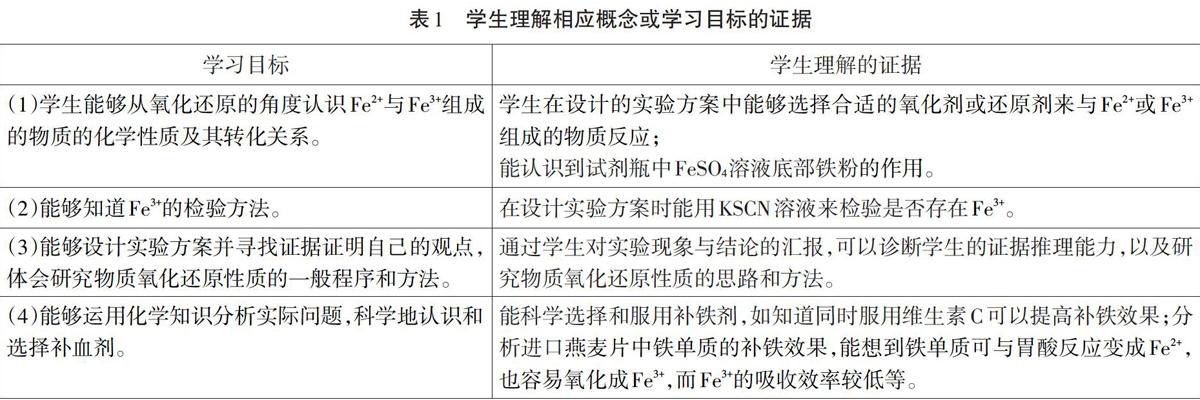
對于無機化合物的教學來說,其主題大概念應該是元素觀。在必修課程階段,元素觀的發展內涵包括:“認識元素可以組成不同種類的物質,根據物質的組成和性質可以對物質進行分類;認識同類物質具有相似的性質,一定條件下各類物質可以相互轉化;認識元素在物質中可以具有不同價態,可通過氧化還原反應實現含有不同價態同種元素的物質的相互轉化[2]。”基于這些核心概念,結合我國2017年發布的《普通高中化學課程標準》,我們把重點聚焦在了“鐵元素在不同物質中的不同價態,以及通過氧化還原反應可實現不同價態同種元素的物質的相互轉化”這一大概念上。據此,對于本單元中“Fe2+、Fe3+的性質及其轉化”這一課時的教學,筆者制定了以下預期目標:(1)學生能夠從氧化還原的角度認識Fe2+與Fe3+組成的物質的化學性質及其轉化關系;(2)能夠知道Fe3+的檢驗方法;(3)能夠設計實驗方案并尋找證據證明自己的觀點,體會研究物質氧化還原性質的一般程序和方法;(4)能夠運用化學知識分析實際問題,科學地認識和選擇補血劑。
2.確定合適的評估證據
基于UbD理論的教學設計要求教師在備課一上課一反思的過程中時刻關注學生的表現,及時捕捉證據,證明學生對概念的理解程度。針對上述預期學習目標,筆者列出了課堂上可以找到的證據(如表1),不僅可以幫助教師判斷學生對概念的理解程度,還可以作為綜合素質評價中學生課堂表現性評價的依據。
3.設計教學活動 學科核心素養指的是“本學科給予學生未來發展必備的品格和關鍵能力;是在解決復雜的不確定性的現實問題過程中表現出來的綜合性品質或能力;是學科的知識和技能、過程與方法、情感、態度和價值觀的整合[3]。”為了創設真實的問題情境,筆者對藥房在售的補鐵劑進行了實際調查,發現補鐵劑不僅有我們常見的速力菲(琥珀酸亞鐵),還有右旋糖酐鐵(一種右旋糖酐與氫氧化鐵的絡合物),也就是說,Fe3+與Fe2+組成的物質都可以起到補鐵的作用。那么含有Fe3+或Fe2+的補鐵劑在化學性質上有何不同?它們之間能不能相互轉化呢?這樣就從補鐵的角度造成了學生的認知沖突,激發了探究的欲望。
探究實驗是大多數學生都喜愛的學習活動,通過選擇氧化劑與還原劑、設計實驗方案以及小組合作動手實驗,學生不僅可以了解不同價態鐵的化合物之間的相互轉化,而且可以將宏觀辨識與微觀探析結合起來,在尋找證據證明自己觀點的過程中提高證據推理能力。此外,通過鐵元素在人體內代謝這樣的跨學科問題的討論,不僅可以引導學生進行知識的遷移和應用,而且可以培養學生分析解決不確定實際問題的能力和敢于質疑的品質。
二、教學實施過程
1.創設問題情境
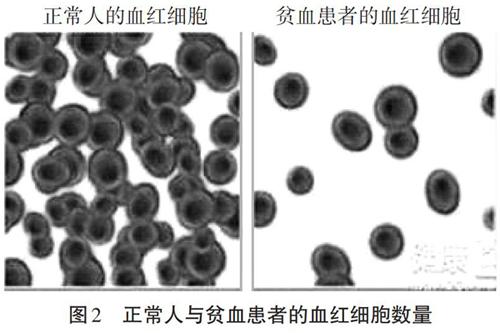
【PPT】展示正常人與貧血患者的血紅細胞數量差異以及人體血紅蛋白分子的結構(如圖2、圖3)。
【教師】對于缺鐵性貧血患者來說,要增加血紅細胞的數量,就需要補充鐵元素。那么常見的補鐵劑有哪些呢?
【PPT】展示補鐵劑速力菲和右旋糖酐鐵的圖片,以及右旋糖酐鐵的藥品成分。
【教師】為什么右旋糖酐鐵中的氫氧化鐵絡合物也可以補鐵?Fe3+可以轉化為Fe2+嗎?
2.探究Fe3+與Fe2+的相互轉化
【PPT】請根據資料卡片和所給試劑,設計實驗證明Fe3+可以轉化為Fe2+。
試劑:Fe粉、FeS04溶液、FeCl3溶液、維生素C、稀硫酸、氯水、KMn04溶液、KSCN。
資料卡片
【學生活動】小組討論設計實驗方案。
【教師】哪個小組愿意分享你們的實驗方案?
【學生1】在試管中加入適量FeCl3溶液,滴入2滴KSCN溶液,溶液變成紅色,再加入鐵粉,紅色變淺,說明鐵粉能將Fe3+轉化成Fe2+。
【教師】很好。我們看到試劑瓶中FeSO4溶液底部有一層灰色的鐵粉,那么鐵粉的作用是什么?
【學生2】防止Fe2+被氧化為Fe3+。
【教師】請根據資料卡片和所給試劑,設計實驗方案證明Fe2+可以轉化為Fe3+。
【學生3】向兩支試管中滴加等量KMn04溶液,然后向其中一支滴加少量FeS04溶液,再向另外一支滴加等量的水,如果看到加FeS04溶液的試管紫色褪去,說明FeSO4被KMn04氧化。
【教師】同學控制變量的意識都很強,下面請兩人一組完成探究實驗,記錄實驗現象。
【學生活動】小組合作動手實驗,記錄實驗現象,完成實驗報告。
【教師】巡視指導學生實驗。組織學生進行匯報。
【實物投影】學生匯報實驗現象及結論。
【學生4】取兩支試管加入等量FeCl3溶液,向其中一支加維生素C粉末,再分別滴加2滴KSCN溶液,若不變紅,說明FeCl3被維生素C還原為Fe2+。
【學生5】向FeSO4溶液中加入適量氯水,再加KSCN溶液顯紅色,證明Fe2+可以氧化為Fe3+。
【教師】大家都能找到合適的氧化劑與還原劑來實現不同價態鐵元素的轉化,如何讓自己的實驗方案更嚴謹呢?
【學生6】向FeSO4溶液中加KSCN溶液不顯紅色,再加入少量氯水變紅色,則證明Fe2+可以氧化為Fe3+。
【教師】先加KSCN溶液就排除了原溶液中Fe3+的干擾,這位同學的證據推理能力很強。 【板書】
Fe2+ 還原劑(鐵粉、維生素C) Fe3+
(還原性)氧化劑(氯水、KMn04)(氧化性)
3.實際問題分析與解決
【PPT】展示鐵元素在人體十二指腸內的代謝過程(圖4)。
【教師】根據鐵元素在人體中的代謝過程,可以看出Fe2+可直接被人體吸收,而Fe3+則需要先被體內的鐵硫蛋白還原為Fe2+再被人體吸收,在人體內運輸時Fe2+則被血漿銅藍蛋白[4]氧化為Fe3+,因此含Fe2+的補鐵劑吸收效果更好,但對胃腸的刺激會比較大,因此小孩可選擇副作用較小的右旋糖酐鐵口服液。
【提問】速力菲的藥品說明書上寫著結合維生素C一起服用效果更好,這是為什么?
【學生7】因為維生素C有還原性,可防止Fe2+被氧化,Fe2+比Fe3+吸收效果更好。
【教師】有些燕麥片中含有還原鐵單質,你覺得可以長期食用來補鐵嗎?
【學生8】單質鐵有還原性,可與胃酸反應轉化為Fe2+,具有一定的補鐵作用。
【學生9】但鐵單質容易被空氣氧化為Fe3+,Fe3+可轉化為Fe2+,但吸收效果相對較差。
【布置作業】什么樣的食物用作日常補鐵效果較好呢?請完成小論文——如何科學補鐵。
【反思小結】教師小結Fe2+與Fe3+的相互轉化關系,以及研究物質氧化還原性質的一般程序和方法。
三、教學反思
1.真實的問題情境源自于生活
從補鐵劑人手來學習鐵及其化合物是許多教師常用的問題情境,然而筆者通過到藥店的實際調研發現了Fe3+在補鐵劑中的重要作用,又通過查閱生物學科文獻,了解到鐵元素不同價態在人體代謝過程中相互轉化的真實問題情境。雖然面對的是多數中考未選化學的學考生,但課堂上學生表現出了強烈的學習動機。因此,要還原給學生一個真實的問題情境,教師必須成為生活中的有心人,親身實踐,放寬眼界,挖掘本學科乃至跨學科問題中的大概念,才能使培養學生的科學素養在課堂上落地生根。
2.捕捉評估證據是促進學生理解的有效手段
本節課在探究實驗結束后,教師通過實物投影的方式將學生設計的實驗方案以及得到的實驗結論充分展示出來,在師生交流、生生評價中獲取了學生對氧化還原相關概念的理解證據。在分析燕麥片里還原鐵粉的補鐵效果的討論中,可以看到學生對鐵與胃酸的反應很容易進行遷移應用,而對于鐵單質易氧化為Fe3+則考慮不足,從而為進一步分析鐵粉的實際補鐵效果造成了障礙。因此,給學生充分表達思維過程的機會,捕捉評估證據并給予及時的評價和反饋,這也給教師提供了解決學生困惑的機會,是促進學生理解的有效手段。
3.表現性評價是綜合素質評價的重要形式之一
UbD理論認為“通過設計,使概念、事實、論證或者經驗既闡釋事物又提出問題時,它們就有了意義,理解才會產生”。因此,要對學生的理解程度進行科學的評估,僅使用常規的習題檢測是不夠的,還需要教師選取真實的開放式的表現性評價方式。通過完成小論文等形式的作業,不僅可以促進學生對相關大概念的理解,同時還為學生的綜合素質評價提供了有力的評估依據。
參考文獻
[1]格蘭特·威金斯,杰伊·麥克泰格.追求理解的教學設計[M].閆寒冰,宋雪蓮,賴平,譯,上海:華東師范大學出版社.2017:4
[2]普通高中化學課程標準修訂組,普通高中化學課程標準(2017年版)解讀[M].北京:高等教育出版社,2018:104
[3]林崇德,中國學生發展核心素養研究報告[J].中學教育科研,2018(3):1
[4]閆有旺,蔡連捷,鐵的生物學功能及代謝[J].化學教學,2002(12):40

