NLR聯合降鈣素原對COPD急性加重期細菌感染患者預后價值探討
羅德云,陳菊屏
慢性阻塞性肺疾病(chronic obstructive pulmonary disease,COPD)急性加重是一種呼吸道癥狀急劇惡化的不良事件,常由氣道細菌(50%)、病毒(30%~60%)感染或其他因素(15%~20%)誘發[1]。
COPD急性加重會增加患者的住院率、死亡率,降低患者的生存質量[2]。因此,早期評估患者的死亡風險十分重要。COPD急性加重常由氣道細菌感染誘發,而降鈣素原(procalcitonin,PCT)與細菌感染的相關性最強,在細菌感染時其水平會明顯升高[3]。另有研究發現,中性粒細胞與淋巴細胞比值(neutrophil to lymphocyte ratio,NLR)與COPD急性加重期患者的預后有關[4]。目前,用NLR聯合PCT預測COPD急性加重期細菌感染住院患者死亡的報道鮮見,本研究旨在探討兩者聯合評估COPD急性加重期細菌感染住院患者死亡的臨床價值。
1 對象與方法
1.1研究對象 2015年1月—2018年8月西南醫科大學附屬醫院共收治239例COPD急性加重期且痰培養至少2次發現有細菌感染的患者,排除缺乏PCT檢查的29例,最終共納入210例。急性加重期的COPD患者均符合2018年全球倡議(GOLD)指南制定的診斷標準[5]。依據出院時的生存狀態分為病死組22例,男15例,女7例,平均年齡(75.23±8.13)歲,有吸煙史者12例(未戒煙者10例,戒煙者2例)。存活組188例,男138例,女50例,平均年齡(71.85±10.08)歲,有吸煙史者113例(未戒煙者100例,戒煙者13例)。2組年齡(t=1.515)、性別(χ2=0.272)、吸煙史(χ2=0.253)差異無統計學意義,具有可比性。
1.2納入與排除標準 納入標準:所有納入的急性加重期COPD患者痰培養至少2次發現細菌感染。排除標準:(1)存在呼吸系統以外系統的感染。(2)存在結締組織疾病。(3)合并惡性腫瘤。(4)合并嚴重的肝腎等臟器疾病。(5)存在甲狀旁腺疾病。(6)本研究涉及的臨床數據[PCT、血氣分析、C反應蛋白(C-reactive protein,CRP)]不完整者。
1.3研究方法 (1)收集所有COPD急性加重期細菌感染患者的臨床資料,比較2組的年齡、性別、住院時間、病程、吸煙史等一般資料。吸煙定義為連續或累計吸煙時間至少6個月。(2)入院后24 h內的炎癥指標:PCT、CRP、白細胞計數(white blood cell,WBC)、中性粒細胞計數(neutrophil count,NEU)、NLR、纖維蛋白原。血氣分析指標:酸堿度、動脈血二氧化碳分壓[arterial carbon dioxide partial pressure,p(CO2)]、動脈血氧分壓[arterial oxygen partial pressure,p(O2)]。血紅蛋白、肌酐、白蛋白等生化指標。(3)采用受試者工作特征(receiver operating characteristic,ROC)曲線分析NLR、PCT及組合后形成的新指標預測患者死亡的曲線下面積(area under the curve,AUC)、最佳界值(cut-off)、約登指數、特異度、敏感度。分析COPD急性加重期細菌感染住院患者死亡的危險因素。
1.4統計學方法 采用SPSS 17.0軟件進行數據統計分析。計量數據符合正態分布的用±s表示,2組間比較用t檢驗;不符合正態分布的用M(P25,P75)描述,組間比較采用Kolmogorov-smirnovZ檢驗。計數資料用例(%)描述,組間比較用χ2檢驗。二分類logistic回歸進行影響因素分析。以P<0.05為差異有統計學意義。
2 結果
2.12組一般資料比較 病死組的住院時間明顯短于存活組(P<0.05),而病程差異無統計學意義,見表1。

Tab.1 Comparison of general data between the two groups表1 2組一般資料比較 [M(P25,P75)]
2.22組生化指標比較 病死組的WBC、NEU、NLR、PCT、CRP、p(CO2)高于存活組,pH值、白蛋白低于存活組(均P<0.05),余指標差異無統計學意義,見表2。
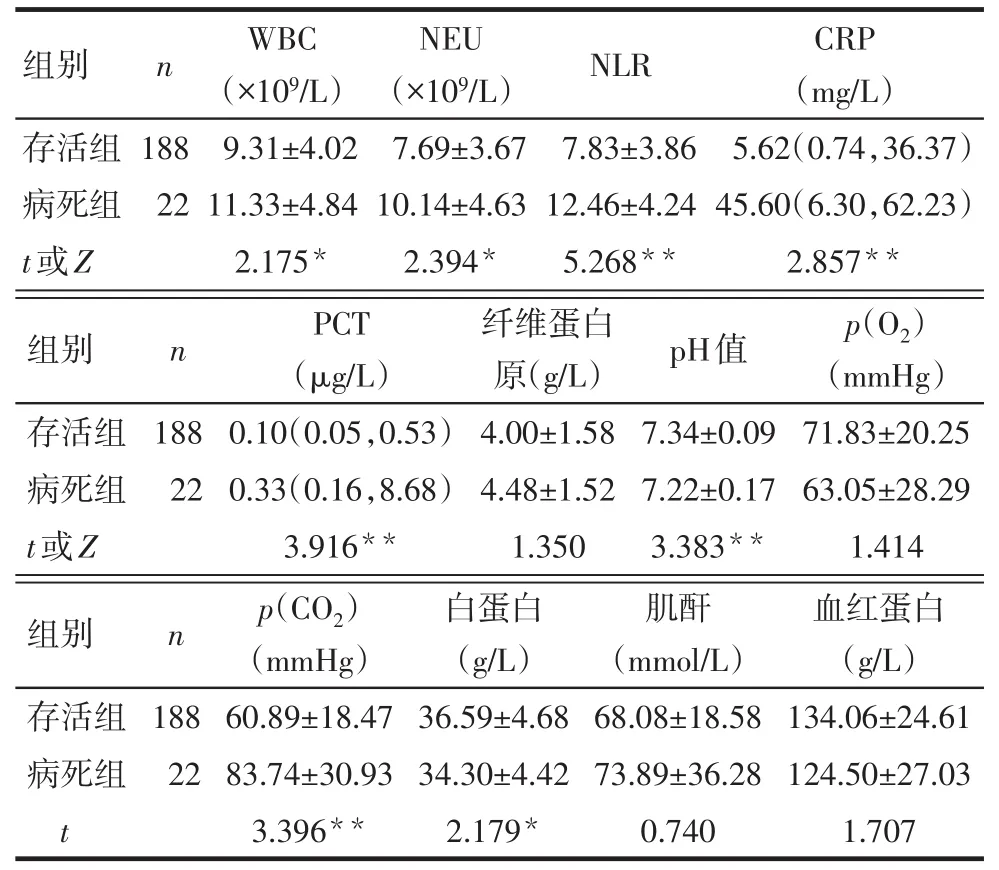
Tab.2 Comparison of biochemical indicators between the two groups表2 2組生化指標比較
2.3COPD急性加重期細菌感染患者死亡的多因素Logistic回歸分析 以是否死亡(存活=0,死亡=1)為因變量,WBC、NEU、CRP、NLR、PCT、p(CO2)、pH值、白蛋白為自變量。二分類Logistic回歸分析顯示,較高的NLR和PCT是患者死亡的危險因素,見表3。
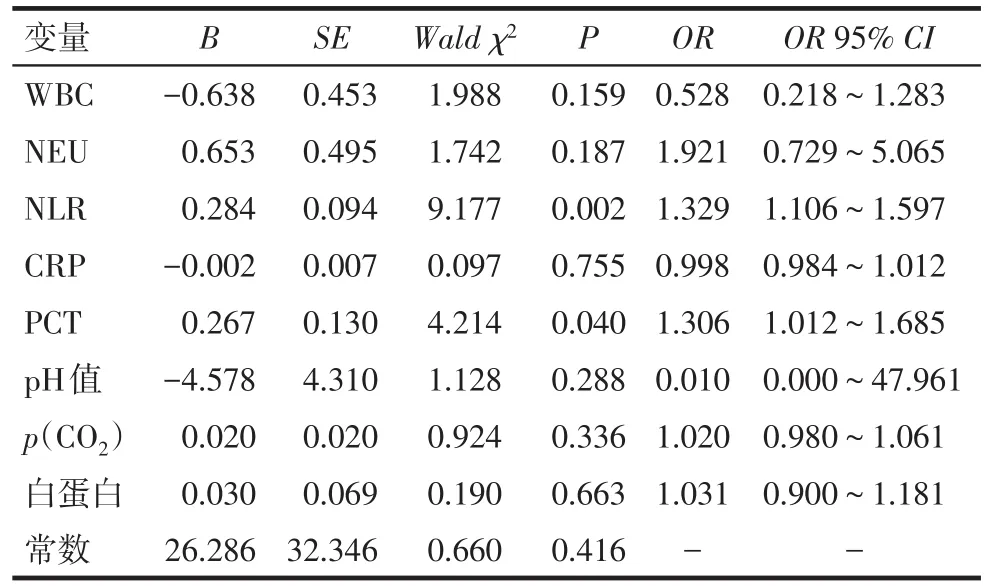
Tab.3 Multivariate Logistic regression analysis of death in patients with bacterial infection of acute exacerbation of COPD表3 COPD急性加重期細菌感染患者死亡的多因素Logistic回歸分析
2.4NLR和PCT及聯合檢測對患者預后的預測價值 以NLR和PCT為自變量作Logistic回歸分析,得到一個預測概率值即聯合檢測指標,以預測概率值為一個新的自變量。以NLR和PCT及聯合檢測指標作ROC曲線分析,結果顯示聯合預測指標的AUC高于單一指標。見表4、圖1。
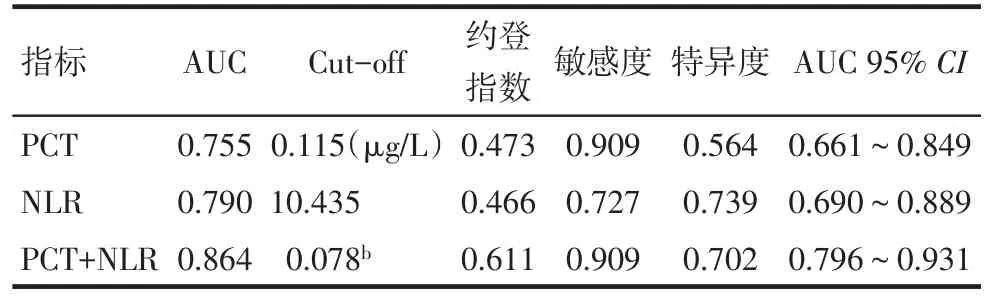
Tab.4 Predictive values of NLR,PCT and NLR combined with PCT for prognosis表4 NLR和PCT及聯合檢測對患者預后預測價值

Fig.1 ROC curves of NLR,PCT and NLR combined with PCT圖1 NLR和PCT及聯合檢測的ROC曲線
3 討論
COPD是全球常見的呼吸系統疾病,其發病率和死亡率逐年上升;造成沉重的個人及社會經濟負擔[5]。COPD急性加重常導致較高的住院率及死亡率,而約50%的COPD急性加重常由氣道細菌感染誘發[6]。本研究結果顯示,病死組的炎癥指標(WBC、NEU、CRP、NLR、PCT)明顯高于存活組。PCT是一種由甲狀腺濾泡旁細胞分泌的,在正常生理狀態下血清中含量極低的降鈣素前體物質。在細菌感染時,尤其是全身性細菌感染時血清中的PCT會明顯升高[3,7]。本研究ROC曲線顯示PCT預測患者死亡的AUC大于0.7,為0.755,最佳界值為0.115μg/L,敏感度0.909,特異度0.564,可見PCT具有良好的預測價值。同時,Logistic回歸分析顯示,患者的死亡風險與PCT值呈正相關,隨著PCT值的升高而增加。研究顯示,PCT值為2~10μg/L時,常提示患者存在膿毒癥的可能;PCT>10μg/L時,應高度懷疑存在嚴重的細菌感染或膿毒性休克[3]。可見PCT值越高,細菌感染越重,嚴重的感染會并發膿毒癥、膿毒性休克、多器官功能衰竭,從而增加患者的死亡風險。
慢性炎癥為COPD的重要發病機制,不僅存在于氣道,全身也存在持續的炎癥反應[8]。COPD急性加重會增強全身炎癥反應,促進大量的炎癥細胞、炎癥介質釋放,從而導致外周炎癥標志物升高。NLR是一種臨床上易獲取、廉價的炎癥指標,可用于描述系統性炎癥水平[9]。研究認為,NLR比傳統的炎癥指標(WBC、CRP、血沉)能更敏感地反映機體感染細菌時的炎癥水平[10]。另有研究發現,NLR能反映COPD患者的病情惡化程度[11]。Aksoy等[12]研究認為,NLR為13.0~14.0的患者需考慮入住重癥監護病房。Teng等[13]研究認為,NLR能預測COPD急性加重期患者的病死率。本研究結果顯示,病死組的NLR明顯高于存活組;ROC曲線顯示NLR的AUC為0.790,最佳界值為 10.435,敏感度 0.727,特異度0.739;Logistic回歸分析顯示,較高的NLR是患者死亡的危險因素。Yao等[14]對303例COPD急性加重期患者的研究發現,NLR≥6.24是患者死亡的高危因素。本研究中預測患者死亡的NLR界值較高,可能與本研究納入的對象均合并細菌感染有關。
目前,已有研究發現PCT聯合NLR能降低COPD急性加重期細菌感染的漏診率[15]。而將兩者聯合用于預測COPD急性加重期細菌感染住院患者死亡的報道少見。單一診斷指標之間可能會存在相互混雜的影響,通過對多個指標進行Logistic回歸分析后得到的預測概率值進行ROC曲線分析這種方法,不僅能同時校正各指標,也能排除各指標間的混雜影響及提高ROC曲線的工作性能[16-17]。目前,多指標聯合診斷的統計學方法廣泛運用于腫瘤[18]、循環系統[19]等領域。本研究通過對NLR和PCT進行Logistic回歸分析,將回歸方程新形成的預測概率值作為一個獨立的預測指標進行ROC曲線分析,ROC曲線顯示NLR聯合PCT的AUC高于單一指標,AUC為0.864,可見兩者聯合預測患者死亡的價值高于單一指標。
另外,評估COPD急性加重期細菌感染患者的死亡風險還應綜合考慮其他影響因素。呼吸道細菌感染是導致COPD急性加重的常見原因,而支原體等非典型病原體感染也會誘發COPD急性加重。本研究納入的多數患者入院前已使用抗菌藥物,可能會影響PCT和NLR。因此,還應重視非典型病原體感染誘發的急性加重情況。

