乙酰肝素酶、E-cadherin、N-cadherin和vimentin蛋白在胃癌中的表達及其意義
申志華,黃薩礎拉,#,馬秀梅*
(1.內蒙古醫科大學,內蒙古 呼和浩特010000;2.內蒙古醫科大學附屬醫院病理科,內蒙古 呼和浩特 010000)
乙酰肝素酶(heparitinase)是目前發現的哺乳動物細胞中唯一能切割細胞外基質和基底膜中硫酸乙酰肝素的內源性糖苷酶[1]。研究顯示,乙酰肝素酶的高表達與胃癌侵襲程度密切相關,與脈管內瘤栓、淋巴結或遠處轉移、高臨床分期和高微血管密度有關[2]。上皮間質轉化(epithelial-mesenchymal transition,EMT)是指上皮細胞失去其形態和功能后,逐漸轉化為間質細胞的過程,伴隨相關基因表達的改變,此改變常伴隨上皮細胞標志物鈣黏蛋白(E-cadherin)、上皮細胞黏附分子(epithelial cell adhesion molecule,EpCAM)、細 胞角蛋白(cytokeratin,CK)表達減少和間質細胞標志物波形蛋白、N-鈣黏蛋白(N-cadherin)纖維連接蛋白表達增加。EMT是癌細胞發生侵襲轉移的重要機制[3-4],由絲裂原活化蛋白激酶(mitogen-activated protein kinase,MAPKS)信號轉導通路、FAS 信號通路等多種細胞傳導途徑激活,及E-cadherin、N-cadherin 和vimentin 蛋白表達的改變將對胃癌侵襲、轉移,早期診斷有重要意義[5]。本實驗通過研究人胃癌組織中乙酰肝素酶、上皮細胞標志物E-cadherin 蛋白,間質細胞標志物N-cadherin、vimentin蛋白的表達情況與人胃癌組織臨床病理特征的關系以及它們之間的相關性,探討胃癌發生侵襲、轉移的機制。
1 材料與方法
1.1 標本來源
收集內蒙古醫科大學第一附屬醫院2015—2017年手術切除標本,病例資料完整并經病理醫師診斷為胃癌的病例91例,所有患者均知情同意,且本研究已獲得該院倫理委員會批準。標本中年齡最小者24歲,最大者81 歲;男性71 例,女性20 例;腫瘤最大者15 cm,最小者直徑為0.4 cm;低分化41例,中-低分化37例,高-中分化13例;有淋巴結轉移70例,無淋巴結轉移21 例;腫瘤位于賁門26 例,胃體30 例,胃竇及幽門35例。
1.2 主要試劑
E-cadherin 兔抗人多克隆抗體、β-catenin 兔抗人多克隆抗體、N-cadherin兔抗人多克隆抗體、vimentin兔抗人多克隆抗體,均購自博奧森生物技術公司。即用型SP 試劑盒、DAB 顯色劑,均購自邁新生物技術公司。
采用4 μm連續切片,常規脫蠟和水化。3% H2O2滅活內源性過氧化物酶,采用枸櫞酸鹽緩沖液(0.01 mol/L,pH=6.4)在800 W 微波爐中進行抗原修復,每次3 min,間隔1 min。分別加入兔抗人多克隆抗體HPA (1∶100 稀 釋)、E-cadherin(1∶250 稀 釋)、Ncadherin (1∶250 稀釋)和vimentin(1∶100 稀釋)4 ℃孵育過夜。然后加入IgG(HRP復合體在37 ℃恒溫箱孵育30 min。DAB 顯色,蘇木精復染細胞核。每次以PBS代替一抗作為陰性對照,以已知陽性反應切片作為陽性對照。
1.3 對照設置及結果判定
兩名病理醫師按半定量評分方法獨立評分:每例切片隨機選取5 個高倍視野,無色計為0 分,淡黃色為1分,棕黃色為2分,棕褐色為3分;陽性細胞數≤5%時計為0分,>5%~25%為1分,>25%~50%為2分,>50%~75%為3分,>75%為4分。染色強度得分與陽性細胞數得分相乘。
1.4 統計學分析
HPA、E-cadherin、N-cadherin 和vimentin 蛋白陽性表達率與人胃癌臨床病理指標的關系,胃癌起始部位與侵襲深處表達情況,采用卡方檢驗;HPA蛋白在人胃癌中陽性表達率與E-cadherin、N-cadherin 和vimentin 蛋白陽性表達率的相關性,采用Spearman 等級相關。
2 結 果
2.1 HPA、E-cadherin、N-cadherin 和vimentin 蛋白在胃癌中的表達
91 例人胃癌組織中HPA 蛋白陽性表達率75.82%,主要定位在人胃癌細胞胞漿(圖1);Ecadherin 蛋白陽性表達率為51.65%,主要在高分化胃癌細胞胞膜高表達,低分化胃癌中低表達(圖2);Ncadherin蛋白陽性表達率為54.95%,vimentin蛋白陽性表達率為23.08%,在癌細胞胞膜、胞漿均有所表達,且在低分化胃癌呈高表達(圖3、4)。
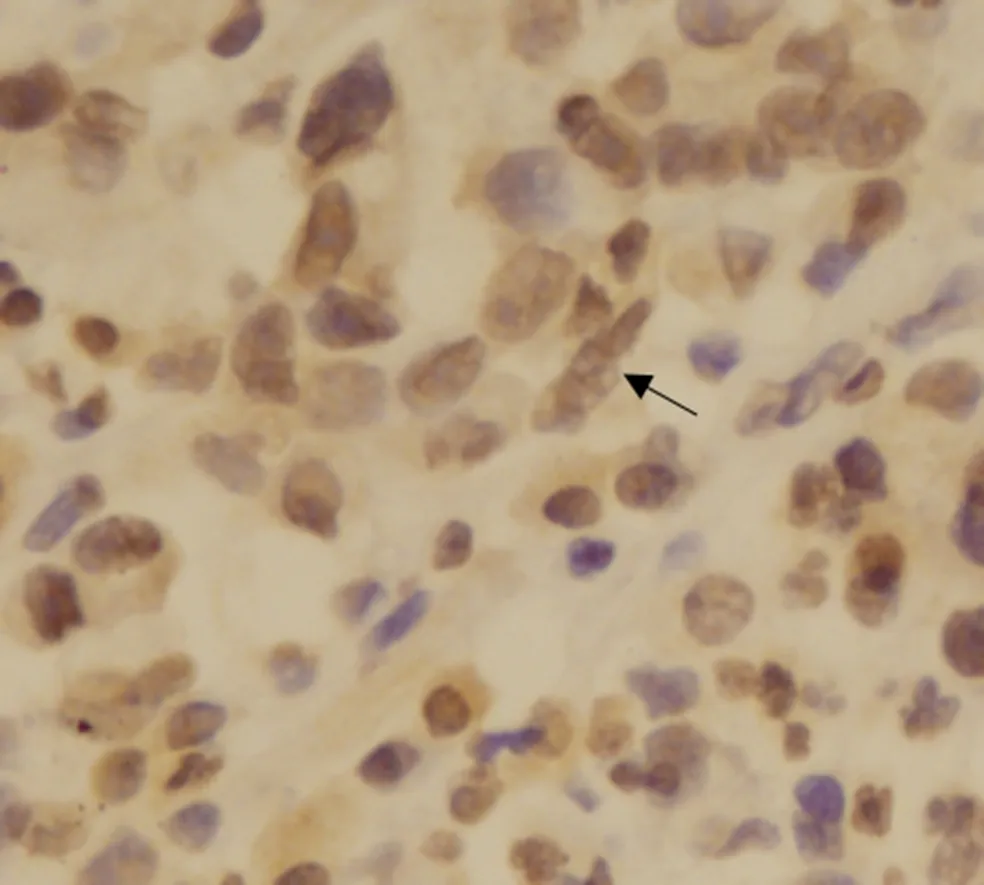
圖1 免疫組化染色顯示HPA 在中分化人胃癌細胞胞漿中表達,呈棕褐色(×400)

圖2 免疫組化染色顯示E-cadherin 在高分化胃癌細胞胞膜中表達,呈棕褐色(×400)
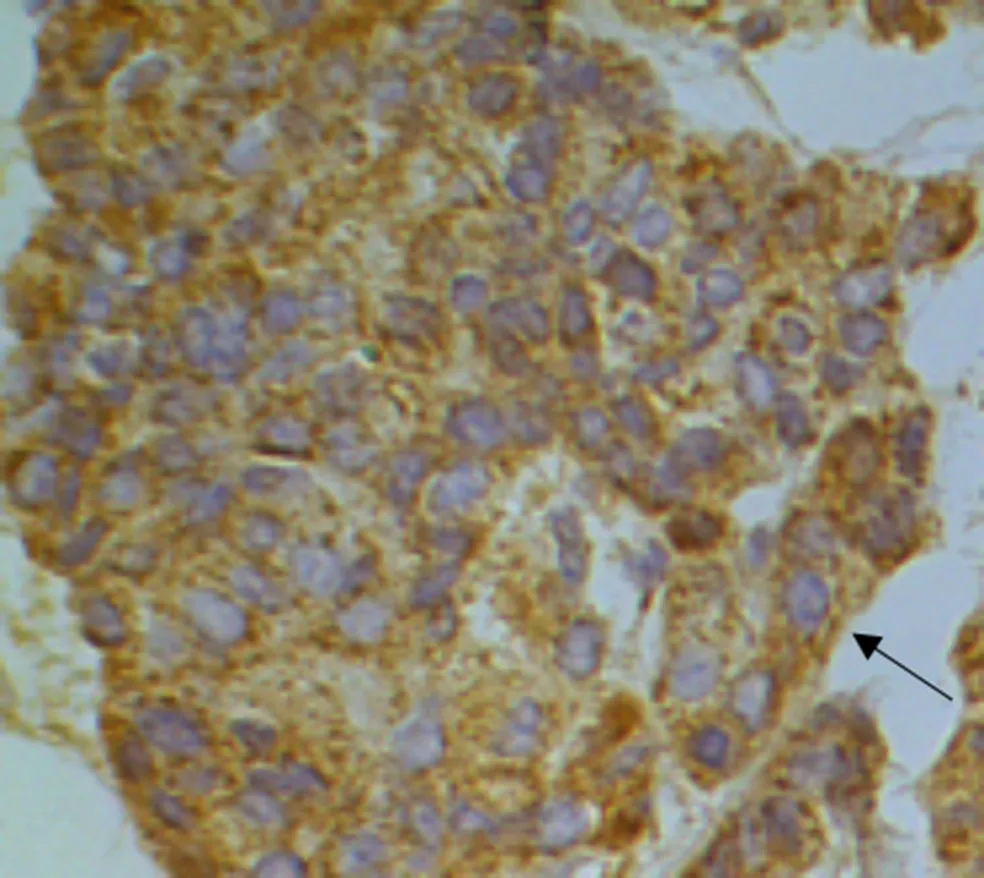
圖3 免疫組化染色顯示N-cadherin 在低分化胃癌中表達,呈棕褐色(×400)
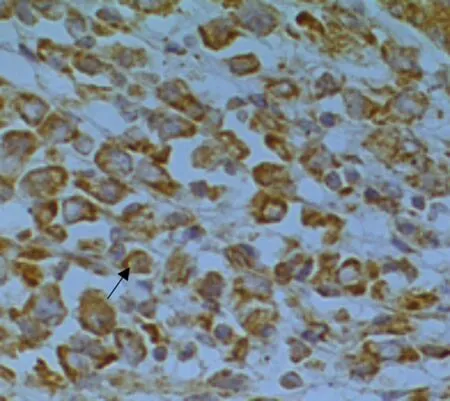
圖4 免疫組化染色顯示vimentin 在低分化胃癌中表達,呈淡黃色(×400)
2.2 人胃癌組織中HPA 蛋白表達與臨床病理指標的關系
人胃癌組織中HPA蛋白陽性表達率與不同臨床病理指標的關系見表1。HPA 蛋白陽性率在不同患者年 齡(χ2=0.124,F=0.725)、性別(χ2=0.009,P=0.922)和胃癌大小(χ2=0.018,P=0.892)間的差異無統計學意義,而在不同發生部位、分化程度、淋巴結轉移情況間的差異具有統計學意義(P<0.05)。其中賁門部胃癌HPA蛋白陽性率為88.46%,胃體胃癌HPA 蛋白陽性率為86.67%,胃竇、幽門部胃癌HPA 陽性率為57.14%,賁門部胃癌HPA蛋白陽性率明顯高于胃體、胃竇及幽門部胃癌(χ2=10.852,P=0.004);低分化胃癌HPA蛋白陽性率為92.68%,高/中分化胃癌HPA 蛋白陽性率為62%,低分化胃癌HPA蛋白陽性率明顯高于高、中分化胃癌(χ2=9.956,P=0.002);有淋巴結轉移者HPA 蛋白陽性率為82.86%,無淋巴結轉移者HPA蛋白陽性率為52.38%,有淋巴結轉移者HPA蛋白陽性率明顯高于無淋巴結轉移者(χ2=8.185,P=0.004)。
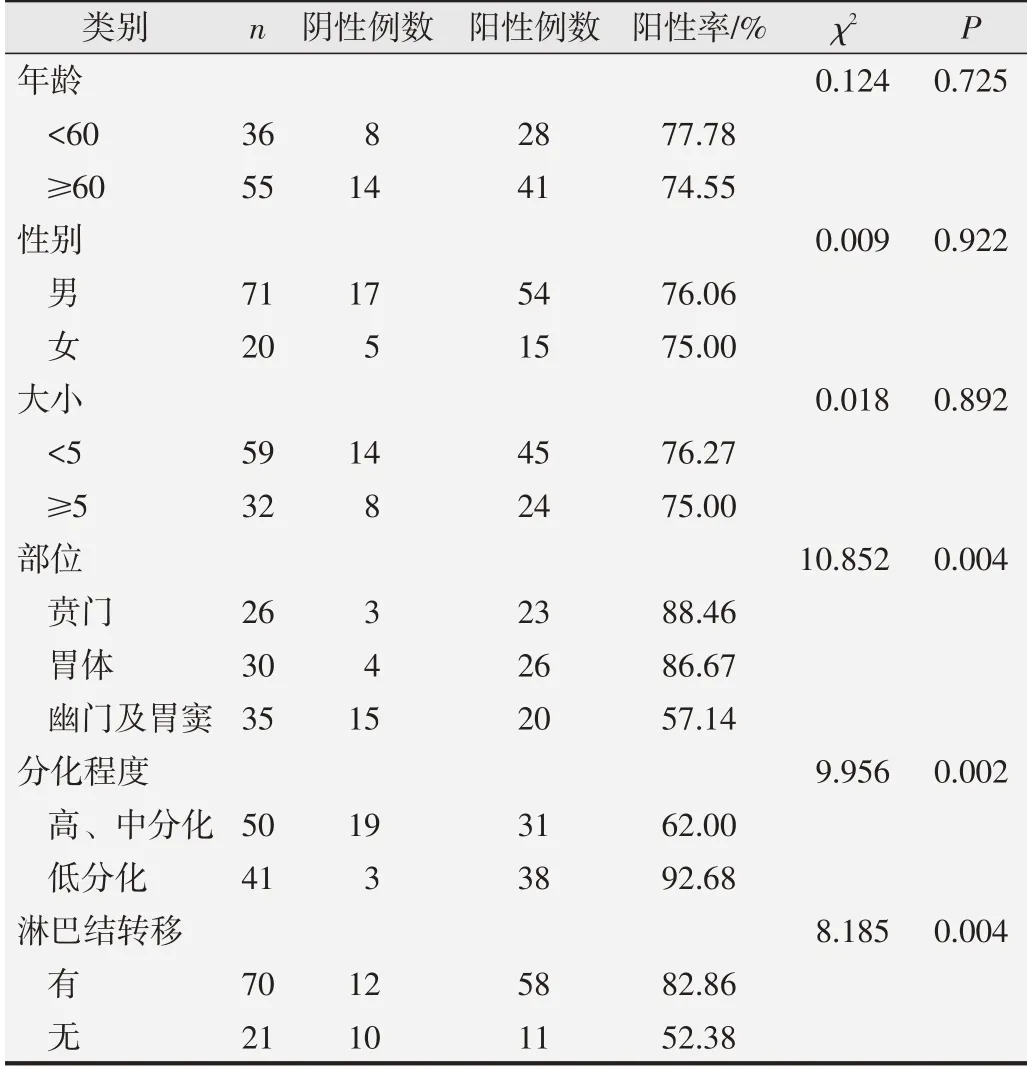
表1 HPA蛋白陽性表達率與不同臨床病理指標的關系
2.3 人胃癌組織中E-cadherin 蛋白表達與臨床病理指標的關系
人胃癌組織中E-cadherin 蛋白陽性表達率與不同臨床病理指標的關系見表2。E-cadherin蛋白陽性表達率 在 不 同 患 者 年 齡(χ2=3.155,P=0.078)、性 別(χ2=0.454,P=0.501)、胃癌大小(χ2=0.043,P=0.836)間的差異無統計學意義(P>0.05),而在不同胃癌發生部位、分化程度、淋巴結轉移情況間的差異具有統計學意義(P<0.05)。E-cadherin蛋白在賁門部胃癌患者中陽性率為34.62%,在胃體胃癌患者中陽性率為36.67%,胃竇、幽門部胃癌患者陽性率為74.14%,E-cadherin 在賁門部胃癌患者中陽性率明顯低于胃體、胃竇及幽門部(χ2=14.826,P=0.001);高/中分化胃癌患者中陽性率為74%,低分化胃癌患者中陽性率為24.39%,高/中分化胃癌患者中陽性率明顯高于低分化者(χ2=22.201,P=0.000);有淋巴結轉移者陽性率為40%,無淋巴結轉移者陽性率為90.48%,有淋巴結轉移者陽性率低于無淋巴結轉移者(χ2=14.522,P=0.000)。
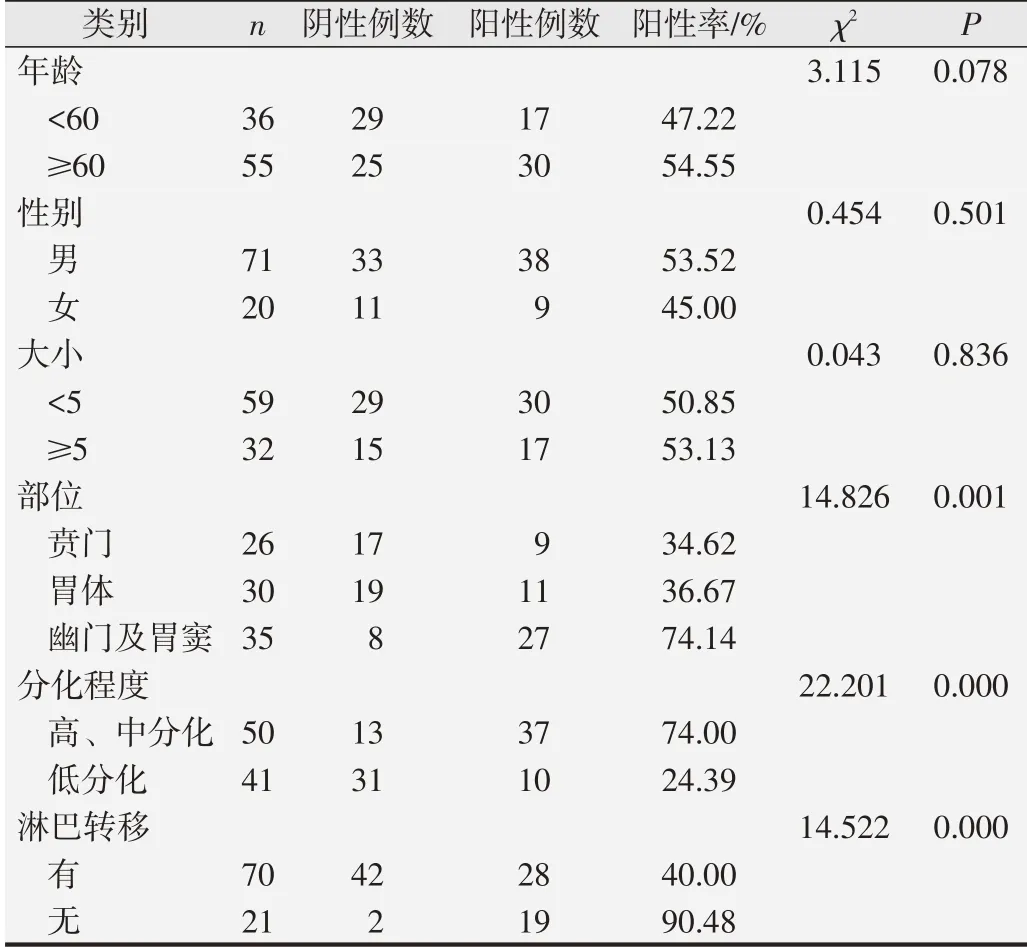
表2 E-cadherin蛋白陽性表達率與不同臨床病理指標的關系
2.4 人胃癌組織中N-cadherin 蛋白表達與臨床病理的指標關系
N-cadherin 蛋白在人胃癌組織中陽性表達率為54.95%,在不同患者年齡(χ2=0.009,P=0.925)、性別(χ2=1.024,P=0.312)、胃癌大小(χ2=1.138,P=0.286)間的差異無統計學意義(P>0.05),而在不同發生部位、分化程度、淋巴結轉移情況間的差異具有統計學意義(P<0.05)。N-cadherin蛋白在賁門部胃癌患者中陽性率為69.23%,胃體胃癌患者中陽性率為66.67%,胃竇、幽門部胃癌患者中陽性率為34.29%,N-cadherin蛋白在賁門部胃癌患者中陽性率明顯高于胃體,胃竇及幽門部患者,差別具有統計學意(χ2=9.843,P=0.007);N-cadherin蛋白在低分化胃癌患者中陽性率為68.29%,高/中分化胃癌患者中陽性率為44%,低分化胃癌患者中陽性率明顯高于高/中分化者,差別具有統計學意義(χ2=5.370,P=0.02);N-cadherin 蛋白在有淋巴結轉移者陽性率為65.71%,無淋巴結轉移者陽性率為19.05%,有淋巴結轉移者陽性率明顯高于無淋巴結轉移者,差別具有統計學意義(χ2=14.211,P=0.00)。詳情見表3。
2.5 人胃癌組織中vimentin蛋白表達與臨床病理指標的關系
Vimentin 蛋白在人胃癌組織中表達為23.08%,在不同 患者 年 齡(χ2=0.443,P=0.506)、性 別(χ2=0.053,P=0.817)、胃癌大小(χ2=0.040,P=0.841)間的差異無統計學意義(P>0.05),而在不同發生部位、分化程度、淋巴結轉移情況間的差異具有統計學意義(P<0.05)。其中vimentin 蛋白在賁門胃癌患者中陽性率為30.77%,胃體胃癌病例中vimentin 蛋白陽性率為30.00%,胃竇、幽門部胃癌患者中陽性率為11.43%,賁門胃癌患者中陽性率明顯高于胃體、胃竇及幽門部,差 別 具 有 統 計 學 意 義(χ2=10.195,P=0.006);vimentin 蛋白在高/中分化胃癌患者中陽性率為12%,低分化胃癌患者中陽性率為36.59%,高/中分化胃癌患者中陽性率明顯低于低分化著,差別具有統計學意義(χ2=7.671,P=0.006);vimentin 蛋白在有淋巴結轉移者中陽性率為28.57%,無淋巴結轉移者中陽性率為4.76%,有淋巴結轉移者中陽性率明顯高于無淋巴結轉移者,差別具有統計學意義(χ2=3.905,P=0.048)。詳細結果見表4。
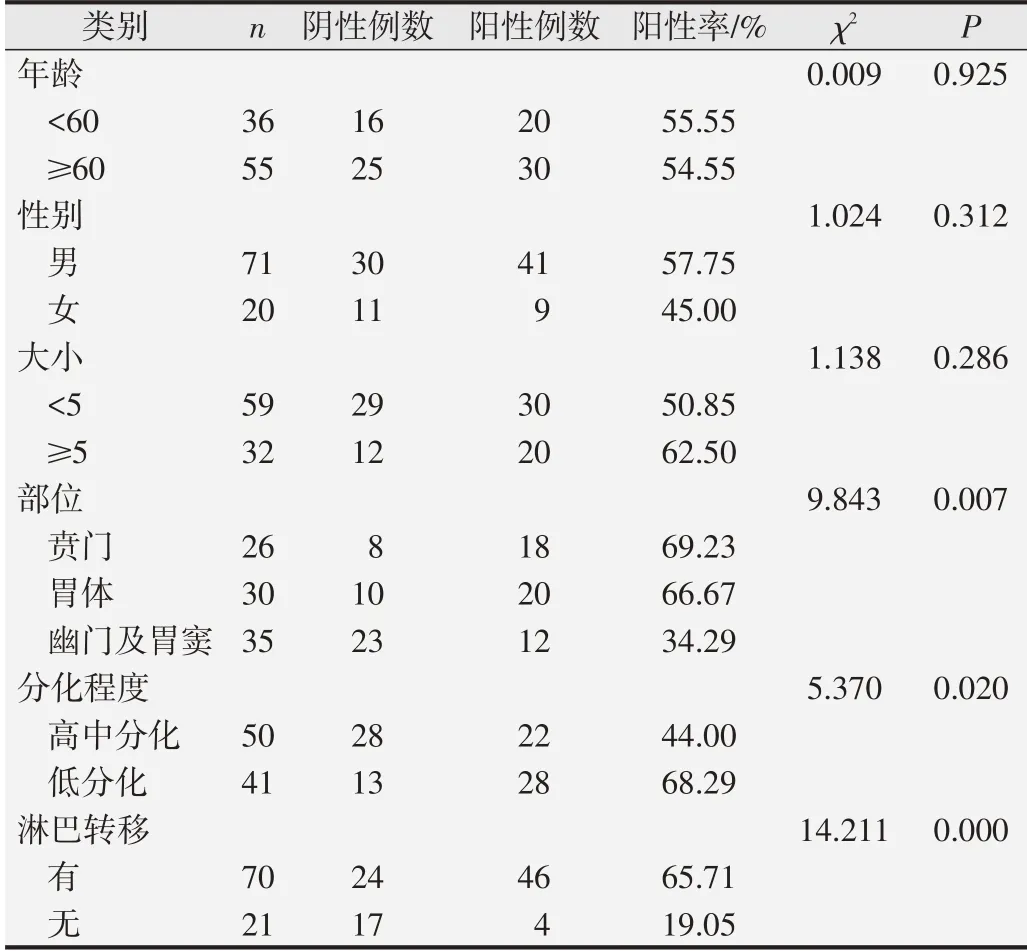
表3 N-cadherin的表達與胃癌臨床病理指標的關系
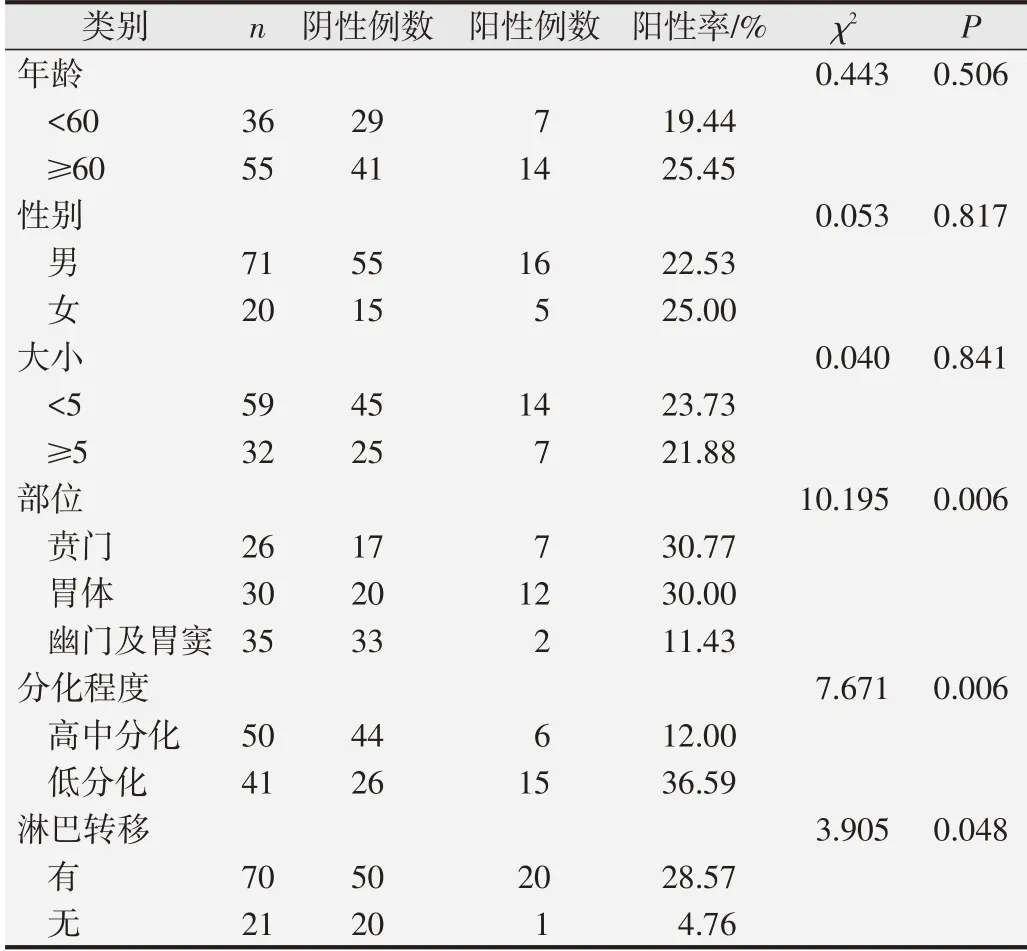
表4 vimentin蛋白在人胃癌組織中的陽性表達率與不同臨床病理指標的關系
2.6 HPA、E-cadherin、N-cadherin 和vimentin 蛋白在胃癌原發灶與侵襲深處的表達
HPA、E-cadherin、N-cadherin 和vimentin 蛋白在胃癌原發灶與侵襲深處表達差異有統計學意義(P<0.05)。其中HPA 蛋白在胃癌原發灶陽性率為75.82%,在胃癌侵襲深處陽性率為87.91%,HPA在胃癌原發灶陽性率明顯低于胃癌侵襲深處(χ2=4.479,P=0.027)。E-cadherin 蛋白在胃癌原發灶陽性率為51.65%,在胃癌侵襲深處陽性率為36.26%,E-cadherin 蛋白在胃癌原發灶陽性率明顯高于胃癌侵襲深處(χ2=4.372,P=0.026)。N-cadherin 蛋白在胃癌原發灶陽性率為54.95%,在胃癌侵襲深處陽性率為73.63%,Ncadherin蛋白在胃癌原發灶陽性率明顯低于胃癌侵襲深處(χ2=6.916,P=0.013)。vimentin 蛋白在胃癌原發灶陽性率為23.08%,在胃癌侵襲深處陽性率為38.46%,vimentin蛋白在胃癌原發灶陽性率明顯低于胃癌侵襲深處(χ2=5.056,P=0.025)。詳情見圖5~8和表5。
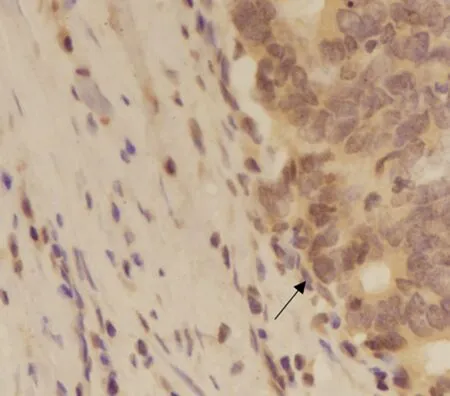
圖5 免疫組化染色顯示HPA在胃癌侵襲深處陽性表達(×400)
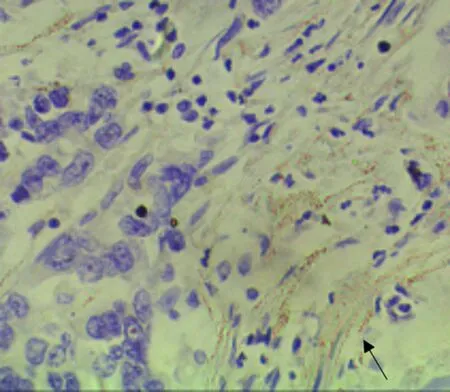
圖6 免疫組化染色顯示E-cadherin 在胃癌侵襲深處表達,呈棕黃色(×400)
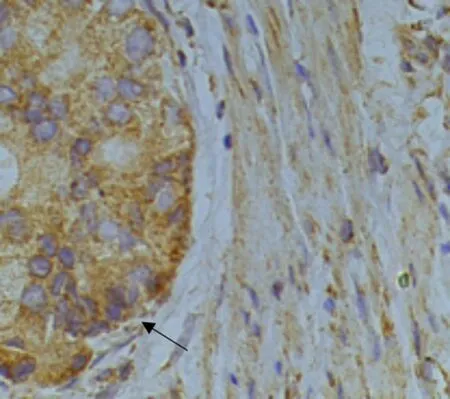
圖7 免疫組化染色顯示N-cadherin 在胃癌侵襲深處表達,呈棕褐色(×400)
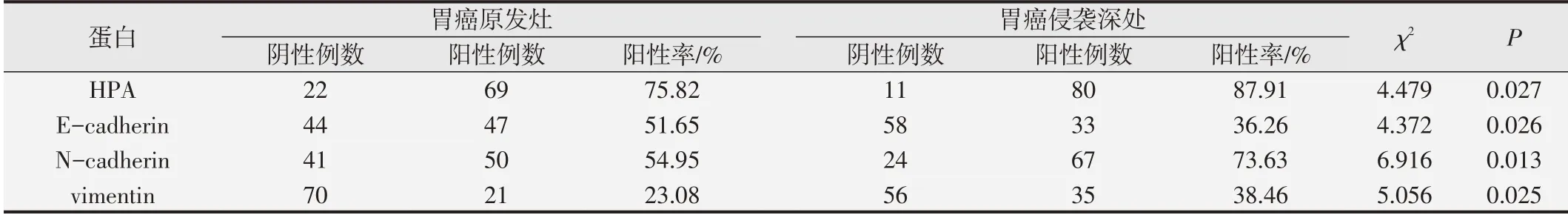
表5 胃癌原發灶與侵襲深處HPA、E-cadherin、N-cadherin、vimentin蛋白表達
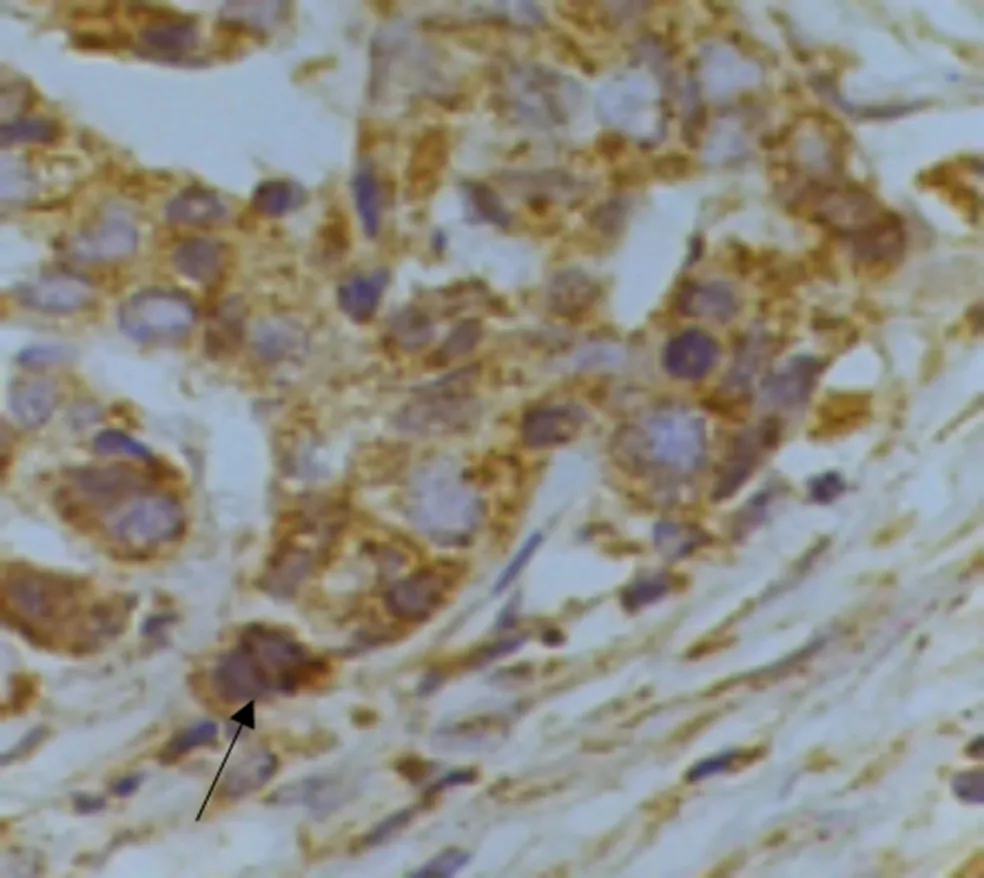
圖8 免疫組化染色顯示vimentin 在胃癌侵襲深處表達,呈棕黃色(×400)
2.7 人胃癌組織中HP 與E-cadherin、HPA 與Ncadherin、HPA與vimentin蛋白相互關系
在人胃癌細胞中,HPA、E-cadherin、N-cadherin和vimentin 蛋白的表達與人胃癌組織的位置、分化程度、有無淋巴結轉移密切相關,經Spearman等級相關分析(表6)顯示HPA、E-cadherin、N-cadherin和vimentin蛋白之間也存在相關性,HPA與Ecadherin蛋白在胃癌組織中陽性率呈負相關性,結果有統計學意義(r=-0.341,P=0.005)。HPA 與N-cadherin 蛋白在人胃癌組織中的表達呈正相關(r=0.366,P=0.001),HPA 與vimentin 蛋白在人胃癌組織中的表達呈正相關性(r=0.248,P=0.038),結果有統計學意義。
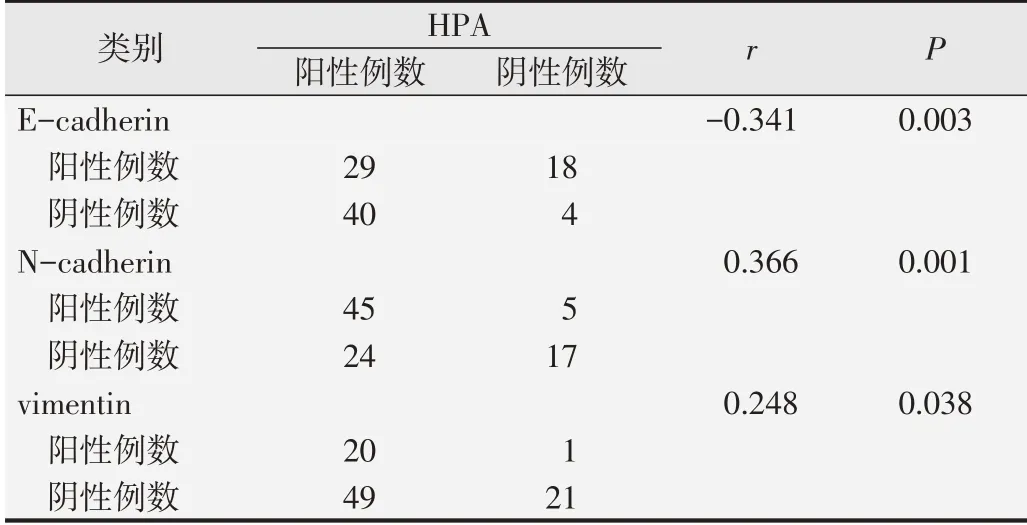
表6 HPA與E-cadherin、N-cadherin、vimentin蛋白表達的關系
3 討 論
HPA主要在造血細胞和胎盤中表達,其他組織未見,而在很多腫瘤組織,乙酰肝素酶mRNA 和蛋白質均呈高表達,而腫瘤周圍正常組織檢測不到。一些學者研究顯示,HPA的高表達與結腸癌、胰腺癌、膀胱癌和宮頸癌等惡性腫瘤的高淋巴結轉移、高遠處轉移、高微血管密度和預后差有關。因HPA的存在細胞更易于被轉移性癌細胞和免疫系統細胞入侵[6]。沉默HPA基因可抑制腫瘤細胞的增殖和轉移,其機制可能與HPA 蛋白基因可抑制腫瘤細胞的增殖與轉移有關[7]。本研究發現人胃癌組織中HPA、N-cadherin 和vimentin 蛋白在低分化者明顯高于高分化者;有淋巴結轉移者明顯高于無淋巴結轉移者,可見HPA、Ncadherin和vimentin蛋白與胃癌惡性程度高,侵襲、轉移有關。E-cadherin 蛋白在高中分化胃癌者陽性表達率明顯高于低分化胃癌者、無淋巴結轉移者明顯高于有淋巴結轉移者。可見E-cadherin 蛋白與胃癌惡性程度高,侵襲、轉移無關。Yang 等[8]的研究結果也發現,HPA 蛋白除通過降解HS 促進腫瘤進展外,還通過增加syndecan-1 從腫瘤細胞表面脫落促進腫瘤進展,其機制可能增強細胞的黏附性和信號轉導(如蛋白激酶B/AKT、Src、表皮生長因子、肝細胞生長因子和胰島素受體通路)等途徑來促進腫瘤細胞發生侵襲和轉移。
EMT 是腫瘤進展中的關鍵事件[9],伴隨著各種蛋白標志物的改變與相關信號通路的激活和抑制。Ecadherin 蛋白減少或丟失及N-cadherin、vimentin 蛋白表達增強是EMT 的標志,本研究發現HPA、Ncadherin和vimentin蛋白陽性表達率在侵襲深處明顯高于起始部位,可見這3 種蛋白與胃癌侵襲轉移有關;E-cadherin 蛋白陽性表達率在侵襲深處明顯低于原發灶,可見E-cadherin 蛋白缺失或者減少,與胃癌侵襲轉移無關。因此,胃癌的侵襲、轉移發生著EMT。EMT是指上皮細胞能夠在細胞基質間自由移動演變成間質細胞過程,也是癌細胞從原發灶脫落轉移的過程,眾多相關研究發現,在膀胱癌、食管癌、非小細胞肺癌、乳腺癌等許多來源于上皮的腫瘤,均常常發生E-cadherin 蛋白表達的缺失或減少[10]。研究還表明N-cadherin 蛋白的上調促進腫瘤細胞侵襲[11]。Ecadherin 蛋白減少和N-cadherin、vimentin 蛋白增加隨后發生EMT的潛在分子機制尚未研究清楚。近期,有些學者研究顯示,纖維母細胞生長因子-2(fibrolast growth factor-2,FGF-2)誘導腎小管上皮細胞發生EMT中HPA蛋白是必需的。本實驗通過免疫組化學方法檢測了人胃癌組織中HPA、E-cadherin、Ncadherin、vimentin 蛋白與不同病理指標的關系。發現HPA 與N-cadherin、HPA 與vimentin 蛋 白 呈 正 相 關,而與E-cadherin 蛋白呈負相關,所以HPA蛋白可能誘導胃癌細胞發生EMT。Zhang 的研究證實了EMT 與食管癌的發生發展密切相關[12]。對于HPA蛋白通過何種調節途徑促進胃癌細胞發生EMT 促使胃癌發生浸潤,轉移的機制還需深入研究。這將為胃癌特異性治療提供新的思路和依據,具有廣泛的臨床意義和良好的應用前景。本研究還存在一定的不足和局限性,選取樣本量較小,對于患者HPA、E-cadherin、N-cadherin、Vimientin 蛋白與其臨床病理特征相關研究不夠完善,需進一步擴大樣本數量,增加相關性研究的深度。
有研究表明,通過阻斷HPA 蛋白抑制胃癌發生EMT途徑,有望抑制胃癌侵襲和轉移。我們的下一步研究是關于HPA蛋白誘導胃癌發生EMT的機制。EMT賦予腫瘤細胞轉移與侵襲能力的啟動步驟,為腫瘤細胞穿透基底膜、通過血液和淋巴循環轉移至遠端組織器官提供了前提條件,獲得遷移能力的腫瘤細胞對放化療的耐受性也增加,進而增加了術后復發與轉移的風險[13-14]。

