肉芽腫性多血管炎合并彌漫性肺泡出血一例報道并文獻復習
陸翠,蘇禹同,滕佳臨,楊程德,葉俊娜*
本文價值:
彌漫性肺泡出血是肉芽腫性多血管炎的罕見表現,表現為咳嗽、呼吸困難和咯血等,一旦發生,進展迅速,死亡率高。本文報道1例肉芽腫性多血管炎合并彌漫性肺泡出血患者,早期診斷后即給予積極治療,預后良好。提示對此類患者早期識別和積極搶救對預后至關重要。
肉芽腫性多血管炎(GPA)曾被稱為韋格納肉芽腫(WG),是一種少見的全身性疾病,其特征為壞死性肉芽腫性血管炎,主要影響上呼吸道、肺部和腎臟[1]。彌漫性肺泡出血(DAH)是GPA的罕見表現,一旦出現,病情危重,死亡率高,目前僅有少數個案報道[2-12]。本研究報道上海交通大學醫學院附屬瑞金醫院風濕免疫科收治的1例GPA合并DAH患者,并結合相關國內外文獻,分析該病的病因、臨床表現、實驗室及影像學特征、治療和預后,以期提高臨床醫生對該病的認識。
1 病例簡介
患者,女,24歲,因鼻腔血性分泌物3個月、咳嗽1個月于2018-10-11入本院。患者2018年7月開始出現反復鼻腔血性分泌物,外院鼻竇CT提示鼻竇炎,給予抗感染等治療,效果不佳。1個月前出現咳嗽、痰中帶血,伴胸痛、聽力下降,2周前出現反復結膜充血,伴雙下肢麻木、疼痛不適,病程中發熱2次,肉眼血尿1次,無呼吸困難、咯血,無皮疹、關節腫痛。有重癥肌無力病史。查體:神清,氣平,持續性咳嗽,雙眼球結膜充血(見圖1),鼻腔血性分泌物,上頜竇壓痛(+),雙肺呼吸音低,未聞及啰音。輔助檢查:白細胞計數(WBC)9×109/L,血紅蛋白(Hb)108 g/L,血小板計數(PLT)308×109/L;紅細胞沉降率(ESR)74 mm/1 h;尿常規:蛋白(+),紅細胞31~50個/HPF,隱血(+++);24 h尿蛋白定量326 mg;抗中性粒細胞胞質抗體(c-ANCA)陽性,蛋白酶3特異性抗中性粒細胞胞質抗體(PR3-ANCA)209.90(參考范圍<20.00),抗中性粒細胞核周抗體(p-ANCA)陰性,髓過氧化物酶抗體(MPO)陰性;血清清蛋白26 g/L;血肌酐處于參考范圍內;抗核抗體(ANA)陰性、抗雙鏈DNA(dsDNA)抗體陰性、抗可溶性抗原抗體(ENA)陰性;類風濕因子(RF)陰性;補體處于參考范圍內。胸部CT:雙肺多發斑片、結節及索條影伴實變影;左肺門飽滿、右肺門增大,兩側主氣管及部分支氣管管腔變窄、管壁增厚(見圖2A);肌電圖:左側正中神經傳導延遲。診斷:GPA,因患者劇烈咳嗽、胸部CT較2周前新發彌漫性斑片狀陰影,考慮合并DAH,予甲潑尼龍500 mg沖擊治療3 d,逐漸減量,并靜脈注射人丙種球蛋白(IVIG)20 g 5 d,環磷酰胺(CTX)0.4 g沖擊治療1次,第5天復查胸部CT雙肺斑片狀磨玻璃影、實變影明顯好轉(見圖2B),第12天復查胸部CT病灶進一步被吸收(見圖2C),1個月后復查c-ANCA陰性,PR3-ANCA 136.64,隨訪半年,病情穩定,CTX沖擊治療共7次,未再出現DAH。
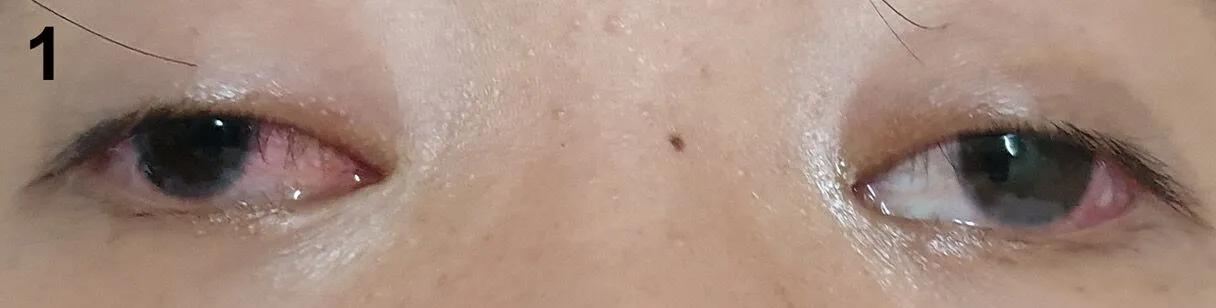
圖1 雙眼球結膜充血Figure 1 Binocular conjunctival congestion
2 文獻檢索
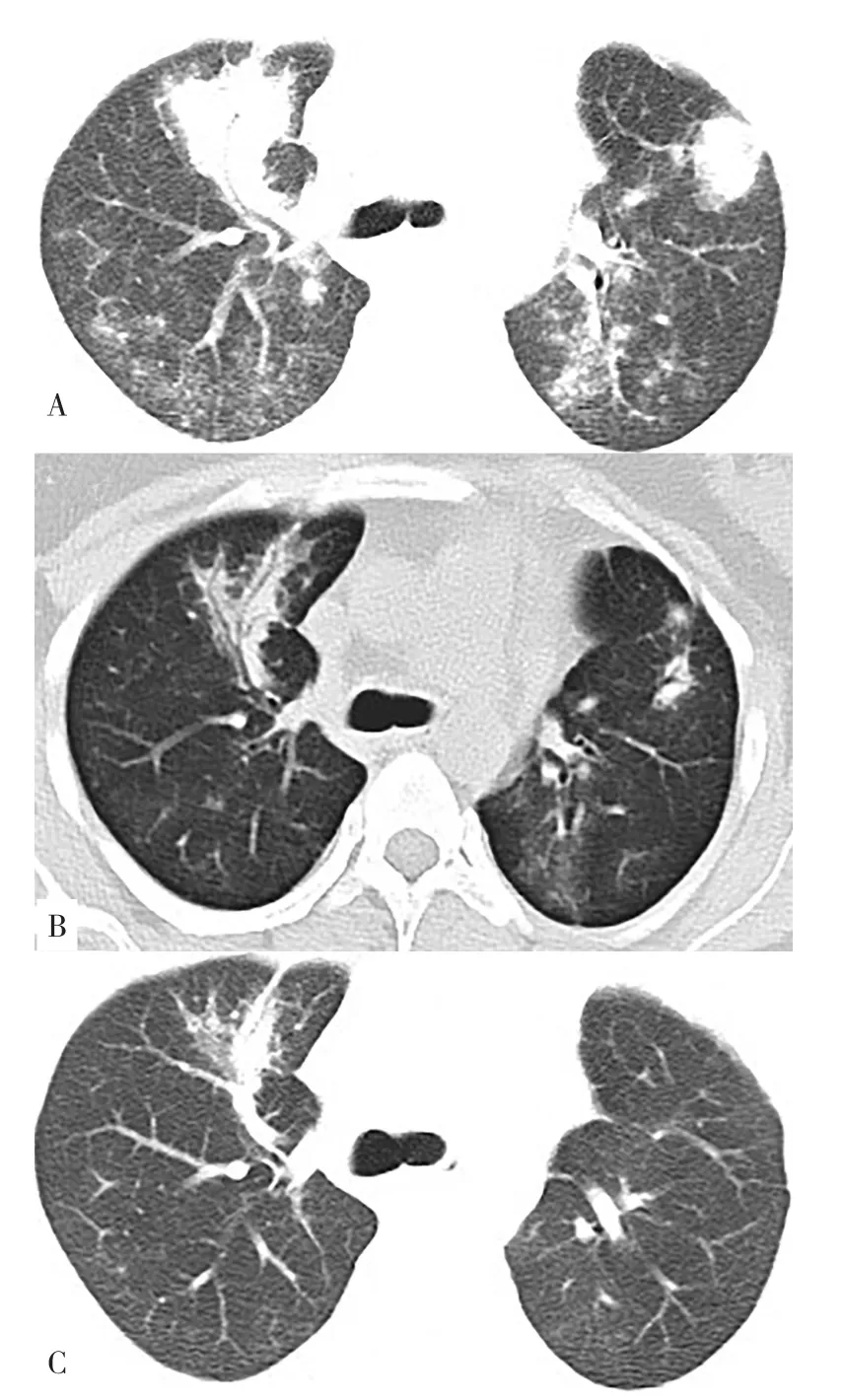
圖2 胸部CT檢查結果Figure 2 The results of chest computed tomography
以“韋格納,血管炎,肉芽腫性多血管炎,肺出血,肺泡出血”為關鍵字,搜索萬方數據知識服務平臺、中國知網、PubMed數據庫1980年1月—2019年2月公開發表的GPA/WG合并DAH的病例。納入標準:有具體病例資料,診斷明確。排除標準:重復報道、同時合并其他結締組織病、薈萃分析和綜述。
共收集到國內外文獻報道13例,剔除同時合并系統性紅斑狼瘡(SLE)1例,共12例[2-12],結合本病例,共納入13例患者。其中男7例,女6例;年齡7~70歲,平均年齡(38.6±19.3)歲;病程1 d~6個月,平均病程(72.1±62.7)d,病程較短,多數在發病3個月內發生DAH;治療多選擇大劑量激素沖擊治療和CTX治療;死亡率23.1%(3/13);詳見表1。
13例患者中,10例患者有Hb記錄,其Hb為(75.8±24.9)g/L;多數患者伴發熱,合并腎臟、眼、耳、鼻等多器官受累,常見咳嗽(83.3%)、呼吸困難(83.3%)、咯血(41.7%)等表現,胸部影像學檢查多見多發斑片、磨玻璃影或彌漫性浸潤影、結節、實變影等(見表2)。1例行右上肺葉切除術,病理示肺泡壁彌漫性增厚,含中等量單核細胞,偶見嗜酸粒細胞;肺泡含有大量巨噬細胞(其中一些含有含鐵血黃素);小范圍組織性肺炎并壞死[2]。1例于就診當天死亡,尸檢肺部病理示:肺彌漫性水腫,左肺上葉結節,彌漫性肺泡損傷及DAH,出血區域見毛細血管炎,肺泡間隔被中性粒細胞破壞[6]。
3 討論
GPA是一種與抗中性粒細胞胞質抗體(ANCA)相關的血管炎,主要累及小血管,其特征是壞死性肉芽腫性炎癥,臨床表現和預后因不同的受累器官及系統而有所差異,發病初期可表現為非特異性全身癥狀,以后可累及重要臟器,威脅生命。DAH是肺血管炎的嚴重表現,最常見于小血管炎,特別是GPA和顯微鏡下多血管炎(MPA),也可見于Goodpasture綜合征、過敏性紫癜和SLE,少見繼發于感染和藥物或毒素[13]。GPA合并DAH臨床較為罕見,一旦出現多急性起病,病情進展迅速,死亡率高。本研究報道1例GPA合并DAH患者,結合相關國內外文獻,分析該病的病因、臨床特點、治療和預后,以期提高臨床醫生對該病的認識。本例患者經早期診斷及積極救治,預后良好,因此提高對該病的認識、早期積極治療對該病的預后至關重要。
3.1 流行病學 雖然肺是GPA中最常見的靶器官,但出現DAH者較為罕見,發生率僅為6.1%~14.9%[14-15]。本研究發現該病平均年齡40歲左右,兒童及老年人較少見,男女比無明顯差異。
3.2 病因和發病機制 ANCA可誘導中性粒細胞脫顆粒,產生氧自由基和釋放蛋白酶,導致肺血管內皮和毛細血管損傷,引起小血管彌漫性肺泡內出血[16],這可能是GPA患者發生DAH的原因。
3.3 臨床表現 本研究文獻分析顯示,DAH多在GPA起病3個月內出現,前期可有發熱,同時伴結膜炎、鼻塞、鼻腔血性分泌物、中耳炎、皮疹、關節痛、腎臟損害等其他系統表現,其中以腎臟損害(83.3%)最常見。SAUVAGET等[17]曾報道66例GPA,其中合并DAH的9例均伴有急進性腎炎。
本研究文獻分析顯示,肺部表現主要為咳嗽(83.3%)、呼吸困難(83.3%)、咳痰(41.7%)、咯血(41.7%)、胸痛(25.0%)和痰中帶血(25.0%),多數有嚴重呼吸困難,需氣管插管等輔助通氣支持。本例患者表現為呼吸困難及咳嗽,咳嗽為難以控制的刺激性咳嗽,并痰中帶血,但無咯血。有研究認為約1/3的DAH患者不會出現咯血,因為肺泡體積足以容納血液并阻止其擴散到支氣管中[18]。
DAH可作為GPA患者的首發表現,也可在其他系統表現之后出現或在糖皮質激素和免疫抑制治療期間出現,甚至有報道顯示在大劑量激素沖擊治療后出現DAH[3-4,19],DAH經治療好轉后仍有復發可能[11,19],因此不論在疾病的任何階段均需要警惕DAH的發生。
3.4 實驗室檢查 本研究文獻分析顯示,GPA患者血常規多見輕到中度貧血,提示短期內出現不明原因的Hb下降需特別注意DAH的發生。尿液檢查可見蛋白尿、血尿,少見尿管型,可伴24 h尿蛋白定量升高。ESR多增快,提示DAH多在疾病活動時發生。所有患者有c-ANCA或PR3陽性,病情好轉后可轉陰或滴度下降[11],本例患者經治療好轉,1個月后復查,c-ANCA轉陰,PR3滴度明顯下降。因此,c-ANCA或PR3可作為疾病治療后療效判定的指標之一。部分GPA患者可有血肌酐升高、血清清蛋白下降,肝功能多正常。ANA、抗腎小球基底膜抗體(GMB)、MPO、p-ANCA陰性可與其他彌漫性結締組織病及小血管炎鑒別。
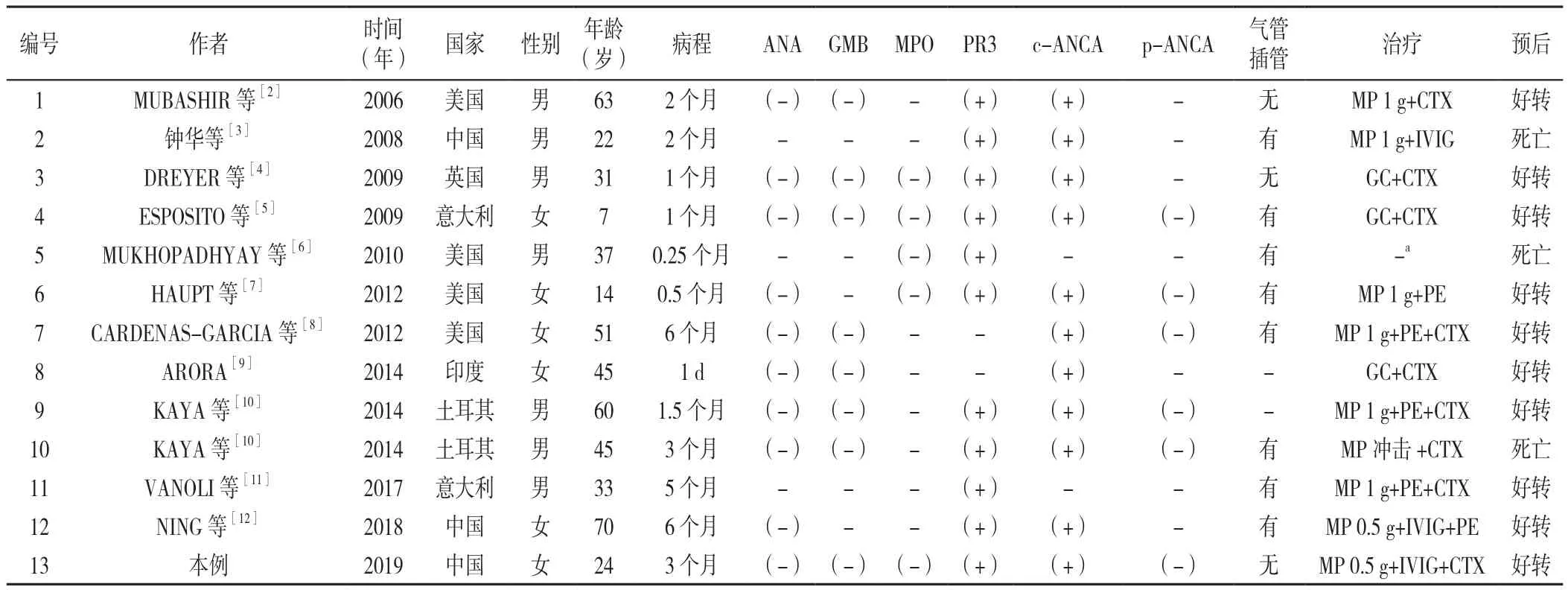
表1 GPA合并DAH患者基本情況Table 1 The general information of granulomatosis with polyangiitis patients with diffuse alveolar hemorrhage
3.5 胸部影像學檢查 胸部影像學檢查在GPA合并DAH診斷中具有重要作用。本研究文獻分析顯示,胸部X線片或胸部CT最常見的影像學表現為雙肺多發斑片狀、磨玻璃影或彌漫性浸潤影(84.6%),局部實變影(69.2%),部分可及支氣管空氣征、胸腔積液,少見白肺(7.7%),GPA特異的結節樣病灶僅見于38.5%的患者;關于肺部結節的檢出率,胸部CT明顯優于胸部X線片。治療后肺部影像可在短期內明顯好轉,NING等[12]報道1例患者治療第2天復查胸部X線片即明顯好轉,而本例患者治療4天后肺部CT復查病灶明顯吸收。有時DAH與肺部感染、急性肺水腫較難區分,需注意鑒別。
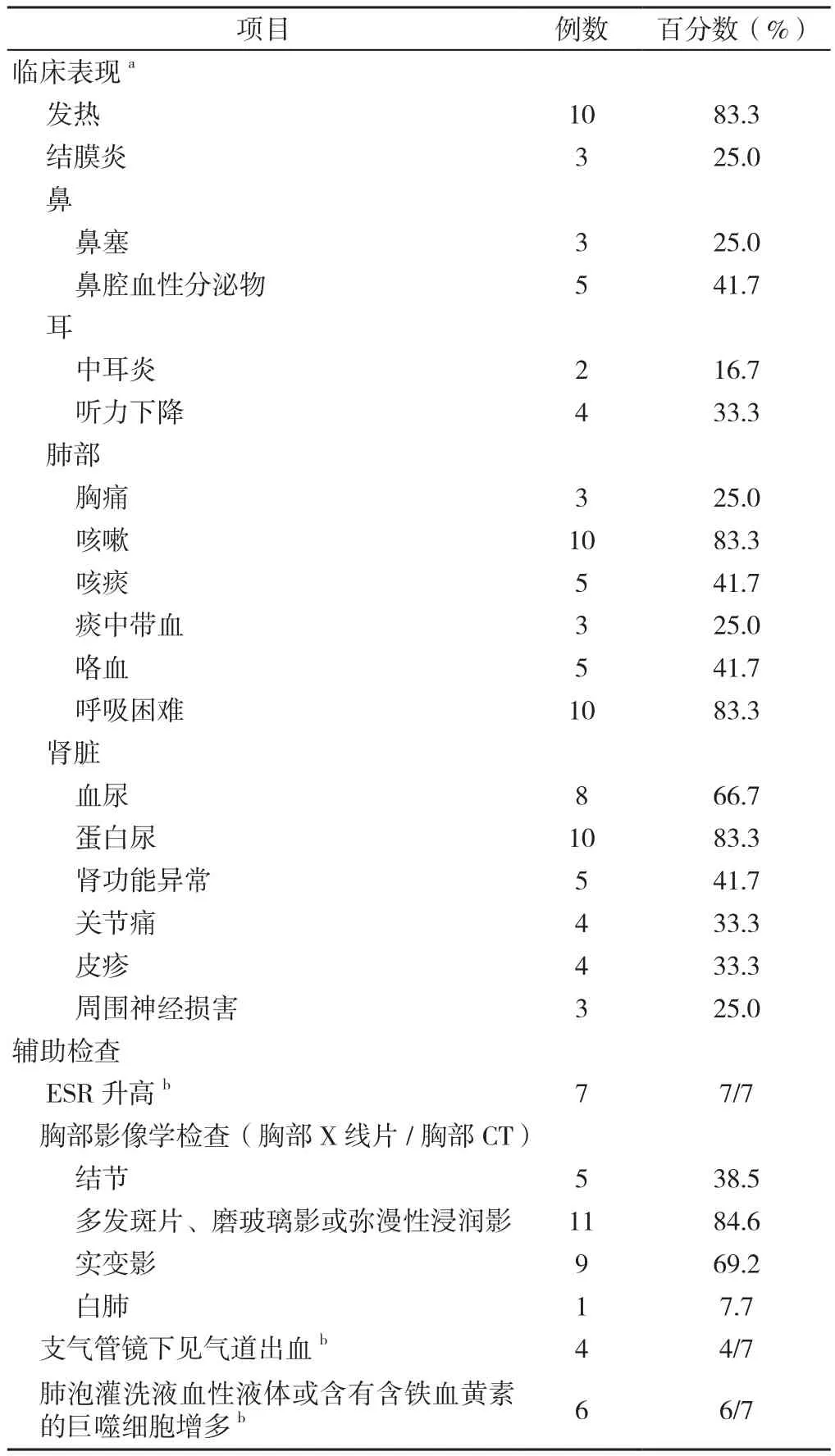
表2 GPA合并DAH患者臨床表現及輔助檢查結果Table 2 Clinical characteristics,laboratory and chest roentgenogram features of granulomatosis with polyangiitis patients with diffuse alveolar hemorrhage
3.6 支氣管鏡 支氣管鏡和肺泡灌洗液在確診DAH中占重要地位,本研究文獻分析顯示,部分GPA患者可在支氣管鏡下直接見到氣道出血(57.1%),而多節段肺泡灌洗液呈血性或肺泡巨噬細胞含有含鐵血黃素亦可確診DAH,支氣管鏡下還可同時進行細胞分析、肺活檢除外感染、腫瘤。
3.7 病理 因取材困難,目前的病理研究資料較為有限。本研究文獻分析顯示,肺毛細血管炎為DAH主要的病理表現,可見肺泡壁彌漫性增厚,含中等量單核細胞,偶見嗜酸粒細胞;肺泡結構被中性粒細胞破壞;肺泡內可見含有含鐵血黃素的巨噬細胞[2,6]。
3.8 治療和預后 本研究文獻分析顯示,GPA治療均選用激素,多選擇大劑量激素沖擊(0.5~1.0 g/d)治療約3 d后逐漸減量,同時進行CTX沖擊治療和/或血漿置換、IVIG等。也有少數患者選擇利妥昔單抗(RTX),VANOLI等[11]報道1例GAP合并DAH,經上述方案治療好轉2個月后再次復發,給予激素沖擊和RTX治療后再次緩解。GPA進展迅速,死亡率高達23%~60%[20],預后不良,診斷明確后需盡早進行激素沖擊治療,本例患者入院當天即給予大劑量激素沖擊治療,預后較好,臨床如不能及時做出準確判斷,大量肺泡出血后多數繼發感染,將極大增加治療難度。多數GPA合并DAH患者有嚴重呼吸困難,需氣管插管輔助通氣,部分患者在氣管插管時吸出大量鮮紅色血性液體,可幫助明確DAH診斷,而需要機械通氣可能預示了預后不良[21];除呼吸系統損害外,合并有其他重要臟器損害(常見腎功能衰竭)、繼發難以控制的感染也是GPA患者預后不良的影響因素。接受免疫抑制治療的患者感染風險高,而治療原發病免疫抑制劑為基礎用藥,在如何恰當選擇免疫抑制劑治療原發病和預防感染的發生之間掌握平衡一直是風濕科醫生面臨的一項重要挑戰。有數據表明,用甲氧芐啶-磺胺甲基異惡唑(TMP-SMX)治療可能有助于降低GPA患者緩解后的復發率[22],本研究中共有38.5%(5/13)的患者(包括本例患者)接受了TMP-SMX治療[2,4,8,12],5例患者在隨訪中均長期存活,因此 GPA 合并DAH患者使用TMP-SMX可能能改善預后。
總之,DAH是GPA的一種嚴重臨床綜合征,臨床表現為咳嗽、呼吸困難、咯血等,同時合并腎功能損害的患者發生DAH風險較高,短期內不明原因的Hb下降、肺部影像學檢查顯示彌漫性浸潤影和實變影提示DAH可能,支氣管鏡和肺泡灌洗液見血性液體及含有含鐵血黃素的巨噬細胞可明確診斷。其治療多選擇大劑量激素沖擊治療、CTX和血漿置換等。GPA一旦發生DAH,多病情危重,威脅生命,早期診斷和及時治療可改善預后。
作者貢獻:陸翠進行文章的構思與設計、文獻/資料收集和整理,并撰寫論文;蘇禹同、滕佳臨、葉俊娜進行文章的可行性分析;楊程德、葉俊娜進行論文的修訂;葉俊娜進行英文的修訂;陸翠、葉俊娜對文章整體負責,監督管理。
本文無利益沖突。

