莪術醇固體脂質納米粒的制備及其抗腫瘤活性
王風云,李偉宏
(河南應用技術職業學院,河南 鄭州450042)
莪術是姜科植物蓬莪術、溫郁金或廣西莪術的根莖[1],莪術油是其主要提取物,具有較強的抗腫瘤、抗病毒、抗炎等作用[2-3]。莪術醇是莪術特征性成分,對乳腺癌、卵巢癌、結腸癌、白血病、骨肉瘤等均具有抑制效果[4-6],但藥效不高[7-8]。另外,莪術醇注射液中含有高濃度的增溶劑吐溫-80,臨床應用時易引起溶血、過敏、疼痛等不良反應[7]。
固體脂質納米粒[9-14]是采用與人體生物相容性較好的脂質材料制成的一種新型給藥系統,注射后可顯著增強藥物療效。本實驗制備莪術醇固體脂質納米粒,并對其粒徑、Zeta 電位、形態、體外釋藥、光降解等情況進行考察,MTT 法評價其對人宮頸癌上皮細胞(Caski 細胞) 的抑制作用,以期為進一步相關研究奠定基礎。
1 材料
Agilent 1100 型高效液相色譜儀(美國Agilent公司);JY92-Ⅲ型超聲儀(浙江大天科學儀器有限公司);QUINTX224-1CM 型電子天平 (德國Sartorius公司);Zano-ZS90 型粒度分析儀(英國馬爾文儀器公司);H-800 型透射電子顯微鏡(日本Hitachi 公司);SZCL-H 型溫控磁力攪拌器(鄭州宇華儀器有限公司);Kylin-Bell 型漩渦混合器(海門其林貝爾儀器制造有限公司);FD10-QX 型真空凍干機(上海天賜科學儀器公司);JXDC-400型氮氣吹掃儀(拓赫機電科技上海有限公司);HNA-122DTABA I 型CO2恒溫培養箱(日本三洋公司);MR-96T 型酶標儀(南京貝登醫療股份有限公司)。
莪術醇對照品 (批號100185-201507,純度99.9%,中國食品藥品檢定研究院);莪術醇(批號Y-088-171005,純度98.8%,上海源葉生物科技有限公司);單硬脂酸甘油酯(批號T160522,德國巴斯夫有限公司);大豆卵磷脂(批號PC-98T,上海輔必成醫藥科技有限公司);泊洛沙姆188(批號WPW1602B,德國巴斯夫公司);胎牛血清(FBS)、RPMI-1640 培養基 (美國Gibco 公司);胰蛋白酶(美國Hyclone 公司);四甲基偶氮唑鹽(MTT,批號1524B37)、二甲基亞砜 (DMSO)(美國Amresco 公司)。
人宮頸癌上皮細胞(Caski 細胞,上海研域生物工程有限公司)。
2 方法與結果
2.1 莪術醇固體脂質納米粒制備 采用乳化超聲分散法(避光操作)。稱取20 mg 莪術醇、80 mg大豆磷脂、300 mg 單硬脂酸甘油酯,溶于10 mL溫度為(60±1) ℃的無水乙醇中,作為有機相;另取0.2 g 泊洛沙姆188,溶于30 mL 溫度為(60±1) ℃的蒸餾水中,作為水 相。在轉速1 000 r/min條件下,將有機相逐滴加入水相中,繼續攪拌3 h,得到初乳(體積約15 mL),將其置于超聲波細胞粉碎儀中超聲處理8 min (功率600 W,每超聲3 s 間隔2 s) 后立即放到-20 ℃冰箱中固化,蒸餾水定容至30 mL,即得。
2.2 莪術醇含有量測定
2.2.1 色譜條件 Hypersil ODS-C18色譜柱(250 mm×4.6 mm,5 μm);流動相乙腈-水(40 ∶60);體積流量1.0 mL/min;柱溫35 ℃;檢測波長215 nm;進樣量20 μL。
2.2.2 線性關系考察 稱取10.20 mg 莪術醇對照品于100 mL 量瓶中(避光操作),加入70 mL 甲醇超聲溶解,靜置30 min 后甲醇定容至刻度,得到102 μg/mL 貯備液,放到冰箱中保存,流動相逐步稀釋成 5.1、10.2、25.5、51.0、102.0 μg/mL,在“2.2.1” 項色譜條件下進樣測定。以溶液質量濃度為橫坐標(X),峰面積為縱坐標 (Y) 進行回歸,得方程為Y=1.414 6X-0.063 8 (r=0.999 5),在5.1~102.0 μg/mL范圍內線性關系良好。
2.2.3 供試品、空白溶液制備 精密稱取莪術醇固體脂質納米粒混懸液0.5 mL 于10 mL 量瓶中(避光操作),加入5 mL 乙腈超聲提取3 min,靜 置 30 min 后甲醇 定容至刻度,15 000 r/min離心15 min,取上清液,即得。同法制備空白溶液。
2.2.4 方法學考察分別取 102.0、51.0、5.1 μg/mL “2.2.2” 項下對照品溶液作為高、中、低質量濃度,在“2.2.1” 項色譜條件下進樣測定6 次,測得莪術醇峰面積RSD 分別為0.18%、0.13%、0.43%,表明儀 器精密 度良好。取“2.2.3” 項下供試品溶液,于0、2、4、8、12、24 h,在“2.2.1” 項色譜條件下進樣測定,測得莪術醇峰面積RSD 為0.84%,表明溶液在24 h 內穩定性良好。按“2.2.3” 項下方法平行制備6 份供試品溶液,在“2.2.1” 項色譜條件下進樣測定,測得莪術醇峰面積RSD 為1.46%,表明該方法重復性良好。取6.5 mL 102.0 μg/mL對照品溶液于10 mL 量瓶中,甲醇定容至刻度(66.3 μg/mL),取0.8、1.0、1.2 mL于0.5 mL 空白固體脂質納米粒混懸液中,各平行3 份,按“2.2.3” 項下方法制備供試品溶液,在“2.2.1” 項色譜條件下進樣測定,測得莪術醇平均加樣回收率分別為99.01%、100.23%、99.87%,RSD 分別為1.14%、0.69%、1.38%。以上實驗均避光操作。
2.3 包封率、載藥量測定 采用超濾離心法。量取2.0 mL 莪術醇固體脂質納米粒混懸液于超濾離心管 中 (截留分子量 8 000~12 000 Da),15 000 r/min 離心60 min,取濾液,在 “2.2.1”項色譜條件下進樣測定,計算莪術醇含有量(m游離);量取0.5 mL 納米粒混懸液于10 mL 量瓶中,加入5 mL 乙腈超聲3 min,靜置30 min 后甲醇定容,15 000 r/min 離心15 min,在“2.2.1”項色譜條件下進樣測定,計算莪術醇含有量(m總),再測定包封率、載藥量,公式分別為包封率= [(m總-m游離) /m總] × 100%,載藥量=[(m總-m游離) /m總質] ×100%,其中m總質表示莪術醇固體脂質納米粒總質量,平行3 次,取平均值。結果,平均包封率為83.27%,載藥量為3.83%。
2.4 粒徑分布、Zeta 電位測定 平行制備3 批莪術醇固體脂質納米粒混懸液,取0.2 mL 與4.0 mL蒸餾水混勻,取3.5 mL 進行測定,結果見圖1~2。由此可知,平均粒徑為(198.84±4.17) nm,PDI為0.151±0.013,Zeta 電位為(-21.8±2.5) mV。
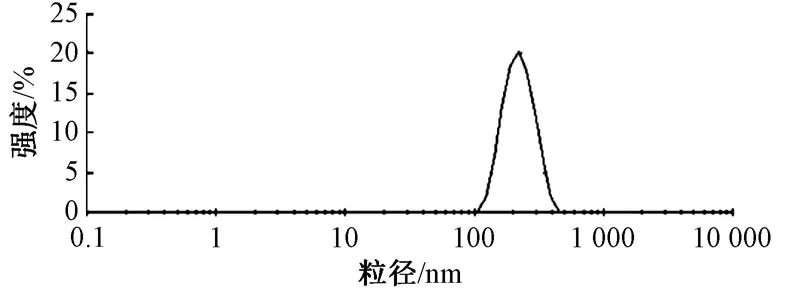
圖1 莪術醇固體脂質納米粒粒徑分布Fig.1 Particle size distribution of curcumolloaded solid lipid nanoparticles
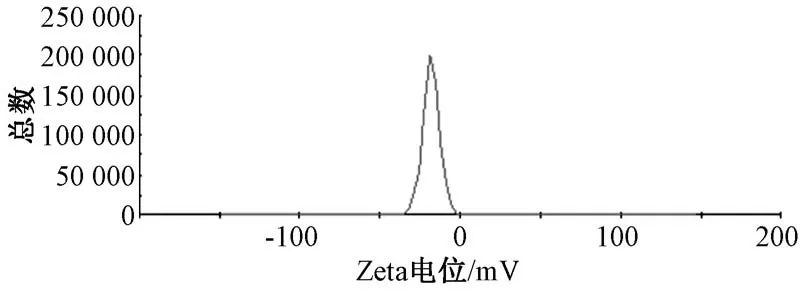
圖2 莪術醇固體脂質納米粒Zeta 電位Fig.2 Zeta potential of curcumol-loaded solid lipid nanoparticles
2.5 形態觀察 取100 μL 莪術醇固體脂質納米粒,加入900 μL 蒸餾水,滴加到有支持膜的銅網上,均勻鋪展后靜置15 min,濾紙吸干,放到5%磷鎢酸溶液中浸泡8 min 染色,自然晾干,在透射電鏡(TEM) 下觀察形態,選定區域后拍攝電鏡照片,結果見圖3。由此可知,所制備的莪術醇固體脂質納米粒呈類球形或球形,大小均勻,未見粘連現象。

圖3 莪術醇固體脂質納米粒TEM 圖Fig.3 TEM image for curcumol-loaded solid lipid nanoparticles
2.6 體外釋藥研究
2.6.1 線性關系考察 取“2.2.2” 項下對照品貯備液,精密量取2.0 mL 于10 mL 量瓶中,流動相定容至刻度(20.4 μg/mL),流動相逐步稀釋成10.2、5.1、0.51、0.051 μg/mL 的對照品溶液,在“2.2.1” 項色譜條件下進樣測定。以溶液質量濃度為橫坐標(X),峰面積為縱坐標(Y) 進行回歸,得方程為Y=1.607 5X-0.078 1 (r=0.999 7),在0.051~20.4 μg/mL 范圍內線性關系良好。
2.6.2 方法學考察 分別取“2.6.1” 項下20.4、5.1、0.051 μg/mL 對照品溶液作為高、中、低質量濃度,在“2.2.1” 項色譜條件下進樣測定6次,測得莪術醇峰面積RSD 分別為0.62%、1.15%、1.38%,表明儀器精密度良好。取5 mL莪術醇固體脂質納米粒混懸液(0.64 mg/mL),置于活化的透析袋中 (截留分子量 8 000~14 000 Da),兩端扎緊,溶出介質無250 mL 脫氣蒸餾水,設置溶出儀溫度為(37±1)℃,轉速為100 r/min,6 h 時取樣2 mL,濾過,取續濾液,作為供試品溶液,分別于0、2、8、12、24、36 h,在“2.2.1” 項色譜條件下進樣測定,測得莪術醇峰面積RSD 為1.63%,表明溶液在36 h 內穩定性良好。取0.8、1.0、1.2 mL 5.1 μg/mL 對照品溶液,加到1.0 mL 供試品溶液中,各平行3 份,濾過,在“2.2.1” 項色譜條件下進樣測定,測得平均加樣回收率分別為 99.12%、100.86%、99.05%,RSD 分別為1.71%、1.09%、1.53%。
2.6.3 體外溶出實驗 取5 mL 莪術醇固體脂質納米粒混懸液(0.64 mg/mL) 和3.2 mg 莪術醇原料藥(加入5 mL 乙醇),置于活化的透析袋中(截留分子量8 000~14 000 Da),兩端扎緊(避光操作),溶出介質為250 mL 脫氣蒸餾水,設置溶出儀溫度為(37±1)℃,轉速為100 r/min,于0、0.5、0.75、1、1.5、2、4、6、8、12、24、36 h各取樣2 mL,并立即補加2 mL 脫氣蒸餾水,在“2.2.1” 項色譜條件下進樣測定,計算累積釋放度,繪制釋藥曲線,結果見圖4,可知莪術醇在4 h內幾乎全部溶出,而其固體脂質納米粒在體外具有明顯緩釋特征,36 h 內累積溶出度為61.81%;體外釋藥擬合結果見表1,可知它更符合Weibull 模型(R2=0.960 5)。
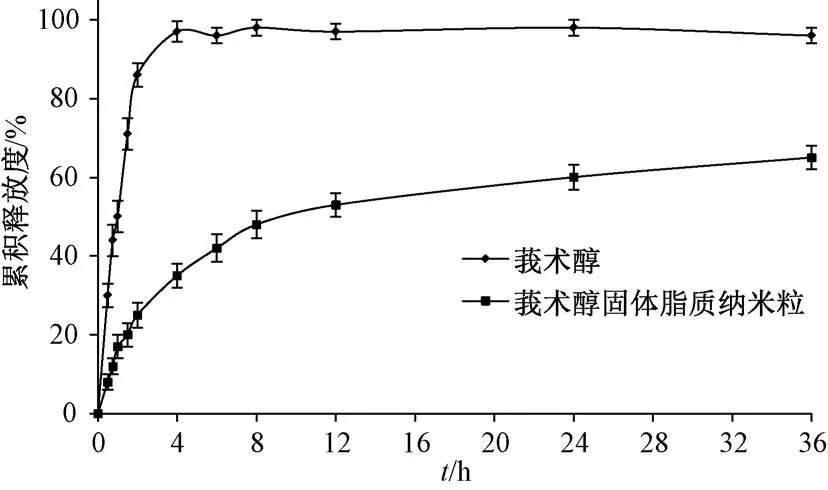
圖4 莪術醇、莪術醇固體脂質納米粒體外釋藥曲線Fig.4 In vitro drug release curves for curcumol and curcumol-loaded solid lipid nanoparticles

表1 體外釋藥擬合結果Tab.1 Results of in vitro drug release fitting
2.7 光穩定性評價 分別配制6 份50 mL 莪術醇溶液及其固體脂質納米粒混懸液,置于透明錐形瓶中,質量濃 度均為 0.2 mg/mL 于日光 燈(4 500 lx,25 ℃) 下照射,于0、2、4、8、12、24 h 各精密取樣1 mL,置于5 mL 量瓶中,甲醇定容,在“2.2.1” 項色譜條件下進樣測定,結果見表2,可知固體脂質納米粒可顯著提高莪術醇光穩定性。
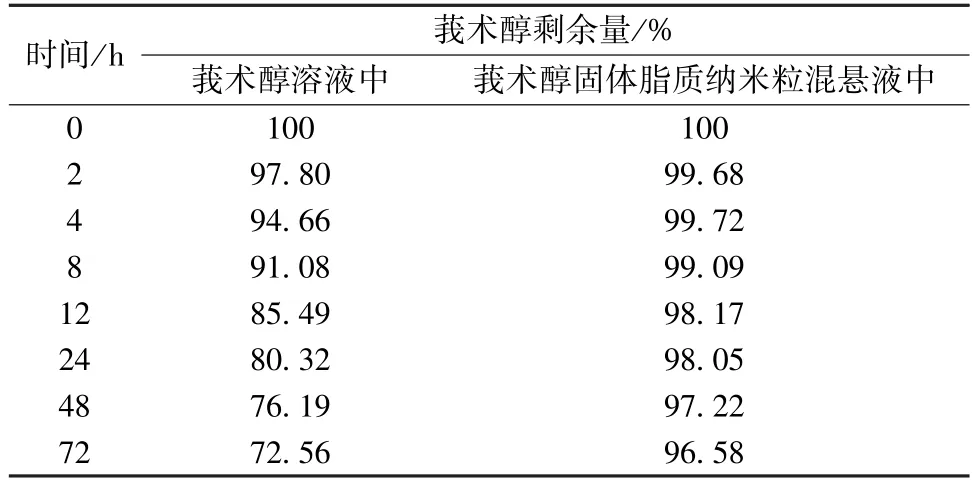
表2 莪術醇光穩定性試驗結果Tab.2 Results of light stability tests for curcumol
2.8 抗腫瘤活性研究
2.8.1 給藥液制備 10.0 mg 莪術醇用50 mL DMSO 溶解,得到200 μg/mL 母液,臨用前用含10% FBS 的RPMI-1640 培養液 稀釋成25、50、100、150 μg/mL;取適量莪術醇固體脂質納米粒混懸液(莪術醇含有量為0.64 mg/mL),臨用前用含10% FBS 的RPMI-1640 培養液稀釋成25、50、100、150 μg/mL,即得。
2.8.2 細胞培養 Caski 細胞于RPMI1640 培養基中培養(含10% 胎牛血清、100 μg/mL 鏈霉素、100 U/mL 青霉素),并置于溫度37 ℃、5% CO2、飽和濕度培養箱中。
2.8.3 實驗方法 取對數生長期的Caski 細胞,0.25%胰蛋白酶消化后輕輕吹打成單細胞懸液,用含10% FBS 的RPMI1640 培養液調整細胞濃度至5×104/mL,接種于96 孔板中,每孔100 μL,置于溫度37 ℃、5%CO2、飽和濕度培養箱中培養24 h,待細胞貼壁后棄去培養液。設置空白溶劑組(培養液)、溶劑對照組(培養液+細胞)、莪術醇組、莪術醇固體脂質納米粒組,每個質量濃度設置3 個復孔,培養24、48、72 h 后取出96 孔板,每孔加入20 μL 5 mg/mL MTT 溶液,于37 下℃繼續孵育4 h,甩板后棄去殘留液體,每孔加入150 μL DMSO,置于搖床上振蕩0.5 h 充分溶解藍紫色結晶,酶標儀在490 nm 波長處測定吸光度(A),計算細胞生長抑制率,公式為抑制率= [1 -(A給藥-A空白溶劑) / (A空白對照-A空白溶劑)] ×100%。
2.8.4 增殖抑制率測定 表3 顯示,不同質量濃度莪術醇溶液及莪術醇固體脂質納米粒混懸液作用一段時間后,Caski 細胞生長均受到抑制,隨著用藥量升高而更明顯,并且在用藥量相同的條件下作用時間延長時亦然,即呈明顯的量效和時效關系。另外,在相同用藥量的條件下莪術醇固體脂質納米粒的抑制效果均高于莪術醇,作用48、72 h 后更明顯(P<0.05,P<0.01)。
表3 Caski 細胞抑制率測定結果(, n=3)Tab.3 Results of inhibitory rate determination of Caski cells (, n=3)
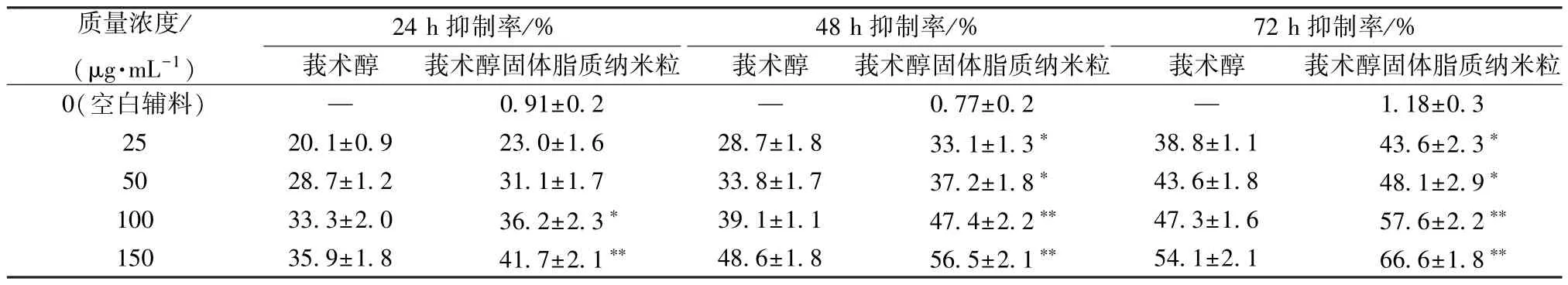
表3 Caski 細胞抑制率測定結果(, n=3)Tab.3 Results of inhibitory rate determination of Caski cells (, n=3)
注:與莪術醇比較,?P<0.05,??P<0.01。
3 討論
納米給藥系統已成為藥劑學研究熱點之一[15-16],應用于抗腫瘤藥物給藥時體現出巨大的優勢[14]。本實驗制備的莪術醇固體脂質納米粒采用混合脂質材料作為藥物載體,包封率達83.27%。可能是混合脂質載體可增加晶格混亂程度,使更多藥物被包裹進入納米粒[17-18]。
體外抗腫瘤實驗結果顯示,莪術醇及其固體脂質納米粒對Caski 細胞生長的抑制具有時效和量效關系,以后者抑制效果更強,可能與納米粒增強莪術醇光穩定性有關[19],一方面固體脂質納米粒對光的散射作用降低了莪術醇與光的接觸幾率;另一方面,固體脂質納米粒對莪術醇包裹后降低了外部環境對其影響,從而提高了穩定性。
體外釋藥實驗結果顯示,莪術醇固體脂質納米粒具有明顯的緩釋特征[20],與體外抗腫瘤實驗結果一致,可能是因為載藥納米粒高效擴散進入細胞后可持續、緩慢地釋放藥物,從而有效抑制Caski腫瘤細胞生長。
對莪術油新劑型的研究較多,但由于它是一種混合物,不僅影響了制劑含藥量,也容易導致制劑穩定性較差、產生毒性的問題[21],故將有明確療效的單體(如莪術醇等) 進行新制劑研究具有較大意義。今后,將把研究重點放在莪術醇固體脂質納米粒凍干粉末的制備、表面修飾、作用機制[22]、體內藥動學及抑瘤效果上,為相關制劑研發及臨床應用提供資料。

