阿帕替尼聯合TACE術治療中晚期肝癌有效性與安全性的Meta分析
唐貴菊 田塬 王繼婷 蘇松 李亞玲
中圖分類號 R735.7 文獻標志碼 A 文章編號 1001-0408(2020)12-1487-08
DOI 10.6039/j.issn.1001-0408.2020.12.15
摘 要 目的:系統評價阿帕替尼聯合經動脈化療栓塞術(TACE)治療中晚期肝癌的有效性和安全性,旨為臨床合理用藥提供循證參考。方法:計算機檢索Cochrane圖書館、Embase、PubMed、Web of Science、中國生物醫學文獻服務系統、中國知網、萬方數據、維普網等數據庫,收集阿帕替尼聯合TACE術(試驗組)對比TACE術(對照組)治療中晚期肝癌的隨機對照試驗(RCT),檢索時限均為建庫起至2019年9月。篩選文獻、提取資料并采用Cochrane系統評價員手冊5.1.0推薦的偏倚風險評估工具和改良Jadad量表評價納入文獻的質量后,采用 Stata 12.0軟件進行Meta分析。結果:共納入16項RCT,合計1 043例患者。Meta分析結果顯示,試驗組患者客觀有效率[OR=3.10,95%CI(2.38,4.03),P<0.001]、疾病控制率[OR=3.56,95%CI(2.62,4.83),P<0.001]、生存率[OR=2.40,95%CI(1.86,3.10),P<0.001]以及腹瀉[OR=2.27,95%CI(1.21,4.24),P=0.011]、血壓升高[OR=6.97,95%CI(1.21,40.15),P=0.030]、蛋白尿[OR=12.44,95%CI(2.51,61.71),P=0.002]、手足綜合征[OR=32.50,95%CI(12.03,87.77),P=0.001]發生率均顯著高于對照組,而治療后血清血管內皮細胞生長因子[SMD=-3.64,95%CI(-5.06,-2.22),P<0.001]、基質金屬蛋白酶9[SMD=-3.21,95%CI(-4.31,-2.10),P<0.001]、甲胎蛋白[SMD=-3.54,95%CI(-7.03,-0.06),P=0.046]水平以及骨髓抑制[OR=0.61,95%CI(0.39,0.97),P=0.035]、發熱[OR=0.63,95%CI(0.42,0.95),P=0.027]、惡心嘔吐[OR=0.70,95%CI(0.51,0.97),P=0.030]發生率均顯著低于對照組;兩組患者腹痛[OR=0.87,95%CI(0.54,1.39),P=0.547]、皮膚瘙癢[OR=1.63,95%CI(0.36,7.50),P=0.530]發生率比較,差異均無統計學意義。結論:阿帕替尼聯合TACE術能顯著提高中晚期肝癌患者的臨床療效、延長生存時間、減少腫瘤復發及轉移,并降低骨髓抑制等TACE術后相關不良反應的發生,但會增加腹瀉等阿帕替尼相關不良反應的發生。
關鍵詞 阿帕替尼;經動脈化療栓塞術;中晚期肝癌;有效性;安全性;Meta分析
Efficacy and Safety of Apatinib Combined with TACE in the Treatment of Moderate and Advanced Liver Cancer: A Meta-analysis
TANG Guiju1,TIAN Yuan1,WANG Jiting1,SU Song2,LI Yaling3(1. School of Pharmacy, Southwest Medical University, Sichuan Luzhou 646000, China; 2. Dept. of Hepatobiliary, the Affiliated Hospital of Southwest Medical University, Sichuan Luzhou 646000, China; 3. Dept. of Pharmacy, the Affiliated Hospital of Southwest Medical University, Sichuan Luzhou 646000, China)
ABSTRACT ? OBJECTIVE: To systematically evaluate the efficacy and safety of apatinib combined with transcatheter arterial chemoembolization (TACE) in the treatment of moderate and advanced liver cancer, and to provide evidence-based reference for rational drug use in the clinic. ?METHODS: Retrieved from Cochrane Library, Embase, PubMed, Web of Science, SinoMed, CNKI, Wanfang, VIP database, RCTs about apatinib combined with TACE (trial group) versus TACE (control group) in the treatment of moderate and advanced liver cancer were collected from inception to Sep. 2019. After screening the literature and extracting the data, the quality of included literatures was evaluated by using bias risk assessment tool recommended by the Cochrane system evaluator manual 5.1.0 and the modified Jadad scale. Meta-analysis was carried out by using Stata 12.0 software. RESULTS: Totally 16 RCTs were included, involving 1 043 patients. Results of Meta-analysis showed that objective response rate [OR=3.10, 95%CI(2.38,4.03), P<0.001], disease control rate [OR=3.56, 95%CI(2.62, 4.83), P<0.001] and survival rate [OR=2.40, 95%CI(1.86, 3.10), P<0.001], the incidence of diarrhea [OR=2.27,95%CI(1.21,4.24),P=0.011], hypertension [OR=6.97,95%CI(1.21,40.15),P=0.030], proteinuria [OR=12.44,95%CI(2.51,61.71),P=0.002] and hand foot syndrome [OR=32.50,95%CI(12.03,87.77),P=0.001] of trial group were significantly higher than those of control group. The serum level of VEGF [SMD=-3.64, ?95%CI(-5.06, -2.22), P<0.001], MMP-9 [SMD=-3.21, 95%CI(-4.31, -2.10), P<0.001], AFP [SMD=-3.54, ? ?95%CI(-7.03, -0.06), P=0.046] after treatment, the incidence of myelosuppression [OR=0.61,95%CI(0.39,0.97),P=0.035], fever [OR=0.63,95%CI(0.42,0.95),P=0.027], nausea and vomiting [OR=0.70,95%CI(0.51,0.97),P=0.030] in trial group were significantly lower than those of control group. There was no statistical significance in the incidence of abdominal pain [OR=0.87, 95%CI(0.54, 1.39), P=0.547] and skin itching [OR=1.63, 95%CI(0.36, 7.50), P=0.530] between 2 groups. CONCLUSIONS: Apatinib combined with TACE can significantly improve clinical efficacy, prolong survival time, reduce tumor recurrence and metastasis. It can reduce the occurrence of related ADR as diarrhea after TACE, but increase the occurrence of apatinib-related ADR as myelosuppression.
KEYWORDS Apatinib; Transcatheter arterial chemoembolization; Moderate and advanced hepatocellular carcinoma; Efficacy; Safety; Meta-analysis
我國癌癥發病率、患者病死率隨人口老齡化加劇而逐年上升,現已位列全球首位[1]。目前,肝癌位居我國癌癥發病率第5位(26.92%)和病死率第2位(23.72%)[2],嚴重威脅患者的健康,給患者及其家屬帶來了巨大痛苦和負擔。手術切除、介入治療、靶向治療等是肝癌治療的主要方法[3]。早期肝癌患者經手術切除后可獲得治愈;但多數患者確診時已進展為中晚期,以介入治療為主要手段[4]。經動脈化療栓塞術(Transcatheter arterial chemoembolization,TACE)是最為常用的介入治療手段,但單純的TACE術存在腫瘤細胞滅活不徹底的缺點[5],易導致患者術后復發,且上述復發與新生血管生成直接相關[6]。
阿帕替尼是我國首個完全自主研發的新型靶向抗血管生成藥物[7]。研究發現,中晚期肝癌患者在TACE術后使用阿帕替尼,可抑制新生血管生成、減緩癌癥進展、延長患者生存期、減少復發及轉移[8-10]。但這些研究樣本量較小,大多局限于單中心、回顧性研究,且阿帕替尼聯合TACE術治療中晚期肝癌尚缺乏充分的證據。為此,本研究采用Meta分析的方法系統評價了阿帕替尼聯合TACE術治療中晚期肝癌的有效性和安全性,旨為臨床合理用藥提供循證參考。
1 資料與方法
1.1 納入與排除標準
1.1.1 研究類型 國內外公開發表的隨機對照試驗(RCT);語種限定為中文和英文。
1.1.2 研究對象 經影像檢查和病理活檢確診的中晚期肝癌患者;患者年齡、性別不限。
1.1.3 干預措施 對照組患者采用TACE術,術后給予止吐、護胃、保肝等常規治療。試驗組患者在對照組治療的基礎上給予阿帕替尼,用藥1~2周后根據其耐受情況調整劑量:若耐受良好或出現輕度不良反應,可適當增加或維持起始劑量;若出現明顯不良反應,則應減少劑量或短期(不超過1個月)停藥觀察,待不良反應減輕或消失后再逐步恢復并調整劑量。
1.1.4 結局指標 ①客觀有效率(ORR);②疾病控制率(DCR);③生存率;④治療后血清血管內皮細胞生長因子(VEGF)水平;⑤治療后血清基質金屬蛋白酶9(MMP-9)水平;⑥治療后血清甲胎蛋白(AFP)水平;⑦不良反應發生情況。參照實體瘤療效評價標準1.1版將療效分為完全緩解(CR)、部分緩解(PR)、穩定(SD)和進展(PD);ORR=(CR例數+PR例數)/總例數×100%;DCR=(CR例數+PR例數+SD例數)/總例數×100%[11]。
1.1.5 排除標準 ①主題不符的文獻、二次文獻(如綜述、Meta分析);②回顧性研究、基礎研究(包括動物實驗、細胞試驗)、案例報道、經驗總結、會議論文;③無上述結局指標或無法提取可用數據的文獻;④重復發表的文獻。
1.2 文獻檢索策略
計算機檢索Cochrane 圖書館、Embase、PubMed、Web of Science、中國生物醫學文獻服務系統(SinoMed)、中國知網、萬方數據、維普網等數據庫。中文檢索詞為“中晚期肝癌”“阿帕替尼”“TACE”“經動脈化療栓塞術”;英文檢索詞為“Moderate and advanced hepatocellular carcinoma”“Apatinib”“TACE”“Transcatheter arterial chemoembolization”。檢索時限均為各數據庫建庫起至2019年9月。采用主題詞與自由詞相結合的檢索方式。
1.3 文獻篩選與資料提取
由2位研究者獨立檢索文獻,根據納入與排除標準篩選文獻并交叉核對;如遇分歧通過討論解決或請第3位研究者協商裁定。提取資料包括第一作者、發表年份、患者例數、性別、年齡、干預措施、Child-Pugh肝功能分級、功能狀態評分(KPS)、隨訪時間、結局指標等。
1.4 納入文獻質量評價
采用Cochrane系統評價員手冊5.1.0推薦的偏倚風險評估工具對納入研究的質量進行評價,具體包括隨機方法是否正確;是否分配隱藏;是否采用盲法;結果數據是否完整;是否選擇性報告研究結果;是否存在其他偏倚來源;各項均分為“低偏倚風險”“高偏倚風險”“不清楚”[12]。同時,采用改良Jadad量表對納入研究的質量進行評分,具體包括:隨機序列的產生(恰當2分,不清楚1分,不恰當0分)、分配隱藏(恰當2分,不清楚1分,不恰當0分)、盲法(實施2分,不清楚1分,未實施0分)、撤出與失訪(描述1分,未描述0分);0~3分為低質量研究,4~7分為高質量研究[13]。
1.5 統計學方法
采用Stata 12.0軟件進行Meta分析。二分類變量采用比值比(OR)及其95%置信區間(CI)表示;連續型變量采用標準化均數差(SMD)及其95%CI表示。若各研究間無統計學異質性(P>0.1,I 2<50%),采用固定效應模型進行分析;反之,則采用隨機效應模型進行分析。對結果的穩定性進行敏感性分析。采用Beggs檢驗和Eggers檢驗進行發表偏倚分析。P<0.05為差異有統計學意義。
2 結果
2.1 文獻檢索結果與納入研究基本信息
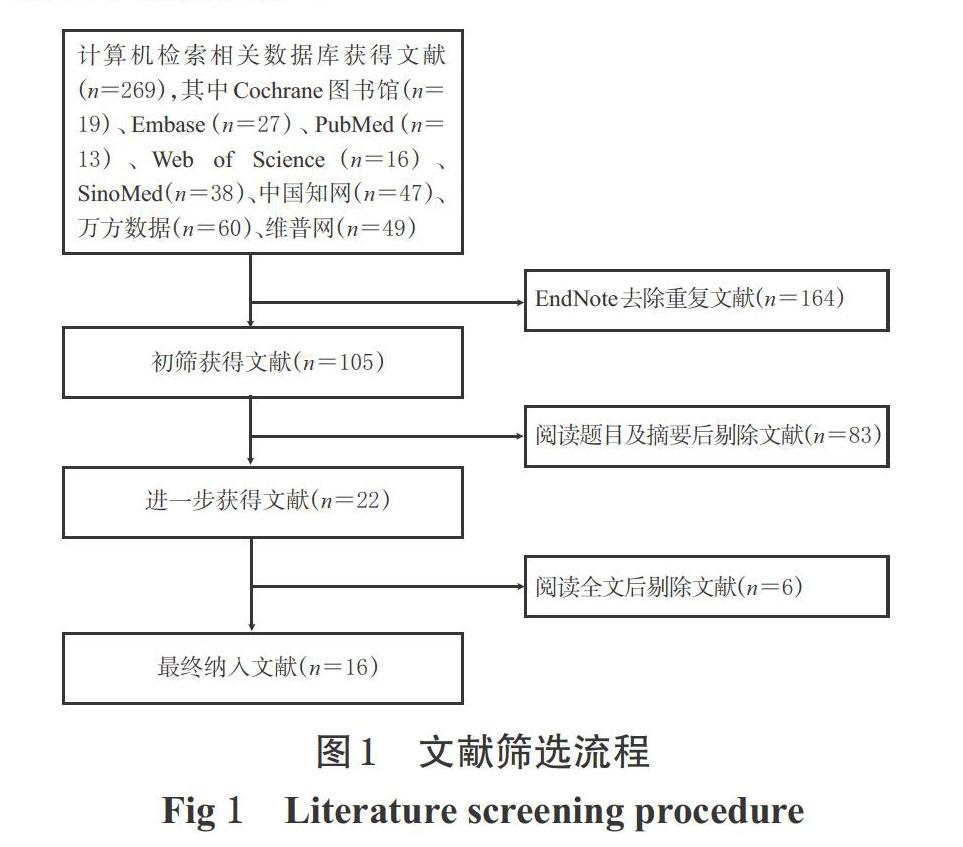
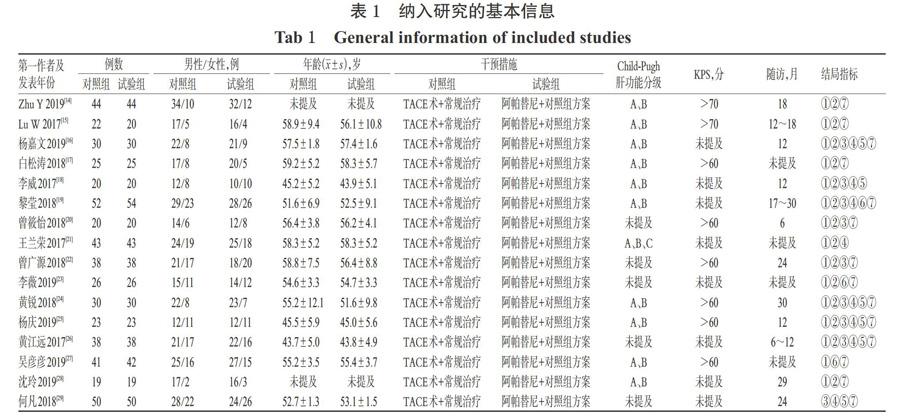
初檢得到相關文獻269篇,采用EndNote X8軟件去除重復發表的文獻,經仔細閱讀題目、摘要和全文后,最終納入文獻16篇[14-29],共計1 043例患者,其中對照組521例、試驗組522例。文獻篩選流程見圖1;納入研究的基本信息見表1。
2.2 納入研究質量評價結果
所有研究[14-29]均為RCT;8項研究[15-16,18,21,23-26]描述了隨機分組方法,均為隨機數字表法;1項研究[20]實施了雙盲法;2項研究[15,28]描述了撤出與失訪情況;所有研究[14-29]均不清楚是否采用分配隱藏;均未發現選擇性報告結果及是否存在其他偏倚來源。10篇[15-16,18,20-21,23-26,28]為高質量研究,6篇[14,17,19,22,27,29] 為低質量研究,詳見表2。
2.3 Meta分析結果
2.3.1 ORR 15項研究[14-28]報道了ORR,各研究間無統計學異質性(P=0.995,I 2=0),采用固定效應模型進行Meta分析,詳見圖2。Meta分析結果顯示,試驗組患者的ORR顯著高于對照組[OR=3.10,95%CI(2.38,4.03),P<0.001]。
2.3.2 DCR 14項研究[14-26,28]報道了DCR,各研究間無統計學異質性(P=1.000,I 2=0),采用固定效應模型進行Meta分析,詳見圖3。Meta分析結果顯示,試驗組患者的DCR顯著高于對照組[OR=3.56,95%CI(2.62,4.83),P<0.001]。
2.3.3 生存率 9項研究[16,18-20,22,24-26,29]報道了生存率,各研究間無統計學異質性(P=0.999,I 2=0),采用固定效應模型進行Meta分析。Meta分析結果顯示,試驗組患者的生存率顯著高于對照組[OR=2.40,95%CI(1.86,3.10),P<0.001 ]。其中,有7項研究[16,18,20,24-26,29]報道了 6個月生存率,各研究間無統計學異質性(P=0.941,I 2=0),采用固定效應模型進行Meta分析。Meta分析結果顯示,試驗組患者的6個月生存率顯著高于對照組[OR=2.48,95%CI(1.64,3.77),P<0.001]。有7項研究[16,18,22,24-26,29]報道了12個月生存率,各研究間無統計學異質性(P=0.953,I 2=0),采用固定效應模型進行Meta分析。Meta分析結果顯示,試驗組患者的12個月生存率顯著高于對照組[OR=2.16,95%CI(1.43,3.26),P<0.001]。4項研究[19,22,24,29]報道了24個月及以上生存率,各研究間無統計學異質性(P=0.960,I 2=0),采用固定效應模型進行Meta分析。Meta分析結果顯示,試驗組患者的12個月生存率顯著高于對照組[OR=2.69,95%CI(1.59,4.56),P<0.001],詳見圖4。
2.3.4 治療后血清VEGF水平 8項研究[16,18-19,21,24-26,29]報道了治療后血清VEGF水平,各研究間有統計學異質性(P<0.001,I 2=97.1%),采用隨機效應模型進行Meta分析,詳見圖5。Meta分析結果顯示,試驗組患者治療后VEGF水平顯著低于對照組[SMD=-3.64,95%CI(-5.06,-2.22),P<0.001]。
2.3.5 治療后血清MMP-9水平 6項研究[16,18,24-26,29]報道了治療后血清MMP-9水平,各研究間有統計學異質性(P<0.001,I 2=92.8%),采用隨機效應模型進行Meta分析,詳見圖6。Meta分析結果顯示,試驗組患者治療后血清MMP-9水平顯著低于對照組[SMD=-3.21,95%CI(-4.31,-2.10),P<0.001]。
2.3.6 治療后血清AFP水平 3項研究[19,23,27]報道了治療后血清AFP水平,各研究間有統計學異質性(P<0.001,I 2=98.3%),采用隨機效應模型進行Meta分析,詳見圖7。Meta分析結果顯示,試驗組患者治療后血清AFP水平顯著低于對照組[SMD=-3.54,95%CI(-7.03, -0.06),P=0.046]。
2.3.7 不良反應 14項研究[14-17,19-20,22-29]報道了不良反應發生情況。試驗組患者骨髓抑制、發熱、惡心嘔吐發生率均顯著低于對照組,而腹瀉、血壓升高、蛋白尿、手足綜合征發生率均顯著高于對照組(P<0.05);兩組患者腹痛、皮膚瘙癢發生率比較,差異均無統計學意義(P>0.05),詳見表3。
2.4 敏感性分析
以治療后血清MMP-9水平為有效性指標進行敏感性分析,在剔除楊慶等[25]的研究后,各研究間無統計學異質性(P=0.182,I 2=35.9%),采用固定效應模型進行Meta分析。Meta分析結果顯示,試驗組患者治療后血清MMP-9水平顯著低于對照組[SMD=-2.20,95%CI(-2.47,-1.92),P<0.001],與“2.3.5”項一致,提示結果穩定、可信。以蛋白尿發生率為安全性指標進行敏感性分析,在剔除楊嘉文[16]的研究后,各研究間無統計學異質性(P=0.844,I 2=0),采用固定效應模型進行Meta分析。Meta分析結果顯示,試驗組患者蛋白尿發生率顯著高于對照組[OR=27.30,95%CI(9.06,82.26),P<0.001],與“2.3.7”項一致,提示結果穩定、可信。
2.5 發表偏倚分析
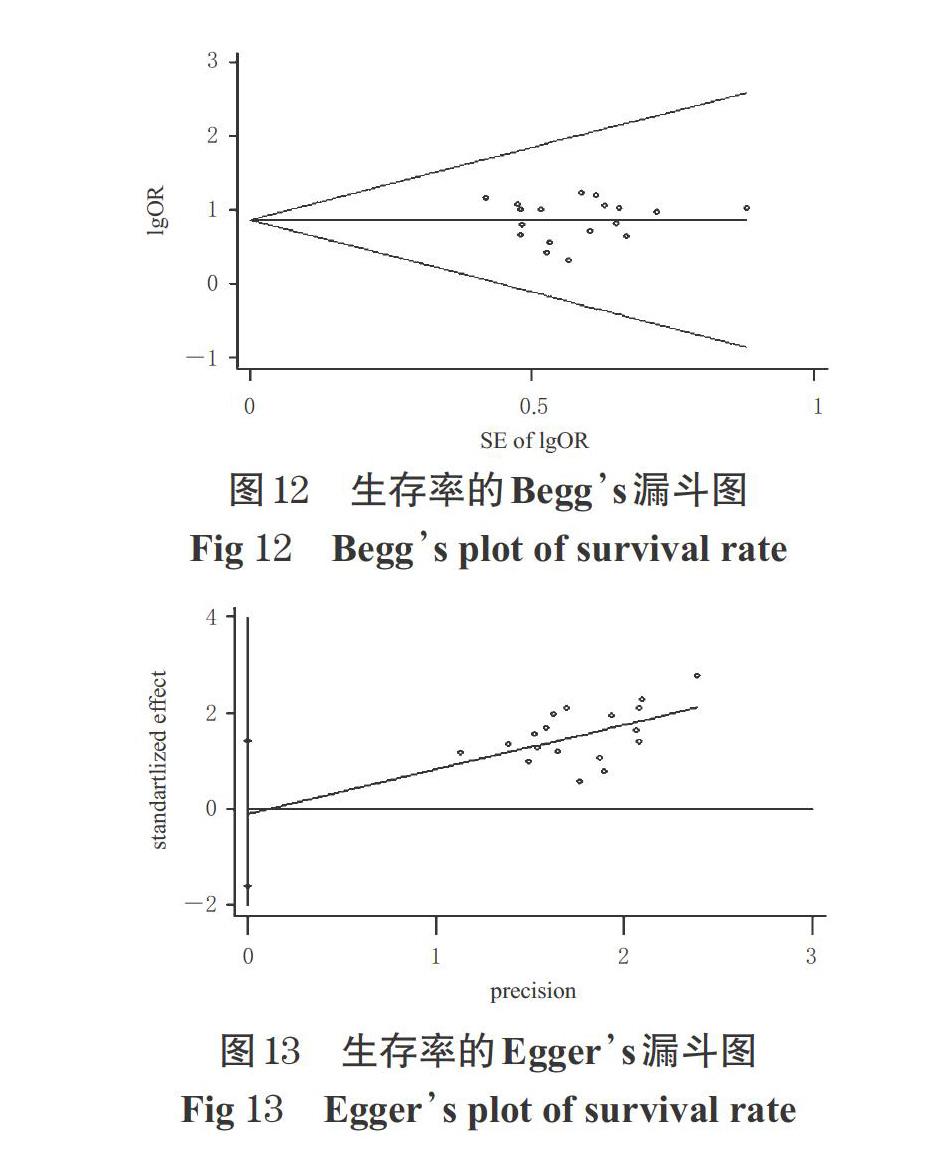
以ORR、DCR、生存率為指標,分別采用Beggs檢驗和Eggers檢驗進行發表偏倚分析,以每項獨立研究OR值對數的標準誤為橫坐標、OR值的對數為縱坐標繪制漏斗圖,結果見圖8~圖13。由圖8~圖13可見,ORR的 Beggs檢驗的P值為0.124,大于0.05,提示存在發表偏倚的可能性較小;Eggers檢驗的P值為0.017,小于0.05,提示存在一定發表偏倚。 DCR的Beggs檢驗的P值為0.112,Eggers檢驗的P值為0.21,均超過0.05,提示存在發表偏倚的可能性較小。生存率的Beggs檢驗的P值為0.495,Eggers檢驗的P值為0.899,均超過0.05,提示存在發表偏倚的可能性較小。
3 討論
肝癌是發病率高、預后較差的惡性腫瘤,由于早期癥狀不明顯、病灶隱匿且進展迅速,多數患者確診時已處于中晚期甚至已轉移[4]。根據國內外肝癌的診療規范與實踐指南,TACE術為中晚期肝癌患者的一線推薦治療方案[30-32]。TACE術可直接增加腫瘤組織局部的化療藥物濃度,增強藥物的殺傷作用;可阻斷腫瘤細胞的血液供應,導致其缺血、缺氧,促使腫瘤細胞壞死、凋亡[8-10]。但 TACE術后,殘存的肝癌細胞可因缺血、缺氧而導致VEGF(與腫瘤血管生成緊密相關)表達增加,引起轉移和復發[33-34]。有研究認為,MMP-9在腫瘤血管生成、腫瘤生長及轉移中具有重要作用,可與VEGF協同刺激新生血管生成,使殘存的肝癌細胞通過新生血管獲得營養物質而致腫瘤復發及轉移[18,35-36] 。AFP是肝癌特異性標志物,在肝癌診斷及早期篩查中具有重要意義,AFP的高表達提示肝癌患者預后不良[37]。由此推測,TACE術后聯合使用抗血管生成的靶向藥物,可能是提高肝癌患者療效的有效途徑。
阿帕替尼為一種新型的小分子酪氨酸激酶抑制劑,其與血管內皮細胞生長因子受體2(VEGFR-2)的親和力是索拉非尼(該藥是被多個國家批準用于晚期肝癌的一線用藥)的10倍[7-8],可通過競爭性抑制VEGF與VEGFR-2的結合來阻斷腫瘤細胞新生血管生成,并抑制腫瘤細胞增殖、遷移[38-40]。該藥自2014年獲批上市用于治療晚期胃癌及胃-食管結合部腺癌以來,已有大量臨床研究結果顯示,阿帕替尼在多種實體瘤(包括肝癌)中顯示出良好的抗腫瘤活性,且副作用可控性較高[41-44]。此外,阿帕替尼還可通過改善腫瘤細胞的多藥耐藥來提高傳統化療藥物(尤其是鉑類)的療效[45],為中晚期肝癌的治療提供了新的選擇。
本研究結果顯示,試驗組患者ORR、DCR、生存率均顯著高于對照組,提示阿帕替尼聯合TACE術可顯著提高患者的臨床療效、延長其生存時間。試驗組患者治療后血清VEGF、MMP-9、AFP水平均顯著低于對照組,提示阿帕替尼聯合TACE術可降低患者體內VEGF、MMP-9、AFP的表達,阻止腫瘤細胞新生血管的生成,減少腫瘤復發及轉移,改善患者預后。安全性方面,試驗組患者骨髓抑制、發熱、惡心嘔吐發生率均顯著低于對照組,但腹瀉、血壓升高、蛋白尿、手足綜合癥發生率均顯著高于對照組,兩組患者腹痛、皮膚瘙癢發生率比較差異均無統計學意義,提示阿帕替尼聯合TACE術可減少骨髓抑制、發熱、惡心嘔吐等TACE術后相關不良反應的發生,但會增加腹瀉、血壓升高、蛋白尿、手足綜合征等阿帕替尼相關不良反應的發生[37]。本研究納入文獻中,試驗組有3例患者并發嚴重的手足綜合征,其中有2例患者因此終止治療[28];其余患者耐受良好或癥狀輕微,予以減少劑量、暫停給藥及對癥處理后均好轉,表明患者對阿帕替尼引起的不良反應基本耐受。
綜上所述,阿帕替尼聯合TACE術能顯著提高中晚期肝癌患者的臨床療效、延長生存時間、減少腫瘤復發及轉移,并減少TACE術后相關不良反應的發生,但可增加阿帕替尼相關不良反應的發生。本研究的局限性為:(1)納入研究的樣本量較小,可能存在一定的發表偏倚;(2)納入文獻質量不高;(3)多數研究未描述隨機分組方法及盲法,且均未報告分配隱藏方法,可能存在選擇性偏倚和實施性偏倚;(4)受試者均為國內肝癌患者,其結果可能僅適用于我國患者。故此結論尚需更多高質量、多中心、大樣本的RCT進一步證實。
參考文獻
[ 1 ] BRAY F,FERLAY J,SOERJOMATARAM I,et al. Global
cancer statistics 2018: GLOBOCAN estimates of incidence
and mortality worldwide for 36 cancers in 185 countries[J].
CA Cancer J Clin,2018,68(6):394-424.
[ 2 ] European Association for the Study of the Liver,Electronic Address:Easloffice@Easloffice.eu,European Association for the Study of the Liver. EASL clinical practice guidelines:management of hepatocellular carcinoma[J]. J Hepatol,2018,69(1):182-236.
[ 3 ] 崔海忠,戈偉,曹德東,等.甲磺酸阿帕替尼聯合肝動脈栓塞化療治療中晚期原發性肝癌的效果[J].中國醫藥導報,2019,22(14):88-91.
[ 4 ] OZAKYOL A. Global epidemiology of hepatocellular carcinoma(HCC epidemiology)[J]. J Gastrointest Cancer,2017,48(3):238-240.
[ 5 ] 楊澤冉,蘇天昊,尉建安,等.肝動脈化療栓塞術聯合阿帕替尼治療中晚期原發性肝癌療效評價[J].中國腫瘤臨床,2017,44(17):880-885.
[ 6 ] YANG Z,CHEN G,CUI Y,et al. The safety and efficacy of TACE combined with apatinib on patients with advanced hepatocellular carcinoma:a retrospective study[J]. Cancer Boil Ther,2019,20(3):321-327.
[ 7 ] 武姍,花瞻,李建晨,等.阿帕替尼聯合其他方法治療腫瘤的研究進展[J].腫瘤防治研究,2019,46(3):275-280.
[ 8 ] CHEN S,YU W,ZHANG K,et al. Comparison of the efficacy and safety of transarterial chemoembolization with and without apatinib for the treatment of BCLC stage C hepatocellular carcinoma[J]. BMC Cancer,2018. DOI:10.1186/s12885-018-5081-3.
[ 9 ] 陸陽,姜永能,萬程,等.阿帕替尼聯合TACE治療中晚期肝細胞癌的療效研究[J].介入放射學雜志,2019,28(2):162-165.
[10] LIU C,XING W,SI T,et al. Efficacy and safety of apatinib combined with transarterial chemoembolization for hepatocellular carcinoma with portal venous tumor thrombus:a retrospective study[J]. Oncotarget,2017,8(59):100734-100745.
[11] 孫燕.臨床腫瘤內科手冊[M].5版.北京:人民衛生出版社,2007:147-155.
[12] HIGGINS JPT,GREEN S. Cochrane handbook for systematic reviews of interventions version 5.1.0[EB/OL].(2011-03-12)[2018-08-18]. http://www.cochranehand- book.org.
[13] JADAD AR,MOORE RA,CARROLL D,et al. Assessing the quality of reports of randomized clinical trials:is blinding necessary? [J]. Control Clin Trials,1996,17(1):1-12.
[14] ZHU Y,FENG B,MEI L,et al. Clinical efficacy of TACE combined with apatinib in the treatment of advanced hepatocellular carcinoma[J]. J BUON,2019,24(2):608-614.
[15] LU W,JIN XL,YANG C,et al. Comparison of efficacy between TACE combined with apatinib and TACE alone in the treatment of intermediate and advanced hepatocellular carcinoma:a single-center randomized controlled trial[J]. Cancer Biol Ther,2017,18(6):433-438.
[16] 楊嘉文. TACE分別聯合微波消融、125I放射性粒子植入及阿帕替尼靶向治療大肝癌的療效比較[J].中國醫師雜志,2019,13(8):1190-1194.
[17] 白松濤,張月蒙. TACE聯合阿帕替尼對晚期肝癌的臨床療效[J].中國現代醫生,2018,12(2):90-92、95.
[18] 李威,滿文玲,郭歡慶,等. TACE聯合甲磺酸阿帕替尼治療中晚期肝癌的臨床研究[J].腫瘤藥學,2017,12(1):74-78.
[19] 黎瑩,楊冬陽,賴曉嶸,等.阿帕替尼聯合TACE對肝癌患者AFP、VEGF和CEA的影響[J].肝臟,2018,23(5):426-430.
[20] 曾筱怡.阿帕替尼聯合TACE治療原發性肝癌的臨床研究[J].基層醫學論壇,2018,22(11):1442-1444.
[21] 王蘭榮,王钖,曹旸,等.阿帕替尼聯合動脈栓塞介入治療肝癌的效果及對血管內皮生長因子和凋亡相關因子的影響[J].國際醫藥衛生導報,2017,23(7):1015-1017.
[22] 曾廣源,吳龔麗莉,鄭文,等.阿帕替尼片聯合肝動脈化療栓塞術治療中晚期原發性肝癌的臨床研究[J].中國臨床藥理學雜志,2018,34(23):2693-2696.
[23] 李薇.不同方法治療晚期肝癌的效果[J].中國處方藥,2019,17(5):131-132.
[24] 黃銳,姚立正,李文會,等.肝動脈化療栓塞術聯合甲磺酸阿帕替尼片治療中晚期肝癌的療效及安全性評價[J].腫瘤,2018,38(10):965-972.
[25] 楊慶,潘松松,施昌盛,等.甲磺酸阿帕替尼聯合TACE治療中晚期肝癌的效果及對患者血清VEGF和MMP-9的影響[J/CD].中華介入放射學電子雜志,2019,7(2):111- 116.
[26] 黃江遠,黃維,朱橋華.經導管肝動脈化療栓塞聯合甲磺酸阿帕替尼在中晚期肝細胞癌中的應用[J/CD].中國肝臟病雜志:電子版,2017,10(4):78-81.
[27] 吳彥彥.經肝動脈化療栓塞術聯合阿帕替尼對中晚期原發性肝癌患者血清甲胎蛋白異質體的影響[J].中醫藥臨床雜志,2019,31(4):736-738.
[28] 沈玲,楊秀麗,亞國偉,等.小劑量阿帕替尼聯合TACE治療晚期肝癌臨床觀察[J].廣州醫藥,2019,48(2):72-75.
[29] 何凡,陳旭東,林振文,等.中晚期肝癌患者應用經導管肝動脈化療栓塞(TACE)聯合阿帕替尼治療的效果分析[J].腫瘤藥學,2018,8(3):382-386.
[30] 鄭可心,韓冰,祁興順,等.《2018年美國肝病學會實踐指導:肝細胞癌的診斷、分期和管理》摘譯[J].臨床肝膽病雜志,2018,34(6):1181-1182.
[31] 葛寧靈,薛同春,葉勝龍. 《2018年歐洲肝病學會臨床實踐指南:肝細胞癌的管理》解讀[J].臨床肝膽病雜志,2018,34(6):1187-1190.
[32] 吳孟超,湯釗獻,劉允怡,等.原發性肝癌診療規范:2019年版[J].中國實用外科雜志,2020,40(2):121-138.
[33] 何健,陳曉明. 2018年肝癌TACE治療研究進展[J].循證醫學,2019,19(1):21-22、38.
[34] 崔建東,羅敏,李濤,等.阿帕替尼聯合肝動脈化療栓塞治療中晚期肝癌的療效及安全性分析[J].現代腫瘤醫學,2019,27(14):2553-2556.
[35] FAN W,YUAN G,FAN H,et al. Apatinib combined with transarterial chemoembolization in patients with hepatocellular carcinoma and portal vein tumor thrombus:a multicenter retrospective study[J]. Clin Ther,2019,41(8):1463-1476.
[36] LIU J,XU J,ZHANG W,et al. Safety and efficacy of drug-eluting bead transarterial chemoembolization com- bined with apatinib in patients with advanced hepatocellular carcinoma[J]. Acad Radiol,2019. DOI:10.1016/j.acra.2019.07.003.
[37] 武健,尹芳,羅貫虹,等.經肝動脈化療栓塞術聯合阿帕替尼治療中晚期原發性肝癌的效果及安全性分析[J].臨床肝膽病雜志,2018,34(4):775-778.
[38] SCOTT AJ,MESSERSMITH WA,JIMENO A. Apatinib:a promising oral antiangiogenic agent in the treatment of multiple solid tumors[J]. Drugs Today:Barc,2015,51(4):223-229.
[39] ZHANG H. Apatinib for molecular targeted therapy in tumor[J]. Drug Des Devel Ther,2015. DOI:10.2147/DDDT.S97235.
[40] GENG R,LI J. Apatinib for the treatment of gastric cancer[J]. Expert Opin Pharmacother,2015,16(1):117-122.
[41] LI J,QIN S,XU J,et al. Randomized,double-blind,placebo-controlled phase Ⅲ trial of apatinib in patients with chemotherapy:refractory advanced or metastatic adenocarcinoma of the stomach or gastroesophageal junction[J]. J Clin Oncol,2016,34(13):1448-1454.
[42] KOU P,ZHANG Y,SHAO W,et al. Significant efficacy and well safety of apatinib in an advanced liver cancer patient:a case report and literature review[J]. Oncotarget,2017,8(12):20510-20515.
[43] 胡猛,劉星,劉靜,等.阿帕替尼治療惡性腫瘤研究進展[J].中國老年學雜志,2018,38(19):4858-4861.
[44] 王茂勛,關露露,陳小兵.阿帕替尼治療惡性腫瘤的現狀和進展[J].腫瘤研究與臨床,2018,30(4):281-285.
[45] 張雪慧.阿帕替尼聯合TACE治療對原發性肝癌的療效及安全性研究[D].邯鄲:河北工程大學,2019.
(收稿日期:2019-11-03 修回日期:2020-04-28)
(編輯:陳 宏)

