Ⅳ型胃神經內分泌腫瘤的臨床病理特征及影響術后復發的危險因素分析
王延旭,劉 苗,張瑞星
(河北醫科大學第四醫院 消化內科,河北 石家莊 050000)
胃神經內分泌腫瘤(G-NENs)是一類異質性腫瘤,主要起源于胃內神經內分泌細胞。既往認為這是一類罕見病,但近年來此類腫瘤的發病率呈逐漸上升趨勢[1-3]。2010年世界衛生組織(WHO)按照每10個高倍視野(HPF)下的核分裂像數和Ki67指數將G-NENs分為G1~3級[4]。2016年中國胃腸胰神經內分泌腫瘤專家共識根據臨床病理特征的差異,將G-NENs的臨床分型分為4型,Ⅰ型為血清胃泌素升高同時伴有胃酸分泌減少的胃神經內分泌瘤(G-NET G1/G2),Ⅱ型為血清胃泌素升高伴胃酸分泌過多的胃神經內分泌瘤(G-NET G1/G2),Ⅲ型為血清胃泌素及胃酸分泌均正常的胃神經內分泌瘤(G-NET G1/G2/G3),Ⅳ型為惡性度較高的胃神經內分泌癌(G-NEC)和胃混合性腺神經內分泌癌(G-MANEC)[5]。目前認為Ⅳ型患者的預后最差,那么同屬于Ⅳ型的G-NEC和G-MANEC之間的臨床病理特征及預后有無差異呢?影響G-NEC和G-MANEC術后復發的危險因素是否有差異?不同輔助化療方案對患者術后復發的影響有無顯著差異?為探討這些問題,本研究回顧性分析69例Ⅳ型G-NENs的臨床病理資料和隨訪資料,探索其臨床病理特征、不同化療方案對預后的影響及影響復發的危險因素,以期為臨床診療提供依據。
1 資料與方法
1.1病例選擇 2013年1月1日至2017年12月31日于河北醫科大學第四醫院行胃癌根治術、術后病理診斷為Ⅳ型胃神經內分泌腫瘤(G-NENs)的患者共69例。根據2010年世界衛生組織提出的G-NENs病理分級標準分為2組,胃神經內分泌癌組(G-NEC)19例,男18例,女1例,平均年齡(59.1±5.7)歲;胃混合性腺神經內分泌癌組(G-MANEC)50例,男44例,女6例,平均年齡(62.2±6.8)歲。2組性別、年齡等一般資料差異無統計學意義(P>0.05),具有可比性。
1.2入選及排除標準 入選標準:①行胃癌根治術及D2淋巴結清掃術;②術后病理診斷為胃神經內分泌癌或胃混合性腺神經內分泌癌;③術后病理切緣陰性。排除標準:①術后病理分期為Ⅳ期(AJCC第8版);②隨訪期間并發其他惡性腫瘤;③術前或術后接受放療;④術后1個月內復發。
1.3方法 通過門診及電話隨訪,隨訪內容包括患者生存狀態、治療情況、復查情況、有無復發及其具體日期等。隨訪終點為影像學提示疾病復發。隨訪截止時間為2019年12月31日。
1.4觀察指標 從患者的病歷資料中收集性別、年齡、發病部位、首診癥狀、腫瘤最大直徑、病理分級(2010年WHO標準)、浸潤深度、淋巴結清掃個數、淋巴結陽性個數、腫瘤pTNM分期(AJCC第8版)、脈管瘤栓、神經受侵、術后免疫組織化學結果(Syn、CgA、Ki67)、是否行輔助化療、輔助化療方案、首診時中性粒細胞計數、首診時淋巴細胞計數、術前中性粒細胞淋巴細胞比值(NLR)、無復發生存時間(RFS)等臨床病理資料。
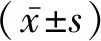
2 結 果
2.1隨訪結果 對2013年1月1日至2017年12月31日于河北醫科大學第四醫院行胃癌根治術、術后病理診斷為Ⅳ型胃神經內分泌腫瘤的76例患者進行隨訪。截至2019年12月31日,術后復發患者25例,未復發患者44例,失訪患者7例,失訪率約為9.2%,69例患者隨訪時間為2.6~80.2個月,中位隨訪時間為36.8個月。
2.2Ⅳ型G-NENs的臨床病理特征分析 患者首次就診時主要癥狀以進食不順最多見19例(27.5%),其次為一些常見消化系統疾病癥狀,如腹痛17例(24.6%),上腹不適14例(20.3%),消化道出血(包括嘔血、黑便)8例(11.6%),腹脹6例(8.7%),其他癥狀(包括惡心、嘔吐、噯氣)3例(4.3%),無癥狀通過查體而發現者2例(2.9%),全組患者均無類癌綜合征表現。 兩組性別、年齡、發病部位、T分期、N分期、pTNM分期、術前NLR水平、腫瘤最大直徑、是否術后2年內復發等方面的比較,差異均無統計學意義(P>0.05)。見表1。

表1 兩組臨床病理特征比較[例(%)]
2.3影響Ⅳ型G-NENs患者術后復發的危險因素 69例患者使用EP方案化療者9例(G-NEC3例,G-MANEC6例),使用SOX方案化療者16例(G-NEC3例,G-MANEC13例)。將病理分級(G-NEC與G-MANEC)、年齡、T分期、N分期、pTNM分期(Ⅱ期與Ⅲ期)、腫瘤最大直徑、術前NLR、是否行輔助化療、化療方案(EP與SOX)納入生存分析,以復發為終點事件,用Kaplan-Meier法繪制生存曲線,同時采用Log-rank檢驗行單因素分析,結果顯示病理分級(P=0.017)、是否行輔助化療(P=0.000)對術后復發的影響有統計學意義。見圖1、2。化療方案(EP與SOX)對術后復發的影響無統計學意義(P=0.193),見圖3。將病理分級、T分期、N分期、腫瘤最大直徑、是否行輔助化療納入COX比例風險回歸模型,顯示病理分級(P=0.014)、是否行輔助化療(P=0.000)是影響術后復發的獨立危險因素,見表2、3。
圖1 病理分級與復發的關系 圖2 Ⅳ型G-NENs患者是否化療與復發的關系

表2 賦值表

表3 Ⅳ型G-NENs術后復發的危險因素
2.4根據Ⅳ型G-NENs的病理分級進行分層分析
2.4.1影響G-NEC患者術后復發的危險因素 將年齡、T分期、N分期、pTNM分期(Ⅱ期與Ⅲ期)、腫瘤最大直徑、術前NLR、是否行輔助化療納入生存分析,以復發為終點事件,用Kaplan-Meier法繪制生存曲線并行Log-rank檢驗,顯示腫瘤最大直徑(P=0.037)、是否行輔助化療(P=0.005)是影響術后復發的危險因素,見圖4。由于G-NEC患者應用EP及SOX方案化療的病例數有限,未對比其差異。將T分期、N分期、腫瘤最大直徑、是否行輔助化療納入COX比例風險回歸模型,多因素分析顯示是否行輔助化療(P=0.012)是影響術后復發的獨立危險因素,見表4、5。
圖3 Ⅳ型G-NENs患者化療方案與復發的關系

表4 賦值表

表5 G-NEC術后復發的危險因素
2.4.2影響G-MANEC患者術后復發的危險因素 將年齡、T分期、N分期、pTNM分期(Ⅱ期與Ⅲ期)、腫瘤最大直徑、術前NLR、是否行輔助化療、化療方案納入生存分析,以復發為終點事件,采用Kaplan-Meier法繪制生存曲線,同時進行Log-rank檢驗行單因素分析,結果提示是否行輔助化療(P=0.000,見圖5)是影響術后復發的危險因素。化療方案(EP與SOX)對術后復發的影響無統計學意義(P=0.887,見圖6)。將T分期、N分期、是否行輔助化療納入COX比例風險回歸模型進行多因素分析,結果顯示是否行輔助化療(P=0.003)是影響術后復發的獨立危險因素,見表6、7。
圖5 G-MANEC患者是否化療與復發的關系 圖6 G-MANEC患者化療方案與復發的關系
3 討 論
近年國內外研究觀察均發現G-NENs的發病呈上升趨勢[1-3],這可能與近年來檢查及診斷水平的提高有關。根據不同的臨床表現、病理分級與分化程度、胃內pH值及血清胃泌素水平等可將G-NENs分為4種類型,其中Ⅳ型G-NENs(包括G-NEC、G-MANEC)預后最差[4-5]。本研究Ⅳ型患者多為中老年男性,發病部位以賁門部為主,這些特征與一些現有研究結果相似[6-7]。男性發病多于女性,考慮可能與男性有較多不良生活習慣如吸煙、飲酒等有關,另外性激素也可能在性別差異中起到一定作用。G-NENs可被分為功能性和非功能性兩類[8]。類癌綜合征是由神經內分泌腫瘤釋放大量激素引起的相關臨床癥狀,常表現為皮膚潮紅、頭痛、心動過速、高血壓等,出現上述癥狀即屬于功能性腫瘤[9]。本研究除2例無癥狀,其余患者均表現為常見消化系統疾病癥狀,有研究顯示約70%~80%的G-NENs患者是行胃鏡檢查時偶然發現的[10]。通過以上特征可以發現,臨床表現上鑒別G-NENs與其他胃部疾病有很大困難,因此對以上述癥狀就診,尤其伴有報警癥狀(如消化道出血、進行性消瘦等)的中老年患者應警惕本病,必要時應行內鏡檢查。另外,由于本病發病后可無任何臨床癥狀,因此建議高發病年齡人群在體檢時行胃鏡檢查,爭取早發現早治療,避免延誤病情。
本研究中,雖然G-NEC與G-MANEC在性別、年齡、發病部位、T分期、N分期、pTNM分期、術前NLR、腫瘤最大直徑等臨床病理特征上均無顯著差異,但其預后卻不同,認為G-MANEC較G-NEC預后好,與Kim等[11]和Park等[12]的研究結果一致。但Ishida等[13]認為二者的預后并無差別,也有研究認為G-MANEC較G-NEC預后差[14]。這種預后的差異可能與G-NEC中所含具體細胞成分(如小細胞、大細胞)的不同有關,另外G-MANEC中神經內分泌成分與腺癌成分的構成比及相對活性不同也可能影響預后。此外,目前對G-MANEC的組織學起源尚不十分清楚。一種觀點認為G-MANEC中的神經內分泌成分和腺癌成分起源于同一種干細胞,這種干細胞在腫瘤生長過程中分化出神經內分泌癌及腺癌兩種細胞成分,而另一種觀點則認為兩種細胞成分的起源是不同的[13, 15-16]。這些因素可能都會對G-NEC及G-MANEC的預后產生影響,遺憾的是目前相關研究較少,而本研究由于條件限制未對腫瘤中各細胞成分及其活性做區分,因此未能對上述推測做進一步論證。
本研究顯示,是否行輔助化療是影響Ⅳ型G-NENs患者術后復發的獨立危險因素,與Grande等[17]的研究結果相同。目前有研究認為,IP(伊立替康+順鉑)方案可作為G-NENs患者的術后化療方案[18-19]。本研究共有59例患者行輔助化療,主要方案為EP、SOX,其他化療方案包括TO方案、XELOX方案、FOLFOX方案等,本研究選取了主要使用EP、SOX方案行輔助化療的患者進行研究,結果顯示在Ⅳ型患者及G-MANEC患者中,EP、SOX方案對術后復發的影響不具有統計學意義,由于G-NEC患者樣本量限制,未對該型患者進行EP、SOX方案化療療效的研究。G-NEC特殊的生物學行為導致治療策略與胃腺癌不同[20]。有觀點認為,對于G-MANEC化療方案的選擇,應注意根據腫瘤原發灶含神經內分泌成分和腺癌成分的構成比、兩種成分各自的活性以及淋巴結轉移以哪種成分占優勢來綜合考慮。本研究由于條件限制未對G-MANEC進一步分組研究,且存在樣本量較少的問題,因此其療效尚需大樣本研究,在此僅做初步探索。雖然目前對G-NENs最優化療方案的選擇尚存在爭議[21],但本研究認為輔助化療可以降低G-NENs患者術后復發的風險是肯定的。
綜上所述,Ⅳ型G-NENs患者的臨床癥狀不典型,多見于中老年男性,因此對中老年初診患者要認真鑒別,避免漏診、誤診。Ⅳ型G-NENs的腫瘤成分較為復雜,這可能是影響其預后及化療有效性的因素。在本研究中,雖然使用EP、SOX方案行輔助化療對術后復發的影響無統計學意義,但可以肯定的是行輔助化療的患者術后不易復發,因此對已確診為Ⅳ型G-NENs的患者應根據病情積極給予輔助化療。本研究由于病例數及時間有限,所得結論尚需大樣本研究加以證實。

