完全性脊髓損傷亞急性期腦運動控制功能變化的功能磁共振研究
劉舒佳 ,張軍衛,王方永,唐和虎,白金柱,呂振,李建軍
1.首都醫科大學康復醫學院,北京市 100068;2.中國康復研究中心北京博愛醫院脊柱脊髓外科,北京市 100068;3.北京腦重大疾病研究院神經損傷與修復研究所,北京市 100068;4.北京市神經損傷與康復重點實驗室,北京市 100068
脊髓損傷后運動功能重建是近年的臨床熱點[1],其前提是人腦依然保有產生運動指令的能力。電生理學和功能神經影像學研究顯示,中樞神經損傷后,人腦能夠廣泛重組,具有可塑性[2-4],但重組方式卻存在爭論。功能磁共振成像(functional magnetic resonance imaging,fMRI)因具有較高的時空分辨率,對神經元活動定位較準確,可重復性較好,被廣泛應用于腦科學研究[5]。脊髓損傷患者損傷遠端肢體感覺和運動功能缺失,意象運動(motor imagery,MI)和試圖運動(attempted movement,MA)成為腦功能研究的主要運動任務[6]。
MI 是指想像、模擬特定動作的動態過程,而不伴有任何明顯的實際動作[7-8],等同于運動準備和再現[9]。與之對應的是實際運動(executive movement,ME)。MI 和ME 均依賴類似的運動再現,激活共同的腦皮質區域[10-11];在行為學水平,二者保持相同的時間結構并遵循同樣的運動規律[12-13]。MA 則是指盡力去做某一動作,不論該動作最終是否能夠完成。MA所興奮的神經網絡與健康人實際執行該動作時所興奮的網絡相同。
本研究觀察通過不同運動任務下,脊髓損傷患者腦皮質激活區域和強度的變化,揭示腦運動控制功能的可塑性改變。
1 資料與方法
1.1 一般資料
選取2017 年1 月至2019 年1 月北京博愛醫院脊柱脊髓外科收治的完全性脊髓損傷患者為患者組,符合美國脊髓損傷協會殘損分級(American Spinal Injury Association Impairment Scale,AIS)[14]的診斷標準。
納入標準:①AIS 分級A 級;②病程3~6 個月,度過脊髓休克期;③足背伸功能缺失(經體格檢查、運動誘發電位檢查證實)[15];④MI 形象度問卷(Vividness of Motor Imagery Questionnaire,VMIQ)[16]評分<60分。
排除標準:①不能接受MRI 檢查;②顱腦外傷、神經疾患,或積極性不高;③并發四肢骨折或其他嚴重損傷。
共納入外傷致脊柱骨折/脫位患者11 例,其中男性9例,女性2例;年齡18~48歲,平均32.6歲;滑鐵盧利足量表評定為右利足;高中以上文化程度;損傷節 段T74 例,T102 例,T4、T6、T8、T11、L2各1 例;病程3~6個月,平均4.1個月。
在MRI 掃描前1 d 再次查體,確認仍為完全性脊髓損傷,沒有恢復。1 例患者在掃描中表現緊張,檢查發現心率加快等類幽閉恐懼癥;1 例掃描發現顳葉部分缺如,但無任何體征、癥狀;1 例發現顳極部圓形短T2信號灶,追問病史發現曾應用顱環牽引治療,推測固定螺栓位置可能有金屬殘留;1 例掃描后表示不能清楚區分音頻指令與掃描過程中的噪音。均予排除,按照納入標準補足。
對照組共納入健康志愿者12例,均為本院職工和進修醫師。兩組性別、年齡和VMIQ 均無顯著性差異(P>0.05)。見表1。
所有參與者均簽署知情同意書。本研究獲中國康復研究中心醫學倫理委員會批準(No.2019-113-1)。
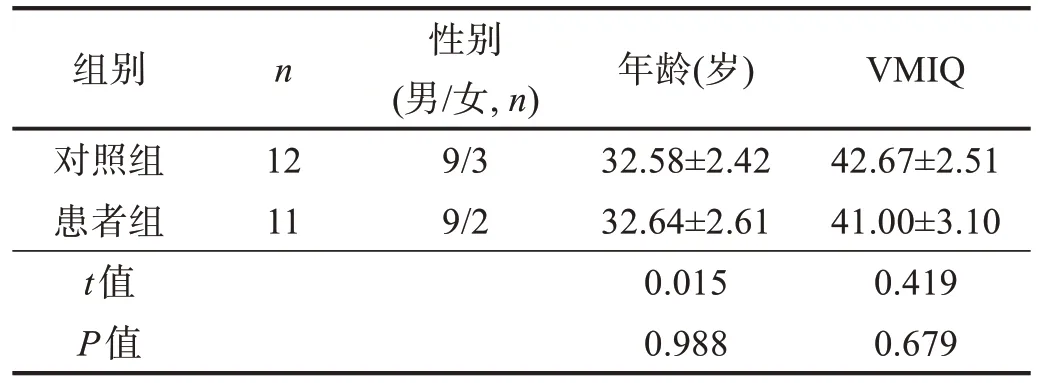
表1 兩組一般情況比較
1.2 方法
采用1.5 T Signa Excite 超導磁共振成像系統(美國GE 公司),標準正交頭顱線圈。以正中矢狀面圖像為定位圖像,獲取橫斷面T1WI 和T2WI 圖像,掃描基線與前-后聯合連線平行。T1WI 成像參數:TR/TE 2925 ms/10.4 ms,層厚/間隔5 mm/0 mm,視野24 cm,激勵次數4 次。T2WI 采用GE-EPI 序列,TR 3000 ms,TE 40 ms,翻轉角90°,激勵次數1 次,矩陣64×64,視野24 cm,層厚/間隔5 mm/0 mm。
首先行定位掃描。28層無間隔掃描線的標記要確保頂葉能完全包括在內。然后按照功能相-解剖相-功能相的順序掃描。每個功能相時長504 s,前24 s為預掃描期,無數據產生。兩次功能相掃描間隔以解剖相掃描,避免患者疲勞和重復任務執行帶來的興奮性下降。
采用組塊設計(block-design)模式,靜息狀態與運動任務執行過程交替進行,以靜息-想象-靜息-運動為1 個循環,共4 個循環。具體的音頻組成:靜息21 s,指令3 s,MI 21 s,靜息21 s,指令3 s,MA/ME 21 s,4 個循環共360 s。指令為“準備想象/運動開始”;最后指令為“停”,1 s,任務結束。
預先錄制好的音頻文件通過MRI 內部系統播放,輔以內部通話系統指導研究。
受檢者每天晨起和睡前各伴隨音頻指令進行練習2次,約30 min,共6 d,第7天進行掃描。
1.2.1 MA/ME任務
對照組完成ME。閉目平臥,聽到指令后將優勢足維持于背屈中立位21 s。用力適度,以僅能對抗令足背下垂的重力為準。以長腿石膏模具的前托規范背屈角度。
脊髓損傷患者無法活動足部,完成MA,即盡最大努力去“命令”優勢足背伸。
1.2.2 MI任務閉目平臥,聽到指令后僅想象MA/ME 任務中描述的內容,而并不實際完成。
1.3 統計學分析
以疊加于T1解剖相上的后驗概率圖(posterior probability maps,PPMs)顯示不同運動任務下,兩組腦運動功能網絡的激活區域和程度。
采用運行于MATLABR 2007b 平臺的SPM5 軟件包進行數據后處理。數據依次進行運動校正、功能像與結構像配準、歸一化和平滑。運動校正以第一時段成像數據的第一幅掃描圖像為基準,對同一受試者兩個時段的成像數據進行基于剛體模型的運動校正。空間平滑采用9×9×9 mm 全寬半高高斯核進行[17]。運動校正后,使用SPM5 提供的Bayes 推斷進行激活/抑制體素識別,所得PPMs 投射到運動校正后寫出的T1解剖相上。
采用SPM5 軟件包提供的Bayes 推斷法進行組間分析,效應水平閾值采用SPM5 給出的γ 值,概率閾值設為0.95。效應水平閾值γ相當于背景噪音的水平。
2 結果
2.1 MA/ME
對照組ME 激活區僅見于右側側初級感覺(primary somatosensory cortex,S1)、頂下小葉(inferior parietal lobule,IPL)、殼核及小腦后葉(圖1、圖4)。患者組MA 激活區包括雙側S1/初級運動皮層(primary motor cortex,M1)、輔助運動區(supplementary motor area,SMA)、背側運動前區(premotor dorsal cortex,PMd)、扣帶回運動區(cingulate motor area,CMA)、外側蒼白球、小腦,左側腹側運動前區(premotor ventral cortex,PMv)、丘腦腹后外側核、殼核和右側頂下小葉(圖2、圖4)。患者組MA 所激活程度高于ME 的區域包括雙側M1/S1、SMA、上頂葉皮質(superior parietal cortex,SP)、CMA、小腦、島葉、丘腦、殼核,右側頂下小葉(圖3、圖4)。
2.2 MI
對照組MI激活區域位于左側M1,雙側SMA、顳上回,右側PMd(圖5、圖8)。患者組MI 激活區域位于雙側SMA、前額葉皮質(prefrontal cortex,PFC)、島葉,左側PMv、基底核,右側PMd、PMv、頂下小葉(圖6、圖8)。患者組激活程度更高的區域存在于右側SMA、M1、PMd,左側SMA、頂下小葉、島葉、基底核(圖7、圖8)。
2.3 MI和MA/ME比較
對照組MI 時,左側PFC,雙側CMA、M1/S1、SMA 較ME時興奮;ME時沒有比MI更多的激活區域(圖9)。患者組MA 時,左側M1,雙側CMA 和SMA,右側小腦較MI 時興奮;MI 時沒有比MA 更多的激活區域(圖10)。
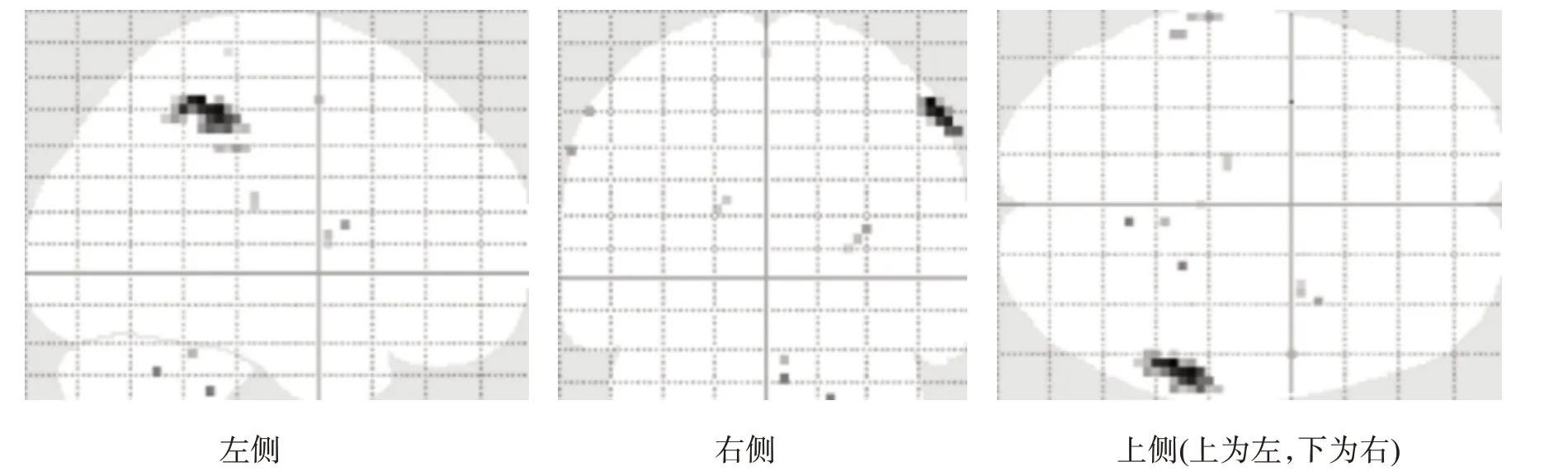
圖1 ME時激活腦區簡圖

圖2 MA時激活腦區簡圖
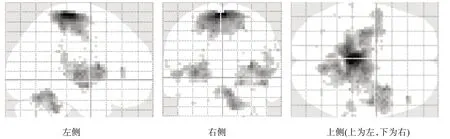
圖3 患者組較對照組激活程度更高的腦區
3 討論
許多重建脊髓損傷后運動功能的治療方案均假設腦運動控制功能完整。事實上,脊髓損傷后腦皮質結構會發生適應性重塑[18-19],尤其是在接受某些康復訓練后[20]。Dias Leao 等[21]的研究發現,僅僅在脊髓休克期后幾天內,大腦皮質就發生了重組。
腦運動功能網絡分布廣泛,大腦、基底節、丘腦、小腦等均有涉及。Oni-Orisan 等[2]對病程2 年以上完全性脊髓損傷患者進行fMRI 掃描,發現感覺運動皮質激活模式已發生重組。本研究顯示,脊髓損傷患者M1、SMA 等運動皮質興奮,表明腦運動控制功能仍保留。但也發現一些腦激活紊亂情況,如頂葉和小腦等感覺運動整合區域的激活增加,蒼白球-丘腦-皮質環路募集增多等。頂葉是感覺運動整合的關鍵結構,在運動技巧的習得和喚醒中扮演重要角色;后頂葉皮質對運動準備和運動編程起一定作用[2,22]。殼核與技巧性行為的長期保持有關。丘腦腹后外側核接受PFC 和邊緣系統的輸入并轉繼至PFC 聯合區,在注意、計劃、組織、摘要思考、多任務、激活記憶方面發揮重要作用。這些區域的異常激活,反映脊髓損傷患者組織動作計劃能力的變化。至于它們究竟是代表興奮增多還是抑制增多,有待進一步研究。
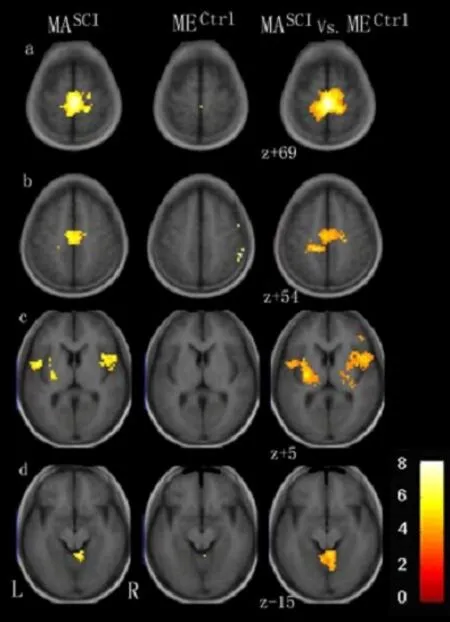
圖4 兩組MA/ME激活模式比較

圖5 對照組MI時激活腦區

圖6 患者組MI時激活腦區
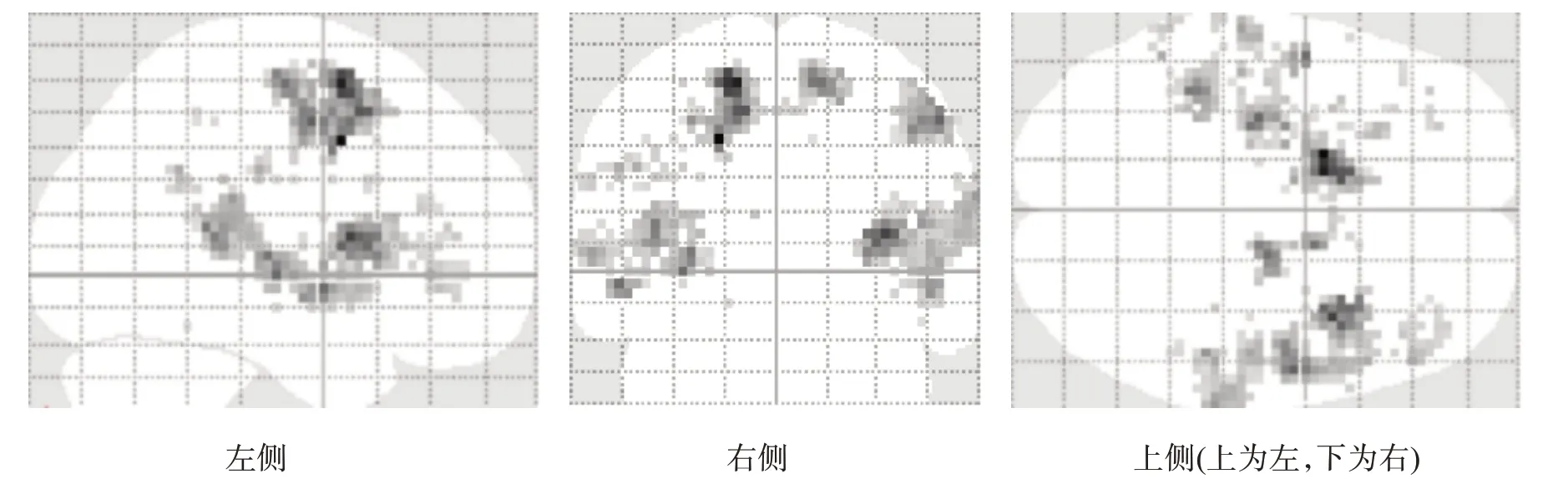
圖7 患者MI激活程度較對照組更高的腦區
本研究顯示,脊髓損傷患者MA 與健康人ME 相比,激活區域較多,激活程度更高。可能的原因是:①足部適度背屈對于健康人而言非常簡單,皮質興奮很低,而脊髓損傷患者則要“用盡全力”,從而誘發較廣范圍的腦區激活[23];②由于脊髓損傷患者沒有實際的感覺反饋,所以在MA 過程中會持續提高皮質興奮程度。本研究發現,脊髓損傷患者MA 與健康人ME 時,運動相關皮質的激活情況類似,說明MA 與ME 在相當程度上共享一套神經網絡;脊髓損傷后短時期內,患者腦運動控制系統有較多保留。
MI 時,脊髓損傷患者同樣激活了更多區域。可能的原因是健康人MI 時,那些直接或間接聯系到脊髓的區域被積極抑制,激活較少。Porro等[24]研究這一效應對M1 影響,認為信號強度降低70%。脊髓損傷患者的MI 無需任何動作抑制,沒有發現信號減低。所以M1/S1 感覺輸入和運動輸出的長期缺失所致腦皮質抑制減少,可能是脊髓損傷患者MI 時皮質和及皮質廣泛顯著激活的原因。由此可見,皮質重組是生理需求、病變程度、病變時程、大腦內部聯系以及大腦和外周聯系的綜合反應,是大腦適應內部和外部環境變化進行調整的結果。
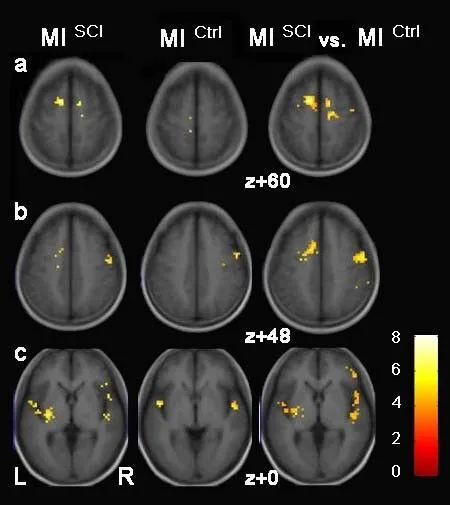
圖8 兩組MI激活模式比較
綜上所述,病程3~6 個月的完全性脊髓損傷患者依然保有區分MA 與MI 的能力,執行運動任務時M1、SMA 的興奮模式基本正常,表明腦運動控制功能基本保留,運動相關網絡較為完整。但脊髓損傷后感覺缺失和運動障礙已經對腦興奮模式產生一定影響,頂葉和小腦等感覺運動整合區域的激活增加,說明腦功能已經發生了某種適應性重組。
本研究采用的運動任務較為簡單,誘發的激活效應較低,有待今后研究改進。
利益沖突聲明:所有作者聲明不存在利益沖突。
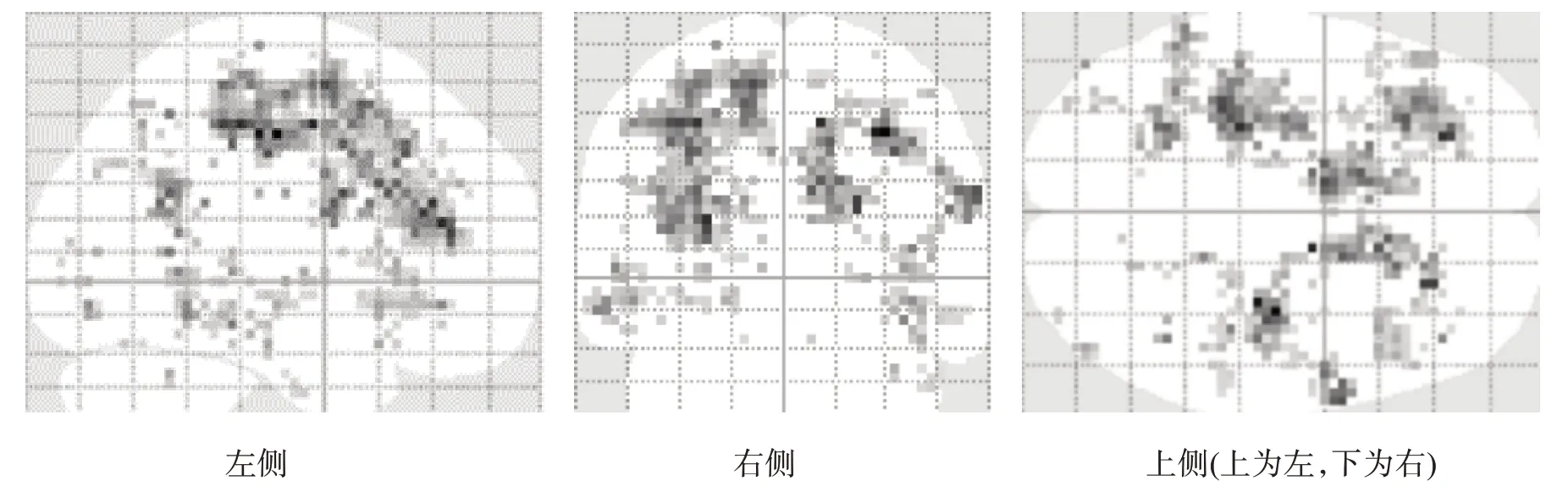
圖9 對照組MI較ME激活程度更高的腦區

圖10 患者組MA較MI激活程度更高的腦區

