lncRNA ZNF571-AS1對前列腺癌細胞增殖及侵襲能力的影響
楊凌博 楊金輝 魯帥奇 李小輝 盧績
1鄭州大學附屬洛陽中心醫院泌尿外科(河南洛陽471009);2吉林大學附屬第一醫院泌尿外科(長春130021)
前列腺癌是男性泌尿生殖系統最常見的惡性腫瘤之一,前列腺癌的發病率逐年增加,嚴重威脅男性健康[1]。早期前列腺癌的治療方式是根治性手術,治療效果較好[2]。但由于早期前列腺癌多無明顯癥狀,導致多數患者發現時已是中晚期前列腺癌[3]。探究前列腺癌發生、發展的分子機制,可能對前列腺癌的早期診斷和分子靶向治療具有重要臨床意義。長鏈非編碼RNA(long non-coding RNA,lncRNA)存在于真核細胞,長度大于200個核苷酸,不能編碼蛋白質[4]。在人類幾乎所有惡性腫瘤中存在lncRNA的異常表達,其表達水平與腫瘤細胞的各種生物學行為相關[5]。前列腺癌中存在lncRNA的異常表達,通過檢測前列腺癌組織或患者血清lncRNA的表達可能有助于前列腺癌的早期診斷[6]。ZNF571-AS1是近年來新發現的lncRNA,可能參與急性髓細胞性白血病的發生、發展[7]。ZNF571-AS1在前列腺癌組織中的表達和分子機制尚不清楚。本研究擬分析ZNF571-AS1在前列腺癌組織和細胞系中的表達,觀察ZNF571-AS1對前列腺癌細胞增殖和侵襲的影響,探討其可能的分子機制。
1 材料和方法
1.1 材料
1.1.1 臨床標本52例前列腺癌組織及癌旁組織均取自2018年3月至2019年5月鄭州大學附屬洛陽中心醫院泌尿外科住院患者。所有組織標本均經兩名以上病理學專家確診,所有患者術前均未接受過放療和化療。患者年齡平均(59.43±14.63)歲。Gleason評分:<7分27例,7分25例。臨床分期:Ⅰ和Ⅱ期33例,Ⅲ和Ⅳ期19例。本研究經本院醫學倫理委員會批準,患者均簽署知情同意書。
1.1.2 細胞與試劑正常前列腺上皮細胞(RWPE-1)和前列腺癌細胞系(DU-145、C4-2B、LNCaP、PC-3)購于中國典型培養物保藏中心。qPCR試劑盒購于南京建成生物工程研究所。沉默ZNF571-AS1基因的質粒和陰性對照質粒購于上海吉瑪基因股份有限公司。Matrigel基質膠、一抗和二抗購于美國BD公司。培養基和胎牛血清購于美國Hyclone公司。轉染試劑LipofectamineTM 3000購于美國Invitrogen公司。Transwell小室購于美國Corning公司。噻唑藍(methyl thiazol tetrazolium,MTT)試劑盒購于南京凱基生物科技發展有限公司。
1.2 方法
1.2.1 細胞培養和轉染前列腺癌細胞系用含10%胎牛血清的RPMI-1640培養基培養,正常前列腺上皮細胞用含10%胎牛血清的KSFM培養基培養。將對數生長期的DU-145細胞采用LipofectamineTM 3000試劑轉染沉默ZNF571-AS1基因的質粒和陰性對照質粒,命名為實驗組和對照組,轉染操作按照說明書進行。
1.2.2 qPCR 檢測ZNF571-AS1、miR-301b-3p 和AR mRNA 的表達TRIzol法提取組織及細胞總RNA,進一步逆轉錄為cDNA。建立qPCR反應體系,以GAPDH作為內參,檢測ZNF571-AS1和AR mRNA的表達;以U6作為內參,檢測miR-301b-3p的表達。引物序列如下,ZNF571-AS1正向引物:GGTCTCGGTACATGCGTGGA,反向引物:TGGCAGTATAACAGGCTCCC;miR-301b-3p正 向 引 物:GGGCTTTGACAATATCATTG,反向引物:CAGTGCGTGTCGTGGAGT;GAPDH正向引物:CTGGGCTACACTGAGCACC,反向引物:AAGTGGTCGTTGAGGGCAATG;AR正向引物:CCAGGGACCATGTTTTGCC,反向引物:CGAAGACGACAAGATGGACAA。U6正向引物:CTCGCTTCGGCAGCACA,反向引物:AACGCTTCACGAATTTGCGT。應用2-ΔΔCt方法計算相對表達量。
1.2.3 MTT 法檢測DU-145 細胞的增殖能力收集兩組細胞,分別以3 × 103個/孔接種于96孔板。檢測時每孔加入20 μL MTT試劑,繼續培養4 h。加150 μL/孔二甲基亞砜,振蕩10 min,酶標儀測定每孔450 nm波長處的光密度(OD)值,分別檢測第1、2、3、4、5天細胞的增殖活性。
1.2.4 小室(Transwell)實驗檢測DU-145 細胞的侵襲能力采用培養基稀釋Matrigel基質膠,按50 μL每孔包被小室底膜上室。收集兩組細胞,分別以3 × 104個/孔接種于上室,下室加入600 μL含胎牛血清的RPMI-1640培養基。培養箱內培養24 h后,棉簽擦去未侵襲的細胞,采用多聚甲醛固定,采用0.1%結晶紫染液染色,PBS溶液沖洗。在100倍顯微鏡下每孔隨機取4個視野,計數并拍照。
1.2.5 生物信息學技術預測ZNF571-AS1 的分子機制采用生物信息學網站starBase v2.0預測ZNF571-AS1可互補結合的miRNA。采用生物信息學網站RNAhybrid預測miR-301b-3p可互補結合的靶基因mRNA。
1.2.6 Western blot法檢測AR蛋白和PI3K/Akt信號通路蛋白的表達收集兩組細胞并提取細胞蛋白,測定蛋白濃度。采用10%十二烷基硫酸鈉聚丙烯酰胺凝膠垂直電泳分離蛋白,轉膜后應用5%脫脂牛奶封閉。采用一抗孵育,在4 ℃下過夜。洗膜后,采用二抗在室溫下孵育。洗膜后,采用ECL法發光、顯影。
1.2.7 統計學方法所有數據均采用SPSS 19.0軟件統計分析,計量資料以均數±標準差表示,組間均數比較采用方差分析及t檢驗,以P <0.05為差異有統計學意義。
2 結果
2.1 前列腺癌組織和癌旁組織中ZNF571-AS1 的表達前列腺癌組織和癌旁組織中ZNF571-AS1的表達分別為(5.71 ± 0.61)和(0.69 ± 0.18),前列腺癌組織中ZNF571-AS1表達顯著高于癌旁組織(P <0.01),見圖1。
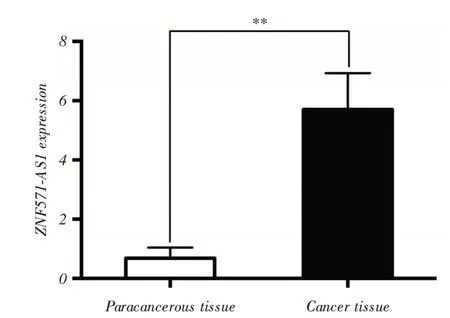
圖1 前列腺癌組織和癌旁組織中ZNF571-AS1 的表達Fig.1 ZNF571-AS1 expression in prostate cancer tissues and adjacent tissues
2.2 前列腺癌細胞和正常前列腺上皮細胞中ZNF571-AS1的表達與正常前列腺上皮細胞相比,前列腺癌細胞系中ZNF571-AS1的表達顯著較高(P <0.05),DU-145細胞中ZNF571-AS1的表達最高(P <0.01),因而選擇DU-145細胞進行研究。見圖2。
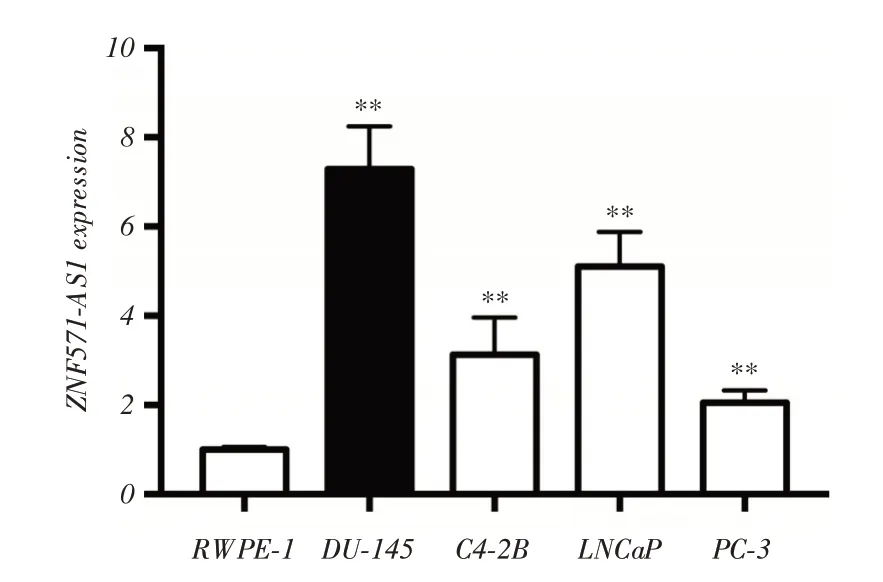
圖2 前列腺癌細胞和正常前列腺上皮細胞中ZNF571-AS1 的表達Fig.2 ZNF571-AS1 expression in prostate cancer cells and normal prostate epithelial cells
2.3 兩組DU-145 細胞中ZNF571-AS1 的表達qPCR結果顯示,實驗組和對照組DU-145細胞中ZNF571-AS1表達分別為(0.17 ± 0.04)和(1.01 ±0.06),實驗組顯著低于對照組(P <0.01),提示轉染成功。
2.4 低表達ZNF571-AS1抑制DU-145細胞的增殖能力MTT法結果顯示,從 第2天起,實驗組DU-145細胞增殖能力顯著低于對照組(P <0.05)。見圖3。
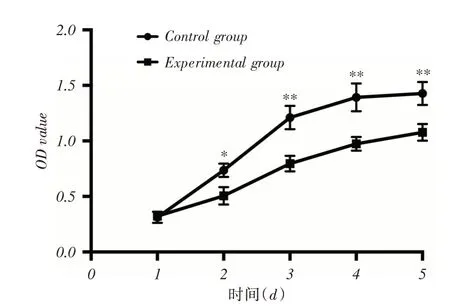
圖3 MTT 檢測ZNF571-AS1 對DU-145 細胞增殖能力的影響Fig.3 MTT was used to detect the effect of ZNF571-AS1 on the proliferation ability of DU-145 cells
2.5 低表達ZNF571-AS1 抑制DU-145 細胞的侵襲能力小室(Transwell)實驗顯示,實驗組和對照組DU-145細胞侵襲細胞數分別為(33.37±5.33)個和(87.55±6.72)個,與對照組相比,低表達ZNF571-AS1后顯著抑制DU-145細胞的侵襲能力(P <0.01),見圖4。
2.6 生物信息學技術預測ZNF571-AS1 的分子機制采用生物信息學網站starBase v2.0預測ZNF571-AS1可互補結合miR-301b-3p。采用生物信息學網站RNAhybrid預測miR-301b-3p可互補結合AR mRNA。見圖5。
2.7 低表達ZNF571-AS1 的前列腺癌細胞中miR-301b-3p 和AR mRNA 的表達qPCR結果顯示,實驗組和對照組DU-145細胞miR-301b-3p的表達分別為(5.28±0.49)和(1.08±0.40),低表達ZNF571-AS1可促進miR-301b-3p的表達(P <0.01)。實驗組和對照組DU-145細胞AR mRNA的表達分別為(0.38 ± 0.05)和(1.01 ± 0.06),提示miR-301b-3p表達增加后,AR mRNA表達降低(P <0.01)。
2.8 低表達ZNF571-AS1促進AR蛋白表達Western blot結果顯示低表達ZNF571-AS1引起AR蛋白表達升高,AR蛋白表達升高后,造成PI3K/Akt信號通路蛋白如p-PI3K、p-Akt及p-GSK3β蛋白表達降低,PI3K/Akt信號通路轉導被抑制。見圖6。
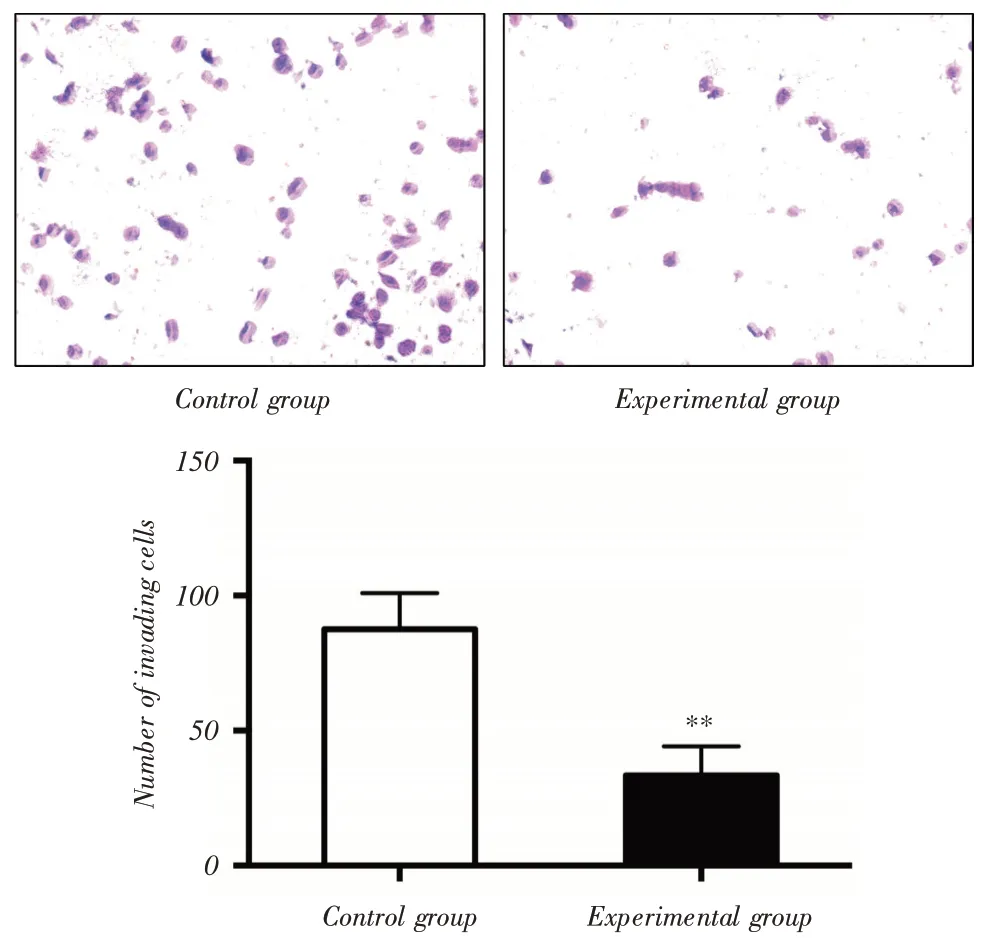
圖4 小室(Transwell)實驗檢測ZNF571-AS1 對DU-145 細胞侵襲能力的影響Fig.4 Transwell invasion test was used to detect the effect of ZNF571-AS1 on the invasion ability of DU-145 cells

圖5 生物信息學技術預測ZNF571-AS1 的分子機制Fig.5 Bioinformatics technology predicted the molecular mechanism of ZNF571-AS1
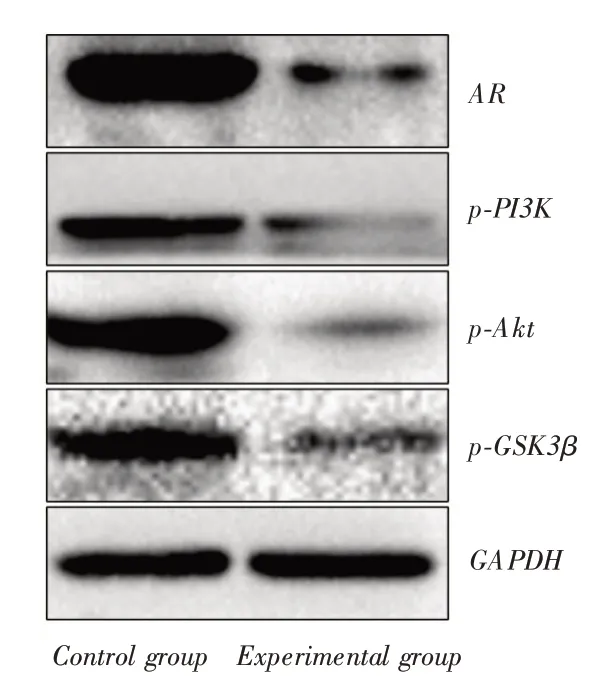
圖6 Western blot 法檢測AR 蛋白及PI3K/Akt 信號通路蛋白表達情況Fig.6 Western blot method was used to detect the expression of AR protein and PI3K/Akt signaling pathway proteins
3 討論
lncRNA是一類內源性非編碼RNA,缺乏開放閱讀框[8]。lncRNA可調控基因的轉錄和翻譯,參與包括前列腺癌在內的各種腫瘤的發生、發展[9]。越 來 越 多 的lncRNA如MNX1-AS1[10]、GAS5[11]、PCAT1[12]、CCAT1[13]、LINC01638[14]等被發現在前列腺癌中異常表達,影響前列腺癌細胞的生物學行為。ZNF571-AS1是近年來新發現的長鏈非編碼RNA,有研究[7]表明,ZNF571-AS1可能發揮癌基因作用,促進急性髓細胞性白血病的發生、發展。ZNF571-AS1在前列腺癌中的表達和功能尚不明確。本研究中,ZNF571-AS1在前列腺癌組織和細胞系中均呈高表達,表明其可能在前列腺癌細胞中發揮癌基因作用。MTT實驗和小室實驗顯示,下調ZNF571-AS1可抑制前列腺癌細胞的增殖和侵襲能力,進一步證明ZNF571-AS1在前列腺癌細胞中發揮腫瘤促進作用。
lncRNA攜帶有特定miRNA的“種子序列”,可吸附結合miRNA,阻止miRNA與其靶基因mRNA結合,從而抑制miRNA對靶基因表達的干擾作用[15]。本研究采用starBase v2.0網站預測,ZNF571-AS1可互補結合miR-301b-3p。miR-301b-3p可能在肝癌組織和細胞系中表達降低,上調miR-301b-3p具有抑制肝癌細胞增殖、遷移和侵襲的作用[16]。本研究發現,下調ZNF571-AS1后,前列腺癌細胞中miR-301b-3p表達增加,提示ZNF571-AS1可能通過吸附結合miR-301b-3p。miRNA主要通過結合靶基因mRNA區域,抑制其翻譯或者直接導致其降解,從而抑制靶基因的表達[17]。本研究采用RNAhybrid網站預測,miR-301b-3p可互補結合雄激素受體(Androgen receptor,AR)mRNA。AR屬于類固醇激素受體家族,定位于Xq11-12[18-19]。AR在前列腺癌組織和細胞系中表達明顯增加,與前列腺癌的發生、發展顯著相關[20]。下調AR表達可明顯抑制前列腺癌細胞的生長和轉移[21]。本研究發現,miR-301b-3p表達增加后,前列腺癌細胞中AR基因表達下調,提示miR-301b-3p可能具有抑制AR基因表達的作用。有研究[22]表明,AR通過促進PI3K/Akt信號通路轉導,促進細胞的生長和轉移。本研究證明,AR基因表達降低后,PI3K/Akt信號轉導通路蛋白如p-PI3K、p-Akt及p-GSK3β表達明顯降低,表明PI3K/Akt信號通路轉導被干擾。本研究下一步將通過雙熒光素酶報告基因實驗驗證ZNF571-AS1與miR-301b-3p及miR-301b-3p與AR mRNA之間的結合。
綜上所述,lncRNA ZNF571-AS1在前列腺癌組織和細胞系中高表達,下調ZNF571-AS1可能通過調控miR-301b-3p/AR信號通路抑制前列腺癌細胞的增殖和侵襲能力。因此,ZNF571-AS1在前列腺癌分子靶向治療中具有一定的研究價值。

