宮頸癌組織bFGF 表達與臨床病理特征及HR-HPV病毒載量的關系
馬金平,王雅莉,婁歡,李紅娟
(鄭州大學附屬鄭州中心醫院婦科,河南 鄭州 450000)
細胞因子或者癌基因水平的改變,能夠影響到柱狀上皮的早期異常分裂過程,最終促進宮頸癌的發生發展[1]。生長因子調控蛋白的波動能影響癌基因的激活,加劇癌基因對腫瘤增殖的影響[2]。堿性成纖維細胞生長因子(bFGF)是生長因子家族成員,其對于下游癌細胞內信號通路的上調作用,能夠促進腫瘤信號通路蛋白的交錯激活,促進了癌細胞對于局部癌旁組織的侵襲[3]。有部分研究者探討了b FGF 在宮頸癌患者中的表達情況,認為在宮頸癌患者中,bFGF 蛋白的表達濃度明顯上升[4],但關于其與宮頸癌患者體內高危型人乳頭瘤狀病毒 (HRHPV)載量關系的研究甚少。本研究探討了宮頸癌組織bFGF 表達情況及其與宮頸癌病理學特征、高危型人乳頭瘤狀病毒(HR-HPV)病毒載量的關系,旨在為宮頸癌的發生發展機制提供參考依據。
1 研究對象與方法
1.1 研究對象的資料情況 選取 2018 年 1 月-2019 年1 月病理科收集的90 例宮頸癌組織作為宮頸癌組,癌旁組織標本為對照組。年齡44~65 歲,平均54.3±7.4 歲,依據國際婦產聯盟分期(FIGO)標準:其中Ⅰ期宮頸癌22 例,Ⅱ期宮頸癌42 例,Ⅲ期宮頸癌20 例,Ⅳ期宮頸癌6 例;宮頸癌組織病理學分化情況:高、中、低分化患者分別為31 例、35例、24 例;其中檢測出淋巴結轉移患者39 例;肌層浸潤深度≥1/2 的宮頸癌患者有35 例;腫瘤病灶:≥3.0 cm 47 例。
1.2 納入及排除標準 納入標準:⑴符合中華婦產科學會制定的《宮頸癌診斷與治療指南(第四版)》中的宮頸癌診斷標準[5];⑵經病理學檢查證實,病理診斷標準符合中華醫學會病理學分會女性生殖系統疾病學組及中國優生科學協會陰道鏡與宮頸病理學會病理學組發布的 《宮頸癌及癌前病變病理診斷規范》中規定的取材、操作及診斷標準;⑶均為首次診斷的患者,既往無放化療史;⑷本研究符合《赫爾透辛基宣言》相關醫學倫理規定,并經我院倫理委員會批準。排除標準:⑴伴有其他部位的惡性腫瘤;⑵手術后復發的宮頸癌患者;⑶甲狀腺功能障礙患者;⑷合并宮頸、生殖系統其他重大疾病的宮頸癌患者。
1.3 免疫組化檢測 采用石蠟切片,脫水操作后采用3%H2O2室溫條件下孵育20min, 磷酸鹽緩沖液清洗3 次,每次5min,磷酸鹽緩沖液稀釋后的山羊血清封閉抗體5min,倒去血清后不清洗,加入一抗(購自賽默飛世爾中國 濃度:1:1000)5ml,37℃孵育2h,或者放置4℃冰箱過夜孵育,磷酸鹽緩沖液清洗3 次,每次5min,加入生物素熒光標記的二抗(購自賽默飛世爾中國 濃度:1:2000)3ml,37℃孵 育20~30min,磷酸鹽緩沖液清洗 3 次,每次 5min,加入Streptavidin/HRP 辣根酶標記鏈霉卵白素,37℃孵育20~30min,磷酸鹽緩沖液清洗3 次,每次5min,增強型HRP-DAB 底物顯色試劑盒 (PA110)顯色,自來水沖洗,復染,封片。
bFGF 蛋白主要表達在宮頸癌組織細胞的細胞漿,顯微鏡下觀察呈黃色、棕黃色、褐色則表現為陽性表達[9],⑴依據bFGF 蛋白陽性染色強度:無色(0 分)、淡黃色(1 分)、棕黃色(2 分)、褐色(3 分);⑵bFGF 蛋白陽性表達細胞占視野下所有細胞的比例:占比≤10%為 1 分、占比范圍 11%~50%(2 分)、占比范圍 51%~75%(3 分)、占比范圍>75%(4 分),染色強度與陽性染色細胞占比范圍積分的乘積為總分,總分<3 分為陰性、≧3 分為陽性。
1.3 HC2-HPV-DNA 檢測及評價 常規窺器暴露宮頸后,將HPV 采樣刷放置于宮頸口按逆時針轉3圈,并停留10s。將需要部分采樣刷留在標本儲藏瓶中,密閉后做好標記并送檢。采用雜交捕獲法并應用基因雜交信號放大系統(DML2000TM,美國Digene 公司提供) 進行 HC2-HPV-DNA 檢測,HPV試劑盒為上海萊特公司提供,嚴格按照說明書進行操作。以光量讀數與陰性測定值的比值(RLU/CO)對HPV 病毒載量進行劃分, 由于RLU/CO 離散度較大,因此對其進行常用對數轉換(即lg RLU/CO)將 HPV 病毒載量分為<1,1~<2,2~<3,≥3 四個等級。HR-HPV 載量分析:同一級別宮頸病變,HPV載量越高,患病的危險度越高;不同級別宮頸病變,HPV 載量越高,患高級別病變的危險度越高。
1.4 統計學方法 本研究收集的所有數據均在SPSS21.0 中進行統計分析,年齡采用進行統計描述,數據比較分析應用t 檢驗;χ2檢驗分析bFGF蛋白陽性表達率;bFGF 蛋白陽性表達率與HRHPV 病毒載量的關系采用Mann-Whitney U 檢驗;P<0.05 為差異具有統計學顯著性。
2 結果
2.1 兩組bFGF 蛋白陽性表達率比較 宮頸癌組bFGF 蛋白陽性表達率明顯高于對照組,差異有統計學意義(P<0.05),見表 1。
2.2 宮頸癌組織中的bFGF 蛋白陽性表達率與患者臨床病理特征的關系 不同FIGO 分期、 是否發生淋巴結轉移的宮頸癌患者癌組織中bFGF 蛋白陽性表達率差異有統計學意義(P<0.05);不同組織學分化程度、分型、不同病灶大小、不同肌層浸潤深度的宮頸癌組織中bFGF 蛋白陽性表達率差異無統計學意義(P>0.05),見表 2。
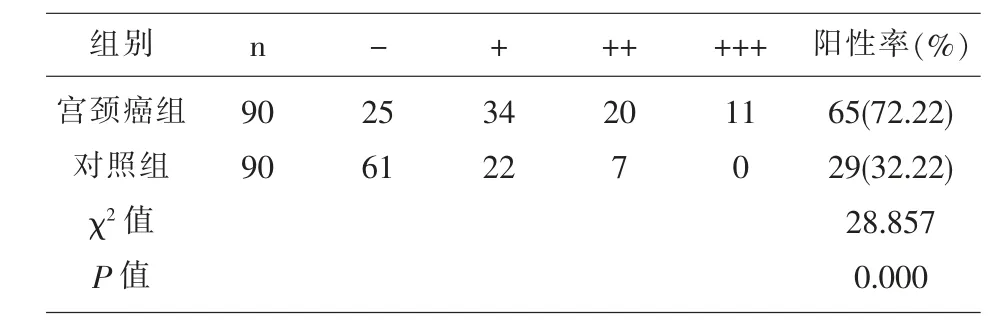
表1 二組bFGF 蛋白陽性表達率比較

表2 宮頸癌組織中的bFGF 蛋白陽性表達率與患者病理學特征的關系
2.3 宮頸癌組織中的bFGF 蛋白陽性表達率與HR-HPV 病毒載量的關系 宮頸癌組織中bFGF蛋白陽性表達與陰性表達者HR-HPV 病毒載量的總體分布差異具有統計學意義(P<0.05)見表3。
3 討論
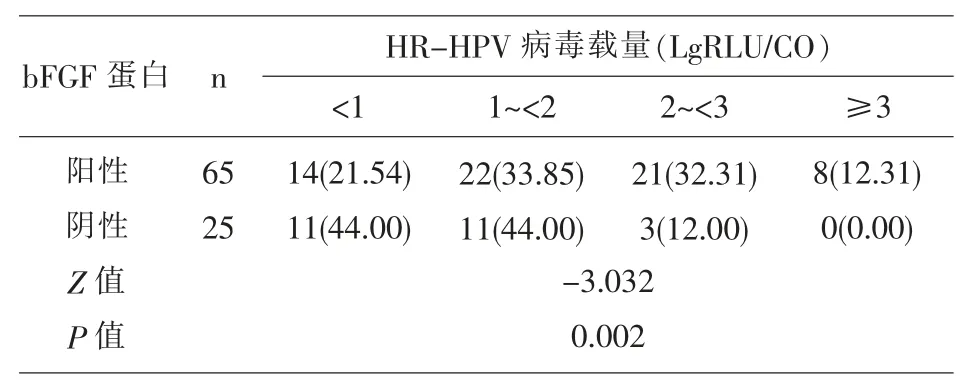
表3 宮頸癌組織中的bFGF 蛋白陽性表達率與HR-HPV 病毒載量的關系
高危型HPV 病毒特別是HPV16、HPV18 病毒感染,能顯著促進宮頸柱狀上皮細胞異常分裂,在E6/E7 蛋白高度整合宿主細胞的過程中, 高危型HPV 感染導致的宮頸癌發病率持續上升[6]。臨床上宮頸癌患者的中晚期階段病情進展速度較快,遠期帶瘤生存時間較短,宮頸癌復發轉移的風險較高[7,8]。現階段缺乏對宮頸癌綜合性病情評估的可靠指標,雖然鱗狀上皮細胞抗原能發揮一定作用,但評估宮頸癌臨床病理特征的滿意度仍然較低[9,10]。本次研究通過對宮頸癌患者病灶組織中bFGF 蛋白的表達進行分析研究,不僅能深入揭示宮頸癌發生發展的可能機制,而且還能為宮頸癌臨床病理特征或者綜合性病情評估提供依據。
bFGF 蛋白主要表達于間質組織、胚胎組織及未分化成熟組織中,在炎癥、損傷修復或者惡性腫瘤患者中,由于機體反饋性調節系統的激活,bFGF蛋白的表達濃度均可顯著上升。bFGF 蛋白對上皮細胞增殖狀態的誘導作用能提高上皮細胞的擴增風險,抑制早期癌細胞的凋亡。部分學者的研究認為bFGF 蛋白的高表達能夠促進卵巢癌或者子宮內膜癌的發生[11],但關于其與宮頸癌臨床病理特征的關系研究較少,同時未能深入揭示bFGF 蛋白與HR-HPV 的關系。
本研究免疫組化結果提示,宮頸癌組織中bFG F 蛋白陽性表達率明顯高于癌旁組織。bFGF 蛋白的高表達主要在腫瘤生物學特征惡化、腫瘤信號通路激活或者癌基因損傷修復方面發揮作用,進而持續維持癌細胞的增殖轉錄過程。有研究發現,在宮頸癌組織中,bFGF 蛋白陽性表達率可超過65%,而在有明顯的宮旁組織或盆腔淋巴結轉移的患者中,bFGF 蛋白陽性表達率可進一步升高[12,13],提示bFGF 蛋白陽性表達能顯著加劇宮頸癌進展。分析原因可能與bFGF 蛋白高表達能提高腫瘤細胞浸潤范圍,促進其對陰道壁或宮旁組織的侵襲,最終促進宮頸癌進展有關;而bFGF 蛋白對淋巴結轉移的影響, 主要在于其能提高淋巴結內皮黏附分子snail 的激活程度,而最終促進淋巴結轉移的發生。而本研究結果顯示,bFGF 蛋白表達并不會影響癌細胞的分化過程。
宮頸癌組織bFGF 蛋白陽性表達的患者中,HR-HPV 病毒載量較高,表明宮頸癌患者HR-HPV病毒載量可能影響bFGF 蛋白的表達。而以往研究認為,HPV E6 蛋白是HR-HPV 的主要轉化蛋白,主要通過使P53 泛素化分解而使其失去對細胞生長的負調節作用,最終引起細胞過度增生并向惡性轉化[14-16]。HR-HPV 可能就是通過P53 調節通路上調bFGF 蛋白表達,而顯著加劇病毒顆粒基因對于宮頸細胞的整合程度,進而導致宮頸上皮細胞的癌變過程, 這也可能是HR-HPV 導致宮頸癌發生發展的機制之一[17], 但仍有待進一步的研究予以證實。
綜上所述,bFGF 蛋白在宮頸癌組織中呈高表達,與FIGO 分期、淋巴結轉移情況密切相關,HRHPV 可能通過上調bFGF 蛋白表達而促進宮頸癌的發生發展。

