Ⅱ型排卵障礙患者不同助孕治療的妊娠結局分析
關少艮,馮月枝,黃永漢
(佛山市第一人民醫院生殖醫學中心,佛山 528031)
據世界衛生組織(WHO)統計,已婚夫婦中有約8%~12%為不育夫婦[1]。排卵障礙性不孕癥(ovulatory disorder infertility,ODI)是一種涉及多種原因的常見病癥,主要表現為卵泡發育、卵母細胞成熟和排卵功能多方面異常,是引發不孕癥的重要原因之一,占不孕癥的25%~30%[2]。排卵障礙多采用WHO的分類方法[3],主要分為3種類型:Ⅰ型,下丘腦和(或)垂體功能減退所致,表現為閉經、低促性腺激素(Gn)和低雌激素;Ⅱ型,下丘腦-垂體-卵巢軸(HPO軸)功能失調引起,表現為稀發或無排卵月經、Gn及雌激素水平正常或LH/FSH失調;Ⅲ型,下丘腦和垂體功能正常,表現為高Gn及低雌激素水平,與高齡、卵巢儲備功能下降有關。本研究回顧性分析2019年1~12月期間在佛山市第一人民醫院生殖醫學中心就診的244例Ⅱ型排卵障礙患者的臨床資料(共432個促排卵治療周期),以探討各種因素對Ⅱ型排卵障礙性不孕患者妊娠結局的影響。
資料與方法
一、研究對象
研究對象為2019年1~12月期間在佛山市第一人民醫院生殖醫學中心診斷為Ⅱ型排卵障礙的患者。
納入標準:診斷為Ⅱ型排卵障礙;多囊卵巢綜合征(PCOS)患者和非PCOS患者,PCOS的診斷符合2003年鹿特丹的診斷標準;促排卵前均經過短效口服避孕藥或加上二甲雙胍治療2~3個月;年齡20~35歲;經腹腔鏡或子宮輸卵管造影術顯示至少一側輸卵管通暢;男方精液常規正常或標準符合宮腔內人工授精(IUI)條件。
排除標準:子宮內膜異位癥、子宮腺肌癥或子宮肌瘤致宮腔變形患者;合并宮腔病變,如子宮畸形、宮腔粘連、子宮內膜息肉未處理者;患有其他未控制的內分泌疾病或內外科疾病。
共納入244人次,促排卵治療共432個周期,按照是否為PCOS患者分為PCOS組(283個周期)和非PCOS組(149個周期)。其中,PCOS組又分為IUI組(143個周期)和單純促排卵治療組(非IUI組,140個周期),非PCOS組均行IUI治療(149個周期)。
二、診療回顧
1.促排卵方法:月經周期第3~5天或者撤藥性出血第3~5天開始口服枸櫞酸氯米芬片(高特制藥,塞浦路斯)50 mg qd或來曲唑(LE,浙江海正藥業)2.5 mg qd或他莫昔芬(TMX,江蘇揚子江藥業)10 mg bid。上述用藥5 d后均行陰道B超監測。若未見優勢卵泡,添加Gn[包括尿促性素(HMG,寧波人健藥業)或者尿促卵泡素(FSH,珠海麗珠制藥)37.5~75 U/d進一步促進卵泡發育,并根據卵泡發育情況調整用藥劑量,直至HCG日。或者月經周期第3~5天/撤藥性出血第3~5天開始肌肉注射HMG或者FSH 37.5~150 U/d,連用5 d后行陰道B超監測,根據卵泡發育情況調整用藥方案或劑量,直至HCG日。根據用藥情況的不同,分為3組:口服藥物組(111個周期)、注射Gn組(205個周期)和聯合藥物組(116個周期)。
2.助孕方式:當B超監測優勢卵泡直徑達16~18 mm時,結合性激素水平[LH、E2、孕酮(P)],注射HCG(珠海麗珠制藥)10 000 U或促性腺激素釋放激素激動劑(GnRH-a,達必佳,輝凌,瑞士)0.1 mg誘發排卵(卵泡數≤2個,肌肉注射HCG 5 000~10 000 U;卵泡數≥3個,皮下注射達必佳0.2 mg);IUI組于24 h后行IUI,非IUI組指導患者次日同房。
3.黃體支持及臨床結局隨訪:HCG日2 d后回院復查B超確認排卵后開始口服地屈孕酮(達芙通,雅培,荷蘭)10 mg bid。14 d后自行驗尿試紙或血HCG檢測,HCG陽性者5周后行B超檢查,見宮腔內有明確孕囊或胎心博動者確診為臨床妊娠;未見明確孕囊而妊娠丟失為生化妊娠。早期流產是指發生在妊娠12周以前的臨床妊娠丟失。
三、觀察指標
比較各組患者的一般資料,包括年齡、不孕年限、體重指數(BMI)、基礎內分泌指標;促排卵治療資料,包括HCG日內分泌指標、HCG日優勢卵泡數(≥14 mm)、子宮內膜厚度及Gn使用總量;妊娠結局,包括臨床妊娠率、生化妊娠率、早期流產率、多胎妊娠和異位妊娠發生率等。
四、統計學方法

結 果
一、總體治療結局
本研究共納入432個促排卵周期。女方年齡20~35歲。
1.患者類型(PCOS及非PCOS)比較:在PCOS組中,IUI和非IUI組的BMI、抗苗勒管激素(AMH)、基礎激素水平、HCG日激素水平、HCG日內膜厚度及HCG日優勢卵泡數等比較均無顯著性差異(P>0.05);IUI組的女方年齡、不孕年限及Gn總量均顯著大于非IUI組(P<0.05),IUI組的繼發不孕比例顯著高于非IUI組(P<0.05);兩亞組間的臨床妊娠率、生化妊娠率、早期流產率、異位妊娠率及多胎率比較均無顯著性差異(P>0.05)(表1)。

表1 各組患者臨床資料及妊娠結局比較[(-±s),%]
非PCOS組患者只行IUI治療。
2.助孕類型(IUI及非IUI)比較:IUI治療方案中,PCOS組的女方年齡、基礎FSH及HCG日子宮內膜厚度均顯著小于非PCOS組(P<0.05);PCOS組的BMI、AMH、基礎LH、基礎T、HCG日E2水平、HCG日優勢卵泡數、Gn總量及臨床妊娠率均顯著高于非PCOS組(P<0.05)。IUI治療方案中PCOS與非PCOS組間的不孕年限、不孕類型、生化妊娠率、早期流產率、異位妊娠率及多胎率比較均無顯著性差異(P>0.05)(表1)。
二、不同促排卵方案妊娠結局的比較
納入的432個促排卵周期中,口服藥物組、聯合藥物組和注射Gn組分別是111、116和205個周期,其臨床妊娠率分別為15.3%、22.4%和17.6%,聯合藥物組的臨床妊娠率最高,而口服藥物組的臨床妊娠率最低,但各組臨床妊娠率的比較尚無顯著性差異(χ2=2.050,P=0.359);3組早期流產率分別為11.8%、11.5%和13.9%,各組比較亦無顯著性差異(χ2=0.153,P=0.962)(表2)。
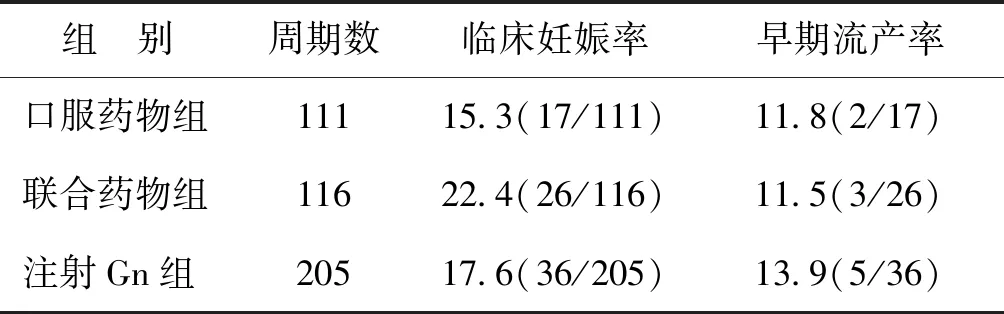
表2 不同促排卵方案組妊娠結局的比較(%)
三、女方因素對排卵障礙患者妊娠結局的影響分析
在多因素Logistic回歸分析中,把女方年齡、女方BMI、不孕年限、基礎FSH、基礎LH、基礎T、AMH、不孕類型、患者類型、促排卵方案、HCG日子宮內膜厚度、HCG日E2及P水平、HCG日優勢卵泡數及Gn總量等女方因素納入方程,分析發現患者類型(P=0.016)及HCG日子宮內膜厚度(P=0.004)是臨床妊娠結局的影響因素(表3)。

表3 Ⅱ型排卵障礙患者妊娠結局影響變量的多因素Logistic回歸分析
討 論
Ⅱ型排卵障礙屬于Gn水平正常的排卵障礙類型,約占排卵障礙的70%~85%,多見于PCOS、體重異常,以及部分甲狀腺、腎上腺功能異常等疾病。排卵障礙是不孕門診常見的不孕類型,誘導排卵是其主要的治療方式,也是基層醫院可以通過單純促排卵治療即能獲得理想妊娠結局的不孕癥類型。臨床上較少對Ⅱ型排卵障礙進行單獨的研究和討論,故本研究搜集Ⅱ型排卵障礙患者的臨床數據進行分析,討論不同的促排卵方案和助孕治療方案下,其妊娠結局及影響因素,以期指導臨床工作。
一、Ⅱ型排卵障礙患者的妊娠結局
PCOS是最常見的婦科內分泌疾病之一[4],是排卵障礙性不孕癥的主要原因。在臨床上以雄激素過高的臨床或生化表現、持續無排卵、卵巢多囊改變為特征,常伴有胰島素抵抗和肥胖。PCOS患者具有較高的卵巢儲備,臨床和實驗研究也表明PCOS患者的初始卵泡募集較正常人亢進,其基礎竇卵泡計數(AFC)及血清AMH水平明顯高于正常人群,PCOS患者的絕經年齡也比正常對照組延遲2年[5]。關于PCOS患者的妊娠結局觀點不一,部分研究者認為PCOS患者的內分泌異常可影響卵母細胞成熟及胚胎發育潛能,導致臨床妊娠率低而流產率高;但Sigala等[6]的前瞻性研究發現,行ICSI助孕時,PCOS組的平均獲卵數、MⅡ卵泡數目、胚胎數目較正常卵巢對照組高,但MⅡ卵比例、正常形態卵母細胞比例、D3優胚數及著床率、臨床妊娠率在兩組間差異無統計學意義。本研究將Ⅱ型排卵障礙分為PCOS組和非PCOS組,發現PCOS組中的基礎內分泌指標與非PCOS組比較差異有統計學意義,反映了PCOS患者的內分泌特征。但進行人工授精助孕治療時,PCOS組的臨床妊娠率顯著高于非PCOS組;多因素回歸分析中以PCOS患者為參照,非PCOS患者妊娠結局的調整OR值為0.225(P=0.016)。有研究結果提示PCOS患者有較強的生育潛能,雖然存在內分泌異常,但經過系統的內分泌治療及體重管理后能得到較理想的臨床妊娠率[7]。
二、人工授精的助孕效果
IUI是不孕癥簡單且有效的治療手段[8]。早在2005年,就有學者認為IUI能增加排卵障礙性不孕癥的妊娠率[9]。Atalay等[10]比較克羅米芬促排卵治療的PCOS患者行IUI與指導同房的妊娠結局,結果提示IUI組較指導同房組的妊娠率明顯升高,原因在于IUI組精子經過優化處理,直接放進宮腔,增加活動精子的濃度以提高受精幾率,且減少了宮頸因素的影響,提高了臨床妊娠率。本研究中PCOS患者IUI組的女方年齡、不孕年限及Gn總量均顯著高于非IUI組,且IUI組繼發不孕的比例顯著高于非IUI組,這與進行IUI助孕治療的患者選擇有關,通常年齡較大、不孕年限較長的患者更容易接受IUI治療。然而兩組間臨床妊娠結局包括臨床妊娠率、生化妊娠率及早期流產率等比較均無顯著性差異(P>0.05),提示單純門診促排卵治療也能獲得比較理想的臨床妊娠結局,尤其是年輕、不孕年限較短及原發不孕的患者,可以先在門診予以常規促排卵治療;但如果不孕年限較長,尤其超過2年者可能合并其他心理和生理方面的因素,則可考慮行IUI助孕治療以提高妊娠率。
三、促排卵方案對妊娠結局的影響
誘導排卵(ovulation induction,OI)指對排卵障礙患者應用藥物或手術方法誘發排卵,一般以誘導單卵泡或少數卵泡發育為目的,是治療排卵障礙患者的最主要方法[11]。目前常用的促排卵藥物包括克羅米芬(CC)、LE及Gn類。口服促排卵藥是通過解除對下丘腦-垂體的負反饋作用,促使體內的Gn分泌,進而促進卵泡的發育。LE是一種芳香化酶抑制劑,相對于CC,不影響子宮內膜容受性,能提高臨床妊娠率,已經成為PCOS促排卵治療的一線藥物[12]。Gn種類有尿源性Gn(uHMG、uFSH和uHCG) 和基因重組Gn(r-FSH、r-LH和r-HCG)兩大類,用于口服促排卵藥物效果不佳或中樞性排卵障礙患者。本研究結果顯示不同促排卵方案各組的臨床妊娠率比較無顯著性差異,但可以看到聯合藥物組的臨床妊娠率相對最高(22.4%),而口服藥物組相對最低(15.3%),與既往的研究結果[13-14]一致。排卵障礙患者尤其是PCOS患者,在促排卵過程中Gn劑量不太容易控制,易發生多個卵泡發育甚至卵巢過度刺激的風險,可先予口服小劑量促排卵藥物,增加卵巢對Gn的敏感性,當卵泡發育較慢時,加用Gn聯合促進卵泡發育,發育的優勢卵泡分泌內源性的雌激素促進子宮內膜的生長,不僅能提高子宮內膜容受性,還能減少Gn的用量,達到單卵泡發育的目的,降低多胎妊娠率。
四、子宮內膜容受性對妊娠結局的影響
子宮內膜容受性是指子宮內膜允許胚胎粘附、侵入的能力,是胚胎著床的必要條件。目前,多數生殖中心都是應用陰道超聲來觀察和測量子宮內膜的厚度和類型來評估子宮內膜容受性。近年來多數研究都認為子宮內膜厚度為8~13 mm者臨床妊娠率較高[15],也有研究表明內膜厚度的上限仍無定論,內膜厚度與妊娠率呈正相關[16]。本研究經多因素回歸分析得出HCG日子宮內膜厚度對于妊娠結局的調整OR值是1.284(P=0.004),是排卵障礙患者臨床妊娠的獨立影響因子,與倪麗莉等[17]的研究結果一致。影響子宮內膜厚度的因素有很多,包括藥物(如抗雌激素類藥物CC)、感染(如子宮內膜炎)及損傷(多次人流術后)等,在不孕癥的診治中臨床醫生應該對患者的病史做詳細詢問并完善檢查,排除各種潛在的影響因素,以改善子宮內膜的容受性,提高臨床妊娠率。
此外,在本研究中各組的生化妊娠率和早期流產率比較均無顯著性差異,考慮納入研究的患者比較年輕,均低于35歲,且均為單純Ⅱ型排卵障礙患者有關,即排除了不良孕產史及內外科疾病這些不良因素的影響;PCOS患者促排卵前均予短效口服避孕藥或加用二甲雙胍治療,并強調進行體重管理。結果表明,PCOS患者即使基礎內分泌水平異常,經過調整代謝及內分泌水平后,并沒有增加流產的發生率。但本研究的納入周期數較少,研究結論可能存在一些偏倚,后期尚需要更大樣本量的研究進一步證實。
綜上所述,排卵障礙性不孕癥的主要治療方法是誘導排卵,PCOS患者經過促排卵治療可獲得較理想的臨床妊娠率;對于年齡較大、不孕年限較長的患者建議行人工授精助孕治療;治療過程中必須詳細詢問病史,排除各種不良影響因素,使用適當的促排卵方案,以爭取更好的臨床結局,并降低患者經濟負擔及減少并發癥的發生。本研究的不足主要是樣本量較小,后期仍需要多中心、更大樣本量的隨機對照研究,并著重關注對子代的隨訪及健康問題。

