先天性心臟病合并肺動脈高壓患兒行根治術后的預后影響因素分析
王曉紅,史少娟,劉 學,楊 華
0 引 言
先天性心臟病為先天畸形的最常見類型,由于其存在心內或大動脈水平的非限制性左向右分離,可增加肺血流量,導致肺動脈高壓[1]。肺動脈高壓以肺血管收縮、重構及原位血栓形成、右心后負荷增加為主要表現,又可繼發肺血管內皮損傷,導致系列病理學變化,為具有潛在破壞力、嚴重的慢性心肺血管疾病,其致殘率及病死率極高[2]。臨床對于先天性心臟病合并肺動脈高壓的早期診治有重要作用。目前先天性心臟病合并肺動脈高壓無法自行愈合,需通過手術根治,臨床研究報道[3-4],動力性肺動脈是因肺動脈內血流量增大所致,手術矯正畸形后能夠恢復正常。但手術治療有一定創傷,術后恢復時間較長,部分患兒可能發生心腔、胸腔積液,心律失常等并發癥。Kruszka等[5]研究表明,近年來先天性心臟病合并肺動脈高壓的治療表現為低齡、低體重及復雜型發展。因此有關先天性心臟病合并肺動脈高壓患兒術后預后的分析為目前研究的重點。本研究主要分析先天性心臟病合并肺動脈高壓患兒術后預后的影響因素,探討相關因素和臨床結局的關系,為臨床預后評估提供參考依據。
1 資料與方法
1.1 一般資料回顧性分析我院2013年3月至2019年1月收治的127例先天性心臟病合并肺動脈高壓患兒臨床資料。納入標準:經體格檢查、心血管造影或超聲心動圖確診為先天性心臟病;患兒在靜息狀態下經右心導管檢查提示肺血管阻力>3 WU,肺毛細血管嵌壓≤15 mmHg(1 mmHg=0.133 kPa),平均肺動脈壓>25 mmHg;均于全身麻醉+體外循環下進行一次性根治手術治療[6]。排除標準:復雜性先天性心臟病;特發性肺動脈高壓,其他疾病所致肺動脈高壓;出血傾向;靜息發紺;左室或右室流出道梗阻;肺動脈瓣狹窄。127例患兒中男69例,女58例;年齡3個月~3歲,平均(1.57±0.22)歲;體重5~14 kg,平均(8.97±1.23)kg;肺動脈壓40~78 mmHg,平均(54.19±6.93)mmHg;體外循環時間35~140 min,平均(54.17±6.33)min;主動脈阻斷時間20~65 min,平均(41.33±5.81)min。先天性心臟病類型:房間隔缺損107例,房間隔缺損合并室間隔缺損9例,其他11例;心功能分級:Ⅱ級78例、Ⅲ級49例。
1.2 資料收集收集患兒術前臨床資料,包含年齡、體重、先天性心臟病類型、肺動脈高壓分級、心功能分級、營養分級、肺動脈高壓危象、手術時間、機械通氣時間、Tei指數、腦鈉肽(BNP)、高敏肌鈣蛋白T(hsTnT)及C反應蛋白(CRP)等資料。
1.3 近期隨訪情況所有先天性心臟病合并肺動脈高壓患兒于入組時均以電話、門診定期復查等方式進行6個月隨訪,明確患兒隨訪期間的生存情況。患兒死于先天性心臟病合并肺動脈高壓相關為終點事件,死于其他疾病、失訪或者隨訪結束時仍存活為截尾數據。

2 結 果
2.1 先天性心臟病合并肺動脈高壓患兒術后預后情況分析127例先天性心臟病合并肺動脈高壓患兒經手術治療后114例存活(存活組),13例死亡(死亡組),其中肺動脈高壓危象4例,右心衰竭5例,大咯血呼吸困難2例,低心排綜合征2例,無患兒死于與先天性心臟病合并肺動脈高壓無關的其他疾病。
2.2 先天性心臟病合并肺動脈高壓患兒不同預后組的臨床資料比較存活組和死亡組性別、先天性心臟病類型、營養分級比較差異無統計學意義(P>0.05);存活組和死亡組年齡、體重、肺動脈高壓分級重度率、心功能分級Ⅲ 級率、肺動脈高壓危象率、手術時間、機械通氣時間、Tei指數、BNP、hsTnT、CRP比較差異均有統計學意義(P<0.05)。見表1。
2.3 先天性心臟病合并肺動脈高壓患兒術后預后危險因素分析以隨訪結束時患兒是否死亡作為因變量,將年齡、體重、肺動脈高壓分級、心功能分級、肺動脈高壓危象、手術時間、機械通氣時間、Tei指數、BNP、hsTnT、CRP作為比較有統計學差異的指標作為自變量納入COX比例風險回歸模型,結果顯示,肺動脈高壓分級、心功能分級、肺動脈高壓危象、手術時間、機械通氣時間、Tei指數、BNP、hsTnT、CRP是影響患兒預后的危險因素(P<0.05),見表2。
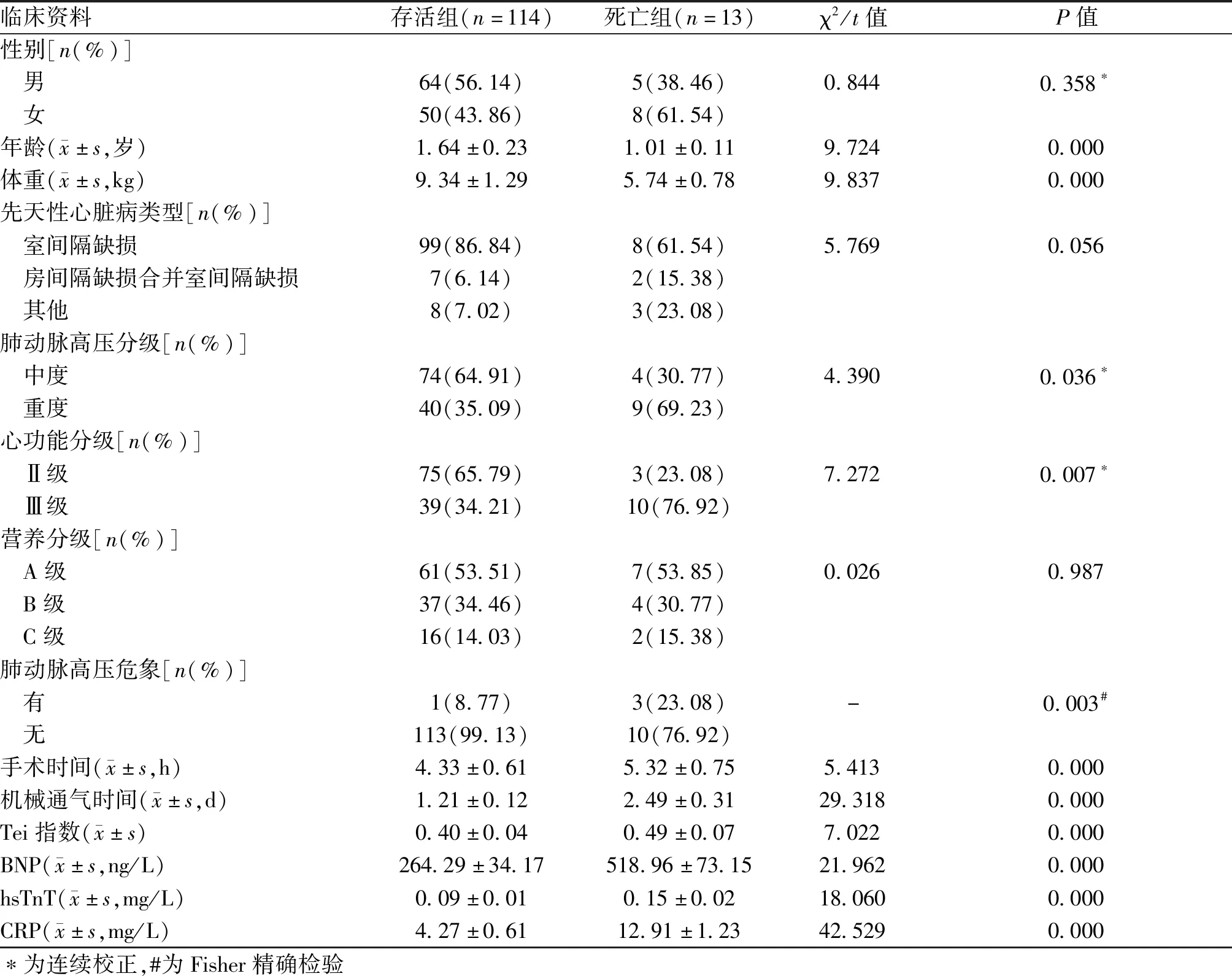
表1 先天性心臟病合并肺動脈高壓患兒不同預后組的臨床資料比較
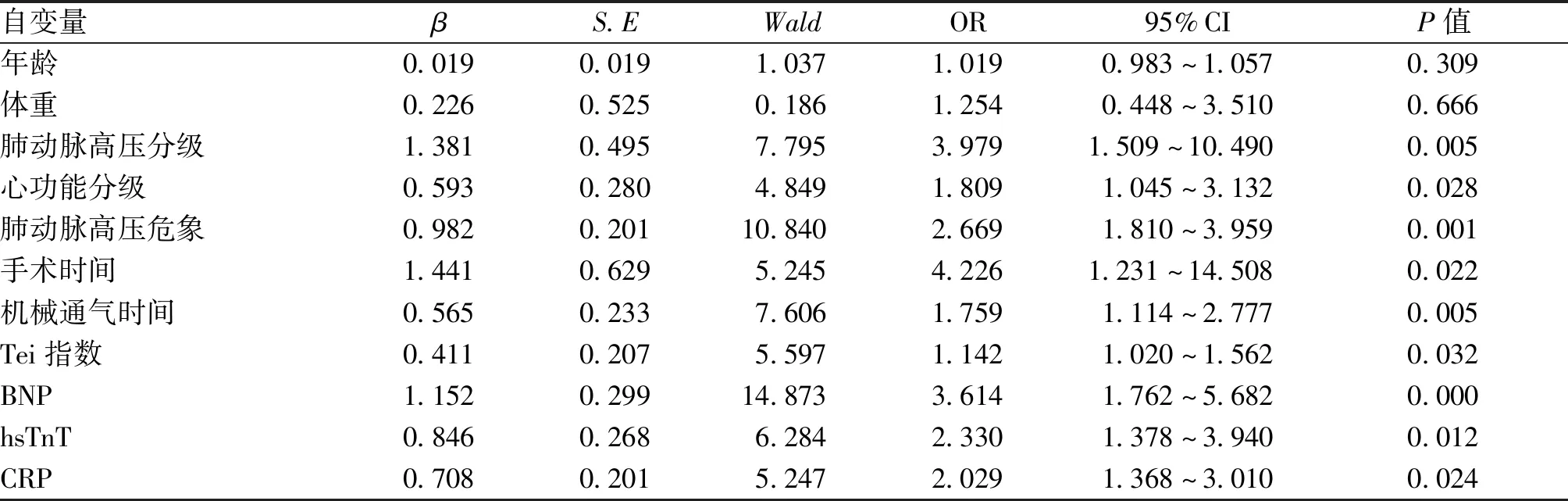
表2 先天性心臟病合并肺動脈高壓患兒術后預后危險因素分析
3 討 論
先天性心臟病為小兒最常見的心臟病,是目前導致嬰幼兒死亡的首要原因,嚴重影響患兒的生命安全[7]。相關研究報道,先天性心臟病能夠引起多種并發癥,其中肺動脈高血壓為其嚴重并發癥之一,左心室和主動脈壓力能夠通過異常通道傳入右心室及肺動脈壓力,導致肺動脈高壓[8-9]。另外肺小血管壁較薄,具有一定彈性,肺循環血流量明顯增加時能夠增加肺動脈壓力。調查研究報道,約有30%先天性心臟病患兒合并肺動脈高壓,主要表現為肺血管阻力的加大及肺動脈壓力的持續性增加,導致有心衰竭,甚至死亡[10]。外科手術是先天性心臟病合并肺動脈高壓患兒的唯一有效治療手段,盡管近年來先天性心臟病合并肺動脈高壓的手術治療不斷成熟,術后監護也相應完善,但仍有部分患兒術后預后不理想[11]。有關先天性心臟病合并肺動脈高壓患兒手術治療效果的影響因素較多,目前缺乏大規模的調查報道。
低年齡的嬰幼兒呼吸調節中樞系統發育尚不完全,胸廓軟小,力量較弱,呼吸頻率低,肺泡和小氣道容易破裂,導致氣道梗死塞,加重肺部損傷[12]。低年齡、低體重的嬰幼兒手術難度相對較大,術中體外循環輔助時間和心律恢復時間較長,容易發生血壓不穩。本研究結果顯示,存活組年齡、體重相對較多,但經COX回歸分析顯示,低年齡、低體重不是影響患兒術后預后的危險因素。
左向右分流型先天性心臟病中異常的血流可增加肺血流,導致充血性肺動脈高壓,異常的血流動力學又可導致血管重建,于血流剪切力作用下引起內皮細胞受損,使肺動脈高壓轉變為梗阻型[13]。隨著肺小動脈中層的增厚、壞死樣變化,肺動脈病變進展至不可逆階段,難以通過手術降低肺動脈壓力,改善右心功能,且可加重右心負荷,引起右心功能衰竭。既往有研究報道,先天性心臟病合并重度肺動脈高壓者術后病死率≥10%[14]。本研究數據顯示,肺動脈高壓分級是影響此類患兒術后預后的危險因素之一。另外本研究結果發現,術前心功能分級也是影響患兒術后預后的危險因素。
肺動脈高壓危象為肺動脈高壓的嚴重臨床綜合征,以肺動脈壓力急劇上升且伴體動脈壓下級極嚴重低氧為主要表現,其病情兇險,合并急性心肺功能衰竭,未經及時處理者容易導致死亡[15-16]。本研究存活組肺動脈高壓危象發生率相對較低,是導致術后患兒死亡的主要危象因素。另外本研究結果顯示,存活組手術時間較死亡組少,經COX回歸分析發現,手術時間是影響先天性心臟病合并肺動脈高壓患兒術后預后的獨立危險因素,提示縮短手術時間對于患兒預后改善有積極作用。手術時間對預后的影響為多個因素的綜合,手術時間的延長相應增加體外循環時間,體外循環技術是心臟外科的輔助手段,能使術中全身血液經多種通道全身泵血,且可吸引回收術中出血,注入驅動停搏液,為手術進行提供基本條件及技術支持,但體外循環時間過長可能導致肺部損傷[17]。一方面血液從體內經過外界體外循環回收至體內期間,血液成分可受到外界因素的影響,激活補體系統,此外白細胞表層黏附因子表達上調能夠導致肺組織受損[18]。另一方面手術期間血液通過上下腔靜脈管道引出體外,導致心臟右心無法經肺動脈為肺臟供血,導致肺部缺血,右心管道拔除后導致肺臟和肺部血管充盈大量血液,引起肺部再灌注損傷,損傷肺功能,不利于術后患兒的恢復[19]。持續機械通氣時間為基本嚴重程度的標志,大部分患兒術后機械通氣時間為24 h內,>48 h提示預后較差,在PICU的觀察時間越長[20]。Alrddadi等[21]研究也表明,機械通氣時間越長,術后患兒發生不良預后事件的風險越高。本研究顯示,死亡組機械通氣時間較存活組長。
Tei指數是評價心臟收縮及舒張整體觀念的指標,具有可靠、測量簡便、不受心肌幾何形狀等因素影響的特點,近年來已用于先天性心臟病兒童右心室功能的評估。相關研究發現,隨著三尖瓣反流程度的加重及肺動脈壓力的上升導致右室功能不全加重,引起Tei指數明顯上升[22]。本研究數據顯示,Tei指數也是影響患兒預后的危險因素。
目前先天性心臟病合并肺動脈高壓尚缺乏有效的指導治療的標志物,BNP主要來自于心室肌細胞,BNP具有強大的利水、利鈉、擴血管等作用,其合成及分泌受到容量負荷及心室壓力負荷調節的影響[23]。BNP和肺動脈高壓的相關性已有研究報道,肺動脈高壓可增加右室壓力,從而刺激BNP分泌。楊雨航等[24]研究表明,BNP能夠反映左向右分流型先天性心臟病患者的心功能情況,隨著肺動脈壓力增加其水平相應上升,可作為病情嚴重程度的評價指標。先天性心臟病合并肺動脈高壓能夠導致右心室功能衰竭,擴大右心室,壓迫冠狀動脈,降低心輸出量,加快心率代償性,引起心肌缺血、受損,導致hsTnT上升[25]。CRP是反映機體組織損傷和低水平炎癥程度的敏感指標,既往研究認為[26],CRP作為血管炎癥指標在心腦血管疾病發生中有重要作用。最近研究報道,CRP可作為先天性心臟病合并肺動脈高壓的危險分層指標[27]。本研究結果顯示,存活組BNP、hsTnT及CRP水平相對較低,COX回歸分析顯示,BNP、hsTnT及CRP均是影響患兒術后預后的危險因素。
綜上所述,先天性心臟病合并肺動脈高壓患兒術后預后和多種因素相關,通過對相關因素的干預可能對預后改善有一定作用。

