尼可地爾對缺血性心力衰竭大鼠心功能的保護作用及機制
邢曉娜, 劉利君, 何元軍
(四川省廣元市中心醫院 心臟血管中心, 四川 廣元, 628017)
尼可地爾是具有硝酸鹽性質的ATP敏感性鉀離子通道開放劑,適用于各類型心絞痛[1], 能顯著降低心血管事件的發生風險,可對心臟病患者的心臟起保護作用[2]。研究[3]認為,尼可地爾可減少冠心病患者心臟重構的發生發展,降低缺血性心力衰竭患者的死亡率[4]。心室重構是指各種損傷使心臟原來存在的物質和心臟形態學發生變化,是機體的一種適應性反應,也是病變修復和心室整體代償繼發的病理生理反應過程[5]。但是,關于尼可地爾是否能抑制缺血性心力衰竭的左室重構及其機制尚未明確。本研究探討尼可地爾對缺血性心力衰竭大鼠心功能和左室重構的影響和機制,現報告如下。
1 資料與方法
1.1 實驗動物
40只雄性SD大鼠,體質量160~200 g, 購于中國食品藥品檢定研究院[(生產許可證號: SCXK(京)2019-0017)]。尼可地爾購于長春大政藥業科技有限公司(國藥準字H22024008)。將40只大鼠隨機分為4組,每組10只。① 空白對照組(Con組): 不進行任何手術干預,僅給予等體積、等時間生理鹽水灌胃。② 尼可地爾組(NIC組): 麻醉滿意后,采用Johns法建立大鼠缺血性心力衰竭模型。麻醉大鼠后,打開胸腔,在無菌手術條件下分離心包,然后抬起左耳廓,心臟被擠出。在大約1/3的下端結扎左冠狀動脈前降支。從尾部記錄每只大鼠的收縮壓、舒張壓和心率,對每個參數進行3次測量。術后3 d至8周末,給予尼可地爾3 mg/kg·d灌胃。③ 生理鹽水組(NS組): 手術方式同NIC組,但給予等體積、等時間生理鹽水灌胃。④ 假手術組(Sham組): 在不結扎冠狀動脈的情況下行開胸手術,灌胃生理鹽水。術后8周對各項指標進行評估,記錄體重、呼吸模式、活動量和毛色。
1.2 超聲心動圖
術后8周所有大鼠均行超聲心動圖檢查。麻醉滿意后,仰臥位固定,胸部備皮,測量室間隔收縮末期厚度(IVSS)、室間隔舒張末期厚度(IVSd)、左室收縮末期內徑(LVIDs)、左室舒張末期內徑(LVIDd)、左室收縮末期后壁厚度(LVPWs)和左室舒張末期后壁厚度(LVPWd)。用Teichholtz方程計算左心室射血分數(LVEF)和左心室短軸收縮分數(LVFS),并計算左心室舒張末期容積(LVEDV)和左心室收縮末期容積(LVESV)。大鼠手術后LVEF均低于50%, 提示心力衰竭。
1.3 左心室重量和肺重的測定
實驗結束后,測量心臟和左心室重量,計算左心室/體重比值(LVW/BW), 評價左心室肥厚程度。取肺稱重,計算肺臟重量指數(LUNGW/BW)作為充血指標。
1.4 組織病理學檢查
處死大鼠后,提取左心室前壁組織。部分組織在液氮中快速冷凍,然后保存在-80 ℃以備分析。甲醛固定和石蠟包埋,切成4 μm的切片,烤片,冷卻后低溫凍存。經二甲苯脫蠟,乙醇梯度水化。蘇木精染色30~60 s, 沖洗5 min, 伊紅染色30 s, 沖洗5 min; 乙醇梯度脫水,干燥,二甲苯透明,中性樹膠封固,晾干,光學顯微鏡下觀察。其余組織采用戊二醛-鋨酸雙重固定,脫水,使用前置于-80 ℃中保存。在電鏡下進行心肌超微結構觀察。
1.5 Western blot檢測
在組織裂解緩沖液中提取蛋白并測定蛋白濃度。從每個樣品中分離等量的蛋白質(40 μg), 并將其電轉移到PVDF膜上。5%的BSA封閉,與一抗在4 ℃孵育過夜。洗膜3次后,將膜與HRP偶聯二抗孵育。使用標準ECL檢測條帶,并使用Image J軟件通過密度分析進行定量。
1.6 統計學分析
2 結 果
2.1 尼可地爾改善缺血性心力衰竭大鼠的一般情況
NS組大鼠除了呼吸急促甚至喘息外,還表現出活動減少和神經松解,體重減輕,毛發顏色暗淡。NIC組大鼠的活動量、體重和整體健康狀況明顯好于NS組。術后8周, Con組、Sham組、NS組、NIC組體重分別為(486.70±29.30)g、(478.40±28.30)g、(369.85±47.26)g、(426.85±51.22)g, NS組體重最低, NIC組次之。
2.2 尼可地爾對缺血性心力衰竭大鼠的降壓作用
術后8周末, NIC組收縮壓和和舒張壓分別為(126.3±6.9)mmHg、(94.0±6.2)mmHg, 均明顯低于NS組的(141.7±10.1)mmHg、(103.1±5.9)mmHg的和Sham組的(159.6±11.3)mmHg、(113.1±8.5)mmHg, 差異有統計學意義(P<0.05)。NS組收縮壓(141.7±10.1)mmHg明顯低于Sham組(159.6±11.3)mmHg和Con組(150.8±10.2)mmHg, 差異有統計學意義(P<0.05)。Sham組舒張壓(113.1±8.5)mmHg與NS組(103.1±5.9)mmHg相比,差異無統計學意義(P>0.05)。
2.3 尼可地爾改善缺血性心力衰竭大鼠的心功能
與Con組及Sham組相比, NS組及NIC組LVEF、E/A均降低,且NS組LVEF低于NIC組,差異有統計學意義(P<0.05)。LVEDV則呈相反趨勢,3組間存在差異, NS組LVEDV最高,差異有統計學意義(P<0.05)。NS組LVESV、LVIDd和LVIDs高于NIC組和Sham組,差異有統計學意義(P<0.05)。NIC組和Sham組之間相關指標水平比較,差異無統計學意義(P>0.05)。各組大鼠的IVSd水平比較,差異無統計學意義(P>0.05)。見表1、圖1。
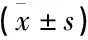
表1 各組大鼠超聲心動圖指標水平比較

A: Sham組; B: NS組; C: NIC組
2.4 尼可地爾對缺血性心力衰竭大鼠左心室肥厚、纖維化和肺充血的影響
HE染色及電鏡下觀察結果均顯示, Sham組大鼠心肌細胞排列規則,橫紋清晰; NS組心肌細胞排列紊亂,形狀不規則,還表現出明顯的纖維組織增生。與NS組相比, NIC組的這些異常明顯減弱,心肌纖維結構趨于正常。Sham組和NIC組LVW/BW和LUNGW/BW均明顯低于NS組,差異有統計學意義(P<0.05)。見表2、圖2。

表2 各組大鼠LVW/BW和LUNGW/BW比較

A、E: Con組; B、F: Sham組; C、G: NS組; D、H: NIC組。
2.5 尼可地爾對大鼠心肌Akt/Bcl-2/Bax信號通路的影響
Western blot檢測顯示,與Con組及Sham組相比, NS組p-Akt、Bcl-2及Bax蛋白相對表達量增加,差異有統計學意義(P<0.05)。與NS組相比, NIC組p-Akt、Bcl-2蛋白相對表達量更高,但Bax蛋白表達量下降,差異均有統計學意義(P<0.05)。見圖3。

圖3 4組p-Akt/Bcl-2/Bax蛋白水平表達圖
3 討 論
尼可地爾是第一種ATP依賴性鉀通道開放劑,作為一種新型血管擴張劑在臨床實踐中表現出獨特的優勢。尼可地爾具有雙重的血管擴張機制[6],通過刺激血管平滑肌細胞中的鳥苷酸環化酶起到硝酸酯類的作用,導致冠狀動脈血流量增加和靜脈擴張[7]。此外,尼可地爾是一種ATP敏感性鉀通道開放劑,可引起血管平滑肌和線粒體鉀離子外流,使細胞電位超極化,誘導電壓門控鈣通道失活,減少細胞內游離鈣離子[8],松弛冠狀動脈和阻力血管,增加流向心肌的血流量。尼可地爾還可擴張全身阻力和容量血管,降低心臟前負荷和后負荷以及心肌耗氧量,緩解冠狀動脈痙攣,增加側支循環和心內膜下血供[9]。本研究發現尼可地爾可改善缺血性心力衰竭大鼠的心功能,并在正常范圍內降低血壓。
研究[10]表明,尼可地爾不僅能緩解缺血性心臟病的癥狀,還能抑制冠心病患者的心肌肥大和重塑。心力衰竭是最常見的心源性死亡原因,心臟重構在其發生發展中起重要作用[11]。本研究結果發現,尼可地爾改善了缺血性心力衰竭大鼠的一般情況,且提高了LVEF、LVFS和E/A,降低了LVEDV、LVESV、LVIDd和LVIDs水平,改善了缺血性心力衰竭大鼠的左室收縮功能。尼可地爾干預后大鼠LVW/BW和LUNGW/BW比值也顯著低于NS組大鼠。本研究組織學觀察結果顯示, Sham組心肌細胞排列規則,橫紋清晰; Con組排列紊亂,形狀不規則,左心室心肌組織呈明顯的纖維組織增生; NIC組心肌細胞的這些病理改變不那么明顯,而且較少出現增生。這提示尼可地爾可改善缺血性心力衰竭時的心功能和左室重構。
尼可地爾的保護機制尚未闡明。RAAS系統激活、氧化應激和心肌內鈣超載在心力衰竭的發生發展中起重要作用,其中鈣超載對心功能影響最大[12]。尼可地爾可以開放線粒體中的鉀通道,抑制氧化應激誘導的心肌細胞凋亡。研究[13]表明,尼可地爾作為NO供體,可能通過激活有絲分裂鉀通道和NO/可溶性鳥苷酸環化酶依賴機制來抑制氧化應激或高氧誘導的心肌細胞凋亡。此外,尼可地爾已被證明與凋亡相關蛋白的調節有關。Bcl-2與Bax共屬于一個家族,通過控制線粒體膜的通透性來調節凋亡激活物。bax二聚體在膜上打開通道,增加細胞膜通透性; bcl-2與bax可形成異聚體,降低細胞通透性[14]。bcl-2水平的升高和bax的降低表明細胞對凋亡的抵抗性增強,為保護藥物發揮作用的標志。本研究中,尼可地爾抑制缺血性心力衰竭引起的大鼠心肌Bax水平的上調,提示尼可地爾對缺血性心力衰竭大鼠的心臟保護作用可能是通過抑制Bax的表達來實現的。鑒于Bax的促凋亡作用,推測尼可地爾的保護作用可能參與控制缺血性心力衰竭大鼠的凋亡過程。
綜上所述,本研究發現,尼可地爾通過改善心功能和左室重塑對缺血性心力衰竭大鼠起到保護作用,其機制可能與尼可地爾抑制Bax蛋白表達有關。

